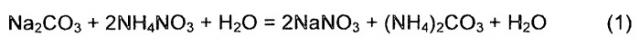Способ реагентной регенерации жидкосолевого нитрит-нитратного теплоносителя
Иллюстрации
Показать всеИзобретение относится к химической промышленности и может быть использовано для реагентной регенерации средне- и высокотемпературных теплоносителей. Карбонат натрия, гидроокись натрия и окись натрия взаимодействуют с насыщенными водными растворами нитрата или нитрита аммония. Мольное отношение водных растворов нитрата или нитрита аммония к карбонату натрия, гидроокиси натрия и окиси натрия составляет 1,01-2,00. Взаимодействие осуществляют при нагревании до температур ниже температуры разложения нитрата или нитрита аммония. Изобретение позволяет достигнуть степени регенерации теплоносителя до 90%. 1 табл., 4 пр.
Реферат
Предлагаемое изобретение относится к области реагентной регенерации средне- и высокотемпературных теплоносителей, в частности, используемых в производстве фталевого ангидрида каталитическим окислением ортоксилола кислородом воздуха.
К нитрит-нитратным теплоносителям относятся, в частности, двухкомпонентный эвтектический сплав нитрита натрия и нитрата калия (сплав СС-3), трехкомпонентный эвтектический сплав нитрата натрия и калия и нитрита натрия (сплав СС-4), относящиеся к анизодесмической подгруппе теплоносителей, а также теплоноситель, используемый при производстве фталевого ангидрида из ортоксилола, имеющий следующий состав: 44% масс. NaNO2 и 55% масс. KNO3.
В условиях длительной эксплуатации при высоких температурах теплоноситель подвергается частичному разложению, что приводит к изменению его теплофизических свойств, что может привести к ухудшению регулировки температуры реактора и выходу его из зоны оптимальных режимов работы, а также к образованию гарнисажного слоя на трубках парогенератора.
Нежелательными компонентами нитрит-нитратных жидкосолевых теплоносителей являются карбонат натрия (Na2CO3), гидроокись натрия (NaOH) и окись натрия (Na2O).
Указанные компоненты имеют повышенные температуры плавления и плохо растворимы в исходном расплаве. Вследствие этого они способны отлагаться на более холодных поверхностях теплообменной аппаратуры (например, парового котла), снижая коэффициент теплопередачи и уменьшая эффективность работы оборудования. (Химическая энциклопедия, Научное изд. «Большая Российская Энциклопедия», 1992 г., т.3, стр.183).
Существующим на данный момент решением проблемы накопления нежелательных компонентов в нитрит-нитратном теплоносителе является полная его замена. Однако замена всего объема теплоносителя (порядка сотен тонн) потребует остановки технологического процесса, стоимость замены высока по причине использования больших объемов нитрит-нитратного теплоносителя. Кроме того, утилизация большого объема достаточно токсичных соединений затруднена по экологическим причинам.
Известны способы реагентной регенерации различных веществ с последующим использованием продуктов регенерации в основном процессе, например способ реагентной регенерации коагулянта из гидроксисодержащего шлама водоочистки, суть которого заключается в регенерации коагулянта из маслогидроксидсодержащего шлама обработкой кислым алюмосодержащим раствором, полученным в промышленных условиях в результате разложения комплекса процесса Фриделя-Крафтса-Густавсона водой (Патент RU 2133225, кл. C02F 1/52; C01F 7/74, опубл. 1999 г.).
Строго говоря, регенерация как таковая не происходит, а осуществляется лишь замена его тем же веществом, но полученным из катализаторного комплекса Фриделя-Крафтса-Густавсона. Кроме того, существенным недостатком известного способа является то, что катализаторный комплекс при взаимодействии компонентов с водой разлагается с выделением органических соединений типа токсичных смол, которые в дальнейшем не используются.
Также известен способ регенерации отработанного теплоносителя энергетических установок на основе четырехокиси азота, заключающийся в конверсии четырехокиси азота при 200-700°С, смешении проконвертированного газового потока с охлажденным потоком жидкого теплоносителя, последующем охлаждении газожидкостной смеси в холодильной установке, сепарации кислорода в потоке жидкого теплоносителя, поступающем на смешение, и понижении содержания окиси азота до в отработанном теплоносителе, поступающем на конверсию, путем ректификации (SU 1456356, публ. 07.02.1989 г.). Основная стадия регенерации осуществляется путем абсорбции газов (NO2, NO), полученных конверсией N2O4, потоком очищенного теплоносителя - жидкого N2O4 с содержанием NO 0,02-0,05 мас.%, поступающего с одной из нижних тарелок ректификационной колонны, в которой осуществляется очистка теплоносителя от примесей и снижение содержания NO до 0,02-0,05 мас.%.
Однако известный способ не позволяет осуществлять восстановление состава жидкосолевого теплоносителя и направлен на снижение энергозатрат при физической балансировке состава газообразного теплоносителя, т.е. не является способом регенерации как таковой.
Известен также способ очистки промывных вод гальванического производства, для осуществления которого промывные воды гальванического производства при нанесении двухслойного никель-хромового покрытия проводят осаждение катионов и анионов с помощью насыщенного при комнатной температуре раствора гидроокиси бария с последующим отделением осадка отстаиванием и доочистку осветленной воды (Патент RU 2288185, кл. C02F 1/66; C02F 1/42; C02F 101/20; C02F 101/22; C02F 103/16, опубл. 2006 г.).
Однако известный способ не предназначен для регенерации жидкосолевых теплоносителей, являющихся расплавами. Кроме того, осуществление способа связано с выбросом в атмосферу тяжелых металлов (никель, барий) и невозможностью утилизации отходов-шламов.
Заявитель не обнаружил способов, близких к заявляемому по технической сущности и достигаемому результату, т.е. тех, которые позволили бы осуществлять регенерацию веществ типа нитрит-нитратных жидкосолевых теплоносителей и одновременно очищать от нежелательных компонентов, а именно - карбоната натрия (Na2CO3), гидроокиси натрия (NaOH) и окиси натрия (Na2O).
Предлагаемое техническое решение прототипа не имеет.
Технический результат выражается в достижении степени регенерации до 90% за счет протекания необратимых химических реакций и образования соединений, являющихся компонентами данного теплоносителя.
Дополнительный эффект выражается в повышении безопасности и обеспечении безотходности процесса за счет выделения в процессе регенерации аммиака в чистом виде.
Сущность изобретения заключается в том, что способ реагентной регенерации жидкосолевого нитрит-нитратного теплоносителя включает химическое взаимодействие карбоната натрия, гидроокиси натрия и окиси натрия, являющихся нежелательными компонентами теплоносителя, с восстанавливающим реагентом, в качестве которого используют насыщенные водные растворы нитрата или нитрита аммония, при этом мольное отношение восстанавливающего реагента к карбонату натрия, гидроокиси натрия и окиси натрия составляет 1,01-2,00, а химическое взаимодействие осуществляют при нагревании до температур ниже температуры разложения восстанавливающего реагента.
При осуществлении химического взаимодействия карбоната натрия (Na2CO3), гидроокиси натрия (NaOH) и окиси натрия (Na2O) протекают следующие химические реакции:
В связи с протеканием реакций (2, 4, 6, 8) и выводом продуктов разложения из реакционного объема, реакции (1, 3, 5, 7) приобретают необратимый характер, в связи с чем вышеперечисленные нежелательные загрязняющие компоненты могут быть полностью преобразованы в допустимые соединения. При этом конечным побочным продуктом является чистый аммиак, который в дальнейшем используется по своему назначению.
Использование нитрата или нитрита аммония является в данном случае единственно возможным, так как продукты их взаимодействия с нежелательными компонентами представляют собой соединения, являющиеся основными компонентами среднетемпературного жидкосолевого нитрит-нитратного теплоносителя. При этом образование нитрата натрия в случае использования нитрата аммония (реакции 1-4) в качестве восстанавливающего реагента не ухудшит качество самого теплоносителя, так как наличие в его составе полученного в результате реакции компонента допустимо в соответствии с приближенностью изначального состава теплоносителя к группе составов нитрит-нитратных теплоносителей различных марок (в частности, к сплавам СС-3 и СС-4) согласно таблице, на которой представлены различные составы нитрит-нитратных смесей, используемых в качестве теплоносителей.
| Таблица | ||
| NaNO2, (%) | NaNO3, (%) | KNO3, (%) |
| 100 | 0 | 0 |
| 50 (СС-3) | 0 | 50 |
| 44 | 3 | 53 |
| 42 | 3 | 55 |
| 40 | 0 | 60 |
| 40 (СС-4) | 7 | 53 |
| 38,5 | 11 | 50,5 |
| 38 | 6 | 56 |
| 35 | 7 | 58 |
| 34 | 13 | 53 |
| 33 | 3 | 63 |
| 30 | 20 | 50 |
| 30 | 10 | 60 |
| 30 | 0 | 70 |
| 0 | 100 | 0 |
| 0 | 0 | 100 |
Характеристики теплоносителя с нежелательными компонентами:
1. Нитрит натрия. Химическая формула: NaNO2. Молярная масса 69 г/моль, плотность: 2,2 г/см2. Температура плавления 271°C, температура разложения выше 320°C. Растворимость в воде составляет 82 г в 100 мл. Чистое вещество не гигроскопично; на воздухе медленно доокисляется до нитрата натрия NaNO3. Является сильным восстановителем. Относится ко II классу опасности, токсичен (метгемоглобинобразующий яд (полулетальная доза ЛД50 180 мг/кг веса)), пожароопасное вещество, способствует самовозгоранию горючих материалов.
2. Нитрат калия (калиевая селитра). Химическая формула: KNO3. Молекулярная масса: 101,1032 г/моль, плотность: 2,109 г/см2 (16°C). Температура плавления 334°C, температура кипения 400°C. Растворимость в воде составляет 13,3 (0°C), 36 (25°C) и 247 (100°C) в 100 мл. Полулетальная доза ЛД50 составляет 3750 мг/кг веса. При 400°C разлагается с выделением кислорода. Пожароопасное вещество, так как является сильным окислителем.
3. Окись натрия (натрия оксид). Химическая формула: Na2O. Молярная масса 62 г/моль. Плотность 2,37 г/см3. Температура плавления 1132°C. Химически активна. Образует с водой NaOH, при взаимодействии с CO2 образует Na2CO3.
4. Гидроокись натрия (едкий натр). Химическая формула: NaOH. Молярная масса: 39,997 г/моль, плотность 1,59 г/см3. Температура плавления 323°C, температура кипения 1403°C. Растворимость в воде составляет 108,7 г в 100 мл. Очень гигроскопично. Является сильным основанием; разрушает кожу, бумагу и другие органические вещества. Не горюче, но особо токсично. Вдыхание аэрозоля вещества может взывать отек легких. ПДК рабочей зоны составляет 0,5 мг/м3.
5. Карбонат натрия. Химическая формула: Na2CO3. Молекулярная масса: 105,99 г/моль, плотность: 2,53 г/см2. Температура плавления 852°C, температура кипения 1600°C. Растворимость в воде составляет 21,8 г в 100 мл (20°C).
Характеристики восстанавливающих реагентов:
1. Нитрат аммония (аммиачная селитра). Химическая формула: NH4NO3. Молярная масса 80,04 г/моль, плотность: 1,725 г/см2. Температура плавления 169,6°C, температура кипения 235°C, температура разложения около 210°C. Растворимость в воде составляет 119 (0°C), 212 (25°C), 346 (50°C), 1024 (100) г в 100 мл. Взрывоопасно в смеси с горючими материалами. Скорость детонации 2570 м/с.
2. Нитрит аммония. Химическая формула: NH4NO2. Молярная масса 64,04 г/моль, плотность: 1,69 г/см2. Разлагается, примерно, при 70°C. Растворимость в воде составляет 180,1 г в 100 мл. Токсичен для человека и водных организмов.
Было обнаружено, что на глубину процесса и степень регенерации в большей степени оказывают влияние такие параметры, как температура среды, в которой проводится регенерация, продолжительность регенерации и эквивалентное мольное соотношение нежелательного компонента и восстанавливающего реагента.
Проведение реагентной регенерации в водном растворе позволяет осуществить процесс при относительно низких температурах ниже температуры разложения восстанавливающего реагента. При этом максимальная температура процесса ограничивается температурой разложения восстанавливающего реагента, что обеспечивает полноту прохождения химических процессов и безопасность.
Эквивалентное мольное отношение восстанавливающего реагента к нежелательному компоненту составляет 1,01-2,00 и зависит от содержания нежелательного компонента в теплоносителе. Величина мольного отношения менее 1 не обеспечивает прохождение химических реакций до конца при ограничении по времени. В то же время величина отношения более 2 является экономически невыгодной с точки зрения перерасхода реагента при той же величине степени регенерации теплоносителя. Заявляемое отношение восстанавливающего реагента к нежелательному компоненту позволяет достигнуть максимально возможной степени регенерации, т.е. более 90%.
При этом продолжительность процесса реагентной регенерации зависит от содержания нежелательного компонента в составе теплоносителя и температуры проведения процесса, которые определяются расчетным путем либо экспериментально.
Кроме того, важным достоинством заявляемого способа является то, что в результате химической реакции выделяется аммиак NH3 в чистом виде, т.е. продукт, который можно использовать в дальнейшем и безопасно утилизировать, тогда как во всех известных способах регенерации будут образованы опасные вещества, попадающие в окружающую среду и загрязняющие ее либо не используемые, т.е. шлам.
Заявляемый способ в лабораторных условиях осуществляется следующим образом.
Готовят модельный расплав теплоносителя расчетного количества со следующим составом: 44% масс. NaNO2; 55% масс. KNO3: 1% масс. NaOH. Либо предварительно определяют состав реального загрязненного теплоносителя из промышленного реактора.
Далее смешивают измельченный расплав с восстанавливающим реагентом в заданном эквивалентном соотношении и выдерживают смесь при заданной температуре в течение заданного времени. Затем продукты реакции подвергают анализу. В результате химических процессов в чистом виде выделяется аммиак, утилизируемый известными способами.
Конкретные примеры осуществления заявляемого способа.
Пример 1. В лабораторных условиях была проведена регенерация образца загрязненного жидкосолевого теплоносителя, взятого из солевой ванны промышленного реактора каталитического окисления о-ксилола кислородом воздуха R-211, установленного в цехе производства фталевого ангидрида предприятия ОАО «Камтэкс-Химпром». Анализ показал, что образец содержал 44% масс NaNO2; 55% масс KNO3; 1% масс. NaOH.
Брали 5 г расплава промышленного теплоносителя, измельчали его, затем смешивали с восстанавливающим реагентом NH4NO3 в эквивалентном соотношении NH4NO3/NaOH=1.04, добавляли воды, нагревали до 80°C и перемешивали в течение 20 минут. Затем смесь анализировали потенциометрическим кислотно-основным титрованием, используя в качестве титранта 0,016 N соляную кислоту. При этом предварительно был подвергнут анализу образец промышленного теплоносителя без проведения регенерации.
Степень регенерации образца реального теплоносителя составила 94,4%.
Пример 2. В лабораторных условиях была проведена регенерация образца загрязненного жидкосолевого теплоносителя, взятого из солевой ванны промышленного реактора каталитического окисления о-ксилола кислородом воздуха R-211, установленного в цехе производства фталевого ангидрида предприятия ОАО «Камтэкс-Химпром». Анализ показал, что образец содержал 44% масс NaNO2; 55% масс KNO3; 1% масс. NaOH.
Брали 5 г расплава промышленного теплоносителя, измельчали его, затем смешивали с восстанавливающим реагентом NH4NO2 в эквивалентном соотношении NH4NO2/NaOH=1,20, добавляли воды, нагревали до 60°C и перемешивали в течение 15 минут. Затем смесь анализировали потенциометрическим кислотно-основным титрованием, используя в качестве титранта 0,016 N соляную кислоту. При этом предварительно был подвергнут анализу образец промышленного теплоносителя без проведения регенерации.
Степень регенерации образца реального теплоносителя составила 90,7%.
Пример 3. Брали 5 г модельного расплава и измельчали его. Затем смешивали с NH4NO3 в эквивалентном соотношении NH4NO3/NaOH=1.5, добавляли воды и перемешивали при 80°C в течение 30 минут. По истечении времени смесь анализировали потенциометрическим кислотно-основным титрованием, используя в качестве титранта 0,016 N соляную кислоту. При этом предварительно был подвергнут анализу раствор образца модельного расплава без проведения регенерации.
В ходе лабораторных испытаний была доказана возможность практического проведения процесса регенерации, а также определена степень регенерации. По результатам эксперимента на модельном расплаве степень регенерации составила 96,1%.
Пример 4. Брали 5 г модельного расплава, содержащего: 44% масс NaNO2; 55% масс KNO3; 1% масс Na2CO3 и измельчали его. Затем смешивали с NH4NO3 в эквивалентном соотношении NH4NO3/Na2CO3=1.5, добавляли воды и перемешивали при 80°C в течение 20 минут. По истечении времени, смесь анализировали потенциометрическим кислотно-основным титрованием, используя в качестве титранта 0,016 N соляную кислоту. При этом предварительно был подвергнут анализу образец модельного расплава без проведения регенерации.
В результате опыта была определена степень регенерации данного образца, которая численно равна 91,3%, что в целом соответствует результатам экспериментов с NaOH в качестве восстанавливающего реагента.
Обработка экспериментальных данных позволила вывести зависимость степени регенерации α (%) от основных параметров процесса:
α=-55,7+1,024·Т+1,404·т+18,0·К,
где Т - температура процесса, °C,
т - время проведения процесса, мин,
К - соотношение натрий гидроокись/нитрат аммония.
Зависимость позволяет задавать условия регенерации при заданной степени регенерации жидкосолевого теплоносителя - 99,9%: длительность - 30,1 мин; температура - 83,5°C; мольное соотношение нитрат аммония/гидроокись натрия К=1,5.
Как показывают эксперименты, способ реагентной регенерации жидкосолевого нитрит-нитратного теплоносителя реализуем практически, и позволяет достичь высоких степеней регенерации - от 90% и выше, а теоретически - до 99,9%.
Способ реагентной регенерации жидкосолевого нитрит-нитратного теплоносителя, включающий химическое взаимодействие карбоната натрия, гидроокиси натрия и окиси натрия, являющихся нежелательными компонентами теплоносителя, с восстанавливающим реагентом, в качестве которого используют насыщенные водные растворы нитрата или нитрита аммония, при этом мольное отношение восстанавливающего реагента к карбонату натрия, гидроокиси натрия и окиси натрия составляет 1,01-2,00, а химическое взаимодействие осуществляют при нагревании до температур ниже температуры разложения восстанавливающего реагента.