Ядерно-химический способ получения меченных тритием кватернизированных структур диазинового ряда
Иллюстрации
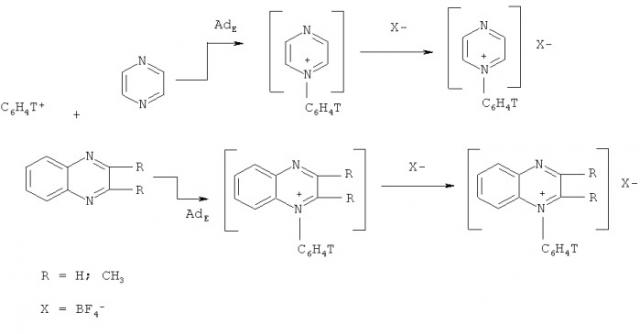
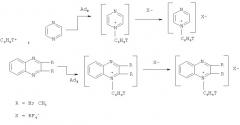
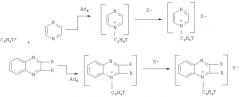
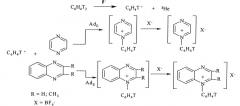
Показать всеИзобретение относится к способу получения меченных тритием кватернизированных структур диазинового ряда, а именно N-фенилдиазиниевых солей, ядерно-химическим методом по реакции:
отличающийся тем, что 1,4-диазины (пиразин, хиноксалин и 2,3-диметилхиноксалин) подвергают ион-молекулярным реакциям со свободными нуклеогенными фенилкатионами, которые генерируются при бета-распаде трития в составе двукратно меченого бензола в замкнутой системе в присутствии стабилизирующей соли - тетрафторбората калия. Технический результат: разработан простой метод получения меченных тритием радиоактивных маркеров для изучения биохимических процессов. 1 ил., 3 пр.
Реферат
Настоящее изобретение относится к способу получения меченных тритием кватернизированных структур диазинового ряда, а именно N-фенилдиазиниевых солей, ядерно-химическим методом по реакции:
Диазины - это шестичленные гетероциклические соединения с двумя гетероатомами, оба из которых являются атомами азота. Циклическая система пиразина образует общий структурный фрагмент 1,4-диазинов. Бензопиразин или хиноксалин, а также хиназолин представляют собой диазиновый цикл с анелированным бензольным кольцом. 1,4-Диазины и конденсированные системы, содержащие пиразиновый цикл, являются важнейшим типом гетероциклических соединений, обладающими высокой биологической активностью [Kaim W. The versatile chemistry of 1,4-diazines: organic, inorganic and biochemical aspects. Angew. Chem. Int. Ed. Engl. 1983. V.22, No. 3. P.171-258]. Пиразиновый цикл встречается как в природных веществах, так и в большом числе синтетических лекарственных препаратов [Cheeseman G.W.H., Werstiuk E.S.G. Recent advances in pyrazine chemistry. Advances in Heterocyclic Chemistry. 1972. V.14. P.99-209]. Большое значение имеют конденсированные гетероциклы, такие как фолиевая кислота, рибофлавин, тетрагидробиоптерин и ксантоптерин, играющие важную роль во многих процессах жизнедеятельности [Иванский В.И. Химия гетероциклических соединений. - М.: Высшая школа. 1978. 559 с.; Pozharskii A.F., Soldatenkov A.T., Katritzky A.R. Heterocycles in Life and Society. New York: Wiley, 1997. P.64-143]. Хиноксалин является структурным фрагментом некоторых природных соединений, например пептидного антибиотика эхиномицина [Dell A., Williams D.H., Morris H.R., Smith G.A., Feeney J., Roberts G.C. K. Structure revision of the antibiotic echinomycin. J. Am. Chem. Soc. 1975. V.97. P.2497-2502]. Различные производные бензопиразинов, то есть хиноксалинов, являются важными антибактериальными лекарственными препаратами - диксин, диоксидин, диоксипласт, хиндиокс, хиноксидин, сульфахиноксалин и т.д. [Rajurkar R.M., Agrawal V.A., Thonte S.S., Ingale R.G. Heterocyclic chemistry of quinoxaline and potential activities of quinoxaline derivatives. A review. Pharmacophore. 2010. V. 1(2). P.65-76]. 1,4-Диазины обладают широким спектром биологической и фармакологической активности, включая не только антибактериальную, но и противоопухолевую и противовирусную, в том числе в отношении вируса иммунодефицита человека [Renault J., Baron M., Mailliet P. & al. Heterocyclic quinones.2.Quinoxaline-5,6-(and 5-8)-diones-Potential antitumoral agents. Eur. J. Med. Chem. 1981. V.16. No 6. P.545-550; Seitz L.E., Suling W.J., Reynolds R.C. Synthesis and antimycobacterial activity of pyrazine and quinoxaline derivatives. J. Med. Chem. 2002. V.45. P.5604-5606; Thomas K..R.J., Velusamy M., Lin J.Т., Chuen C.-H., Tao Y.-T. Chromophore-labeled quinoxaline derivatives as efficient electroluminescent materials. Chem. Mater. 2005. V.17. P.1860-1866; Jaso A., Zarranz В., Aldana I., Monge A. Synthesis of new quinoxaline-2-carboxylate 1,4-dioxide derivatives as anti-Mycobacterium tuberculosis agents. J. Med. Chem. 2005. V.48. P.2019-2025; Sessler J.L., Maeda H., Mizuno Т., Lynch V.M., Furuta H. Quinoxaline-oligopyrroles: Improved pyrrole-based anion receptors. Chem. Commun. 2002. P.862-863; Sessler J.L., Maeda H., Mizuno Т., Lynch V.M., Furuta H. Quinoxaline-bridged porphyrinoid. J. Am. Chem. Soc. 2002. V.124. P.13474-13479; Castro P.P., Zhao G., Masangkay G.A., Hemandez C., Gutierrez-Tunstad L.M. Quinoxaline excision: a novel approach to tri- and diquinoxaline cavitands. Org. Lett. 2004. V.6. P.333-336; Toshima К., Takano R., Ozawa Т., Matsumura S. Molecular design and evaluation of quinoxaline-carbohydratc hybrids as novel and efficient photo-induced GG-selective DNA cleaving agents. Chem. Commun. 2002. P.212-213; Hui X., Desrivot J., Bories C., Loiseau P.M., Franck X., Hocquemiller R., Figade're B. Synthesis and antiprotozoal activity of some new synthetic substituted quinoxalines. Bioorganic & Med. Chem. Lett. 2006. V.16. P.815-820; Kirkovits G.J., Zimmerman R.S., Huggins M.T., Lynch V.M., Sessler J.L. Synthesis, structural characterization and complexation properties of the first "crowned" dipyrrolylquinoxalines. Eur. J. Org. Chem. 2002. P.3768-3778; Aldakov D., Anzenbacher P. Dipyrrolyl quinoxalines with extended chromophores are efficient fluorimetric sensors for pyrophosphate. Chem. Commun. 2003. P.1394-1395; Gao H., Yamasaki E.F., Chan K.K., Shen L.L., Snapka R.M. DNA sequence specificity for topoisomerase II poisoning by the Quinoxaline Anticancer Drugs XK469 and CQS. Mol. Pharmacol. 2003. V.63. No 6. P.1382-1388].
Интерес к 1,4-диазинам сохраняется крайне высоким и в последние годы. Это связано, главным образом, с тем, что пиразиновая система и ее производные являются фрагментами многих биологически важных соединений и медицинских препаратов [Gali-Muhtasib H., Sidani M., Geara F., Mona A.-D., Al-IImaira J., Haddadin M.J., Zaatari G. Quinoxaline 1,4-dioxides are novel angiogenesis inhibitors that potentiate antitumor effects of ionizing radiation. International Journal of Oncology. 2004. V.24. No 5. P.1121-1131; Iwashita A., Hattori K., Yamamoto H., Ishida J., Kido Y., Kamijo K., Murano K., Miyake H., Kinoshita Т., Warizaya M., Ohkubo M., Matsuoka N.. Mutoh S. Discovery of quinazolinone and quinoxaline derivatives as potent and selective poly(ADP-ribose) polymerase-1/2 inhibitors. FEBS Lett. 2005. V.579(6). P.1389-1393; Ishida J., Yamamoto H., Kido Y., Kamijo K., Murano K., Miyake H., Ohkubo M., Kinoshita Т., Warizaya M., Iwashita A., Mihara K., Matsuoka N., Hattori K. Discovery of potent and selective PARP-1 and PARP-2 inhibitors: SBDD analysis via a combination of X-ray structural study and homology modeling. Bioorg Med Chem. 2006. V.14(5). P.1378-1390; Heravi M. M., Bakhtiari K., Tehrani M.H., Javadi N.M., Oskooie H.A. Facile synthesis of quinoxaline derivatives using o-iodoxybenzoic acid (IBX) at room temperature. ARKIVOC. 2006. V.16. P.16-22; Urquiola С., Gambino D., Cabrcra M., Lavaggi M.L., Cerecetto H., Gonzalez M., Lopez de Cerain A., Monge A., Costa-Filho A.J., Torre M.H. New copper-based complexes with quinoxaline N1, N4-dioxide derivatives, potential antitumoral agents. Journal of Inorganic Biochemistry. 2008. V.102. P.119-126; Shindy H.A., Soleiman H.A. Synthesis and spectral behaviour of some quinoxaline cyanine dyes. Canadian Journal on Chemical Engineering & Technology. 2010. V.1. No 4. P.44-59; Kudo K., Momotake A., Kanna Y., Nishimura Y., Arai T. Development of a quinoxaline-based fluorescent probe for quantitative estimation of protein binding site polarity. Chem. Commun. 2011. V.47. No 13. P.3867-3869; Kakodkar N.C., Peddinti R., Kletzel M., Tian Y., Gucrrero L.J., Undevia S.D., Gear D., Chlenski A., Yang Q., Salwen H.R., Cohn S.L. The quinoxaline anti-tumor agent (R+)XK469 inhibits neuroblastoma tumor growth. Pediatr Blood Cancer. 2011. V.56(1). P.164-167; Singh D.P., Deivedi S.K., Hashim S.R., Singhal R.G. Synthesis and antimicrobial activity of some new quinoxaline derivatives. Pharmaceuticals. 2010. V.3(8). P.2416-2425; Ghosh P., Mandal A. Green and selective protocol for the synthesis of quinoxalines. Advances in Applied Science Research. 2011. V.2. (1). P.255-260; Patidar A.K., Jeyakandan M., Moobiya Л.К., Selvan G. Exploring potential of quinoxaline moiety. Internnational Journal of PharmTech Research. 2011. Vol.3. No. 1. P.386-392; Noorulla S., Sreenivasulu N. Antibacterial activity of novel substituted quinoxaline heterocycles with isoniazide. International Journal of Research in Pharmaceutical and Biomedical Sciences. 2011. Vol.2. No. 3. P.1100-1106; Khaksar S., F. Rostamnezhad S. A novel one-pot synthesis of quinoxaline derivatives in fluorinated alcohols. Bull. Korean. Chem. Soc. 2012. Vol.33. No. 8. P.2581-2584; Asif M. Recent efforts for the development of antitubercular drug containing diazine ring. Medicinal chemistry. 2012. Vol.2(7). P.151-167].
В настоящее время прогресс в области биохимии, молекулярной биологии и генетики, а также практической медицины во многом определяется возможностью широкого использования радиоактивных биологических маркеров. Применение меченых, а особенно это касается меченных тритием соединений, позволяет проводить детальные и высокочувствительные исследования механизмов химических и биохимических процессов в живых организмах, установление путей метаболизма природных и синтетических лекарственных препаратов [Sidorov G.V., Myasoedov N.F. Synthesis of tritium-labelled biologically important diazines. Ruissian Chemical Reviews. 1999. Vol.68. No. 3. P.229-240; Egan J.A., Nugent R.P., Filer C.N. Tritium labelling and characterization of the cognition enhancing drug tacrine using several precursors. Applied Radiation and Isotopes. 2002. Vol.57. No. 6. P.837-840; Egan J.A., Filerga C.N. Tritium labeling of the local anesthetic tetracaine via a polyhalogenated precursor. Journal of Radioanalytical and Nuclear Chemistry. 2003. Vol.258. No. 1. P.185-187; Ahem D.G, Laseter A.G., Filer C.N. Tritium labelling of several potent fluorinated antipsychotic drugs at high specific activity," Applied Radiation and Isotopes. 2007. Vol.65. No. 7. P.827-830; Mousseau G., Raffy Q., Thomas О.Р., Agez M., Thai R., Renaul J. P., Pin S., Ochsenbein F., Cintrat J.-C., Rousseau B. Footprinting of protein interactions by tritium labeling. Biochemistry. 2010. Vol.49. No.20. P.4297-4299; Heinkele G., Miirdter T.E. Synthesis of [2H3]-labelled sulfamethoxazole and its main urinary metabolites. Journal of Labelled Compounds and Radiopharmaceuticals. 2007. Vol.50. No. 7. P.656-659; Lee D.Y.W., Ji X.S., Zhang X. Synthesis of tritium-labeled puerarin - a potential antidipsotropic agent. Journal of Labelled Compounds and Radiopharmaceuticals. 2007. Vol.50. No. 8. P.702-705; Pleiss U. 1,4-Dihydropyridines (DHPs) - a class of very potent drugs: syntheses of isotopically labeled DHP derivatives during the last four decades. Journal of Labelled Compounds and Radiopharmaceuticals. 2007. Vol.50. No. 9-10. P.818-830; Hong Y., Bonacorsi Jr. S.J., Tian Y., Gong S., Zhang D., Humphreys W.G., Balasubramanian В., Cheesman E.H., Zhang Z., Castner J.F. Crane P.D. Synthesis of [1,2-3H]ethylamine hydrochloride and [3H]-labeled apadenoson for a human ADME study. Journal of Labelled Compounds and Radiopharmaceuticals. 2008. Vol.51. No. 2. P.113-117; Wheeler W.J., Clodfelter D.K.. Synthesis of the tritiated isotopomers of enzastaurin and its N-des-pyridylmethyl metabolite for use in ADME studies. Journal of Labelled Compounds and Radiopharmaceuticals. 2008. Vol.51. No. 4. P.175-181; Wu S.-Y., Masjedizadeh M.R. Synthesis of tritium labelled thiorphan, an enkephalinase inhibitor. Journal of Labelled Compounds and Radiopharmaceuticals. 2009. Vol.52. No. 1. P.23-28; Zona C., La Feria B. Synthesis of labeled curcumin derivatives as tools for in vitro blood brain barrier trafficking studies. Journal of Labelled Compounds and Radiopharmaceuticals. 2011. Vol.54. No. 9. P.629-632; Malmquist J., Bernlind A., Sandell J., Strom P., M Waldman M. Tritium labeling of a γ-secretase inhibitor and two modulators as in vitro imaging agents. Journal of Labelled Compounds and Radiopharmaceuticals. 2012. Vol.55. No. 2. P.80-83; Lockley W.J.S., McEwen A., Cooke R. Tritium: a coming of age for drug discovery and development ADME studies. Journal of Labelled Compounds and Radiopharmaceuticals. 2012. Vol.55. No. 7. P.235-257].
В связи с этим, одной из важных задач представляется поиск новых, нетрадиционных путей получения производных диазинов и синтез ранее неизвестных соединений пиразинового ряда. А также разработка простых методов получения меченных тритием радиоактивных маркеров для изучения биохимических процессов. Ранее разработанным авторами ядерно-химическим методом была осуществлена неизвестная ранее реакция фенилирования гетероциклического атома азота в различных производных пиридина, хинолина, изохинолина, трициклических производных и успешно синтезированы в одну стадию меченные тритием N-фенильные ониевые соединения, радиоактивные маркеры для биологических исследований (Патент РФ №2439059 от 10.02.2012 г.; Патент РФ №2442776 от 20.02. 2012 г.; Патент РФ №2405773 от 10.12.2010 г.; Патент РФ №2320647 от 27.03.2008 г.).
Пиразины имеют значительный ароматический характер, и основные свойства их реакционной способности могут быть предсказаны исходя из свойств пиридинов, в которые введен еще один атом азота в пара-положении. Атом азота в азинах имеет пару электронов, еще не участвующих в образовании σ или π-связи, эти электроны способны образовывать связь между азотом и углеродом, и в этом случае атом азота становится четвертичным [Duffin G.F. The quatemization of heterocyclic compounds. Advances in Heterocyclic Chemistry. 1964. Vol.3. P.1-56]. Пиразин и хиноксалин обладают слабой основностью (рКа~0,6) [Patidar A.K., Jeyakandan M., Moobiya A.K., Selvan G. Exploring potential of quinoxaline moiety. Internnational Journal of PbarmTech Research. 2011. Vol.3. No. 1. P.386-392; Noorulla S., Sreenivasulu N. Antibacterial activity of novel substituted quinoxaline heterocycles with isoniazide. International Journal of Research in Pharmaceutical and Biomedical Sciences. 2011. Vol.2. No. 3. P.1100-1106; Pilarski В., OsMialowski K. The relationship between Electron Densities and the рКа Values in a Series of Methylpyrazines," International Journal of Quantum Chemistry, Vol.28, No. 2, 1985, pp.239-244], и это являлось причиной, что долгое время реакцию дикватернизации на практике осуществить не удавалось. Предполагалось, что неудачи связаны с понижением нуклеофильности второго атома азота вследствие кватернизации первого атома азота. Но использование борфторидов триалкилоксония, более сильных алкилирующих реагентов позволило получить ряд диквартенизированных пиразиниевых производных [Curphey T.J., Prasad K.S. Diquatemary salts. I. Preparation and characterization of the diquaternary salts of some diazines and diazoles. J. Org. Chem. 1972. Vol.37. No. 14. P.2259-2266]. Успех данного синтеза авторы объясняли предположением об усилении реакционной способности в присутствии двух положительных зарядов в сопряженной системе. Хорошо известно, что все N-фенильные четвертичные соли (за исключением пиридиниевых) невозможно получить реакцией прямой кватернизации, присоединение фенильного заместителя к атому азота должно происходить до замыкания гетероциклического кольца [Duffin G.F. The quaternization of heterocyclic compounds. Advances in Heterocyclic Chemistry. 1964. Vol.3. P.1-56]. К сожалению, до сих пор классическими химическими методами не были получены ароматические производные, а именно N-фенильные кватернизированные соли диазиниев.
Задачей данного изобретения является разработка простого по исполнению, доступного по реагентам, с высокими радиохимическими выходами одностадийного способа получения неизвестных в классической химии N-фенильных солей диазиниевой структуры (пиразиниевых, хиноксалиниевых и диметилхиноксалиниевых производных), меченных тритием, а также разработка простых методов получения меченных тритием радиоактивных маркеров для изучения биохимических процессов.
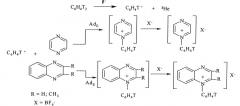
Поставленная задача достигается описываемым новым ядерно-химическим способом получения меченных тритием неизвестных кватернизированных структур диазинового ряда, заключающимся в том, что 1,4-диазины (пиразин, хиноксалин и 2,3-диметилхиноксалин) подвергают ион-молекулярным реакциям со свободными меченными тритием нуклеогенными фенил-катионами, которые генерируются самопроизвольно при бета-распаде трития в составе тритированного бензола, согласно следующей схеме:
R=H; CH3
X=BF4-
При взаимодействии свободных нуклеогенных фенил-катионов с гетероциклической системой исследуемых диазинов происходит неописанная ранее реакция электрофильного присоединения AdE (прямое взаимодействие по неподеленной электронной паре атома азота) с образованием неизвестных фенилзамещенных кватернизированных (четвертичных) диазиниевых производных.
Вышеперечисленная совокупность существенных признаков позволяет получить следующий технический результат. Авторами создан простой по исполнению, доступный по реагентам, с высокими радиохимическими выходами одностадийный способ получения неизвестных N-фенильных производных 1,4-диазинов, меченных тритием, которые могут быть использованы в качестве радиоактивных маркеров при проведении биологических и медицинских исследований. Введение заместителей с индукционным эффектом (аннелированных бензольных колец, а также метальных групп) позволило авторам сместить направление ион-молекулярных взаимодействий в сторону неизвестной реакции прямого фенилирования атома азота в гетероциклическом производном и, соответственно, значительно повысить радиохимический выход кватернизированных солей.
Изобретение иллюстрируется следующими примерами.
Пример 1
Двукратно меченный тритием бензол
Синтез двукратно меченного тритием бензола проводили в вакуумной системе по реакции:
Из 3,4 мг (0,014 ммоль) дибромбензола, 5,0 мкл (0,020 ммоль) трибутиламина в 200 мкл гексана и 3,3 Ки (0,054 ммоль) газообразного трития гидрированием на катализаторе 5% Pd/BaSO4 (предварительную активацию катализатора проводили при 160-180°C в течение 45 мин в динамическом вакууме 10-3 мм рт.ст.) при комнатной температуре в течение 1 ч получали двукратно меченный тритием бензол. Синтезированный бензол выделяли из реакционной смеси совместной дистилляцией с гексаном в вакууме при комнатной температуре в ампулу, охлаждаемую жидким азотом. Химическая чистота синтезированного меченого бензола определена методом ГЖХ. Условия хроматографического анализа: колонка набивная SE-30 на Inerton, длина 2 м; детекторы - катарометр и пропорциональный проточный счетчик; температура колонки - 30°C; температура испарителя - 70°C; температура детекторов - 70°C; объемная скорость потока газа-носителя - 20 см3/мин; газ-носитель - гелий. Наличие на хроматограммах с детектированием по теплопроводности двух пиков - гексана и бензола и одного пика-пика бензола при детектировании по радиоактивности позволяет заключить, что химическая и радиохимическая чистота синтезированного бензола не менее 99%. Измеренная сцинтилляционным методом объемная удельная активность полученного раствора в гексане составила 1 Ки/мл.
Методика ядерно-химического синтеза
Ион-молекулярные реакции осуществляли в запаянных ампулах объемом примерно 0,25 мл, заполненных почти полностью стабилизирующей солью (тетрафторборатом калия), на поверхность которой нанесен используемый субстрат. Для равномерного нанесения субстрата на поверхность соли ее смачивали эфирным или бензольным раствором, содержащим 0,055 ммоля 1,4-диазина. Растворитель удаляли в вакууме при комнатной температуре и в ампулы вводили по 1 мкл гексанового раствора меченного тритием бензола. Ампулы охлаждали жидким азотом, вакуумировали и запаивали. Мольное соотношение бензол : субстрат в реакционных смесях составляло не менее 1:3000. Ампулы с реакционной смесью выдерживают для накопления продуктов реакции в количествах, достаточных для их надежного детектирования по радиоактивности (не менее 1 мес.), непрореагировавший бензол отгоняют в вакуумме, субстрат с продуктами реакции смывали с поверхности стабилизирующей соли ацетоном или ацетонитрилом, и проводили выделение и идентификацию синтезированных соединений методом тонкослойной хроматографии. Радиохроматографию полученных третированных соединений осуществляли на стеклянных пластинках Analtech TLC Uniplates USA (С-18 silica gel matrix, UV) 5см×20см в CH3CN. Измерение β-радиоактивности меченных тритием соединений проводили с помощью жидкостного сцинтилляционного счетчика RackBeta 1215 (LKB Wallac, Finland).
Синтез борфторида N-фенил-2,3-диметилхиноксалиния, меченного тритием
В реакционную ампулу на кристаллы стабилизирующей соли - KBF4 (~200 мг) добавлен эфирный раствор 8,7 мг 2,3-диметилхиноксалина. Затем растворитель отгонялся в вакууме, и в ампулу вводился 1 мкл гексанового раствора С6Н4Т2. Ампулы запаивались и выдерживались некоторое время для накопления продуктов реакции в количествах, достаточных для их надежного определения (не менее 1 месяца). Накопление проводилось в твердой фазе (-15°C). После накопления ампулы вскрывались, и проводилось выделение и идентификация синтезированных соединений. Вскрытие ампул производилось в растворе неактивного носителя - 0,5 мл ацетонового раствора ониевого производного с концентрацией 1 мг/мл. Вследствие отсутствия изотопных свидетелей были использованы изоморфные: для пиразина - немеченая соль N-фенилпиридиния, для хиноксалина и 2,3-диметилхиноксалина - соль N-фенилхинолиния. Затем растворители отгонялись при пониженном давлении (этим одновременно достигается удаление из реакционной ампулы нераспавшегося третированного бензола). В реакционную смесь еще дважды добавлялся бензол (по 0,3-0,5 мл), который каждый раз откачивался под вакуумом. Из сухого остатка после отгонки бензола продукты реакции извлекались ацетоном. Аликвотные части ацетонового раствора (10 мкл) подвергались хроматографическому разделению. Для выделения и идентификации была использована тонкослойная хроматография (ТСХ) на стеклянных пластинках Reverse Phase C18 silica gel UV. Измерение бета-радиоактивности трития в полученных третированных соединениях проводилось с помощью жидкостного сцинтилляционного счетчика RackBeta 1215 (LKB Wallac, Finland) с применением диоксанового сцинтилляционного раствора. Слой адсорбента со стеклянной пластины поэтапно (по 0,5 см) прямо счищался в измерительные кюветы со сцинтиллятором. Точные измерения достигаются только после некоторого нахождения образцов в измерительных кюветах (от 12 до 24 часов). Это время необходимо для установления равновесия между раствором и осадком. Значения относительных выходов продуктов ион-молекулярных реакций определялись авторами по отношению активностей идентифицированных индивидуальных соединений к суммарной активности всех меченых продуктов. Типичная радиохроматограмма приведена на чертеже.
Первый пик на хроматограмме принадлежит N-фенил-2,3-диметилхиноксалиний борфториду, меченному тритием. Радиохимический выход целевого продукта составляет 20,7±1,0. При получении гетероциклических производных с помощью ядерно-химического метода не представляется возможным охарактеризовать полученное соединение обычными физико-химическими методами вследствие получения микроколичеств веществ (10-12 - 10-15 г). Для идентификации используется высокочувствительный радиохимический метод, позволяющий по β-радиоактивности трития фиксировать такие небольшие количества синтезированных веществ. Вследствие этого в ядерно-химическом синтезе используется дважды меченный по тритию прекурсор, который одновременно позволяет получать фенил-катионы, а также меченные по тритию соединения. Идентификация проводилась на основании сравнения хроматографического поведения N-фенилдиазиниевых соединений и изоморфных носителей - аналогичных солей азинов (соответствие пиков активных и неактивных соединений).
Пример 2
Синтез борфторида N-фенилхиноксалиния, меченного тритием
Синтез осуществлялся аналогичным образом, как и в примере 1. В ампулу было внесено 7,2 мг хиноксалина. Выход борфторида N-фенилхиноксалиния, меченного тритием, составляет 6,0±0,5%.
Пример 3
Синтез борфторида N-фенилпиразиния, меченного тритием
Синтез осуществлялся аналогичным образом, как и в примере 1. В ампулу было внесено 4,4 мг пиразина. Выход борфторида N-фенилпиразиния, меченного тритием, составляет 4,0±0,5%.
Способ получения неизвестных меченных тритием кватернизированных структур диазинового ряда, а именно N-фенилдиазиниевых солей, ядерно-химическим методом по реакции: отличающийся тем, что 1,4-диазины (пиразин, хиноксалин и 2,3-диметилхиноксалин) подвергают ион-молекулярным реакциям со свободными нуклеогенными фенилкатионами, которые генерируются при бета-распаде трития в составе двукратно меченого бензола в замкнутой системе в присутствии стабилизирующей соли - тетрафторбората калия.