Мазь с витамином а, восстанавливающая кожу и препятствующая ее избыточному ороговению
Иллюстрации
Показать всеИзобретение относится к области фармацевтики и касается мазевой композиции для уменьшения ороговения эпидермиса, смягчения кожи и стимуляции ее регенерации, содержащей ретинола пальмитат, в качестве стабилизатора - α-токоферол, а также воск эмульсионный, масло вазелиновое, глицерин, спирт этиловый и воду. Композиция обладает высокой эффективностью и стабильностью. 2 ил., 4 табл., 4 пр.
Реферат
Изобретение относится к фармации и касается создания мазевой композиции для местного применения, содержащей ретиноид - ретинола пальмитат, обладающий фармакологическими эффектами в отношении пролиферации и дифференцировки кератиноцитов, предназначенной для смягчения кожи и усиления ее регенерации, а также для применения в комплексной терапии кожных заболеваний.
Биологически активные формы витамина А являются естественными регуляторами морфогенетических процессов в эпидермисе [1]. В дерматологической практике нередко возникает необходимость воздействовать на патогенетические звенья болезней кожи путем модифицирования пролиферации и дифференцировки клеточных элементов эпидермиса и дермы. В последние десятилетия с этой целью широко используются синтетические аналоги витамина А - ретиноиды, одним из которых является ретинола пальмитат (РП) [2].
Установлено, что РП через экспрессию генов дозозависимо усиливает, а при нарастании дозы вводимого витамина А ингибирует пролиферацию кератиноцитов. Известно его тормозящее влияние на терминальную дифференцировку эпителиальных клеток кожи, что способствует омоложению их популяции в эпидермисе. Также РП активизирует синтез гликозаминогликанов в соединительнотканном слое кожи, стимулирует иммунные процессы.
Известен препарат Видестим®, представляющий собой мазь для накожного применения, содержащую 0,5% РП на эмульсионной основе, стабилизаторы и антиоксиданты [3]. Его фармакологическая активность в виде воздействия на регенераторные процессы в коже доказана в экспериментах на животных [4] и подтверждена в клинической практике [5, 6, 7]. Препарат эффективен в терапии экземы, дерматитов, хейлита, поверхностных трещин и ссадин кожи, заболеваний кожи, связанных с нарушениями ее кератинизации, применяется для активации репаративных процессов при различных дерматозах после терапии глюкокортикостероидами. Он разрешен к применению кормящими матерями для устранения трещин сосков [8].
В патентной литературе есть сообщения о мягких лекарственных формах для накожного применения, содержащих РП. Так, патент RU 2115409 защищает косметическое средство по уходу за кожей лица и тела, в состав которого входят РП (витамин А), токоферола ацетат (витамин Е), структурообразователи, пластифицирующие добавки, консерванты, отдушка [9]. Мазевая композиция, описываемая в патенте RU 2146921, состоит из РП, аскорбилпальмитата, токоферола ацетата, эргокальциферола и водно-эмульсионной основы [10]. Названные композиции являются поливитаминными; витамины, входящие в их состав в качестве активных субстанций, и прежде всего ретиноид - РП, подвержены окислению, однако в перечне вспомогательных веществ, использованных в композициях, стабилизаторы с антиоксидантными свойствами отсутствуют.
Наиболее близким по назначению, составу и технической сущности к заявляемому изобретению является патент RU 2036640, описывающий состав мазевой композиции с РП, стабилизированной смесью антиоксидантов и содержащей эмульгатор №1 [11]. Известно, что для предотвращения окисления ретиноидов, и в том числе РП, как правило, используются антиоксиданты - бутилгидрокситолуол (БОТ) и бутилгидроксианизол (БОА) [12, 13]. Эти соединения применяются в фармации и пищевой промышленности, однако установлено, что им присущи и некоторые нежелательные эффекты, например, потенциальные канцерогенные свойства, способность повышать уровень холестерина [14, 15], вызывать заболевания желудочно-кишечного тракта, печени, аллергические реакции [16], оказывать раздражающее действие на кожу, глаза и слизистые оболочки [17]. Входящий в состав композиции эмульгатор №1 представляет собой жирную на ощупь твердую массу в виде плиток массой 10-15 кг; работа с ним требует введения в производственный процесс стадии «Измельчение», сопряженной с производственными потерями и использованием дорогостоящего оборудования.
Таким образом, в целях обеспечения качества и улучшения профиля безопасности лекарственных препаратов разработка современных нетоксичных лекарственных средств для наружного применения является актуальной.
Задачей настоящего изобретения является разработка мази, смягчающей и восстанавливающей кожу, предотвращающей ее избыточное ороговение и обладающей улучшенным профилем безопасности.
В соответствии с изобретением описывается мазевая композиция для наружного применения, стимулирующая в коже процессы регенерации и препятствующая избыточному ороговению и сухости кожи, содержащая в качестве активного вещества ретинола пальмитат, а в качестве вспомогательных веществ α-токоферол, эмульсионный воск, вазелиновое масло, глицерин, спирт этиловый и воду при следующем соотношении компонентов, мас.%:
| Ретинола пальмитат | 0,3-0,7 |
| α-токоферол | 0,15-0,25 |
| Воск эмульсионный | 5,0-15,0 |
| Масло вазелиновое | 5,0-15,0 |
| Глицерин | 5,0-15,0 |
| Этанол 95% | 5,0-15,0 |
| Вода дистиллированная | до 100,0 |
α-токоферол (синтетический аналог природного α-токоферола) представляет собой нетоксичное соединение; в качестве стабилизатора он находит широкое применение в фармацевтике и пищевой промышленности. Использование α-токоферола в качестве вспомогательного вещества с целью предотвращения окисления ретиноида в лекарственных средствах позволяет избежать применения таких компонентов, как БОТ и БОА при сохранении высоких фармакологических и потребительских свойств препарата.
Эмульсионный воск в отличие от эмульгатора №1 представляет собой однородную массу в виде чешуек, легко взвешивается, смешивается с вазелиновым маслом, быстро и равномерно плавится, при его использовании нет потерь. Эмульсионный воск, полученный сплавлением синтетических первичных жирных спиртов с калиевыми солями эфиров фосфорной кислоты, благодаря наличию фосфорных группировок в молекулах высших жирных кислот близок по строению к лецитину и кефалину, входящим в состав кожного жира. Вследствие этого он оказывает на кожу эффективное смягчающее действие, предотвращает потерю ею влаги, не оставляет ощущения жирности [18]. рН эмульсии, полученной с применением эмульсионного воска, близок к естественному значению этого показателя у здоровой кожи.
Эксперимент 1
В заявляемый состав мазевой композиции α-токоферол введен с целью стабилизации ретиноида, и поэтому на первом этапе лабораторных исследований стабильность РП была изучена на примере модельных смесей.
Цель: изучить устойчивость субстанции РП, стабилизированной α-токоферолом.
Объект исследования составили модельные смеси - субстанция РП в вазелиновом масле без антиоксиданта (1) - контроль - и аналогичная комбинация, отличающаяся наличием в ней α-токоферола (2). Начальная концентрация РП в модельных смесях равнялась 1%, концентрация α-токоферола - 0,05%. Образцы были заложены на «ускоренное старение» в стеклянных банках с широким горлом при свободном доступе воздуха в условиях повышенной температуры (40°C).
Метод: спектрофотометрия по отношению к раствору стандартного образца.
Результаты анализа количественного содержания РП в модельных смесях, хранившихся при 40°C, представлены в таблице 1.
| Таблица 1 | |||
| Результаты количественного определения ретинола пальмитата в модельных смесях, хранившихся при 40°C | |||
| № | Срок хранения, сут | Количественное содержание ретинола пальмитата в модельных смесях, % | |
| без α-токоферола (1) | с α-токоферолом (2) | ||
| 1 | 1 | 0,99 | 1,01 |
| 2 | 7 | 0,98 | 0,95 |
| 3 | 22 | 0,98 | 0,99 |
| 4 | 29 | 0,79 | 0,98 |
| 5 | 36 | 0,49 | 0,95 |
| 6 | 42 | 0,14 | 0,90 |
| 7 | 83 | - | 0,15 |
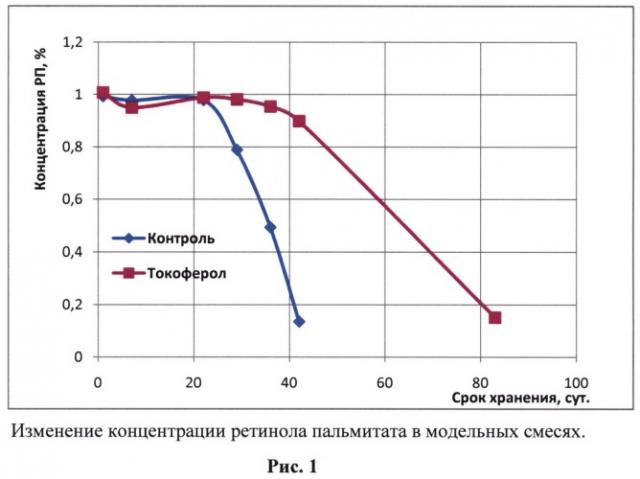
Из этих данных следует, что содержание РП в образцах обеих модельных смесей до 22-го дня наблюдения оставалось практически на одном уровне. В дальнейшем концентрация субстанции в контрольном образце, т.е. в модельной смеси без антиоксиданта (1) стала снижаться. Анализ, проведенный в последующие дни, зафиксировал лавинообразное падение концентрации ретиноида в контрольных образцах (рис.1). В модельной смеси с антиоксидантом (2) концентрация ретиноида сохранялась на первоначальном уровне до 36-го дня наблюдения, и только впоследствии было отмечено ее снижение (см. табл.1, рис.1).
Полученный результат показывает, что присутствие в модельной смеси даже незначительного количества α-токоферола (0,05%) почти в два раза продлевает исходную устойчивость РП, что свидетельствует о наличии у α-токоферола в исследованных условиях выраженного антиокислительного эффекта и, в связи с этим, о перспективности его введения в состав лекарственных средств с целью стабилизации ретиноидов.
Эксперимент 2
Цель: установить эффективную концентрацию α-токоферола, способную затормозить окисление РП на длительный срок.
Объект исследования составили модельные смеси - субстанция РП в вазелиновом масле без антиоксиданта (1) и аналогичные комбинации (2-7), отличающиеся тем, что в них был добавлен α-токоферол в различных концентрациях (табл.2). Начальная концентрация ретиноида в модельных смесях равнялась 1%, α-токоферола - 0,02-0,25%. Образцы были заложены на хранение в стеклянных банках с широким горлом при свободном доступе воздуха при более жестких, чем в 1-м эксперименте, условиях «ускоренного старения» (50°C).
Метод: спектрофотометрия по отношению к стандартному образцу.
| Таблица 2 | |||
| Состав модельных смесей с ретинола пальмитатом, стабилизированным α-токоферолом | |||
| № модельной смеси | Вазелиновое масло, % | Ретинола пальмитат, % | α-токоферол, % |
| 1 | 99,00 | 1,0 | 0 |
| 2 | 98,98 | 1,0 | 0,02 |
| 3 | 98,95 | 1,0 | 0,05 |
| 4 | 98,89 | 1,0 | 0,11 |
| 5 | 98,87 | 1,0 | 0,13 |
| 6 | 98,81 | 1,0 | 0,19 |
| 7 | 98,75 | 1,0 | 0,25 |
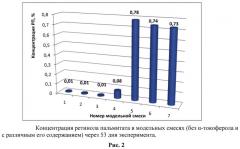
Результаты количественного определения РП в модельных смесях через 53 дня хранения при температуре 50°C представлены на рис.2.
На диаграмме видно, что разные количества α-токоферола в модельных смесях оказывают неравнозначное влияние на устойчивость РП. Добавление антиоксиданта в диапазоне концентраций от 0,02 до 0,05% при хранении в течение 53 суток при 50°C в условиях доступа воздуха оказалось неэффективным. В количестве 0,11% α-токоферол стабилизировал ретиноид, но не в желаемой степени. Наиболее высокие показатели устойчивости РП в исследованных условиях наблюдались при концентрациях α-токоферола в модельных смесях от 0,13 до 0,25% включительно. Т.е. чем больше в смеси антиоксиданта, тем сильнее (до достижения определенной концентрации) проявляется его свойство препятствовать окислению/разрушению фармацевтической субстанции (РП)
Таким образом, экспериментальные исследования стабильности РП при его хранении в условиях ускоренного старения в составе модельных смесей, содержащих α-токоферол, продемонстрировали эффективность выбранного подхода к стабилизации ретиноида, т.е. замены в составе лекарственного препарата смеси антиоксидантов фенольного типа (БОТ и БОА) на синтетический аналог природного витамина Е, и позволили перейти к изучению стабильности РП в составе мазевой композиции заявляемого состава.
Эксперимент 3
Цель: установить продолжительность стабильности РП в качестве фармацевтической субстанции в составе мазевых композиций, содержащих α-токоферол.
Объект исследования составили образцы мазевых композиций, различающихся по содержанию РП и α-токоферола.
Метод: высокоэффективная жидкостная хроматография.
Технология приготовления мази
1. Необходимое количество воды помещают в реактор 1 и нагревают до 75-80°C.
2. Параллельно в реактор 2 помещают необходимые количества вазелинового масла и эмульсионного воска. Смесь разогревают до температуры 75-80 С, расплавляя компоненты.
3. В расплавленную смесь, находящуюся в реакторе 2, отвешивают расчетные количества РП и α-токоферола. Смесь тщательно перемешивают с помощью погружного гомогенизатора.
4. В реактор 1 (см. п.1) опускают головку гомогенизатора, включают его (8-10 тыс. об/мин) и при активном перемешивании смеси в нее медленно, тонкой струйкой добавляют расплав лекарственного и вспомогательных веществ мази из реактора 2.
5. Через 2-5 минут [в зависимости от объема использованного реактора (0,5-3,0 л)] после смешивания всех компонентов препарата мазь гомогенизируют.
6. Спустя 2-5 минут в реактор добавляют смесь этанола (этилового спирта) и глицерола (глицерина), после чего мазь дополнительно гомогенизируют в течение 2 минут. В связи с тем что мазь содержит термолабильные компоненты (РП и α-токоферол), разрушение которых усиливается при высоких температурах, ее принудительно охлаждают.
7. После снижения температуры мази до 35-40°C ее передают на участок фасовки в тубы.
8. Мазь фасуют в алюминиевые тубы, маркируют этикетками и хранят при температуре от 2 до 8°C.
Примеры приготовления конкретных композиций
Пример 4
1. В реактор 1 с эффективной загрузкой в 100 кг мази отмеривают 65,3 л очищенной воды, включают двигатель рамной мешалки и нагревают воду до температуры 75-80ºС.
2. В реактор 2 отвешивают 8 кг эмульсионного воска, 6 кг вазелинового масла, включают двигатель рамной мешалки и, нагревая смесь до температуры 75-80°C, расплавляют ее.
3. После расплавления жировых компонентов в реактор 2 отвешивают 0,5 кг РП и 0,2 кг α-токоферола и тщательно перемешивают.
4. Объединение компонентов мази, находящихся в реакторе 1 и реакторе 2, осуществляют при активном перемешивании с помощью встроенного в систему реакторов роторно-пульсационного аппарата проточного типа.
5. Смешивание содержимого двух реакторов продолжают в течение 20 минут до получения однородной эмульсии, в которую постепенно добавляют смесь 10 кг этилового спирта и 10 кг глицерина.
6. Полученную композицию окончательно гомогенизируют в течение 15 минут, охлаждают до температуры 30-35°C и фасуют в алюминиевые тубы.
Аналогично (по такой же схеме) получены другие мази (примеры 1, 2, 3, 5 в табл.3 и 6, 7 в табл.4).
Результаты
На первом этапе антиоксидантную активность разных концентраций α-токоферола исследовали на примере мазевых композиций, содержание РП в которых составляло 0,5%, т.е. среднее из заявляемых значений. Контролем служила мазевая композиция без стабилизатора (табл.3).
Исследование показало, что в контрольных образцах (пример 1) и при использовании 0,1%-ной концентрации α-токоферола (пример 2) содержание РП в мазевых композициях не выдерживает необходимого срока хранения (2 года). Увеличение концентрации антиоксиданта до 0,15% (пример 3) и выше (примеры 4, 5) позволило достигнуть необходимого эффекта: содержание РП в этих экспериментальных мазевых композициях соответствовало желаемому на протяжении срока, соответствующего 3 годам хранения в условиях, указываемых в проекте НД для таких мазей (2-8°C).
| Таблица 3 | ||||||
| Концентрация ретинола пальмитата в мазевых композициях, стабилизированных α-токоферолом, при определении срока годности по методике «ускоренного старения» при температуре 40°C | ||||||
| Срок экспериментального хранения, сут | Срок годности, годы | Содержание ретинола пальмитата в мазях, % | ||||
| Пример 1 | Пример 2 | Пример 3 | Пример 4 | Пример 5 | ||
| без α-токоферола | 0,1% α-токоферола | 0,15% α-токоферола | 0,2% α-токоферола | 0,25% α-токоферола | ||
| После изготовления | 0,51 | 0,51 | 0,50 | 0,50 | 0,52 | |
| 46 | 1 | 0,49 | 0,52 | 0,50 | 0,51 | 0,50 |
| 69 | 1,5 | 0,48 | 0,51 | 0,51 | 0,50 | 0,51 |
| 92 | 2 | 0,45 | 0,48 | 0,50 | 0,51 | 0,52 |
| 138 | 3 | 0,40 | 0,45 | 0,49 | 0,51 | 0,50 |
Примечание: показатели качества по НД от 0,45% до 0,55%.
На втором этапе антиоксидантную активность минимальной из оптимально эффективных концентраций α-токоферола (0,15%), установленной для мази с 0,5%-ным содержанием РП, изучали на примере мазевых композиций, содержание РП в которых составляло 0,3%, 0,5% и 0,7%, что отражает весь диапазон заявленных концентраций ретиноида (табл.4).
| Таблица 4 | ||||
| Концентрация ретинола пальмитата в мазевых композициях с 0,3%, 0,5% и 0,7%-ным содержанием ретинола пальмитата, стабилизированных 0,15% α-токоферола, при определении срока их годности по методике «ускоренного старения» при температуре 40°C | ||||
| Срок экспериментального хранения, сут | Срок годности, годы | Содержание ретинола пальмитата в мазях, % | ||
| Пример 6 | Пример 3 | Пример 7 | ||
| 0,3% РП | 0,5% РП | 0,7% РП | ||
| После изготовления | 0,31 | 0,52 | 0,71 | |
| 46 | 1 | 0,31 | 0,52 | 0,71 |
| 69 | 1,5 | 0,30 | 0,51 | 0,70 |
| 92 | 2 | 0,31 | 0,51 | 0,68 |
| 115 | 2,5 | 0,30 | 0,51 | 0,67 |
| 138 | 3 | 0,31 | 0,50 | 0,67 |
| Примечание: показатели качества по НД от 0,27% до 0,33%, от 0,45% до 0,55% и от 0,63 до 0,77% соответственно. |
Исследование показало, что минимальная из оптимально эффективных для мази с 0,5% РП концентрация α-токоферола проявляет желаемый стабилизирующий эффект в отношении мазевых композиций, содержащих РП в пределах заявленного диапазона концентраций, и обеспечивает их стабильность в течение срока хранения, предусмотренного в проекте НД.
Литература
1. Афанасьев Ю.И., Ноздрин В.И., Михайлов О.И. и др. Витамин А - регулирующий фактор процессов гистогенеза // Успехи совр. Биол. - 1990. - т. 6, №3. - С.410-418.
2. Гузев К.С., Ноздрин В.И. Новые отечественные лекарственные средства с ретиноидами - М.: ФНПП "Ретиноиды", 2003. - 112 с.
3. Альманах "Ретиноиды". - М.: ФНПП "Ретиноиды", 2000. - Вып.8. - С.3-10.
4. Ноздрин В.И., Яцковский А.Н., Гузев К.С. и др. Экспериментальное исследование специфической фармакологической активности мази Видестим // Альманах "Ретиноиды". - М.: ФНПП "Ретиноиды", 2000. - Вып.8. - С.11-16.
5. Иванов О.Л., Самгин М.А., Паничкина Г.С. Изучение эффективности и переносимости препарата Видестим (мазь с ретинола пальмитатом 0,5%) // Альманах "Ретиноиды". - М.: ФНПП "Ретиноиды", 2000. - Вып.8. - С.38-41.
6. Кубанова А.А., Федоров С.М., Тимошин Г.Г. Клиническое изучение мази Видестим (мазь с ретинола пальмитатом 0,5%) // Альманах "Ретиноиды". - М.: ФНПП "Ретиноиды", 2000. - Вып.8. - С.42-44.
7. Перламутров Ю.Н. Клиническое изучение мази Видестим, содержащей 0,5% ретинола пальмитата // Альманах "Ретиноиды". - М.: ФНПП "Ретиноиды", 2000. - Вып.8. - С.46-48.
8. Альбанова В.И., Пальчик Е.А. Применение мази Видестим® в периоде кормления грудью // Альманах "Ретиноиды". - М.: ФНПП "Ретиноиды", 2006. - Вып.23. - С.41-43.
9. Патент RU 2115409. - Опубл. 20.07.1998.
10. Патент RU 2146921. - Опубл. 27.03.2000.
11. Патент RU 2036640. - Опубл. 10.06.1995.
12. Архапчев Ю.П. Способ определения бутилоксианизола и бутилокситолуола в мази с ретинола пальмитатом методом ВЭЖХ // Фармацевтическая наука в решении вопросов лекарственного обеспечения. М., 1998. - Научные труды. - Т. XXXVII. - С.86-89.
13. Гузев К.С. Теоретическое обоснование и экспериментальное исследование лекарственных форм, содержащих 13-цис-ретиноевую кислоту и ретинола пальмитат: Автореф. дис. докт. фармацевт, наук. - М., 1997. - 50 с.
14. Inai К., Kobuke Т., Nambu S. et al. Hepatocellular tumorigenicity of butilated hydroxytoluene administered orally to B6C3Fi mice // Jpn. J. Cancer Res. (Gann). - 1988. - Vol.79. - P. 49-58.
15. Kahl R., Kappus H. Toxicology of the synthetic antioxidants BHA and BHT in comparison with the natural antioxidant vitamin E // Z. fur Lebensmittel-Untersuchung und-Forchung. - 1993. - Bd. 196, N 4. - S. 329-338.
16. Серов Ю.А. Опасные пищевые Е-добавки. Информационно-справочное пособие. - М., 2006. - 42 с.
17. Решение Комиссии Таможенного союза от 19 мая 2011 г. №646. О проекте Требований к маркировке лекарственных средств. - г. Минск.
18. Войцеховская А.Л., Вольфензон И.И. Химия для Вас. Косметика сегодня. - М.: Химия, 1988. - С.141.
Мазевая композиция для местного применения, уменьшающая ороговение эпидермиса, смягчающая кожу и стимулирующая в ней регенераторные процессы, на основе ретиноида, содержащая ретинола пальмитат, α-токоферол, воск эмульсионный, масло вазелиновое, глицерин, этанол и воду при следующем соотношении компонентов, мас.%:
| Ретинола пальмитат | 0,3-0,7 |
| α-токоферол | 0,15-0,25 |
| Воск эмульсионный | 5,0-15,0 |
| Масло вазелиновое | 5,0-15,0 |
| Глицерин | 5,0-15,0 |
| Этанол 95% | 5,0-15,0 |
| Вода дистиллированная | до 100,0 |