Новые бензолсульфонамидные соединения, способ их получения и применение в терапии и косметике
Иллюстрации
Показать всеИзобретение относится к новым бензолсульфонамидным соединениям, где соединения выбраны из группы следующих соединений, включая аддитивные соли с фармацевтически приемлемой кислотой, аддитивные соли с фармацевтически приемлемым основанием и энантиомеры этих соединений: 1) 3-[(4-бут-2-инилоксибензолсульфонил)-метиламино]-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид, 2) (S)-3-(4-бут-2-инилоксибензолсульфониламино)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид, 3) (S)-3-(4-бензилоксибензолсульфониламино)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид, 4) (S)-3-[(4-бензилоксибензолсульфонил)-метиламино]-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид, 5) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид, 6) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(нафталин-1-илметокси)-бензолсульфониламино]-пропионамид, 7) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-(4-пропоксибензолсульфониламино)-пропионамид, 8) (S)-3-[4-(3-цианобензилокси)-бензолсульфониламино]-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид, 9) (S)-3-[4-(4-цианобензилокси)-бензолсульфониламино]-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид, 10) бензил-4-{(S)-1-гидроксикарбамоил-2-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-этил}-пиперазин-1-карбоксилат, 11) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(2-фенилпиперидин-4-илметокси)-бензолсульфониламино]-пропионамид, 12) (R)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид, 13) (S)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-2-пиперазин-1-илпропионамид, 14) гидрохлорид (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид, 15) дифторацетат трет-бутил-3-{4-[(S)-2-гидроксикарбамоил-2-(4-метансульфонилпиперазин-1-ил)-этилсульфамоил]-феноксиметил}-2-метилиндол-1-карбоксилат, 16) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(хинолин-4-илметокси)-бензолсульфониламино]-пропионамид, 17) (S)-2-(4-бензилпиперазин-1-ил)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид, 18) (S)-2-[4-(4-фторбензил)-пиперазин-1-ил]-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид, 19) (S)-2-(4-этилпиперазин-1-ил)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид, 20) (S)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-2-[4-(4-трифторметилбензил)-пиперазин-1-ил]-пропионамид, 21) (S)-N-гидрокси-2-[4-(4-метилбензил)-пиперазин-1-ил]-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид, 22) (S)-3-[4-(бензоизоксазол-3-илметокси)-бензолсульфониламино]-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид, 23) (S)-N-гидрокси-2-(4-изобутирилпиперазин-1-ил)-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид, 24) (S)-N-гидрокси-2-[4-(2-метилпропан-1-сульфонил)-пиперазин-1-ил]-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид, 25) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(2-трифторметилпиразоло[1,5-a]пиридин-3-илметокси)-бензолсульфониламино]-пропионамид, 26) (S)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-2-[4-(пропан-2-сульфонил)-пиперазин-1-ил]-пропионамид, и 27) (S)-2-(4-бензилпиперазин-1-ил)-N-гидрокси-3-[4-(2-трифторметилпиразоло[1,5-a]пиридин-3-илметокси)-бензолсульфониламино]-пропионамид. Изобретение также относится к фармацевтической и косметической композициям на основе указанных соединений, обладающих активностью в отношении TNFα-конвертирующего фермента (ТАСЕ). Технический результат: получены новые соединения и композиции на их основе, которые могут найти применение в медицине и ветеринарии для лечения ревматоидного артрита, сахарного инсулиннезависимого диабета, болезни Крона или воспалительного заболевания кожи. 15 н. и 20 з.п. ф-лы, 28 пр.
Реферат
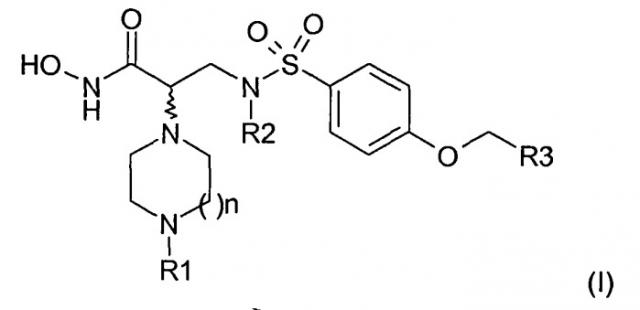
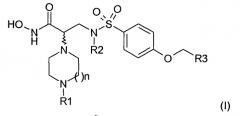
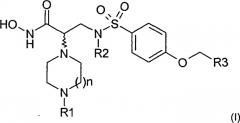
Настоящее изобретение относится к новым бензолсульфонамидным соединениям, отвечающим следующей общей формуле (I):
а также к способу их получения и использования в фармацевтических композициях, предназначенных для применения в медицине или ветеринарии.
Соединения согласно изобретению действуют как ингибиторы THFα-конвертирующего фермента, обозначаемого также ТАСЕ. В этой связи они полезны для лечения заболеваний, при которых снижение продуцирования THFα представляет большой интерес.
Настоящее изобретение относится также к применению соединений, отвечающих общей формуле (I), в косметических композициях.
УРОВЕНЬ ТЕХНИКИ
Адамализины («ADAM» или A Disintegrin and Metalloproteinase (дезинтегрин и металлопротеиназа)) составляют семейство цинксодержащих металлоэндопептидазных ферментов. Их эктодомен содержит протеазный домен, активность которого зависит от цинка, дезинтегриновый домен и домен, обогащенный цистеинами. На сегодняшний день идентифицировано не менее 30 различных ADAMов, из которых первым был описан ADAM17, обозначаемый также ТАСЕ (THFα-конвертирующий фермент) [Gueydan С et al. Med. Sci 1997, 13, 83-88; Black R.A. et al. Nature 1997, 385:729-733; Moss et al. Nature 1997, 385:733-736]. мРНК ТАСЕ находится во многих тканях, в частности, на уровне моноцитов, макрофагов, лимфоцитов Т, а также на уровне, например, кератиноцитов.
ТАСЕ ответственен за отщепление про-THFα, мембранного белка 26 Да, приводящего к высвобождению растворимой формы THFα, биологически активного белка 17 кДа [Schlondorff et al. Biochem. J. 2000, 347, 131-138]. Высвободившийся из клетки растворимый THFα способен воздействовать на сайты, очень удаленные от сайта, ответственного за синтез.
THFα вовлечен в многочисленные биологические провоспалительные процессы [Aggarwal et al., Eur. Cynokine Netw., 1996, 7: 93-124]. Многие фармакологические и клинические исследования со всей очевидностью показали, что блокирование эффектов THFα специфическими или биологическими антителами против THFα (Этанерцепт, Адалимумаб, Инфликсимаб) дает хороший результат при лечении аутоиммунных заболеваний, таких как ревматоидный артрит [Feldman et al. Lancet, 1994, 344, 1105), сахарный инсулиннезависимый диабет [Lohmander L.S. et al. Arthritis Rheum, 1993, 36, 1214-1222], болезнь Крона [MacDonald et al. Clin. Exp. Immunol. 1990, 81, 301].
THFα играет также ведущую роль в течении воспалительного процесса, развивающегося в местах поражения псориазом. У больных псориазом наблюдается высокое содержание THFα в сыворотке крови [Mussi A et а1. J. Biol. Regul. Homeost Agents, 1997, 11, 115-118]; высокое содержание THFα наблюдается также в самих псориатических бляшках [Bonifati С. et al. Clin. Exp. Dermatol., 1994, 19, 383-387]. Ключевыми клетками в физиопатологии псориаза являются кератиноцы, дендритные клетки и некоторые лимфоциты Т. Взаимодействие между этими группами клеток приводит к каскаду воспалительных реакций, приводящих к характерным поражениям при псориазе с высвобождением THFα [Kupper TS, N. Engl. J. Med, 2003, 349, 1987-1990]. Клинические исследования при лечении от умеренной до тяжелой форм бляшковидного псориаза с помощью биологических анти-THFα препаратов (Etanecept, Adalimumab, Infliximab) доказали их эффективность как в отношении псориатических поражений, так и в отношении качества жизни пациентов [Ortonne JP, Annales de dermatologie et de venereologie, 2005, 132 (8-9, часть 2), 4S6-9 и 2005, 132, 9S01-9S70].
Таким образом, соединения, которые ингибируют продуцирование THFα, представляют большой интерес для лечения воспалительных заболеваний и болезней, связанных с высвобождением THFα.
Описание изобретения
Настоящее изобретение описывает новые соединения, которые ингибируют фермент ТАСЕ (THFα-конвертирующий фермент) и, следовательно, ингибируют секрецию клетками растворимой формы THFα (активная форма THFα). Следовательно, эти новые соединения представляют собой потенциальные действующие начала для лечения патологий, вызывая уменьшение или ингибирование продуцирования THFα.
В качестве примеров, но не ограничиваясь ими, такими патологиями являются, например, септический шок, гемодинамический шок, малярия, воспалительные заболевания кишечника (IBD), такие как болезнь Крона и язвенные колиты, воспалительные заболевания костей, микобактерийные инфекции, менингит, фибротические заболевания, сердечные заболевания, ишемический инсульт, отторжение трансплантата, рак, атеросклероз, ожирение, заболевания, в которых задействованы явления ангиогенеза, аутоиммунные заболевания, остеоартрит, ревматоидный артрит, анкилозирующий спондилоартрит, ювенильный хронический артрит, рассеянный склероз, ВИЧ, сахарный инсулиннезависимый диабет, аллергические заболевания, астма, хроническое обструктивное заболевание легких (COPD), воспаление глаз, воспалительные заболевания кожи, псориаз, атопический дерматит и псориатический ревматизм.
Эти соединения представляют собой также потенциальные действующие начала для лечения неврологических патологий с явлениями воспалительного характера, при которых наибольший интерес представляло бы снижение продуцирования THFα. Таким патологиями, перечисленными ниже, но не ограничивающимися ими, являются, например, болезнь Альцгеймера, болезнь Паркинсона, паркинсонизм, боковой амиотрофический склероз, аутоиммунные заболевания нервной системы, заболевания автономной нервной системы, боли в спине, отек мозга, цереброваскулярные нарушения, деменция, аутоиммунные заболевания, обусловленные демиелинизацией нервных волокон нервной системы, диабетические нейропатии, энцефалит, энцефаломиелит, эпилепсия, синдром хронической усталости, артериит гигантоклеточный, синдром Гийена-Барре, головные боли, рассеянный склероз, невралгия, заболевания периферической нервной системы, полинейропатии, полирадикулонейропатия, радикулопатия, паралич дыхательных мышц, болезни позвоночного столба, синдром Туретта, васкулит центральной нервной системы, болезнь Хантингтона и геморрагический инсульт.
Уже известно большое количество разнообразных ингибиторов ТАСЕ, как будет показано ниже. Однако среди этого множества ингибиторов нет ни одного, который действовал бы избирательно на фермент ТАСЕ относительно других ферментов из семейства ADAM и/или металлопротеиназного матрикса (ММР).
Кроме того, неселективное ингибирование представителей этого семейства ферментов приводит к вторичным нежелательным эффектам, наблюдаемым in vivo. Например, ингибирование ММР-1 (коллагеназы-1) ассоциируется с проблемами токсикации мышечно-скелетной ткани.
В качестве неселективного ингибитора можно назвать также Апратастат, известный ингибитор, который прошел химическое тестирование в фазе 2, для лечения ревматоидного артрита (Curr Opin Investig Drugs. 2006 Nov; 7(11), 1014-1019). Этот ингибитор не показал себя селективным к ферменту ТАСЕ относительно некоторых ММР ферментов (WO 00/44709; стр.251, таблица 10, пример 61).
Другие известные ингибиторы ТАСЕ, относящиеся к тому же семейству, что и Апратастат, а именно, к семейству производных циклических бензолсульфонамидов, описаны в WO 00/44709 и WO 97/18194. Другие патенты (WO 96/00214, WO 97/22587) защищают ингибиторы ММР и/или ТАСЕ, у которых бензолсульфонамидная часть отделена от гидроксаминовой кислотной функции только одним атомом углерода. Публикациями, описывающими этот тип ингибиторов ММР более глубоко, являются публикации MacPherson et al. J. Med. Chem. 1997, 40, 2525 и публикация Tamura et al. J. Med. Chem. 1998, 41, 640. Другие примеры ингибиторов ММР/ТАСЕ, у которых сульфонамидная функция отделена от гидроксаминовой кислоты последовательностью двух атомов углерода, образующей цикл, описаны в патентах WO 98/16503, WO 98/16506, WO 98/16514 и WO 98/16520. Другие примеры ингибиторов ММР, у которых сульфонамидная функция отделена от гидроксаминовой кислоты последовательностью двух атомов углерода, образующей цикл, описаны также в патенте WO 2008/045671.
В настоящее время неожиданным и непредсказуемым образом заявителем были обнаружены новые соединения общей формулы (I), которые обладают очень хорошей ингибирующей активностью в отношении ТАСЕ и, в частности, они селективно ингибируют фермент ТАСЕ относительно других ферментов ADAM и ММР.
Таким образом, настоящее изобретение относится к соединениям следующей общей формулы (I):
в которой:
R1 означает водород, алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, аралкил, замещенный аралкил, гетероаралкил, замещенный гетероаралкил, C(O)-R4, -SO2-R4, C(O)OR4, где R4 имеет значения, указанные ниже;
R2 представляет собой водород или низший алкил;
R3 представляет собой алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, арил, замещенный арил, аралкил, замещенный аралкил, гетероциклический радикал, замещенный гетероциклический радикал, циклоалкил, замещенный циклоалкил, гетероарил, замещенный гетероарил, гетероаралкил, замещенный гетероаралкил;
R4 представляет собой алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, арил, замещенный арил, аралкил, замещенный аралкил;
n может принимать значения 0, 1, 2 или 3;
а также к аддитивным солям соединений общей формулы (I) с фармацевтически приемлемой кислотой, аддитивным солям соединений общей формулы (I) с фармацевтически приемлемым основанием и к энантиомерам соединений общей формулы (I).
Среди аддитивных солей соединений общей формулы (I) с фармацевтически приемлемой кислотой можно предпочтительно назвать соли с органической или неорганической кислотой.
Походящими неорганическими кислотами являются, например, соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота и фосфорная кислота.
Подходящими органическими кислотами являются, например, уксусная кислота, трифторуксусная кислота, трихлоруксусная кислота, пропионовая кислота, гликолевая кислота, пирувиновая кислота, сукциновая кислота, бензойная кислота, циннаминовая кислота, манделовая кислота, метансульфоновая кислота, пара-толуолсульфоновая кислота, салициловая кислота, пикриновая кислота, лимонная кислота, оксалиновая кислота, винная кислота, малоновая кислота, малеиновая кислота, камфорсульфоновая кислота и фумаровая кислота.
Среди аддитивных солей соединений общей формулы (I) с фармацевтически приемлемым основанием можно назвать, предпочтительно, соли с органическим или неорганическим основанием.
Неорганическими основаниями являются, например, гидроксид калия, гидроксид натрия, гидроксид лития или гидроксид кальция.
Подходящие органические основания включают в себя амины и аминокислоты. Среди аминов можно назвать, например, первичные, вторичные или третичные алифатические или ароматические амины, такие как метиламин, этиламин, этаноламин, пропиламин, изопропиламин, 4 изомера бутиламина, диметиламин, диэтиламин, диэтаноламин, дипропиламин, диизопропиламин, ди-н-бутиламин, пирролидин, пиперидин, морфолин, диэтанолфениламин, триметиламин, триэтиламин, трипропиламин, хинуклидин, пиридин, хинолин или изохинолин.
Среди аминокислот можно назвать, например, лизин, аргинин и орнитин.
Согласно настоящему изобретению под низшим алкилом понимают насыщенную углеводородную цепь, линейную или разветвленную, содержащую 1-4 атома углерода.
Согласно настоящему изобретению под алкилом понимают насыщенную углеводородную цепь, линейную или разветвленную, содержащую 1-10 атомов углерода.
Согласно настоящему изобретению под алкенилом понимают ненасыщенную углеводородную цепь, линейную или разветвленную, содержащую 2-10 атомов углерода и содержащую одну или несколько двойных связей.
Согласно настоящему изобретению под алкинилом понимают ненасыщенную углеводородную цепь, линейную или разветвленную, содержащую 2-10 атомов углерода и содержащую одну или несколько тройных связей.
Согласно настоящему изобретению под замещенным алкилом понимают насыщенную углеводородную цепь, линейную или разветвленную, содержащую 1-10 атомов углерода и замещенную одним или несколькими радикалами, выбранными из атома галогена, алкоксила, гидроксила.
Согласно настоящему изобретению под замещенным алкенилом понимают ненасыщенную углеводородную цепь, линейную или разветвленную, содержащую 2-10 атомов углерода и содержащую одну или несколько двойных связей и замещенную одним или несколькими радикалами, выбранными из атома галогена, алкоксила и гидроксила.
Согласно настоящему изобретению под замещенным алкинилом понимают ненасыщенную углеводородную цепь, линейную или разветвленную, содержащую 2-10 атомов углерода, содержащую одну или несколько тройных связей и замещенную одним или несколькими радикалами, выбранными из атома галогена, алкоксила и гидроксила.
Согласно настоящему изобретению под циклоалкилом понимают насыщенную циклическую углеводородную цепь, содержащую 3-7 атомов углерода.
Согласно настоящему изобретению под замещенным циклоалкилом понимают насыщенную циклическую углеводородную цепь, содержащую 3-7 атомов углерода и замещенную одним или несколькими радикалами, выбранными из атома галогена, алкоксила и гидроксила.
Согласно настоящему изобретению под арилом понимают один ароматический углеводородный цикл или два сконденсированных ароматических углеводородных цикла.
Предпочтительные арильные радикалы выбирают из фенила и нафтила.
Согласно настоящему изобретению под замещенным арилом понимают один цикл или два сконденсированных цикла ароматический(их) углеводородный(ых), замещенный(ых) одной или несколькими группами атомов, выбранными из алкила, алкоксила, арила, галогена, гидроксила, циано, трифторметила и нитро.
Согласно настоящему изобретению под аралкилом понимают алкил, замещенный арилом.
Согласно настоящему изобретению под замещенным аралкилом понимают алкил, замещенный замещенным арилом.
Согласно настоящему изобретению под гетероциклическим радикалом понимают циклическую или полициклическую углеводородную цепь, насыщенную или ненасыщенную, содержащую один или несколько гетероатомов, выбранных из О, S и N.
Согласно настоящему изобретению под замещенным гетероциклическим радикалом понимают гетероциклический радикал, замещенный одной или несколькими группами атомов, выбранными из алкила, алкоксила, галогена, гидроксила, циано, трифторметила и нитро.
Согласно настоящему изобретению под гетероарильным радикалом понимают ароматический гетероциклический радикал, т.е. ароматическую циклическую или полициклическую углеводородную цепь, содержащую один или несколько гетероатомов, выбранных из О, S и N.
Согласно настоящему изобретению под замещенным гетероарилом понимают гетероарил, замещенный одной или несколькими группами атомов, выбранными, например, из алкила, алкоксила, арила, замещенного арила, галогена, гидроксила, циано, трифторметила и нитро.
Согласно настоящему изобретению под гетероаралкилом понимают алкил, замещенный гетероарилом.
Согласно настоящему изобретению под замещенным гетероаралкилом понимают гетероаралкил, замещенный одной или несколькими группами атомов, выбранными из алкила, алкоксила, галогена, гидроксила, циано, трифторметила и нитро.
Согласно настоящему изобретению под алкоксилом понимают атом кислорода, замещенный алкилом.
Согласно настоящему изобретению под атомом галогена понимают атом фтора, хлора, брома или иода.
Среди соединений общей формулы (I), входящих в объем настоящего изобретения, можно назвать, в частности, следующие соединения:
1) 3-[(4-бут-2-инилоксибензолсульфонил)-метиламино]-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид
2) (S)-3-(4-бут-2-инилоксибензолсульфониламино)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид
3) (S)-3-(4-бензилоксибензолсульфониламино)-N-гидрокси-2- (4-метансульфонилпиперазин-1-ил)-пропионамид
4) (S)-3-[(4-бензилоксибензолсульфонил)-метиламино]-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид
5) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
6) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(нафталин-1-илметокси)-бензолсульфониламино]-пропионамид
7) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-(4-пропоксибензолсульфониламино)-пропионамид
8) (S)-3-[4-(3-цианобензилокси)-бензолсульфониламино]-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид
9) (S)-3-[4-(4-цианобензилокси)-бензолсульфониламино]-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид
10) бензил-4-{(S)-1-гидроксикарбамоил-2-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-этил}-пиперазин-1-карбоксилат
11) (S)-N-гидрокси-2- (4-метансульфонилпиперазин-1-ил)-3-[4-(2-фенилпиперидин-4-илметокси)-бензолсульфониламино]-пропионамид
12) (R)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
13) (S)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-2-пиперазин-1-илпропионамид
14) Гидрохлорид (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
15) Дифторацетат трет.бутил-3-{4-[(S)-2-гидроксикарбамоил-2-(4-метансульфонилпиперазин-1-ил)-этилсульфамоил]-феноксиметил}-2-метилиндол-1-карбоксилат
16) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(хинолин-4-илметокси)-бензолсульфониламино]-пропионамид
17) (S)-2-(4-бензилпиперазин-1-ил)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
18) (S)-2-[4-(4-фторбензил)-пиперазин-1-ил]-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
19) (S)-2-(4-этилпиперазин-1-ил)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
20) (S)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-2-[4-(4-трифторметилбензил)-пиперазин-1-ил] -пропионамид
21) (S)-N-гидрокси-2-[4-(4-метилбензил)-пиперазин-1-ил]-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
22) (S)-3-[4-(бензоизоксазол-3-илметокси)-бензолсульфониламино]-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-пропионамид
23) (S)-N-гидрокси-2-(4-изобутирилпиперазин-1-ил)-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
24) (S)-N-гидрокси-2-[4-(2-метилпропан-1-сульфонил)-пиперазин-1-ил]-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
25) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(2-трифторметилпиразоло[1,5-α]пиридин-3-илметокси)-бензолсульфониламино]-пропионамид
26) (S)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-2-[4-(пропан-2-сульфонил)-пиперазин-1-ил]-пропионамид
27) (S)-2-(4-бензилпиперазин-1-ил)-N-гидрокси-3-[4-(2-трифторметилпиразоло[1,5-α]пиридин-3-илметокси)-бензолсульфониламино]-пропионамид
28) (S)-2-(4-ацетилпиперазин-1-ил)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
29) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-{пропил-[4-(хинолин-4-илметокси)-бензолсульфонил]-амино}-пропионамид
30) (S)-2-(4-бензолсульфонилпиперазин-1-ил)-N-гидрокси-3-[4(пиразоло[1,5-α]пиридин-3-илметокси)-бензолсульфониламино]-пропионамид
31) (S)-2-(4-бензилпиперазин-1-ил)-N-гидрокси-3-[4-(1-метилпиперидин-4-илметокси)-бензолсульфониламино]-пропионамид
32) (S)-2-[4-(4-фторбензоил)-пиперазин-1-ил]-N-гидрокси-3-[4(3-м-толилпропокси)-бензолсульфониламино]-пропионамид
33) (S)-N-гидрокси-3-[4-(2-метилнафталин-1-илметокси)-бензолсульфониламино]-2-(4-пропионилпиперазин-1-ил)-пропионамид
34) (S)-N-гидрокси-3-[4-(4-метилпентилокси)-бензолсульфониламино]-2-(4-фенилацетилпиперазин-1-ил)-пропионамид
35) (S)-N-гидрокси-2-(4-метансульфонилпиперазин-1-ил)-3-[4-(2-метилпиридин-4-илметокси)-бензолсульфониламино]-пропионамид
36) (S)-2-(3-ацетилимидазолидин-1-ил)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
37) (S)-3-[4-(3,5-диметилбензилокси)-бензолсульфониламино]-N-гидрокси-2-имидазолидин-1-ил-пропионамид
38) (S)-N-гидрокси-2-(4-метансульфонил-[1,4]диазепан-1-ил)-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
39) (S)-2-(4-бензил-[1,4]диазепан-1-ил)-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
40) (S)-2-[1,4]диазокан-1-ил-N-гидрокси-3-[4-(2-метилхинолин-4-илметокси)-бензолсульфониламино]-пропионамид
41) (S)-N-гидрокси-3-[4-(2-метилбензофуран-3-илметокси)-бензолсульфониламино]-2-[4-(пропан-2-сульфонил)-пиперазин-1-ил]-пропионамид
42) (S)-2-(4-бензилпиперазин-1-ил)-N-гидрокси-3-[4-(2-изопропил-1Н-индол-3-илметокси)-бензолсульфониламино]-пропионамид
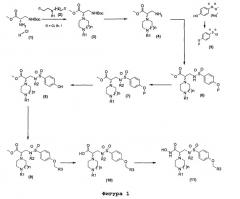
Соединения общей формулы (I) получают согласно реакционной схеме фиг.1, представленной ниже.
Согласно фиг.1 соединения (3) получают путем реакции аминокислоты (1) H-DAP(Boc)-OMe.HCl или Н-(D)-DAP(Boc)-ОМе.HCl с соединением (2) (коммерчески доступным или предварительно полученным) в присутствии третичного органического основания, такого как диизопропилэтиламин или триэтиламин, при температуре между 60°С и 120°С. Соединения (4) получают посредством снятия защиты с аминофункции соединений (3) согласно классическим способам, таким как, например, использование раствора соляной кислоты в изопропаноле.
Реакция между соединением (4) и 4-гидроксибензолсульфонилхлоридом, O-защищенным бензильной группой, например, (P=CH2-Ph) (5), в присутствии третичного основания, такого как например, триэтиламин, в дихлорметане приводит к соединению (6). Последующее N-алкилирование сульфонамидной группы может быть осуществлено путем взаимодействия с алкилгалогенидом в присутствии основания, такого как, например, карбонат калия, в растворителе, таком как ДМФ, для получения производного (7). Соединение (8) получают путем снятия защиты известными специалисту способами снятия защиты с фенольной группы. Соединение (9) получают путем алкилирования фенольной группы соединения (8) в результате взаимодействия с алкилгалогенидом в присутствии основания, такого как, например, карбонат цезия, в ацетоне или в результате реакции Мицунобу с производным первичного спирта в присутствии трифенилфосфина и диизопропилазодикарбоксилата, например. Соединение (10) получают путем реакции омыления в присутствии основания, такого как гидроксид лития, в присутствии, например, воды и тетрагидрофурана. На последней стадии соединение (11) получают реакцией сочетания между, например, O-(трет.бутилдиметилсилил)гидроксиламином и производным (10) в условиях классического пептидного сочетания, используя, например, в качестве агентов сочетания гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида, гидроксибензотриазол или TBTU, а в качестве основания триэтиламин или диизопропилэтиламин в растворителе, таком как дихлорметан или диметилформамид. Снятие защиты с силилированной гидроксаминовой кислоты, полученной на промежуточной стадии, осуществляется in situ или путем промывки водным слабокислым раствором с получением соединения (11).
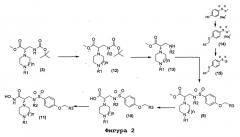
Другой альтернативный вариант получения соединения (11) представлен на фиг.2.
Следуя схеме синтеза на фигуре 2, производное (3) необязательно может быть подвергнуто алкилированию в присутствии основания, такого как гидрид натрия, и алкилгалогенида, например, в диметилформамиде для получения соединения (12), из которого получают соединение (13) согласно классическим способам снятия защиты с аминов, как, например, использованием раствора соляной кислоты в изопропаноле.
Соединение (14) заранее получают из коммерчески доступной натриевой соли 4-гидроксибензолсульфоновой кислоты путем алкилирования с помощью алкилгалогенида в присутствии основания, такого как, например, гидроксид натрия, в смеси растворителей, таких как, например, изопропанол и вода. Тогда соединение (15) получают путем взаимодействием производного (14) с оксалилхлоридом в присутствии диметилформамида, например, в дихлорметане.
Производное (9) получают в результате реакции между соединениями (13) и (15) в присутствии основания, такого как триэтиламин, например, в дихлорметане.
Еще один альтернативный вариант синтеза соединения (11) представлен на фиг.3.
Согласно фиг.3 соединение (17) получают путем взаимодействия аминокислоты (1) H-DAP(Boc)-ОМе.HCl или H-(D)-DAP(Boc)-ОМе.HCl с соединением (16) (предварительно полученным взаимодействием между бис (2-хлорэтил)амином, например, и бензилбромидом в присутствии карбоната калия в ацетонитриле) в присутствии органического третичного основания, такого как диизопропилэтиламин, при температуре примерно 120°С. После снятия защиты в аминофункции соединение (18) конденсируют с сульфонилхлоридом (15) для получения производного (19). Тогда N-алкилирование сульфонамидной группы может быть осуществлено реакцией с алкилгалогенидом в присутствии основания, такого как, например, карбонат калия, в растворителе, таком как ДМФ, для получения производного (20). Согласно классическим условиям гидрирования соединения (20) в присутствии палладия на угле в растворителе, таком как, например, этанол, получают соединение (21). Соединение (9) получают согласно классическим способам синтеза, например, взаимодействием соединения (21) с ацилхлоридом или сульфонилхлоридом в присутствии триэтиламина, или взаимодействием с алкилгалогенидом в присутствии основания, такого как, например, гидрид натрия. Дальнейшее омыление в присутствии основания, такого как гидроксид лития, в присутствии, например, воды и тетрагидрофурана приводит к соединению (10). На последней стадии получают соединение (11) путем сочетания, например, O-(трет.бутилдиметилсилил)гидроксиламина с производным (10) в условиях классического пептидного сочетания, используя, например, в качестве агентов сочетания гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида, гидроксибензотриазол или TBTU, а в качестве основания триэтиламин или диизопропилэтиламин, в растворителе, таком как дихлорметан или диметилформамид. Снятие защиты с силилированной гидроксаминовой кислоты, полученной на промежуточной стадии, осуществляется in situ или путем промывки водным слабокислым раствором с получением соединения (11).
Альтернативный вариант синтеза, предусмотренный для получения соединений, в которых R1 означает радикал -(CO)-R4, описан на фиг.4.
После снятия защиты с аминофункции соединения (17) согласно классическим условиям гидрирования в присутствии палладия на угле, в растворителе, таком как, например, этанол, получают соединение (22). После взаимодействия с ацетилхлоридом R4COCl в присутствии основания, такого как триэтиламин, получают соединение (23). Если R2 означает низший алкил, то N-алкилирование карбамата осуществляют путем взаимодействия с алкилгалогенидом в присутствии основания, такого как, например, карбонат калия, в растворителе, таком как ДМФ, для получения производного (24). Путем омыления в присутствии основания, такого как гидроксид лития, в присутствии, например, воды и тетрагидрофурана, получают соединение (25). Сочетание между, например, гидрохлоридом O-аллилгидроксиламина и производным (25) позволяет получить соединение (26) в классических условиях пептидного сочетания. Для этого используют, например, гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида, гидроксибензотриазол или TBTU в качестве агентов сочетания, и триэтиламин или диизопропилэтиламин в качестве основания. Реакцию осуществляют в растворителе, таком как дихлорметан или диметилформамид. После снятия защиты с аминофункции соединения (26) согласно классическим способам, получают соединение (27). Его подвергают конденсации с сульфонилхлоридом (15) для получения соединения (28). На последней стадии получают соединение (29) путем снятия защиты с гидроксиламинной функции соединения (28) согласно классическим способам, таким как, например, обработка тетракис(трифенилфосфином)палладия (0) и карбонатом калия в метаноле.
Согласно настоящему изобретению предпочтительными соединениями общей формулы (I) являются соединения, у которых:
R1 обозначает водород, алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, аралкил, замещенный аралкил, гетероаралкил, замещенный гетероаралкил, радикал -C(O)-R4, -SO2-R4, C(O)OR4, где R4 имеет значения, указанные ниже;
R2 представляет собой атом водорода или низший алкил;
R3 представляет собой арил, замещенный арил, аралкил, замещенный аралкил, гетероциклический радикал, замещенный гетероциклический радикал, гетероарил, замещенный гетероарил, гетероаралкил, замещенный гетероаралкил;
R4 представляет собой алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, арил, замещенный арил, аралкил, замещенный аралкил,
n может принимать значения 0, 1, 2;
а также их аддитивные соли с фармацевтически приемлемой кислотой, их аддитивные соли с фармацевтически приемлемым основанием и энантиомеры указанных соединений.
Согласно настоящему изобретению особенно предпочтительными соединениями общей формулы (I) являются соединения, у которых:
R1 обозначает водород, алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, аралкил, замещенный аралкил, радикал -C(O)-R4, -SO2-R4, где R4 имеет значения, указанные ниже;
R2 представляет собой атом водорода или низший алкил;
R3 представляет собой арил, замещенный арил, аралкил, замещенный аралкил, гетероциклический радикал, замещенный гетероциклический радикал, гетероарил, замещенный гетероарил, гетероаралкил, замещенный гетероаралкил;
R4 представляет собой алкил, замещенный алкил, арил, замещенный арил, аралкил, замещенный аралкил,
n может принимать значения 1 или 2;
а также их аддитивные соли с фармацевтически приемлемой кислотой, их аддитивные соли с фармацевтически приемлемым основанием и энантиомеры указанных соединений.
Согласно настоящему изобретению особенно более предпочтительными соединениями общей формулы (I) являются соединения, у которых:
R1 обозначает алкил, замещенный алкил, аралкил, замещенный аралкил, радикал -C(O)-R4, -SO2-R4, где R4 имеет значения, указанные ниже;
R2 представляет собой атом водорода;
R3 представляет собой арил, замещенный арил, аралкил, замещенный аралкил, гетероциклический радикал, замещенный гетероциклический радикал, гетероарил, замещенный гетероарил, гетероаралкил, замещенный гетероаралкил;
R4 представляет собой алкил, замещенный алкил, арил, замещенный арил, аралкил, замещенный аралкил,
n обозначает 1;
а также их аддитивные соли с фармацевтически приемлемой кислотой, их аддитивные соли с фармацевтически приемлемым основанием и энантиомеры указанных соединений.
Согласно настоящему изобретению особенно еще более предпочтительными соединениями общей формулы (I) являются соединения, у которых:
R1 обозначает алкил, замещенный алкил, аралкил, замещенный аралкил, радикал -C(O)-R4, -SO2-R4, где R4 имеет значения, указанные ниже;
R2 представляет собой атом водорода;
R3 представляет собой гетероциклический радикал, замещенный гетероциклический радикал, гетероарил, замещенный гетероарил, гетероаралкил, замещенный гетероаралкил;
R4 представляет собой алкил, замещенный алкил, арил, замещенный арил, аралкил, замещенный аралкил,
n обозначает 1;
а также их аддитивные соли с фармацевтически приемлемой кислотой, их аддитивные соли с фармацевтически приемлемым основанием и энантиомеры указанных соединений.
Согласно настоящему изобретению наиболее предпочтительными соединениями общей формулы (I) являются соединения, у которых:
R1 обозначает алкил, замещенный алкил, аралкил, замещенный аралкил, радикал -C(O)-R4, -SO2-R4, где R4 имеет значения, указанные ниже;
R2 представляет собой атом водорода;
R3 представляет собой гетероарил, замещенный гетероарил;
R4 представляет собой алкил, замещенный алкил, арил, замещенный арил, аралкил, замещенный аралкил,
n обозначает 1;
а также их аддитивные соли с фармацевтически приемлемой кислотой, их аддитивные соли с фармацевтически приемлемым основанием и энантиомеры указанных соединений.
Соединения согласно изобретению обладают очень хорошей ингибирующей активностью в отношении ТАСЕ, в частности, они селективно ингибируют фермент ТАСЕ относительно других ферментов ADAM и ММР. Эта ингибирующая активность в отношении фермента ТАСЕ измерялась в ферментативном тесте и количественно оценивалась показателем ИК50 (ингибирующая концентрация, необходимая для достижения 50% ингибирования фермента ТАСЕ), как это описано в примере 28. Соединения согласно изобретению имеют ИК50 в отношении ТАСЕ, ниже или равную 10 мкМ, более конкретно, ниже или равную 1 мкМ. Преимущественно, соединения согласно настоящему изобретению имеют ИК50 в отношении ТАСЕ, ниже или равную 0,5 мкМ.
Преимущественно, эти соединения также высоко селективны в отношении ТАСЕ относительно других ферментов ADAM и ММР (тест описан в примере 29): их ингибирующая активность по меньшей мере в 10 раз выше в отношении ТАСЕ, чем в отношении других ADAM и ММР (т.е. значение ИК50 ТАСЕ по меньшей мере в 10 раз ниже, чем этот же показатель у других ADAM и ММР), преимущественно выше, по меньшей мере, в 100 раз.
ТАСЕ (TNFα-Converting Enzyme) катализирует образование растворимой формы TNF-альфа из протеина-предшественника (трансмембранного TNFα), связанного с мембранами некоторых клеток. TNFα является провоспалительным цитокином, который известен тем, что играет определенную роль в многочисленных патологиях, имеющих воспалительный характер.
Поэтому изобретение относится к применению, по меньшей мере, одного соединения общей формулы (I), которая определена выше, для лечения патологий или нарушений, связанных с высвобождением TNFα. Ингибитор фермента ТАСЕ общей формулы (I) снижает продуцирование TNFα. Следовательно, он полезен для лечения патологий, связанных с высвобождением TNFα.
Изобретение относится также к применению, по меньшей мере, одного соединения общей формулы (I), которое определено выше, для получения фармацевтической или косметической композиции, в которой упомянутое соединение имеет активность, ингибирующую фермент ТАСЕ.
Следовательно, изобретение относится к применению, по меньшей мере, одного соединения общей формулы (I), которое определено выше, для лечения патологий или нарушений, которые облегчаются ингибированием фермента ТАСЕ.
Изобретение относится также к способу терапевтического лечения (человека или животного) или косметического лечения, заключающемуся в том, что вводят или наносят фармацевтическую или косметическую композицию, содержащую соединение общей формулы (I) в качестве ингибитора ТАСЕ и, следовательно, в качестве ингибитора продуцирования растворимого THFα.
Таким образом, изобретение относится к применению, по меньшей мере, одного соединения общей формулы (I), которое определено выше, для лечения патологий или нарушений, связанных с продуцированием TNFα.
Изобретение относится также к применению соединения общей формулы (I), которое определено выше, для получения лекарственного средства, предназначенного для лечения патологий, в которых снижение продуцирования TNFα представляло бы большой интерес.
В самом деле, используемые соединения согласно изобретению особенно хорошо подходят для лечения и профилактики нарушений/заболеваний, таких как воспалительные заболевания, перечисленные ниже, но не ограничиваются ими, такие как септический шок, гемодинамический шок, малярия, воспалительные заболевания кишечника (IBD), такие как болезнь Крона и язвенные колиты, воспалительные заболевания костей, микобактерийные инфекции, менингит, фибротические заболевания, сердечные заболевания, атеросклероз, ожирение, ишемический инсульт, отторжение трансплантата, рак, заболевания, в которых задействованы явления ангиогенеза, аутоиммунные заболевания, остеоартрит, ревматоидный артрит, анкилозирующий спондилоартрит, ювенильный хронический артрит, рассеянный склероз, ВИЧ, сахарный инсулиннезависимый диабет, аллергические заболевания, астма, хроническое обструктивное заболевание легких (COPD), воспалительные заболевания кожи, псориаз, атопический дерматит и псориатический артрит.
Эти молекулы также представляют