Рекомбинантная плазмидная днк ppa-oprf-eta, кодирующая синтез рекомбинантного белка oprf-eta pseudomonas aeruginosa, штамм escherichia coli pa-oprf-eta - продуцент рекомбинантного белка oprf-eta pseudomonas aeruginosa и способ получения рекомбинантного белка oprf-eta pseudomonas aeruginosa
Иллюстрации
Показать всеГруппа изобретений относится к биотехнологии. Рекомбинантная плазмидная ДНК pPA-OPRF-ETA размером 8007 пар оснований кодирует синтез рекомбинантного белка OprF-ETA Pseudomonas aeruginosa. Плазмида содержит следующие фрагменты: Xba I-Hind III фрагмент ДНК размером 177 пар оснований; Hind III-Hind III фрагмент ДНК размером 1059 пар оснований; Hind III-Xho I фрагмент ДНК размером 1598 пар оснований; Sph I-Hind III фрагмент ДНК размером 425 пар оснований; EcoR I - BamH I фрагмент ДНК размером 57 пар оснований. Предложены также штамм бактерий Еscherichia coli PA-OPRF-ETA, продуцирующий белок OprF-ETA и полученный путем трансформации родительского штамма бактерий Escherichia coli BL21(DE3) плазмидной ДНК рРА-OPRF-ETA и способ получения указанного белка OprF-ETA. Группа изобретений позволяет получить целевой продукт с массой около 100 кДа. 3 н.п. ф-лы, 3 ил., 1 табл., 4 пр.
Реферат
Изобретение относится к биотехнологии, а именно к получению гибридного рекомбинантного белка, включающего аминокислотные последовательности белка F наружной мембраны и экзотоксина A Pseudomonas aeruginosa (далее рекомбинантный белок OprF-ETA) для медицинских целей, а также к рекомбинантным штаммам Escherichia coli (далее Е.coli) и плазмидам для его получения.
Pseudomonas aeruginosa (далее P.aeruginosa) является одним из основных возбудителей гнойно-воспалительных заболеваний человека, в частности, вызывает госпитальные инфекции. Широкое распространение синегнойная инфекция получила благодаря неприхотливости в отношении питательных веществ и условий внешней среды, а также высокой резистентности к химиотерапевтическим средствам и антибиотикам.
Активная иммунизация может быть одним из эффективных средств защиты против условно патогенных микроорганизмов, в частности P. aeruginosa. Для индукции противосинегнойного иммунитета в нашей стране разрабатывались препараты на основе инактивированных бактерий, их компонентов и экзопродуктов: поливалентная синегнойная корпускулярная вакцина [1-3], пиоиммуноген [4-5], псевдомонасвакцина [6-9]. По разным причинам в настоящее время для использования в клинической практике не зарегистрировано ни одного препарата, включающего поверхностные антигены синегнойной палочки.
Для иммунопрофилактики и иммунотерапии синегнойных инфекций в НИИ вакцин и сывороток им. Мечникова г.Уфы разработан препарат на основе экзотоксина А P. aeruginosa - анатоксин синегнойной палочки [10-11]. Но выпуск данного препарата приостановлен в связи с коммерческими трудностями.
Трудности создания эффективных иммунопрепаратов против синегнойной палочки заключаются в том, что патогенез развивающихся с ее участием инфекций обусловлен воздействием целого ряда факторов патогенности, среди которых выделить наиболее значимый для разработки вакцинных препаратов представляется сложной задачей. Во время инфицирования, когда происходит проникновение возбудителя в ткани макроорганизма, первичные иммунные реакции формируются в основном на поверхностные антигены бактериальной клетки (компоненты мембраны и клеточной стенки). При исследовании поверхностных белков выявлено, что наибольшей иммуногенностью обладают некоторые белки наружной мембраны (outer protein - Opr) P.aeruginosa, которые отвечают за межклеточный транспорт и сохранение структуры бактериальной мембраны. Наиболее иммунологически исследован мажорный порообразующий белок F наружной мембраны (далее OprF) с молекулярной массой 37,6 кДа, который обладает высокой иммуногенностью. Эти данные обусловили исследования по разработке вакцин на основе очищенных мембранных белков [12]. Однако получение подобных препаратов является проблематичным, поскольку содержание белков наружной мембраны незначительно относительно суммарных белков бактериальной клетки.
Экзотоксин A является одним из главных патогенетических факторов при развитии генерализированных форм инфекций, вызываемых P.aeruginosa [13, 14]. Экзотоксин A имеет молекулярную массу около 70 кДа и представляет собой секретируемый белок, состоящий из полипептидной цепи длиной в 613 аминокислот, формирующих следующие домены: N-концевой домен I (аминокислотные остатки 1-252) необходимый для взаимодействия с поверхностью клеток-мишеней; домен II (аминокислотные остатки 253-404) обеспечивающий эффективный перенос токсина в цитозоль клеток; С-концевой домен III (аминокислотные остатки 405-613), отвечающий за цитотоксическую функцию [15]. Механизм этого процесса представляется следующим: экзотоксин А узнает и взаимодействует с рецептором а2-макроглобулина, также называемым белком, родственным рецептору липопротеина низкой плотности (LRP1) или CD91, присутствующим на эпителиальных и антиген-презентирующих клетках. После связывания с рецептором токсин проникает в клетку при помощи рецептор-опосредованного эндоцитоза, где происходит расщепление домена II в области REDLK при помощи фуриновой протеазы. Домен III, обладающий токсической активностью, катализирует инактивацию эукариотического фактора элонгации 2 (eEF-2) при помощи АДФ-рибозилирования, что приводит к ингибированию белкового синтеза и клеточной гибели [16]. Для защиты организма от поражения экзотоксином A возможно использование препаратов анатоксина, то есть очищенного нативного токсина, химически обработанного для устранения токсичности и сохранения иммуногенности. Созданные для иммунотерапии и иммунопрофилактики отечественные препараты на основе экзотоксина A представляют собой атоксичные формы белка, полученные очисткой культуральной токсинсодержащей среды P.aeruginosa, с последующей детоксикацией [17-20]. Показано, что после их применения в организме человека и животных происходило образование протективных антител. Однако трудоемкость технологических этапов получения, очистки, обезвреживания, а также нестандартность методов оценки специфической активности препаратов, обуславливают целесообразность создания вакцин на основе рекомбинантного анатоксина, а также разработки адекватных стандартных способов оценки специфической активности препарата.
В последнее время при создании вакцинных препаратов все большое внимание уделяется использованию генно-инженерных методов, суть которых заключается во встраивании генов, отвечающих за синтез отдельных протективных антигенов в возбудителях, в геном непатогенного микроорганизма (например, Е.coli или Saccharomyces cerevisiae). Во время культивирования полученных продуцентов, в большом количестве синтезируются целевые продукты (рекомбинантные белки), которые подвергаются простой очистке и могут использоваться для приготовления вакцины. Такая стратегия позволяет вычленить и использовать наиболее иммуногенные компоненты бактерии. При этом процесс производства вакцин исключает контакт с культурами патогенных микроорганизмов, что является существенным технологическим преимуществом, обеспечивающим безопасность персонала.
К настоящему моменту имеются данные об успешном использовании при проведении вакцинных препаратов, созданных с использованием рекомбинантных белков, включающих аминокислотные последовательности белков наружной мембраны P. aeruginosa. В Германии был получен гибридный белок, состоящий из 190-342 аминокислотных остатков OprF и 21-83 аминокислотных остатков Oprl. Для получения продуцента данного белка использован родительский штамм E.coli К-12 и векторная плазмида pGEX. Рекомбинантный белок имел на N-конце дополнительную гистидиновую последовательность и очищался с помощью аффинной хроматографии на никель-активированном сорбенте. Полученный препарат являлся иммуногенным и способствовал защите ожоговых больных от сепсиса, вызываемого синегнойной палочкой [21].
Ранее нами получены две рекомбинантные формы белка OprF P.aeruginosa (полноразмерная и С-концевая область, включающая 192-342 аминокислотные остатки). Показано, что эти белки обладали иммуногенными свойствами, сыворотки к ним обладали бактериостатическим эффектом, что было показано in vitro. Рекомбинантные формы белка OprF, а также иммунные сыворотки к ним способствовали защите мышей от экспериментальной инфекции, вызываемой P.aeruginosa [22]. С целью разработки препарата, предназначенного для стимуляции антитоксического иммунитета, то есть для нейтрализации такого значимого фактора патогенности как экзотоксин A, нами получены рекомбинантный экзотоксин А [23] и его атоксические формы [24].
Технической задачей изобретения является получение рекомбинантной плазмидной ДНК pPA-OPRF-ETA, кодирующей гибридный рекомбинантный белок, включающий аминокислотные последовательности белка F наружной мембраны и экзотоксина A Pseudomonas aeruginosa (OprF-ETA), и штамма-продуцента рекомбинантного белка OprF-ETA с использованием Е. coli штамма BL21(DE3).
Указанная задача решалась созданием рекомбинантной плазмидной ДНК рРА-OPRF-ETA и штамма Е. coli PA-OPRF-ETA.
Плазмида pPA-OPRF-ETA имеет 8007 пар оснований и характеризуется наличием следующих фрагментов:
Hind III фрагмента ДНК размером 1059 пар оснований, содержащего последовательность гена oprF P. aeruginosa.
Hind III - Xho I - фрагмента ДНК размером 1598 пар оснований, кодирующей первые два и часть третьего домена экзотоксина A P.aeruginosa.
Xba I - Hind III - фрагмента ДНК размером 177 пар оснований, содержащего последовательность сайта посадки рибосомы и последовательности, кодирующие стартовый кодон и шесть гистидинов.
Sph I - Hind III - фрагмента ДНК размером 425 пар оснований, содержащего модифицированный промотор бактериофага Т7, лактозный оперон, последовательность сайта посадки рибосомы и последовательности, кодирующие стартовый кодон и шесть гистидинов.
EcoR I - BamH I фрагмента ДНК размером 57 пар оснований, содержащего сайт посадки рибосомы, стартовый ATG-кодон и последовательность, кодирующую шесть гистидинов.
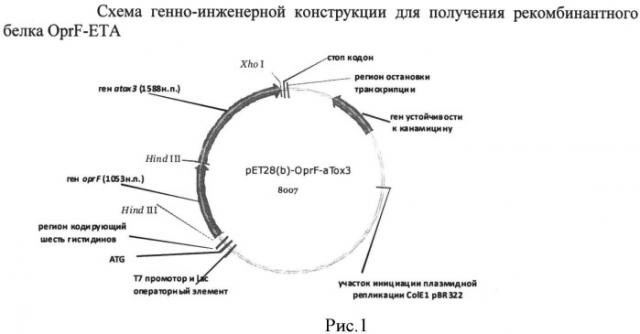
На рисунке 1 представлена схема плазмиды pPA-OPRF-ETA.
На рисунке 2 приведена аминокислотная последовательность рекомбинантного белка OprF-ETA, закодированная в плазмиде pPA-OPRF-ETA.
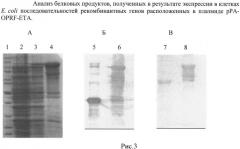
На рисунке 3 представлен анализ белковых продуктов, полученных в результате экспрессии в клетках Е.coli последовательностей рекомбинантных генов, расположенных в плазмиде pPA-OPRF-ETA.
В таблице 1 представлены данные по анализу защитных свойств рекомбинантного белка OprF-ETA от живой вирулентной культуры P.aeruginosa штамма РА 103.
Штамм Е.coli PA-OPRF-ETA получен трансформацией клеток родительского штамма Е.coli BL21(DE3) с использованием традиционной генно-инженерной технологии.
Штамм Е.coli PA-OPRF-ETA характеризуется следующими признаками:
Культурально-морфологические признаки
Клетки мелкие, прямые, утолщенной палочковидной формы, грамотрицательные, неспороносные.
Клетки хорошо растут на простых питательных средах. При росте на агаре «Дифко» колонии круглые, гладкие, выпуклые, мутные, блестящие, серые, края ровные. При росте в жидких средах (на минимальной среде с глюкозой или LB-бульоне) образуют интенсивную ровную муть.
Физико-биологические признаки
Аэроб. Температурный диапазон роста 4-42°C при оптимуме pH в пределах 6,5-7,5.
В качестве источника азота микроб использует как минеральные соли в аммонийной и нитратной формах, так и органические соединения в виде аминокислот, пептона, триптона, дрожжевого экстракта и т.д.
В качестве источника углерода микроб использует аминокислоты, глицерин, углеводы. Клетки проявляют устойчивость к канамицину (до 100 мкг/мл). Штамм Е. coli PA-OPRF-ETA - продуцент рекомбинантного белка OprF-ETA. Способ, условия и состав среды для хранения штамма:
LB-бульон с 10% глицерином и антибиотиками при -70°C в ампулах и в лиофилизированном состоянии в ампулах при 4°C.
Штамм Е.coli PA-OPRF-ETA идентифицирован по «Определителю Берги» (1974) как штамм вида Е.coli.
Особенностью заявляемого способа является разработка технологии, позволяющей получать комплексный высокоочищенный антиген P.aeruginosa сравнительно более простым способом и в более короткие сроки, по сравнению с традиционными методами получения бактериальных белков. При этом в одном белковом препарате объединены поверхностный антиген, необходимый для стимуляции иммунитета против микробной клетки и анатоксин, необходимый для стимуляции иммунитета, с целью нейтрализации экзотоксина А. Объединение двух антигенов в одном белковом препарате способствует более унифицированному методу их получения.
Способ включает следующие этапы.
Культивирование в питательной среде штамма Е.coli PA-OPRF-ETA; Осаждение биомассы центрифугированием.
Разрушение клеток микроорганизма при растворении их в денатурирующем буфере, содержащем 8 М мочевину.
Очистка с помощью аффинной хроматографии на никель-активированных сорбентах. Ренатурация очищенного рекомбинантного анатоксина с помощью диализа.
Оптимальными условиями проведения отдельных стадий получения рекомбинантного анатоксина являются следующие.
Разрушение клеток осуществляют в результате растворения биомассы в 8 М буферном растворе мочевины.
Удаление нерастворимых компонентов клетки осуществляют центрифугированием.
Ренатурацию проводят при температуре 4°C путем ступенчатого диализа против 50 мМ буферного раствора Tris-HCl (pH 9,0).
Выход рекомбинантного белка OprF-ETA в результате применения способа в оптимальном режиме составляет не менее 20 мг очищенного рекомбинантного белка OprF-ETA с 1 л культуральной среды, уровень экспрессии рекомбинантного белка OprF-ETA - не менее 30 мг с 1 л культуральной среды.
Сущность и преимущества заявляемой группы изобретений иллюстрируется следующими примерами.
Пример 1. Получение рекомбинантной плазмиды ДНК pPA-OPRF-ETA
Основой для получения плазмиды ДНК pPA-OPRF-ETA служили плазмидная конструкция, предназначенная для экспрессии рекомбинантной атоксичной формы экзотоксина A P.aeruginosa [24]. Данная конструкция представляла собой плазмиду рЕТ28(b) со встроенным по сайтам рестрикции Hind III и Xho I геном экзотоксина A P. aeruginosa с делецией области, кодирующей 106 С-концевых аминокислотных остатков.
В качестве матрицы для получения гена oprF служила плазмидная конструкция, предназначенная для экспрессии рекомбинантного OprF [22]. При амплификации гена oprF с целью его встраивания в конструкцию с геном анатоксина использовалась следующая пара праймеров: 5'-GAT AAG СТТ ATG AAA CTG AAG AAC АСС ТТА G и 5'-САТ AAG СТТ СТТ GGC ТТС AGC ТТС ТАС. Первый праймер соответствовал началу гена oprF, а второй был комплементарен концу гена oprF. Оба праймера содержали на 5'-конце дополнительный сайт рестрикции Hind III (подчеркнут).
Процесс амплификации гена oprF состоял из следующих стадий: прогревания при 94°C в течение 3 мин; 30-ти циклов ПЦР (94°C - 1 мин, 30 сек 65°C - 1 мин, 72°C - 1 мин) и инкубации при 72°C в течение 2 мин. ПЦР проводили при следующих реакционных условиях: 50 шМ КС1, 10 тМ Tris - HCl, 0,1% Triton Х-100, 1,5 тМ MgCl, 0,120 тМ dNTP, (рН 9,0). На 50 мкл реакционной смеси использовали 3 ед. TAQ-полимеразы (Fermentas) и 0,1 мкг геномной ДНК. Реакцию проводили в амплификаторе "Терцик". Процесс амплификации состоял из следующих стадий: прогревания при 94°C в течение 3 мин; 30-ти циклов ПЦР (94°C - 1 мин, 30 сек 65°C - 1 мин, 72°C - 1 мин) и инкубации при 72°C в течение 2 мин.
Амплифицированную ДНК обработали рестриктазой Hind°III. Одновременно этой же рестриктазой обработали плазмидную конструкцию, предназначенную для экспрессии рекомбинантной атоксичной формы экзотоксина A P.aeruginosa.
Оба рестрикта очистили в агарозном геле и объединили в одну конструкцию при реакции лигирования. В результате была получена рекомбинантная плазмида рРА-OPRP-ETA (рис.1). Аминокислотная последовательность рекомбинантного белка, полученная в результате трансляции встроенных слитых генов в плазмиде pPA-OPRF-ЕТА (которая осуществлялась в компьютерной программе OMIGA) представлена на втором рисунке (рис.2).
Пример 2. Получение штамма Е.coli PA-OPRF-ETA - продуцента рекомбинантного белка OprF-ETA
Штамм-продуцент Е.coli PA-OPRF-ETA получали путем трансформации клеток родительского штамма Е.coli BL21(DE3) рекомбинантной плазмидой pPA-OPRF-ETA с последующим отбором рекомбинантных клонов на среде, содержащей канамицин (50 мкг/мл) при температуре 37°C.
Первичный отбор рекомбинантных плазмид проводили с использованием рестриктного анализа и секвенирования.
Далее отбор продуцентов проводили по способности контролируемого синтеза рекомбинантного белка в клетках. Для этого инокулировали бактериальной колонией 3 мл среды LB, содержащей канамицин в концентрации 50 мкг в мл. Выращивали в термостатированном шейкере со скоростью орбитального вращения 250 об/мин в течение 12-16 часов и температуре 37°C. Затем в 5 мл свежей среды вносили 100 мкл выросшей культуры и инкубировали в прежних условиях в течение 2-3 часов до достижения культурой активной фазы роста (0,6 оптических единиц при длине волны 600 нм). Добавляли 5 мкл 1 М водного раствора химического индуктора изопропил-P-d-тиогалактопиранозид (далее ИПТГ). Инкубацию продолжали в прежних условиях 4 часа, после чего осаждали полученную биомассу.
В качестве контроля использовали бактериальную культуру продуцента, инкубированную при тех же условиях, но без добавления ИПТГ. Белковые продукты анализировали электрофорезом в полиакриламидном геле по методу Лэммли.
В результате экспрессии конструкции pPA-OPRF-ETA в клетках Е.coli штамма BL21(DE3) наблюдался синтез рекомбинантного продукта с массой около 100 кДа (рис.3A). Расчетная масса рекомбинантного белка OprF-ETA составляла 105 кДа. Рекомбинантный белок имел на N-конце дополнительную аминокислотную последовательность, включающую шесть гистидиновых остатков, что позволило их очистить в колонках с Ni-сефарозой. Очищенный продукт оказался специфичным в иммуноблоттинге при реакции с кроличьей сывороткой против рекомбинантного белка OprF и против синегнойного анатоксина, в той же степени, что и с отдельными рекомбинантными белками, против которых были получены данные сыворотки (рис.3Б и 3В).
В качестве контроля использовали бактериальную культуру продуцента, инкубированную при тех же условиях, но без добавления ИПТГ. Белковые продукты анализировали электрофорезом в полиакриламидном геле по методу Лэммли с последующей окраской Кумасси R-250 (рис.3А).
В результате экспрессии конструкции pPA-OPRF-ETA в клетках Е. coli штамма BL21(DE3) наблюдался синтез рекомбинантного продукта с массой около 100 кДа (трэк A3). Расчетная масса рекомбинантного белка OprF-ETA составляла 105 кДа. Белковые продукты в опытных трэках сравнивали с белками весового белкового маркера, нанесенного в трэк А1. В то же время белки продуцента, полученные при выращивании биомассы без индукции экспрессии (то есть без добавления ИПТГ), не содержали специфического продукта (трэк А2). Рекомбинантный белок имел на N-конце дополнительную аминокислотную последовательность, включающую шесть гистидиновых остатков, что позволило их очистить в колонках с Ni-сефарозой (трэк А4).
Иммунологическая специфичность рекомбинантных белков оценивалась в иммуноблоттинге. На рисунке 3Б представлена нитроцеллюлозная мембрана после иммуноблоттинга с сывороткой к рекомбинантному OprF, а на рисунке 3В - нитроцеллюлозная мембрана после иммуноблоттинга с сывороткой к рекомбинантному анатоксину.
Очищенный продукт оказался специфичным в иммуноблоттинге при реакции с кроличьей сывороткой против рекомбинантного белка OprF (рис.3Б, трэк 6) и против синегнойного анатоксина (рис.3В, трэк 8), в той же степени, что и с отдельными рекомбинантными белками (положительные контроли в иммуноблоттинге), против которых были получены данные сыворотки. Очищенный рекомбинантный белок OprF был нанесен в пятый трэке (рис.3Б, трэк 5), а очищенный рекомбинантный анатоксин в седьмой трэк (рис.3В, трэк 7).
Пример 3. Получение рекомбинантного белка OprF-ETA из штамма Е.coli PA-OPRF-ЕТА
Получение рекомбинантного белка OprF-ETA проводили в 4 этапа:
1 этап. Культивирование штамма Е.coli PA-OPRF-ETA с индукцией экспрессии рекомбинантного гена.
2 этап. Получения клеточного лизата штамма Е.coli PA-OPRF-ETA после экспрессии рекомбинантного гена.
3 этап. Хроматографическая очистка рекомбинантного белка OprF-ETA.
4 этап. Растворение и ренатурация рекомбинантного белка OprF-ETA.
Культивирование штамма Е.coli PA-OPRF-ETA с индукцией экспрессии рекомбинантного гена.
Выращивали посевной материал штамма Е.coli PA-OPRF-ETA в 500 мл среды LB содержащей канамицин в концентрациии 50 мкг в мл. Культивирование проводили в течение 12 ч при температуре 37°C в термостатированном шейкере со скоростью орбитального вращения 250 об/мин.
Полученную культуру асептически вносили в лабораторный ферментер с 10 л стерильной среды LB, содержащей канамицин в концентрациии 50 мкг в мл. Выращивание в ферментере проводили при температуре 37°C, концентрации растворенного кислорода 30%, оборотов мешалки 300 об/мин.
При достижении плотности культуры 0,6 оптических единиц при длине волны 600 нм в ферментер вносили 10 мл 1 М водного раствора ИПТГ. Инкубацию продолжали в прежних условиях 4 часа.
Получения клеточного лизата штамма Е.coli PA-OPRF-ETA после экспрессии рекомбинантного гена.
Биомассу осаждали в центрифуге Beckman J2-21 (ротор JA-14) со скоростью вращения 3000 об/мин в течение 10 мин. Осадок собирали и растворяли в одном литре следующего раствора: 8 М мочевина; 0,1 М NaH2PO4; 0,01 М Tris-HCl; pH - 8,0. Растворение биомассы проводили в орбитальном шейкере при вращении 250 об/мин в течение 12 ч при комнатной температуре.
Затем лизат освобождали от нерастворенных фрагментов клетки в центрифуге Beckman J2-21 (ротор JA-14) со скоростью вращения 15000 об/мин при комнатной температуре в течение часа. Супернатант переносили в чистую стерильную колбу.
Хроматографическая очистка рекомбинантного белка OprF-ETA.
К осветленному лизату добавляли 20 мл суспензии Ni-агарозы (QIAGEN) и инкубировали 1 час на комнатной температуре в орбитальном шейкере при легком покачивании (40 об/мин).
Полученную суспензию пятью этапами пропускали через колонку для хроматографии (Bio-Rad) объемом 250 мл и диаметром 5 см. В результате из колонки удалялась жидкая фаза лизата и оставался сорбент со связанным рекомбинантным белком.
Далее через колонку пропускали два литра промывочного раствора следующего состава: 8 М мочевина; 0,1 М NaH2PO4; 0,01 М Tris-HCl; pH - 6,3.
Для эллюции рекомбинантного белка через колонку пропускали десять раз по 15 мл первого эллюционного раствора и десять раз по 15 мл второго эллюционного раствора, собирая каждую фракцию в отдельную пробирку. Растворы для эллюции имели тот же состав, что и раствор для промывки, только первый эллюционный раствор имел pH - 5,9, а второй - 4,5.
С аликвотами от собранных фракций проводили электрофорез в полиакриламидном геле. После анализа результатов электрофореза отбирали фракции, содержащие очищенный белок.
Растворение и ренатурация рекомбинантного белка OprF-ETA
Очищенный рекомбинантный белок растворяли в 50 мМ Tris-HCl (pH 9,0) с помощью ступенчатого диализа при температуре 4°C и перемешивании буфера на магнитной мешалке. Для этого фракции, содержащие очищенный белок, объединяли и переносили в диализный мешок.
Завязанный диализный мешок помещали в емкость, содержащую 1 литр следующего раствора: 6 М мочевина; 50 мМ Tris-HCl; pH - 9,0. Через два часа поочередно меняли содержимое на буферные растворы с содержанием 4, 2 и 1 М мочевины.
Затем в емкость для диализа наливали чистый буферный раствор (50 мМ Tris-HCl, pH 9,0). Его трижды меняли каждые два часа.
Содержание белков в препарате определяли спектрофотометрически при длине волны 280 нм. При расчете концентрации рекомбинантных белков использовали коэффициент экстинкции 0.85, рассчитанный в программе OMIGA.
Препараты очищенного рекомбинантного белка OprF-ETA хранили в аликвотах по 5 мл в стерильных пробирках при -70°C.
Пример 4. Оценка защитных свойств рекомбинантного белка OprF-ETA
Для оценки защитных свойств рекомбинантного белка OprF-ETA использовали живую вирулентную культуру P.aeruginosa штамма РА 103, который характеризуется высоким уровнем синтеза экзотоксинов и подобен большинству штаммов встречающихся в клинике.
Исследование рекомбинантного белка OprF-аТох3 проводили в сравнении отдельными белками OprF и аТох3. Для этой цели сформировали четыре группы животных. Первая группа состояла из мышей, получавших инъекции по 50 мкг гибридного белка OprF-аТох3. Вторая и третья группы включали животных, получавших препараты рекомбинантных белков в отдельности (OprF и аТох3). Четвертая группа, состоящая из интактных мышей, являлась контрольной. Препараты белков вводили двукратно с двухнедельным интервалом. Через две недели после курса иммунизации мышам вводили различные дозы (от 12,5 до 200 млн микробных клеток) живой вирулентной культуры P.aeruginosa высокотоксигенного штамма РА-103. Контрольной группе вводили от 6,25 до 100 млн микробных клеток (млн м.к.). Подсчет погибших и выживших животных проводили в течение семи последующих дней (табл. 1). Для группы интактных мышей ЛД50 соответствовала 30,8 млн м.к; в группе животных иммунизированных анатоксином - 61,6 млн м.к.; OprF - 66 млн м.к.; гибридным белком 93,3 млн м.к.
Иммунизирующая доза составляла 50 мкг. В каждой группе присутствовало по 20 особей. После курса иммунизации мышам вводили от 5 до 160 млн микробных клеток живой вирулентной культуры P. aeruginosa штамма РА 103. Учет павших животных проводили в течение течение пяти дней (табл. 2). ЛД50 в группе интактных мышей (контрольной) составила 12,3 млн микробных клеток. В группе иммунизированных мышей значение ЛД50 достигло 32,5 млн микробных клеток. Таким образом, индекс эффективности был равен 2,6.
Индексы эффективности (ИЭ) протективных свойств (отношение ЛД50 для иммунизированных мышей к ЛД50 в контрольной группе) анатоксина и OprF составили 2,0 и 2,1. При иммунизации рекомбинантным белком OprF-аТох3 налицо увеличение защитных свойств. ИЭ в этом случае составил 3,0 (табл.1).
Источники информации
1. Мороз А.Ф., Констанинов Б.А., Анциферова Н.Г., Радкевич С.А., Ковырялкина О.В. Применение поливалентной синегнойной вакцины для профилактики послеоперационных гнойно-септических осложнений в кардиохирургии // Современная госпитальная инфекция. Тезисы докладов. Л., - 1980, - С.92.
2. Мороз А.Ф. Применение поливалентной вакцины с защитным эффектом против Pseudomonas aeruginosa II I Всесоюзная конференция по ранам и раневой инфекции. М., - 1977, - С.73-74.
3. Титова Т.И., Сидорова Т.Н., Радкевич С.А. и др. Получение и изучение свойств поливалентной корпускулярной синегнойной вакцины // Журн. микробиол. -1985. - №8. - С.80-84.
4. Станиславский Е.С., Joo I. Вакцины против Pseudomonas aeruginosa инфекции: итоги и перспективы исследований // Бактериальные антигены, Сборник трудов - М., - 1982. - С.3-14.
5. Станиславский Е.С., Joo I., Северцева М.К. и др. Иммунологическая эффективность и безвредность в эксперименте пиоиммуногена-вакцины против инфекции Pseudomonas aeruginosa II Журн. микробиол. - 1982. - №5. - С.70-75.
6. Бандман О.А., Едвабная Л.С., Булк В.Ф. и др. Бесклеточная вакцина псевдомонас: иммунохимическая характеристика и иммуногенность // Журн. микробиол. - 1987. - №11. - С.44-47.
7. Едвабная Л.С., Зайднер И.Г., Макаренко Т.А. и др. Белковые протективные антигены Pseudomonas aeruginosa // Журн. микробиол. - 1985. - №11. - С.18-23.
8. Макаренко Т.А., Балаян С.С, Сергиенко А.И. и др. Иммунологический ответ у доноров-добровольцев, иммунизированных вакциной псевдомонас // Журн. микробиол. - 1991. - №11. - С.39-41.
9. Макаренко Т.А., Станиславский Е.С. Иммунологическое изучение белков клеточной стенки Pseudomonas aeruginosa // Журн. микробиол. - 1996. - №2. - С.7-9.
10. Пат. 1410527 C СССР, С12Р 1/04. Способ получения экзотоксина A синегнойной палочки // Н.А.Михайлова, Т.Н.Кузнецова, Ф.А. Шаймухаметов, А.Ф. Мороз, И.А. Баснакьян. - Заявл. 10.09.86; Опубл. 09.06.95 // БИПМ. - 1995.
11. Пат. 1481962 С СССР, А61К35/74. Способ обезвреживания очищенного экзотоксина A синегнойной палочки // Н.А.Михайлова, Ф.А.Шаймухаметов, Т.Н.Кузнецова, А.Ф.Мороз. - Заявл. 15.07.87; Опубл. 09.06.95 // БИПМ. - 1995.
12. Lee NG, Jung SB, Ahn BY, Kim YH, Kim JJ, Kim DK, Kim IS, Yoon SM, Nam SW, Kim HS, Park WJ. Immunization of burn-patients with a Pseudomonas aeruginosa outer membrane protein vaccine elicits antibodies with protective efficacy // Vaccine - 2000 - №18 - P.1952-1961.
13. Liu P.V. Exotoxins of Pseudomonas aeruginosa. I. Factors that influence the production of exotoxin A. J. Infect. Dis. 1986 128:506-513.
14. Mugabe C., Halwani M., Azghani A.O., Lafrenie R.M. and Omri A. Mechanism of Enhanced Activity of Liposome-Entrapped Aminoglycosides against Resistant Strains of Pseudomonas aeruginosa Antimicrobial agents and chemotherapy, June 2006, p.2016-2022.
15. Allured V.S., Collier R.J., Carroll S.F. and McKay D.B. Structure of exotoxin A of Pseudomonas aeruginosa at 3 A angstrom resolution. Proc Natl Acad Sci USA, 1986, 83: 1320-1324.
16. Armstrong S., Yates S.P. and Merrill A.R. Insight into the Catalytic Mechanism of Pseudomonas aeruginosa Exotoxin A. The journal of biological chemistry, 2002, Vol.277, No. 48, Issue of November 29, pp.46669-46675.
17. Бодрова Г.Н. Получение и изучение активности антитоксической противосинегнойной плазмы. Диссертация на соискание уч. степ. канд. мед. наук. 1997.
18. Михайлова Н.А., Кузнецова Т.Н., Шаймухаметов Ф.А., Мороз А.Ф. и Баснакьян И.А. Пат. 1410527 С СССР, С12Р 1/04. Заявл. 10.09.86; Опубл. 09.06.95.
19. Михайлова Н.А., Шаймухаметов Ф.А., Кузнецова Т.Н., Мороз А.Ф. Пат. 1481962 С СССР А61К 35/74. Способ обезвреживания очищенного экзотоксина A синегнойной палочки. Заявл. 15.07.87; Опубл. 09.06.95.
20. Подгорная Л.Г., Дзюбан Н.Ф. Антигенные свойства анатоксина синегнойнолй палочки и протективное действие антитоксической противосинегнойной сыворотки // Журн. микробиол. 1986, №6 67-69.
21. Mansouri Е, Blome-Eberwein S, Gabelsberger J, Germann G, von Specht BU. Clinical study to assess the immunogenicity and safety of a recombinant Pseudomonas aeruginosa OprF-OprI vaccine in burn patients. FEMS Immunology Medical Microbiology. 2003, 37:161-6.
22. Kaloshin A.A., Gatypova E.V., Mikhailova N.A. Obtaining Recombinant Forms of the Outer Membrane Protein F of Pseudomonas aeruginosa and Assessment of Their Immunogenic Properties. Applied Biochemistry and Microbiology, 2011, 47(8):780-788.
23. Исаков M.A., Калошин A.A., Михайлова H.A. Получение рекомбинантного экзотоксина A Pseudomonas aeruginosa. Биотехнология. 2009, №3, с.29-33.
24. Исаков М.А., Солдатенкова А.В, Калошин А.А., Михайлова Н.А. Изучение иммунобиологических свойств рекомбинантных атоксичных форм экзотоксина A Pseudomonas aeruginosa // Журнал микробиологии, эпидемиологии и иммунобиологии. 2011. №.2, с.37-42.
| Таблица 1 | ||||
| Исследование защитных свойств рекомбинантного белка OprF-ETA. | ||||
| Группа животных | Доза заражения, млн | Количество мышей павших/выживших | ЛД50, млн м/к | ИЭ |
| Иммунизированные OprF-ETA | 200 | 8/2 | 93,3 | 3,0 |
| 100 | 4/6 | |||
| 50 | 2/8 | |||
| 25 | 1/9 | |||
| 12,5 | 1/9 | |||
| Иммунизированные анатоксином (аТох3) | 200 | 9/1 | 61,6 | 2 |
| 100 | 7/3 | |||
| 50 | 3/7 | |||
| 25 | 2/8 | |||
| 12,5 | 1/9 | |||
| Иммунизированные OprF | 200 | 8/2 | 66 | 2,1 |
| 100 | 6/4 | |||
| 50 | 4/6 | |||
| 25 | 2/8 | |||
| 12,5 | 1/9 | |||
| Контроль (интактные мыши) | 100 | 9/1 | 30,8 | - |
| 50 | 7/3 | |||
| 25 | 4/6 | |||
| 12,5 | 2/8 | |||
| 6,25 | 0/10 |
1. Рекомбинантная плазмидная ДНК pPA-OPRF-ETA, кодирующая синтез рекомбинантного белка OprF-ETA Pseudomonas aeruginosa, размером 8007 пар оснований, содержащая: Xba I-Hind III фрагмент ДНК размером 177 пар оснований, содержащего последовательность сайта посадки рибосомы и последовательности, кодирующие стартовый кодон и шесть гистидинов; Hind III-Hind III фрагмент ДНК размером 1059 пар оснований, содержащего последовательность гена oprF P.aeruginosa; Hind III-Xho I фрагмент ДНК размером 1598 пар оснований, кодирующую первые два и часть третьего домена экзотоксина A P.aeruginosa; Sph I-Hind III фрагмент ДНК размером 425 пар оснований, содержащего модифицированный промотор бактериофага Т7, лактозный оперон, последовательность сайта посадки рибосомы и последовательности кодирующие стартовый кодон и шесть гистидинов; EcoR I - BamH I фрагмент ДНК размером 57 пар оснований, содержащего сайт посадки рибосомы, стартовый кодон ATG-кодон и последовательность, кодирующую шесть гистидинов, при этом в результате экспрессии данной конструкции происходит синтез рекомбинантного продукта с массой около 100 кДа.
2. Штамм бактерий Еscherichia coli PA-OPRF-ETA - продуцент рекомбинантного белка OprF-ETA P.aeruginosa, полученный путем трансформации родительского штамма бактерий Escherichia coli BL21(DE3) рекомбинантной плазмидной ДНК рРА-OPRF-ETA.
3. Способ получения рекомбинантного белка OprF-ETA P.aeruginosa с использованием штамма Е.coli PA-OPRF-ETA по п.2, включающий его культивирование в питательной среде, разрушение клеток микроорганизма, очистку полученного продукта с использованием аффинной хроматографии на никель-активированных сорбентах и растворением с ренатурацией очищенного препарата в нативных условиях при помощи ступенчатого диализа.