Способ лечения переломов у животных
Иллюстрации
Показать всеИзобретение относится к медицине, в частности к области хирургии и травматологии, и предназначено для лечения опорно-двигательного аппарата. В процессе операции в качестве электрофизического воздействия на открытые кости, надкостницу и окружающие ткани используют факел аргоновой плазмы. По методу аргоноплазменной аблации (АПА) последним обрабатывают собранные костные элементы области перелома, надкостницу, соединительные элементы и окружающие ткани. Для проведения аргоноплазменной аблации зоны переломов используют аргонусиленный высокочастотный электрохирургический аппарат «ФОТЕК ЕА 141», оборудованный электродом для АПА при выходной мощности 35-75 Вт и расходе аргона 4-8 л/мин в режиме «СПРЕЙ». Процесс обработки составляет от 1 до 5 минут, а расстояние от среза электрода до обрабатываемой поверхности выдерживают 5-15 мм. При этом нейтральный электрод электрохирургического аппарата при лечении переломов у животных располагают под телом животного, смачивая электрод физиологическим раствором для обеспечения плотного электрического контакта с телом животного. Способ позволяет, за счет использования аргоноплазменного воздействия на операционное поле, надкостницу и открытые кости, сократить процесс и сроки лечения переломов. 2 з.п.ф-лы, 6 ил.
Реферат
Изобретение относится к медицине, в частности к области хирургии и травматологии, к способам лечения опорно-двигательного аппарата, точнее переломов костей, с использованием в процессе оперативного лечения электротехнологий и факторов немеханического воздействия на раны и окружающие ткани вне зависимости от способов фиксации костных обломков.
Известны способы и технологии по использованию ультразвука в оперативном лечении переломов костей путем применения ультразвуковых пил и других инструментов, уменьшающих травмирование костной ткани и способствующих более быстрому сращиванию костей, разрезанных или сформированных ультразвуковым инструментом (см. Акопян В.Б. Лечит ультразвук, М. Колос, 1983, с.95-99).
Недостатками использования ультразвука при лечении переломов костей является то, что ультразвук используют в основном как дополнение к механической обработке костей, что требует изготовления специального уникального оборудования и особых инструментов, повышая затраты на проведение операций. К недостаткам способа относится и то, что он сохраняет сравнительно высокую вероятность развития остеомиелита и имеет слабую стимуляцию остеогенеза. Это связано с тем, что несмотря на обработку антисептиками и антибиотиками костных фрагментов, они не обеспечивают полную стерильность в зоне перелома.
Известно также применение гелий-неоновых и инфракрасных лазеров путем облучения кожных покровов в области травмы при лечении переломов костей плотностью потока мощности излучения до 25 мВт/см2, при времени воздействия на одно поле - до 5 мин, на курс лечения - до 15 ежедневных процедур (см. Илларионов В.Е. Основы лазерной терапии. - М. «РЕСПЕКТ», 1992 г. с.87).
Недостатком такого применения является его послеоперационное действие, не оказывающее существенного влияния на ход и качество операции.
Известно также применение в хирургии в качестве физического фактора, воздействующего на мягкие ткани во время выполнения операций, факела аргоновой плазмы, под действием которого происходит аргоноплазменная коагуляция ткани (АПК).
Под воздействием плазмы происходит локальный нагрев и коагуляция ткани, вследствие чего мелкие сосуды и капилляры сжимаются и тромбируются - осуществляется гемо- и лимфостаз, часть жидкости, содержащейся в ткани, испаряется.
АПК обычно применяют для обеспечения гемостаза рассеченных тканей и для обработки поверхностно поврежденных болезнью тканей, приводящей к замещению их здоровыми тканями, при операциях на паренхиматозных органах (см. RU 2339334 С1, 27.11.2008), в онкологии (RU 2255697 С1, 10.07.2005), в гинекологии (RU 2406458 С1, 20.12.2010).
Ограничением в применении АПК является необходимость плотного контакта нейтрального электрода из токопроводящей резины с телом пациента, рану которого обрабатывают ионизированным факелом аргона, что ограничивает применение АПК на операциях у животных, имеющих грубую кожу, покрытую шерстью, затрудняющих электрический контакт и работу аппарата, причем для обработки костной ткани и надкостницы, особенных по своему составу и морфологии от мягких тканей, такие методы ранее не применяли.
Задачей изобретения является разработка способа обработки раны надкостницы и костей при оперативном лечении переломов, в частности трубчатых костей у животных, использующего в процессе лечения многофункциональное медицинское оборудование с минимальными доработками, обеспечивающее сокращение процесса и сроков лечения при минимальных осложнениях и затратах, при повышении эффективности первичной хирургической обработки раны за счет снижения вероятности развития остеомиелита и активации остеогенеза.
Задача решается тем, что в процессе операции в качестве электрофизического воздействия на операционное поле используют факел аргоновой плазмы, по методу аргоноплазменной аблации (АПА), которым обрабатывают собранные костные и соединяющие элементы области перелома, надкостницу и окружающие ткани, при этом для проведения аргоноплазменной аблации зоны переломов используют аргонусиленный высокочастотный электрохирургический аппарат «ФОТЕК ЕА 141», оборудованный электродом для АПА при выходной мощности 35-75 Вт и расходе аргона 4-8 л/мин, в режиме «СПРЕЙ», при этом процесс обработки составляет от 1 до 5 минут, а расстояние от среза электрода до обрабатываемой поверхности выдерживают 5-15 мм, причем нейтральный электрод располагают под животным, смачивая его физиологическим раствором для обеспечения плотного электрического контакта с телом животного.
При аргоноплазменном воздействии, по сути - бесконтактном, факел аргоновой плазмы выступает сфокусированным газообразным продолжением активного электрода, что исключает микробную контаминацию и прилипание к нему ткани. Кроме того, поток аргона вытесняет кислород из зоны воздействия, препятствуя окислению (карбонизации) обрабатываемой ткани. Пучок ионизированного аргона имеет низкую теплоемкость, он не способен разогреть ткани. Таким образом, при надежной коагуляции мелких сосудов и качественном гемостазе не возникает грубого термического повреждения ткани, если сравнивать с контактной электрокоагуляцией.
Аргоноплазменная коагуляция дает также заметные преимущества клинического свойства. Одно из главных - возможность полного гемостаза на большой поверхности с созданием тонкого (около 1-2 мм) надежного струпа или слоя с минимальным риском возникновения повторных кровотечений. Именно поэтому после воздействия аргон-усиленного коагулятора разрушение и некроз ткани меньше, чем при классической электрохирургии. Итог - более быстрое заживление раны.
Благодаря инертным свойствам аргона доступ кислорода к поверхности ограничен. Поскольку аргон не поддерживает горение, не происходит обугливание в зоне обработки, а запах и дым практически отсутствуют. Более того, аргоусиленный коагулятор - безопасный инструмент, т.к. пучок аргона в нем имеет ограниченную температуру, а лен, хирургическая марля, хирургические перчатки, синтетический шовный материал из-за такой температуры не воспламеняются.
При исследовании воздействия плазменного потока аргона на возбудителей раневой инфекции ранее были получены данные о бактерицидном действии плазмы аргона на контрольные штаммы S.Aureus, E.coli и K.pneumoniae in vitro. Был также установлен выраженный бактерицидный эффект преимущественно на грамотрицательные бактерии и на биологические свойства бактерий, в основном грамположительных.
Для проведения АПК можно использовать соответствующее оборудование различных фирм, применяя рекомендации производителя по выбору режима коагуляции. В частном случае предлагается использовать аргонусиленные высокочастотные электрохирургические аппараты «ФОТЕК ЕА 141» при выходной мощности 50-75 Вт и расходе аргона 5-8 л/мин производства ООО «ФОТЕК», город Екатеринбург.
Авторы использовали аппарат «ФОТЕК ЕА141» при выходной мощности 35-75 Вт и расходе аргона 5-8 л/мин. В процессе исследований было установлено, что наилучший результат при обработке переломов костей получается при использовании режима «СПРЕЙ» (мягкая плавная аргоноплазменная аблация). Мягкий прогрев надкостницы и костей, возникающий после воздействия на нее факела аргоновой плазмы, устраняет раневой экссудат и препятствует его образованию в рассеченных тканях, предотвращая воспалительный процесс, снижая вероятность развития остеомиелита при активации остеогенеза.
Для проведения экспериментов и опытов, при оперативном вмешательстве с целью репозиции отломков костей разными способами консолидации (интрамедуллярный, чрескостный, накостный остеосинтез), применяли после репозиции отломков аргоноплазменную аблацию надкостницы по месту перелома при помощи аппарата ФОТЕК ЕА 141 в режиме «СПРЕЙ».
Животных, у которых при операции применяли аргонплазменную аблацию, считали опытными. В этой группе состояло 12 собак и 5 кошек. Контролем служили 7 собак и 3 кошки с аналогичными переломами, близкие по возрасту, полу и массе опытным, но без воздействия аргона при операции. Тестом для определения ускорения регенерации костей служили биохимические, гематологические, рентгенографические и функциональные исследования больных конечностей с фотофиксацией объектов. Исследования проводили через каждые 5 дней после операции одновременно у опытных и контрольных животных на протяжении первых 20 дней, затем через каждые 10 дней в течение месяца. Фрагменты исследований представлены ниже.
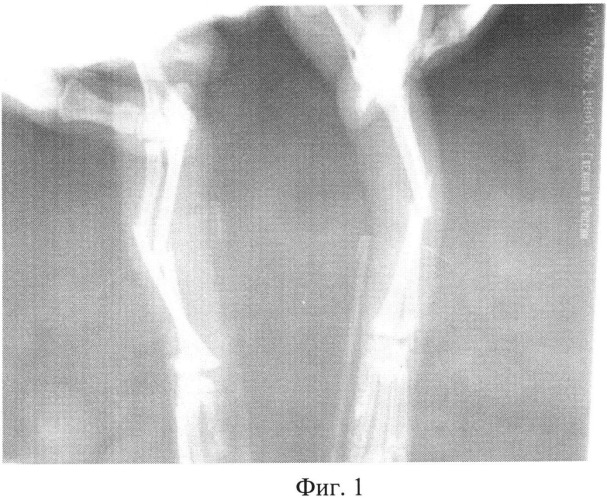
На Фиг.1 - Двусторонний перелом предплечья у кошки (рентген снимок до операции).
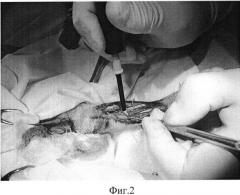
На Фиг.2 - Агроноплазменная обработка надкостницы и мягких тканей при фиксации отломков у кошки (фото).
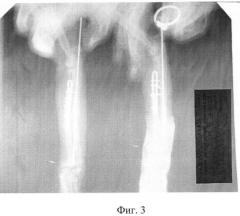
На Фиг.3 - Тот же перелом предплечья у кошки после металлостеосинтеза. Перелом правого предплечья обработан аргоном, что привело к меньшему остеолизу концов отломков.
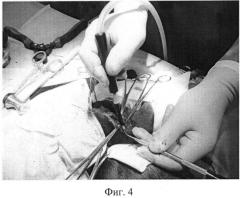
На Фиг.4 - Интрамедуллярный металлоостеосинтез бедренной кости тойтерьера с последующей аргоноплазменной обработкой надкостницы и прилежащих мягких тканей.
На Фиг.5 - Рентгенограмма предплечья тойтерьера через 2 месяца после аргоноплазменного воздействия на кость и прилежащие мягкие ткани. Наблюдается компактная костная мозоль с хорошо проявляющимся известкованием по месту перелома, что в эти сроки для данной породы собак является редкостью.
На Фиг.6 - Тот же тойтерьер, чьи рентгенграммы представлены выше. У животного проявляется двигательная активность, свойственная здоровой собаке этой породы - массой порядка 20 кг.
При интерпретации биохимических показателей установили, что в крови опытных животных активность щелочной фосфатазы была выше на 28%, трансфераз меньше на 12% по сравнению с контрольными собаками. Кальций-фосфорное отношение нормализовалось быстрее у опытных животных. Таким образом, биохимические исследования показывают на более интенсивное заживление кости у собак опытной группы.
При анализе гематологических показателей было выявлено, что уровень эритроцитов был одинаков в крови обеих групп собак и колебался от 5,5 после операции до 7,2 1012 /л к 20 дню после хирургического вмешательства. Количество лейкоцитов у опытных животных к 10 дню восстанавливалось до предоперационного уровня, тогда как у контрольных животных эта тенденция просматривалась только к 12-16 дню.
При рентгенологических исследованиях установлено (Фиг.5), что у опытных животных формирование костной мозоли по месту перелома происходило в более ранние сроки в среднем на 3-4 дня. Костная мозоль у них была более компактная с хорошо выраженными границами. У этих же животных наблюдалась ускоренная резорбция концов отломков при формировании костной мозоли. Заживление кости у опытных собак завершалось, в среднем, раньше на 5-10 дней, что позволяло снимать фиксирующие кость устройства в более ранние сроки.
Функциональные исследования заключались в визуальном определении использования конечности в движении, наличия или отсутствия хромоты (Фиг.6). При сравнении подвижности животных в наблюдаемых группах установлено, что опытные собаки меньше хромали и по времени, и по интенсивности по сравнению с контрольными собаками, что связываем с меньшими размерами костной мозоли, и снижение, в следствие этого, механического раздражения прилегающих мягких тканей.
Результаты экспериментов и опытов дали возможность прийти к однозначному выводу о возможности и эффективности аргоноплазменного воздействия для увеличения скорости регенеративных процессов в костной ткани после остеосинтеза длинных трубчатых костей у собак и кошек (Фиг.3 и Фиг.5). Учитывая, что в 100 мл воды при 20°С растворяется 3,3 мл аргона, а при электрическом возбуждении смеси аргона и хлора (получаемого из плазмы крови) возможна газофазная реакция с образованием ArCl (a возможно участие и других соединений с водородными связями), образуются соединения-включения (клатраты), где атом аргона, как своего рода «гость», находится в полости, образованной в кристаллической решетке молекулами вещества-хозяина, и, возможно, эти молекулы и являются стимуляторами регенеративных процессов в тканях организма. При этом обеспечивается профилактика развития остеомиелита и других гнойных осложнений, а также ускоряется остеогенез. Благодаря этому сокращаются сроки и повышается эффективность лечения больных животных.
1. Способ лечения переломов у животных, включающий подготовку пациента, проведение операции с применением электрофизического воздействия и послеоперационное лечение, отличающийся тем, что в процессе операции в качестве электрофизического воздействия на операционное поле, открытые кости и надкостницу используют факел аргоновой плазмы, по методу аргоноплазменной аблации (АПА), которым обрабатывают собранные костные элементы области перелома, надкостницу, соединительные элементы и окружающее операционное поле.
2. Способ лечения переломов у животных по п.1, отличающийся тем, что для проведения аргоноплазменной аблации зоны переломов используют аргонусиленный высокочастотный электрохирургический аппарат «ФОТЕК ЕА 141», оборудованный электродом для АПА при выходной мощности 35-75 Вт и расходе аргона 4-8 л/мин в режиме «СПРЕЙ», при этом процесс обработки составляет от 1 до 5 минут, а расстояние от среза электрода до обрабатываемой поверхности выдерживают 5-15 мм.
3. Способ лечения переломов у животных по п.1, отличающийся тем, что нейтральный электрод электрохирургического аппарата при лечении переломов у животных располагают под телом животного, смачивая электрод физиологическим раствором для обеспечения плотного электрического контакта с телом животного.