Молекулярная визуализация
Иллюстрации
Показать всеИзобретение относится к молекулярной визуализации. Система визуализации содержит источник излучения, которое пересекает область обследования, детектор излучения и формирования сигнала, характеризующего энергию обнаруженного излучения, селектор данных, который выполняет дискриминацию сигнала по энергии на основании относящихся к энергетическим спектрам установочных параметров, соответствующих первой и второй спектральным характеристикам контрастного вещества, введенного в субъект, и блок реконструкции сигнала на основании первой и второй спектральных характеристик и формирования данных объемного изображения, характеризующих мишень. Контрастное вещество имеет первую спектральную характеристику ослабления при присоединении к мишени и вторую отличающуюся спектральную характеристику в состоянии неприсоединения к мишени. Использование изобретения позволяет расширить объем получаемой информации о составе ткани субъекта. 9 з.п. ф-лы, 14 ил.
Реферат
Настоящее изобретение относится, в общем, к молекулярной визуализации. Хотя изобретение описано относительно конкретного применения к компьютерной томографии (CT), изобретение относится также к другим областям применения медицинской визуализации и немедицинской визуализации.
Компьютерные томографические (CT-) сканеры формируют изображения, характеризующие ослабление рентгеновского излучения исследуемым объектом. Рентгеновские трубки, применяемые в CT-сканерах, обычно генерируют рентгеновское излучение, имеющее одиночный, относительно широкий энергетический спектр. Аналогично, детекторы, используемые в данных системах, обычно обеспечивают ограниченную, если вообще обеспечивают, информацию об энергетическом спектре регистрируемого излучения. Хотя упомянутые сканеры обеспечивают ценную информацию о внутренней структуре исследуемого объекта, данные сканеры только в ограниченной степени способны обеспечивать информацию о составе материала объекта, особенно когда разные соединения характеризуются сходными коэффициентами ослабления излучения.
Так как разные соединения могут изменять спектр ослабляемого излучения различным образом, то, в качестве метода повышения потенциальных возможностей классификации материалов, предложено спектральное CT-сканирование. Идея заключается в сканировании с использованием, по меньшей мере, двух разных спектров рентгеновского излучения или в получении данных с использованием детекторов, которые обеспечивают спектральную информацию. Способность определять состав материала исследуемого объекта может иметь различные области применения. Особенно важной особенностью новых способов, предлагаемых в настоящем изобретении, является возможность надежного различения, по меньшей мере, двух материалов высококонтрастного типа, даже если упомянутые материалы одновременно присутствуют в теле.
Один метод получения данных, содержащих несколько энергетических каналов или окон, состоит в переключении напряжения рентгеновской трубки между несколькими значениями (например, 140 кВ и 80 кВ) в последовательных кадрах. Другой метод состоит в обеспечении фильтра излучения после рентгеновской трубки, при этом фильтр для последовательных кадров поочередно сменяется. В другом методе используют мультиэнергетические детекторы, например детекторы на основе нескольких сцинтилляционных слоев. В другом методе используют две независимые рентгеновские трубки и две матрицы детекторов в одном сканере. В еще одном методе используют детекторы, работающие в режиме счета фотонов, например детекторы на основе детекторов с прямым преобразованием или на основе сцинтиллятора с коротким временем высвечивания, связанного с фотодетектором с высоким коэффициентом усиления.
Один из подходов к обработке данных спектральной компьютерной томографии (CT) заключался в выполнении декомпозиции по материалам при измерениях проекций перед этапом реконструкции. Второй подход заключался в выполнении, после обработки, манипулирования с изображениями, реконструированными по каждому из энергетических окон.
Сходная аналогия имеет место в области магнитно-резонансой томографии (MRI), в которой в общем случае используют сильное магнитное поле для ориентирования ядерного намагничивания (обычно) атомов водорода в воде в теле или других подходящих элементов. Для систематического изменения ориентации упомянутого намагничивания применяют радиочастотные поля, что вынуждает ядра водорода (или других элементов) формировать вращающееся магнитное поле, регистрируемое сканером. Данным сигналом можно манипулировать посредством дополнительных магнитных полей, чтобы собрать достаточно информации для построения изображения тела и специальных контрастных материалов. MRI может также обнаруживать уникальные признаки релаксации ядерного спина относительно сильного магнитного поля. Протокол визуализации, который измеряет спин-решеточную релаксацию в направлении магнитного поля, называется T1-взвешиванием, и протокол, который измеряет спин-решеточную релаксацию перпендикулярно магнитному полю, называется T2-взвешиванием. Измерение характеристик как T1, так и T2 может способствовать более надежному различению контрастных материалов разных типов, которые совместно присутствуют в теле.
Сходная аналогия имеет место также в области радионуклидной диагностики и однофотонной эмиссионной компьютерной томографии (SPECT). Как правило, радиоактивный изотопный материал вводится в субъекта и испускает гамма-фотоны с энергетическим спектром с известными характеристиками. Детекторы излучения регистрируют упомянутые фотоны и измеряют их энергии. Можно различить, по меньшей мере, два разных типа радиофармпрепаратов, которые одновременно присутствуют в теле, если каждый радиофармпрепарат испускает фотоны с разным энергетическим спектром.
При компьютерной томографии (CT) в пациента перед сканированием вводят контрастное вещество, например внутривенное иодированное контрастное вещество, чтобы улучшить визуализацию некоторых анатомических структур (например, кровеносных сосудов) относительно других анатомических структур (например, окружающей ткани) или функциональной информации (например, кровотока) в полученном изображении. Основой контрастного вещества в компьютерной томографии (CT) обычно являются тяжелые элементы, так как их коэффициент ослабления излучения намного выше, чем коэффициент ослабления биологических тканей. Примеры других, часто используемых контрастных веществ содержат контрастные вещества на основе бария, сульфата бария, гастрографина и гадолиния. Предложены другие контрастные материалы на основе более тяжелых элементов, например золота и висмута. Для более специфических структур, например опухолей, бляшек или тромбозов, последней тенденцией было применение контрастных веществ направленного действия. Упомянутые вещества предназначены для накопления в заданной биологической мишени, которая может указывать на конкретные функциональные, анатомические или медицинские состояния. Как было показано, разнотипные контрастные материалы, применяемые совместно в одном субъекте, могут быть различены и могут указывать на разные физиологические функции во время одного сканирования, когда используют спектральную компьютерную томографию (CT).
К сожалению, какая-то часть контрастного материала также распределяется и/или накапливается в других областях тела, где мишень отсутствует. Например, при использовании контрастных веществ направленного действия, которые содержат наночастицы тяжелых элементов, частицы обычно захватываются макрофагами, которые не имеют отношения к мишени. В результате полученное изображение может содержать высококонтрастный фоновый шум и/или ложно положительные участки накопления. Другой недостаток упомянутых веществ состоит в том, что время циркуляции может быть продолжительным, пока упомянутые вещества не вымываются, и контрастное вещество не остается, по существу, только в сайтах-мишенях. Другая возможная проблема состоит в том, что концентрация в сайтах-мишенях или концентрация структурных элементов контрастного вещества, присоединенных к сайтам-мишеням, может быть недостаточно высокой для функциональной молекулярной визуализации вследствие практических ограничений устройства медицинской визуализации.
Аспекты настоящей заявки относятся к вышеупомянутым и другим вопросам.
В соответствии с одним аспектом система визуализации содержит источник излучения, который излучает излучение, которое пересекает область обследования, и детектор, который регистрирует излучение, пересекающее область исследования и субъекта, расположенного в данной области, и формирует сигнал, характеризующий энергию зарегистрированного излучения. Селектор данных выполняет дискриминацию сигнала по энергии на основании относящихся к энергетическим спектрам установочных параметров, соответствующих первой и второй спектральным характеристикам контрастного вещества, введенного в субъект, при этом контрастное вещество имеет первую спектральную характеристику ослабления при присоединении к мишени и вторую отличающуюся спектральную характеристику в состоянии неприсоединения к мишени. Блок реконструкции реконструирует сигнал на основании первой и второй спектральных характеристик и формирует данные объемного изображения, характеризующие мишень.
В соответствии с другим аспектом способ содержит этап обнаружения биохимического компонента в биологической пробе посредством изменения спектра ослабленного рентгеновского излучения биохимического компонента или синтетического компонента, присоединенного к нему, при посредстве гибридизационной цепной реакции олигонуклеотидных структур, включающих в себя, по меньшей мере, две разных наночастицы, имеющих разные спектральные характеристики ослабления рентгеновского излучения.
В соответствии с другим аспектом способ содержит этап обнаружения биохимического компонента в биологической пробе посредством изменения сигнала ядерного магнитного резонанса биохимического компонента или синтетического компонента, присоединенного к нему при посредстве гибридизационной цепной реакции олигонуклеотидных структур с участием, по меньшей мере, двух разных наночастиц, имеющих разные отклики ядерного магнитного резонанса.
В соответствии с другим аспектом способ содержит этап обнаружения биохимического компонента в биологической пробе посредством изменения средней энергии гамма-фотонов, излучаемых при радиоактивном распаде, при посредстве гибридизационной цепной реакции олигонуклеотидных структур с участием, по меньшей мере, двух разных радиоактивных частиц.
В соответствии с другим аспектом способ содержит контрастный материал, который можно обнаружить с помощью средства визуализации, при этом контрастный материал самопроизвольно изменяет, по меньшей мере, одну регистрируемую характеристику, когда контрастный материал связывается со специфической биологической мишенью.
В соответствии с другим аспектом способ содержит этап введения в субъекта, подлежащего сканированию, зонда, содержащего область прицельного связывания, которая связывается только с выбранной биологической мишенью, и область инициатора, доступную для гибридизации, когда зонд связывается со специфической мишенью. Дополнительно вводят в субъекта, по меньшей мере, два мономерных компонента HCR (т.е. вступающих в гибридизационную цепную реакцию (HCR)), которые полимеризуются в процессе цепной реакции с инициатором, когда область инициатора становится доступной для взаимодействия, и вводят в субъекта, по меньшей мере, один компонент, содержащий две конъюгированных разных частицы, каждая из которых выполнена из разных материалов, при этом каждая из частиц показывает отличающийся отклик в данных сканирования, и только первая частица остается гибридизированной с полимеризованным комплексом HCR (полученным в результате гибридизационной цепной реакции (HCR)), а вторая частица отделяется от полимеризованного комплекса HCR. Способ дополнительно содержит этап выполнения сканирования с использованием устройства визуализации, которое регистрирует пространственные и временные характеристики концентраций двух разных частиц, и этап формирования информации, которая отражает агрегацию двух разных материалов, на основании данных сканирования. В настоящем тексте термин «олигонуклеотидная структура» имеет такое же значение, как термин «мономер HCR» или просто «мономер».
В соответствии с другим аспектом способ содержит этап введения вещества, которое содержит множество молекулярных структурных элементов метастабильных мономеров HCR, по меньшей мере, двух разных типов, при этом мономер, по меньшей мере, одного из типов конъюгирован с двумя разными наночастицами, причем первая наночастица остается присоединенной к сформированному комплексу-продукту полимеризации по HCR, и вторая наночастица отделяется от комплекса в результате процесса HCR, и относительные концентрации двух наночастиц обнаруживаются на основании спектральных характеристик ослабленного рентгеновского излучения.
В соответствии с другим аспектом способ содержит этап введения вещества, которое содержит множество молекулярных структурных элементов метастабильных мономеров HCR, по меньшей мере, двух разных типов, при этом мономер, по меньшей мере, одного из типов конъюгирован с двумя разными наночастицами, причем первая наночастица остается присоединенной к сформированному комплексу-продукту полимеризации по HCR, и вторая наночастица отделяется от комплекса в результате процесса HCR, и относительные концентрации двух наночастиц обнаруживаются на основании характеристик ядерного магнитного резонанса.
В соответствии с другим аспектом способ содержит этап введения вещества, которое содержит множество молекулярных структурных элементов метастабильных мономеров HCR, по меньшей мере, двух разных типов, при этом мономер, по меньшей мере, одного из типов конъюгирован с двумя разными радиоактивными частицами, причем первая частица остается присоединенной к сформированному комплексу-продукту полимеризации по HCR, и вторая частица отделяется от комплекса в результате процесса HCR, и относительные концентрации двух радиоактивных частиц обнаруживаются на основании энергий излучаемых гамма-фотонов посредством гамма-камеры.
Дополнительные аспекты настоящего изобретения станут понятными специалистам со средним уровнем компетентности в данной области техники после прочтения и изучения нижеприведенного подробного описания.
Изобретение может осуществляться с использованием различных компонентов и схем расположения компонентов и различных этапов и схем расположения этапов. Чертежи предназначены только для иллюстрации предпочтительных вариантов осуществления и не подлежат истолкованию в смысле ограничения изобретения.
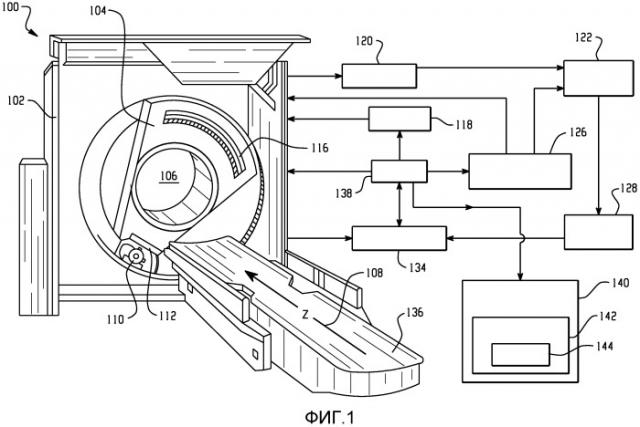
Фигура 1 - система визуализации.
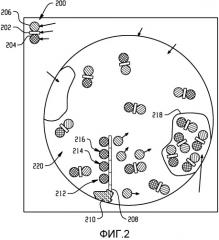
Фигура 2 - примерное контрастное вещество, которое изменяет свои спектральные свойства при присоединении к мишени.
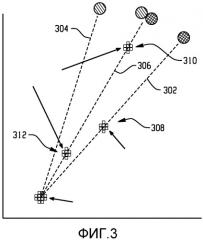
Фигура 3 - кривые ослабления рентгеновского излучения контрастного вещества, показанного на фигуре 2.
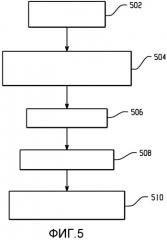
Фигуры 4-6 - примеры способов.
Фигуры 7-14 - другие примеры контрастных веществ.
На фигуре 1 представлена система 100, которая содержит по существу стационарный гентри 102 и поворотный гентри 104, который установлен с возможностью поворота в стационарном гентри 102. Поворотный гентри 104 поворачивается вокруг области 106 исследования вокруг продольной или z-оси 108. Рентгеновский источник 110, например рентгеновская трубка, установлен на поворотном гентри 104 и испускает излучение. Коллиматор 112 коллимирует пучок излучения для формирования, в общем, конического, веерного, клиновидного или имеющего другую форму пучка излучения, который пересекает область 106 исследования. Детекторная решетка 116, чувствительная к излучению, регистрирует фотоны, которые пересекают область 106 исследования. Показанный детектор 116 является детектором с энергетическим разрешением, например детектором с прямым преобразованием (например, Si, Ge, GaAs, CdTe, CdZnTe и т.п.) или сцинтилляционным детектором, который содержит сцинтиллятор, оптически связанный с фотоприемником, или упомянутый детектор может быть многослойным сцинтилляционным детектором. В альтернативном варианте детектор может не иметь энергетического разрешения, и рентгеновский источник может быть переключаемым между разными спектрами излучения. Детектор 116 формирует электрический сигнал, например электрические токи или напряжения, для каждого регистрируемого рентгеновского фотона или совокупности принятых рентгеновских фотонов в пределах заданного дискретного отсчета.
Инъектор 118 выполнен с возможностью инъекции или введения контрастного вещества в объект или субъекта для сканирования. В альтернативном варианте контрастные вещества могут быть введены вручную врачом или подобным специалистом. Подходящее контрастное вещество содержит контрастное вещество, которое изменяет свою спектральную характеристику ослабления рентгеновского излучения, когда контрастное вещество присоединяется к мишени. Контрастное вещество позволяет отличать накопление контрастного вещества в мишени, фоновое контрастное вещество и накопление контрастного вещества в области, отличающейся от мишени. Как подробно описано ниже, пример упомянутого контрастного вещества содержит контрастное вещество, основанное на биосенсорных методиках, использующих гибридизационные цепные реакции (HCR), и взаимодействии с наночастицами. Примеры подходящих наночастиц содержат, без ограничения, йод и висмут. В одном примере подобное вещество основано на синтезированных молекулах (мономерах ДНК), которые полимеризируются по типу цепной реакции только в случае, когда связываются со специфической мишенью. Данное вещество способствует повышению специфичности обнаружения и позволяет проводить при обнаружении амплификацию на мишени, что повышает чувствительность.
Блок 120 приема данных получает электрические сигналы и формирует поток данных, характеризующих интенсивности и энергетические спектры зарегистрированного излучения. Селектор 122 данных выполняет селекцию полученных данных для их представления в виде наборов искомых энергетических спектров, например предварительно заданных энергетических окон для дальнейшей обработки. Контроллер 126 энергетических спектров устанавливает настраиваемые характеристики искомых энергетических спектров либо в приемной системе, либо в источнике излучения. Контроллер 126 энергетических спектров можно использовать для установки, по меньшей мере, двух энергетических окон или для установки излучаемого излучения в соответствии с характеристиками ослабления наночастиц в контрастном веществе, что может повышать чувствительность в сравнении с конфигурацией, в которой энергетические спектры устанавливают иначе. Процессор 128 данных дополнительно обрабатывает тербуемым образом данные перед реконструкцией. Блок 134 реконструкции изображений селективно реконструирует выделенные сигналы на основании спектральных характеристик для формирования изображений или другой информации, характеризующей сканированный объект.
Опора 136 объекта, например стол, служит опорой для пациента или другого объекта в области 106 исследования. Опора 136 объекта является перемещаемой для ориентации объекта относительно области 106 исследования для выполнения процедуры сканирования. Универсальный компьютер выполняет функцию пульта 138 оператора. Пульт 138 содержит читаемое человеком устройство вывода, например монитор или дисплей, и устройство ввода, например клавиатуру и мышь. Резидентное программное обеспечение пульта 138 позволяет оператору взаимодействовать со сканером 100 посредством графического пользовательского интерфейса (GUI) или иным способом. Упомянутое взаимодействие может содержать выбор подходящего протокола сканирования с учетом введенного контрастного вещества, например с учетом наночастиц, содержащихся в контрастном веществе, настройку порогов дискриминации по энергии, соответствующих контрастному веществу, и т.п.
Процессорный компонент 140 может обрабатывать данные проекций и/или изображений, сформированные сканером 100. В приведенном примере процессорный компонент 140 показан отдельно от сканера 100 и может быть частью рабочей станции, компьютера или подобного устройства. Процессорный компонент 140 может быть расположен в месте расположения сканера 100 (как показано) или удален от сканера, включая компонент системы распределенной обработки данных и т.п. В другом варианте осуществления процессорный компонент 140 входит в состав пульта 138. Показанный процессорный компонент 140 содержит банк 142 инструментальных средств, который содержит, по меньшей мере, одно инструментальное средство 144 для обработки проекции и/или данных изображений. Ниже приведено несколько примеров подходящей обработки данных. Следует понимать, что нижеприведенные примеры приведены только с целью пояснения и не являются ограничивающими.
По меньшей мере, одно из инструментальных средств 144 может различать, по меньшей мере, две наночастицы в контрастном веществе по спектральным свойствам. Кроме того, по меньшей мере, одно из инструментальных средств 144 может вычислять отношение между коэффициентами ослабления, по меньшей мере, двух наночастиц и/или абсолютные значения, по меньшей мере, одной из наночастиц в, по меньшей мере, двух разных локализациях в сканируемом объекте или субъекте, например пациенте, биологической пробе и т.п. Результаты могут представляться на предварительно калиброванной шкале в единицах Хаунсфилда и/или иным способом. При использовании гибридизационной цепной реакции (HCR) с конечным дендритным ростом, для определения количественной оценки сайтов прицельного связывания можно использовать заранее известный коэффициент, который зависит от числа составляющих поколений. По меньшей мере, одно из инструментальных средств 144 может указывать начальное время, когда был обнаружен процесс гибридизационной цепной реакции (HCR).
По меньшей мере, одно из инструментальных средств 144 может оценивать и представлять уровень достоверности для оценки разных элементов. Данная операция может содержать оценку локальной и общей концентраций или количеств биологических сайтов прицельного связывания. По меньшей мере, одно из инструментальных средств 144 может автоматически оценивать материал направленного действия и, следовательно, биологические сайты прицельного связывания. Данная операция может содержать использование анатомической априорной информации. Например, если предполагается, что материал направленного действия находится в конкретных органах, но не в других органах, данную информацию можно взвешивать при вычислении уровней достоверности. По меньшей мере, одно из инструментальных средств 144 может вычислять скорость изменения, относительную и/или абсолютную, наличия наночастиц на изображениях, полученных последовательными или перфузионными сканированиями. Упомянутую информацию можно представлять различными способами, например в численной форме, визуально посредством полутонов и/или цветными накладными изображениями и/или изменениями полупрозрачных цветных накладных изображений.
Видоизменения и другие варианты осуществления.
В одном случае контрастное вещество содержит, по меньшей мере, два материала, имеющих K-край поглощения. В контексте настоящей заявки материалом, имеющим K-край поглощения, называют материал, содержащий тяжелый элемент с энергией K-края в пределах диапазона энергетического спектра излучения, которое применяют при CT-визуализации. Например, одна из наночастиц может содержать материал, имеющий K-край поглощения с энергией в диапазоне 25-55 кэВ, например серебро, индий, йод, барий, гадолиний и т.п., и другая наночастица может содержать материал, имеющий K-край поглощения с энергией в диапазоне 65-95 кэВ, например вольфрам, платину, золото, таллий, висмут и т.п. В приведенном случае контроллер 126 энергетических спектров можно применять для установки и оптимизации соответствующих энергетических спектров, либо излучаемых, либо регистрируемых, в соответствии с энергией K-края. Примеры подходящих материалов содержат, без ограничения, серебро, индий, йод, барий, гадолиний, вольфрам, платину, золото, таллий и висмут.
Следует также понимать, как уже упоминалось, что в качестве дополнения или альтернативы также применимы другие средства визуализации. При использовании отличающегося средства, контрастное вещество содержит наночастицы или другие частицы, соответствующие конкретным средствам визуализации.
В качестве неограничивающего примера, при визуализации методом MRI, одна из частиц может быть на основе гадолиния, который влияет, главным образом, на T1, и вторая частица может быть на основе оксида железа, который влияет, главным образом, на T2. Две разные частицы можно различать подходящим методом MRI, который измеряет и взвешивает как характеристики T1, так и T2. Например, в одном случае частицы можно различать методом объединения измерений T1 и T2, при котором визуализация в режиме T1 выявляет одно известное свойство магнитного резонанса, и визуализация в режиме T2 выявляет другое известное свойство. Для выявления характеристик T1 и/или T2 можно использовать различные последовательности. Возможно также выполнение комбинированной последовательности. Другой возможный вариант состоит в применении двух разных контрастных элементов, которые оба обладают характеристиками T1 или, в альтернативном варианте, оба обладают характеристиками T2, при этом отклики T1 или отклики T2 являются в подходящей степени разными и различимыми. Примеры подходящих материалов содержат, без ограничения, гадолиний и оксид железа.
В случае радионуклидной диагностики частицы могут быть изготовлены из двух разных радиоактивных изотопов, которые пригодны для регистрации гамма-камерой и SPECT (однофотонным эмиссионным компьютерным томографом). Например, одна частица может быть на основе радиоактивного Tc99m, который излучает, в основном, 140-кэВ гамма-фотоны, и вторая частица может быть на основе Tl-201, который излучает, в основном, 70-кЭв гамма-фотоны. Два компонента можно различать известными методами двухизотопной ядерной медицины. Например, было показано, что двухизотопное сканирование является удобным способом радионуклидной диагностики сердца для оценки функций в покое и под нагрузкой, посредством использования радиоактивных изотопов Tc99m и Tl-201. Возможно также использование некоторых других изотопов, которые широко применяются при однофотонной эмиссионной радионуклидной диагностике.
Применительно к флуоресцентной и/или комбинационной спектроскопии, и/или другим методам оптической визуализации, частицы могут иметь разные оптические отклики, при этом каждый оптический отклик находится в отличающемся спектральном диапазоне. Относительные интенсивности спектров могут определяться оптическими средствами.
Как кратко отмечено выше, подходящее контрастное вещество содержит контрастное вещество, которое изменяет свою спектральную характеристику ослабления рентгеновского излучения, когда контрастное вещество присоединятся к мишени, включая контрастное вещество, основанное на HCR. HCR является способом инициированной гибридизации по типу цепной реакции синтезированных молекул нуклеиновых кислот (аналогичных элементам строения биологической ДНК или РНК). Процесс начинается со специальных метастабильных структур нуклеиновых кислот, которые изменяют форму и связываются между собой в процессе актов цепной реакции только при первоначальном инициировании уникальной инициаторной нитью нуклеиновой кислоты. Инициаторная нить становится доступной для гибридизации, только когда она связывается со специфической биологической мишенью, обычно, через другую молекулу-зонд.
Вышеупомянутый контрастный материал может содержать контрастное вещество, в котором первоначально соединены два разных биохимических компонента или наночастицы, и только когда происходит связывание посредством цепной реакции со специфической мишенью, одна из наночастиц высвобождается из гибридизированного компонента в окружающую среду. В результате спектральная характеристика ослабления рентгеновского излучения контрастного вещества изменяется, и высвободившаяся наночастица не влияет на спектральную характеристику ослабления рентгеновского излучения области мишени. Вышеизложенное поясняется со ссылками на фигуры 2 и 3.
Как показано на фигуре 2, контрастное вещество содержит структуру 200 с первым компонентом 202 HCR и первой и второй наночастицами 204, 206, присоединенными к нему. Первая наночастица 204 имеет первую спектральную характеристику ослабления рентгеновского излучения, вторая наночастица 206 имеет вторую спектральную характеристику ослабления рентгеновского излучения, и комбинация наночастиц 204, 206, присоединенных к компоненту 202 HCR, имеет третью спектральную характеристику ослабления рентгеновского излучения. Данная особенность показана в связи с фигурой 3, на которой по y-оси представлено ослабление изображение в низкоэнергетическом окне (в единицах Хаунсфилда (HU)), и по x-оси показано ослабление изображения в высокоэнергетическом окне (в единицах Хаунсфилда (HU)). Первая кривая 302 представляет спектральную характеристику первой наночастицы 204; вторая кривая 304 представляет спектральную характеристику второй наночастицы 206; и третья кривая 306 представляет спектральную характеристику комбинации наночастиц 204, 206.
Как показано на обеих фигурах 2 и 3, часть структуры 200 присоединяется к инициатору 208, присоединенному к специфической мишени 210, как указано позицией 212. Некоторые дополнительные структуры 200 присоединяются к структуре 200, уже присоединенной к мишени 210, либо непосредственно, как указано позицией 214, либо косвенно, как показано позицией 216. Когда структура 200 присоединяется сама по себе, одна из наночастиц, например наночастица 206 высвобождается, и спектральная характеристика ослабления рентгеновского излучения следует первой кривой 302, как указано позицией 308. В приведенном примере в относительно высокой концентрации структуры 200 захватываются макрофагом 218 и в относительно низкой концентрации структуры 200 циркулируют в крови 220. Высвободившиеся наночастицы 206 также могут быть захвачены макрофагом 218 или циркулировать в крови 220. Спектральная характеристика отделившейся наночастицы 206 следует кривой 304, и спектральная характеристика нереагирующей структуры 200 следует кривой 306, включая структуру 200 в макрофагах 218, как показано позицией 310, и структуру 200, циркулирующую в крови 220, как показано позицией 312.
По существу, можно повысить специфичность обнаружения. Кроме того, полимеризация может развиваться линейно или экспоненциально и продолжаться, в принципе, пока доступен запас новых структур 200, или до тех пор, пока не вводят компонент, прерывающий реакцию. По существу, можно повысить чувствительность обнаружения.
Ниже приведено описание различных способов. Следует понимать, что описанные здесь этапы не ограничивают настоящее изобретение. По существу, в других вариантах осуществления порядок этапов может отличаться. Кроме того, другие варианты осуществления могут содержать большее или меньшее число этапов.
На фигуре 4 показан первый способ. На этапе 402, в объект или субъекта вводят молекулярный зонд. В одном случае молекулярный зонд содержит как область прицельного связывания, предназначенную для специфического связывания с выбранной биологической мишенью, так и область инициатора HCR, которая доступна для гибридизации, когда зонд связывается со специфической мишенью. Зонд может быть молекулой, которая может обнаруживать специфическую мишень и связываться с ней. Например, зонд может быть пептидом, аптамером, антителом или его фрагментами, нуклеотидной нитью или небольшой молекулой с нитью ДНК инициатора HCR, присоединенной к упомянутой молекуле и становящейся доступной для взаимодействия, когда зонд присоединяется к искомой мишени. На этапе 404, в объект или субъекта вводят мономерный компонент HCR. В одном случае мономерный компонент HCR может полимеризоваться по типу цепной реакции после инициирования нитью инициатора, доступной для взаимодействия.
На этапе 406, в объект или субъекта вводят контрастное вещество, содержащее структуру, содержащую, по меньшей мере, две частицы с разными спектральными характеристиками. Упомянутое вещество может изменять свои спектральные характеристики, как поясняется в настоящей заявке, например таким образом, что упомянутое вещество имеет одну спектральную характеристику, при присоединении к инициатору, и другую в состоянии неприсоединения к инициатору. Следует понимать, что контрастное вещество можно объединять с одним из мономеров HCR, или контрастное вещество может быть дополнительным компонентом, независимым от мономеров HCR. На этапе 408, объекта или субъекта сканируют, и полученные данные проекций реконструируют для формирования данных изображений. По желанию, на этапе 410, в пациента можно ввести прерыватель реакции для прерывания дальнейшей реакции HCR. Прерыватель реакции вводят по истечении предварительно заданного интервала времени, после специального указания от данных изображений или иначе. На этапе 412, формируют изображения по данным изображений. Данный способ может дополнительно повышать специфичность и чувствительность обнаружения.
На фигуре 5 изображен другой способ. На этап 502, в объект или субъекта вводят инициатор-зонд. На этапе 504, после подходящего времени задержки, обеспечивающего присоединение инициатора к сайту-мишени, в объект или субъекта вводят контрастное вещество, которое содержит компоненты HCR с наночастицами, как изложено в настоящем описании. В одном случае время задержки имеет значение порядка минут, часов и т.п. В другом случае, например, когда инициатор может быть доступен для взаимодействия только тогда, когда зонд присоединяется к сайту-мишени, инициатор и контрастное вещество можно вводить одновременно. На этапе 506, после подходящего времени задержки для обеспечения агрегирования контрастного вещества в сайте-мишени, сканируют объект или субъекта. По желанию, на этапе 508 можно вводить прерыватель реакции. На этапе 510 обрабатываются полученные данные изображения. Обработка может содержать ручной и/или автоматический анализ с использованием алгоритмических и/или программных инструментальных средств, с получением на выходе клинической, физиологической и/или функциональной информации об объекте или субъекте. Упомянутую информацию можно сохранять и/или различным образом представлять врачу. Упомянутый способ может повышать специфичность и чувствительность обнаружения.
На фигуре 6 изображен другой способ. На этапе 602, в объект или субъекта вводят инициатор-зонд. На этапе 604, после подходящего времени задержки, в объект или субъекта вводят контрастное вещество, которое содержит компоненты HCR с наночастицами, как изложено в настоящем описании. На этапе 606, после подходящего времени задержки, объект или субъекта сканируют. На этапе 608 выполняется определение, следует ли выполнять другое сканирование. Если следует, то на этапе 610 выполняется определение, следует ли еще вводить контрастное вещество. Если следует, то повторяют этапы 604-608. Если не следует, то повторяют этапы 606-608. Если дополнительных сканирований выполнять не требуется, то на этапе 612, по желанию, можно ввести прерыватель реакции. Полученные данные изображений обрабатываются и представляются после каждого сканирования и/или после процедуры в виде отдельной и/или суммарной информации сканирований. В одном неограничивающем примере приведенный способ позволяет контролировать изменения во времени и/или идентифицировать время, с которого начинается процесс HCR, например, для определения, когда вводить прерыватель реакции.
Следует понимать, что в связи с отслеживанием фармацевтического препарата, например отслеживанием активирования и/или функционирования лечебного средства (например, для химиотерапии и т.п.) и/или других лекарств, можно применить другие способы. При этом, лекарственные компоненты могут делать нить инициатора HCR доступной для взаимодействия, когда лекарство активируется, или когда лекарство осуществляет свое искомое физиологическое взаимодействие. При необходимости, введение лечебного средства в пациента можно выполнять на первом этапе последовательности клинической процедуры. Нить инициатора может быть частью лечебного средства, или нить инициатора может быть введена на следующем этапе в том случае, если нить инициатора связана с другим компонентом, который прицельно связывается с лекарственным компонентом. При выполнении последовательных сканирований, в пациента можно вводить, по меньшей мере, дополнительные фармацевтические препараты, например, на основании показаний из визуализирующих сканирований и/или по другим показаниям. Благодаря э