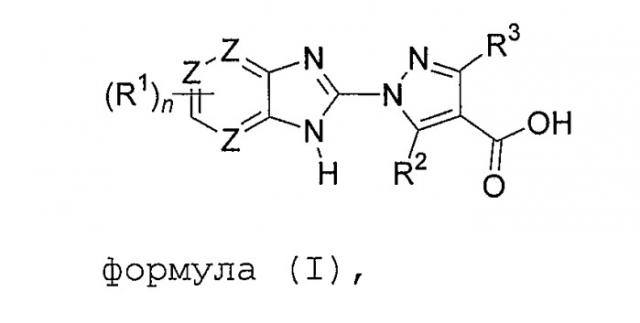
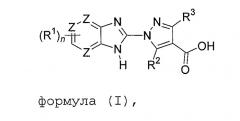
Бензоимидазолы как ингибиторы пролилгидроксилазы
Иллюстрации
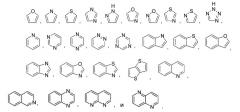
Показать всеИзобретение относится к области органической химии, а именно к производным бензоимидазола формулы (I), а также к их энантиомерам, диастереоизомерам, рацематам и фармацевтически приемлемым солям, где n равно от 2 до 4, каждый из заместителей R1 независимо выбирают из Н, галогена, -С1-4алкила, -С1-4пергалоалкила, трифтор-С1-4алкокси, -NO2, -CN, СО2Н, -ОС1-4алкила, -SC1-4алкила, -S(С1-4алкил)-Rc, -S(O)2(С1-4алкил)-Rc, -S(О)-С1-4алкила, -SO2-С1-4алкила, -S-Rc, -S(O)-Rc, -SO2-Rc, -SO2-NH-Rc, -O-Rc, -CH2-O-Rc, -С(O)NH-Rc, -NRaRb, бензилокси, фенила, необязательно замещенного одним-двумя Rd, цианобифенил-4-илметилсульфанила, цианобифенил-4-илметансульфонила, или -S-(СН2)2-морфолина и две смежные группы R1 могут соединяться с образованием ароматического 5-6-членного кольца, необязательно замещенного одной метильной группой или двумя атомами галогена, необязательно содержащего один или два S или N; Ra и Rb каждый независимо представляет собой Н, С1-4алкил, -C(O)C1-4алкил, -С(O)-Rc, -C(O)CH2-Re, C1-4алкил-Re, -SO2-Rc, -SO2-C1-4алкил, фенил, бензил; или же Ra и Rb вместе с атомом азота, с которым они соединены, образуют моноциклическое 5-6-членное гетероциклоалкильное кольцо, необязательно содержащее один гетероатом, выбранный из О; Rc представляет собой -C3-8циклоалкил, фенил, необязательно замещенный одним-двумя Rd, бензил, необязательно замещенный одним-тремя Rd; морфолин; Rd независимо представляет собой галоген, -OH, -C1-4алкил или -C1-4пергалогеналкил, трифтор C1-4алкокси, -OC1-4алкил, или -O-бензил, необязательно замещенный галогеном; Re представляет собой -C6гетероциклоалкил, необязательно содержащий один или два атомов O или N, необязательно замещенный метильной группой; R2 и R3 оба представляют собой H, -CF3 или C1-3алкил; каждый из Z представляет собой атом C или атом N, при условии что одновременно не более двух Z представляют собой N. Также изобретение относится к конкретным соединениям, фармацевтической композиции на основе соединения формулы (I) или конкретного указанного соединения, способу лечения заболеваний, опосредованных активностью пропилгидроксилазы. Технический результат: получены новые производные бензимидазола, обладающие ингибиторной активностью в отношении PHD. 6 н. и 5 з.п. ф-лы, 1 табл., 186 пр.
Реферат
Область изобретения
Настоящее изобретение относится к определенным соединениям бензоимидазола, содержащим их фармацевтическим композициям и способам их применения для лечения заболеваний, расстройств и состояний, опосредованных активностью пролилгидроксилазы.
Предпосылки создания изобретения
Клетки отвечают на гипоксию активацией считывания информации генов, участвующих в выживании клетки, доставке и использовании кислорода, развитии кровеносных сосудов, клеточном метаболизме, регулировании кровяного давления, гематопоэзе и сохранении ткани. Факторы HIF (факторы, индуцируемые гипоксией) являются основными транскрипционными регуляторами этих генов (Semenza et al., 1992, Mol Cell Biol., 12(12):5447-54; Wang et al., 1993, J Biol Chem., 268(29):21513-18; Wang et al., 1993, Proc Natl Acad Sci., 90:4304-08; Wang et al., 1995, J Biol Chem., 270(3):1230-37). Описаны три формы HIF-α: HIF-1α, HIF-2α и HIF-3α (Scheuermann et al., 2007, Methods Enzymol., 435:3-24). Конъюгация субъединицы HIFα с HIF-1β образует функциональный гетеродимерный протеин, который, в свою очередь, вовлекает другие транскрипционные факторы, такие как p300 и CBP (Semenza, 2001, Trends Mol Med., 7(8):345-50).
Семейство высококонсервативных кислород-, железо- и 2-оксоглутарат-зависимых энзимов пролилгидроксилазы (PHD) являются промежуточным звеном реакции клеток на гипоксию посредством посттрансляционной модификации HIF (Ivan et al., 2001, Science, 292:464-68; Jaakkola et al., 2001, Science, 292:468-72). В условиях нормального снабжения кислородом PHD катализирует гидроксилирование двух консервативных групп пролина в HIF. Протеин фон Гиппеля-Линдау (VHL) избирательно связывается с гидроксилированным HIF. Связывание VHL превращает HIF в мишень для полиубиквитинилирования комплексом E3 убиквитин-лигазы и его последующего разложения протеосомой 26S (Ke et al., 2006, Mol Pharmacol. 70(5):1469-80; Semenza, Sci STKE., 2007, 407(cm8):1-3). Так как сродство PHD к кислороду находится в физиологическом диапазоне кислорода, а кислород является необходимым сопутствующим фактором реакции, PHD инактивируется при снижении давления кислорода. Таким образом, HIF быстро распадается при нормальных условиях снабжения кислородом, но аккумулируется в клетках при гипоксических условиях или ингибировании PHD.
Описаны четыре изотопа PHD: PHD1, PHD2, PHD3 и PHD4 (Epstein et al., 2001, Cell, 107:43-54; Kaelin, 2005, Annu Rev Biochem., 74:115-28; Schmid et al., 2004, J Cell Mol Med., 8:423-31). Различные изотопы находятся повсюду, но регулируются различным образом и играют особые физиологические роли в реакции клеток на гипоксию. Очевидно, что эти различные изотопы имеют разную селективность по отношению к трем разным подтипам HIF (Epstein et al., см. выше). С точки зрения внутриклеточной локализации, PHD1 относится, главным образом, к ядру, PHD2 - к цитоплазме, а PHD3, по-видимому, относится как к ядру, так и к цитоплазме (Metzen E, et al. 2003, J Cell Sci., 116(7):1319-26). PHD2, по-видимому, является доминирующей HIFα пролилгидроксилазой при нормальных условиях снабжения кислородом (Ivan et al., 2002. Proc Natl Acad Sci. USA, 99(21):13459-64; Berra et al., 2003, EMBO J., 22:4082-90). Три изотопа имеют высокую степень аминокислотной гомологии, а активный центр энзима является высококонсервативным.
Продукты целевого для HIF гена участвуют в ряде физиологических и патофизиологических процессов, включая, помимо прочего, следующие: эритро(цито)поэз, развитие кровеносных сосудов, регулирование энергетического обмена, вазомоторная деятельность и апоптоз/разрастание клеток. Первым описанным как целевой для HIF геном был ген, кодирующий эритропоэтин (ЭПО) (Wang et al., 1993, см. выше). Было показано, что снижение кислородопереносной функции крови воспринимается почками и что почки и печень отвечают на это выработкой большего количества ЭПО - гормона, который стимулирует разрастание и созревание эритроцитов. ЭПО оказывает разностороннее воздействие на некроветворные типы клеток и выступает в роли основного органопротективного цитокина (Arcasoy, 2008, Br J Haematol., 141:14-31). Следовательно, ЭПО участвует в процессах заживления ран и развития кровеносных сосудов, а также в реакции тканей на ишемический инсульт. Большинство энзимов, вовлеченных в анаэробный гликолиз, кодированы целевыми генами HIF, в результате чего гликолиз усиливается в гипоксических тканях (Shaw, 2006, Curr Opin Cell Biol., 18(6):598-608). Известные продукты целевого для HIF гена в этом пути метаболизма включают, помимо прочего, следующие: переносчики глюкозы, такие как GLUT-1 (Ebert et al., 1995, J Biol Chem., 270(49):29083-89), энзимы, участвующие в превращении глюкозы в пируват, такие как гексокиназа и фосфоглицераткиназа 1 (Firth et al., 1994, Proc Natl Acad Sci. USA, 91:6496-6500), а также лактатдегидрогеназа (Firth et al., см. выше). Продукты целевого гена HIF также участвуют в регулировании клеточного метаболизма. Например, киназа пируватдегидрогеназы-1 является продуктом целевого гена HIF и регулирует поступление пирувата в Цикл Кребса, снижая активность пируватдегидрогеназы путем фосфорилирования (Kim et al., 2006, Cell Metab., 3:177-85; Papandreou et al., 2006, Cell Metab., 3:187-197). Продукты целевого гена HIF также участвуют в процессе развития кровеносных сосудов. Например, сосудистый эндотелиальный фактор роста (VEGF) (Liu et al., 1995, Circ Res., 77(3):638-43) - это известный регулятор процесса развития кровеносных сосудов, а также образования и развития сосудов (васкулогенез). Продукты целевого гена HIF также выполняют определенные функции в регулировании сосудистого тонуса и включают гемоксигеназу-1 (Lee et al., 1997, J Biol Chem., 272(9):5375-81). Ряд регулируемых HIF генных продуктов, таких как тромбоцитарный (PDGF) (Yoshida et al., 2006, J Neurooncol., 76(1):13-21), сосудистый эндотелиальный фактор роста (Breen, 2007, J Cell Biochem., 102(6):1358-67) и ЭПО (Arcasoy, см. выше), также участвуют в согласованной реакции при заживлении раны.
Намеченное нарушение активности энзима пролилгидроксилазы (PHD) с помощью маленьких молекул потенциально полезно для лечения расстройств восприятия и распределения кислорода. Примеры включают, помимо прочего, следующее: анемию; менискоцитарную анемию; болезнь периферических сосудов; ишемическую болезнь сердца; сердечную недостаточность; защиту тканей от ишемии в таких условиях, как ишемия миокарда, инфаркт миокарда и инсульт; консервацию органов для трансплантации; лечение ишемии тканей посредством регулирования и (или) восстановления тока крови, доставки кислорода и (или) использования энергии; ускорение процесса заживления ран, в частности, у пожилых пациентов и пациентов, страдающих диабетом; лечение ожогов; лечение инфекционных заболеваний; срастание переломов и рост костей. Кроме того, предполагается, что намеченное нарушение PHD будет полезно для лечения таких нарушений обмена веществ, как диабет, ожирение, неспецифический язвенный колит, воспалительное заболевание кишечника, и родственных заболеваний, таких как болезнь Крона. (Recent Patents on Inflammation & Allergy Drug Discovery, 2009, 3, 1-16).
Показано, что HIF является основным транскрипционным фактором, который приводит к повышению продуцирования эритропоэтина в условиях гипоксии (Wang et al., 1993, см. выше). Несмотря на то, что применение рекомбинантного человеческого эритропоэтина показало себя эффективным при лечении анемии, можно ожидать, что ингибирование PHD малыми молекулами будет иметь некоторые преимущества в сравнении с лечением эритропоэтином. В частности, функция других продуктов гена HIF необходима для гемопоэза, а регулирование этих факторов повышает эффективность гемопоэза. Примеры продуктов целевого гена HIF, критичных для гемопоэза, включают: трансферрин (Rolfs et al., 1997, J Biol Chem., 272(32):20055-62), трансферриновый рецептор (Lok et al., 1999, J Biol Chem., 274(34):24147-52; Tacchini et al., 1999, J Biol Chem., 274(34):24142-46) и церулоплазмин (Mukhopadhyay et al., 2000, J Biol Chem., 275(28):21048-54). Экспрессия гепсидина также подавляется HIF (Peyssonnaux et al., 2007, J Clin Invest., 117(7):1926-32), а ингибиторы PHD с малыми молекулами, как было показано, уменьшают выработку гепсидина (Braliou et al., 2008, J Hepatol., 48:801-10). Гепсидин является отрицательным фактором регулирования доступности железа, необходимого для гемопоэза, поэтому ожидается, что уменьшение выработки гепсидина будет благотворно сказываться на лечении анемии. Ингибирование PHD также может быть полезным в сочетании с другим лечением анемии, включая пополнение железа и (или) экзогенный эритропоэтин. Исследования естественных мутаций гена PHD2 у человеческой популяции дают еще одно основание для использования ингибиторов PHD при лечении анемии. В двух последних работах показано, что у пациентов с дисфункциональными мутациями в гене PHD2 наблюдается повышенный эритроцитоз и повышенный уровень гемоглобина в крови (Percy et al., 2007, PNAS, 103(3):654-59; Al-Sheikh et al., 2008, Blood Cells Mol Dis., 40:160-65). Кроме того, ингибитор PHD с малым размером молекулы был испытан на здоровых добровольцах и на пациентах с хроническими заболеваниями почек (Патентная заявка США US2006/0276477, 7 декабря 2006 г.). Содержание эритропоэтина в плазме увеличивалось в зависимости от дозы, а у пациентов с хроническими заболеваниями почек повышалось содержание гемоглобина в крови.
Ишемия представляет опасность для метаболической адаптации и защиты тканей. Ингибиторы PHD повышают экспрессию генов, что приводит к изменениям в процессе обмена веществ, благотворным в ишемических условиях (Semenza, 2007, Biochem J., 405:1-9). Многие из кодируемых генами энзимов, участвующих в анаэробном гликолизе, регулируются HIF, и гликолиз увеличивается путем ингибирования PHD (Shaw, см. выше). Известные целевые гены HIF на этом пути метаболизма включают, помимо прочего, следующие: GLUT-1 (Ebert et al., см. выше), гексокиназу, фосфоглицераткиназу 1, лактатдегидрогеназу (Firth et al., см. выше), киназу пируватдегидрогеназы-1 (Kim et al., см. выше; Papandreou et al., см. выше). Киназа пируватдегидрогеназы-1 подавляет вхождение пируватов в цикл Кребса. HIF выступает в роли посредника в переключении экспрессии цитохромов, участвующих в процессе переноса электрона в митохондрии (Fukuda et al., 2007, Cell, 129(1):111-22). Это изменение строения цитохрома оптимизирует эффективность производства АТФ (аденозинтрифосфат) в условиях гипоксии и снижает производство таких вредных побочных продуктов окислительного фосфорилирования, как перекись водорода и надперекиси. При продолжительном воздействии гипоксии HIF стимулирует аутофагию митохондрий, в результате чего их количество уменьшается (Zhang H et al., 2008, J Biol Chem. 283: 10892-10903). Эта адаптация к хронической гипоксии снижает производство перекиси водорода и надперекиси, тогда как производство энергии клеткой основывается на гликолизе. Еще одна адаптивная реакция, вызванная повышением HIF, заключается в активации факторов выживаемости клеток. К этим факторам относятся следующие: инсулиноподобный фактор роста (IGF) 2, белки, связывающие IGF 2 и 3 (Feldser et al., 1999, Cancer Res. 59:3915-18). Общее аккумулирование HIF в условиях гипоксии управляет адаптивной активацией гликолиза, снижением окислительного фосфорилирования, что приводит к уменьшению производства перекиси водорода и надперекиси, оптимизации окислительного фосфорилирования, защищая клетки от ишемического поражения. Таким образом, предполагается, что ингибиторы PHD будут полезны для консервации органов и тканей для трансплантации (Bernhardt et al., 2007, Methods Enzymol., 435:221-45). Несмотря на то что положительный эффект может быть получен путем назначения ингибиторов PHD до забора органов для трансплантации, введение ингибитора в орган или ткань после забора, при хранении (например, кардиоплегический раствор) или после трансплантации, может также иметь терапевтический эффект.
Предполагается, что ингибиторы PHD будут эффективны для защиты тканей от распространенной ишемии и (или) гипоксии. В том числе от ишемии или гипоксии, связанных, помимо прочего, со следующим: ангиной, ишемией миокарда, инсультом, ишемией скелетной мышцы. Существует целый ряд экспериментальных доказательств того, что ингибирование PHD и последующее повышение HIF является целесообразным способом консервации ишемической ткани. Недавно было показано, что ишемическое прекондиционирование - это явление, зависящее от HIF (Cai et al., 2008, Cardiovasc Res., 77(3):463-70). Ишемическое прекондиционирование - это известное явление, в соответствии с которым короткие периоды гипоксии и (или) ишемии защищают ткань от последующих более продолжительных периодов ишемии (Murry et al., 1986, Circulation, 1986 74(5):1124-36; Das et al., 2008, IUBMB Life, 60(4):199-203). Известно, что ишемическое прекондиционирование наблюдается у людей, а также у экспериментальных животных (Darling et al., 2007, Basic Res Cardiol., 102(3):274-8; Kojima I et al., 2007, J Am Soc Nephrol., 18:1218-26). Несмотря на то, что концепция прекондиционирования более всего известна благодаря своим защитным воздействиям в сердце, она также применимо и к другим тканям, включая, помимо прочего, следующие: печень, скелетную мышцу, легкое, почку, кишечник и мозг (Pasupathy et al., 2005, Eur J Vasc Endovasc Surg., 29:106-15; Mallick et al., 2004, Dig Dis Sci., 49(9):1359-77). Экспериментальное подтверждение тканепротективных эффектов ингибирования PHD и повышения HIF получено на ряде животных моделей, включая: нокаутирование зародышевой линии PHD1, которая обеспечивала защиту скелетной мышцы от ишемического инсульта (Aragonés et al., 2008, Nat Genet., 40(2):170-80), выключение PHD2 путем применения siRNA (короткая интерферирующая РНК), которая защищала сердце от ишемического инсульта (Natarajan et al., 2006, Circ Res., 98(1):133-40), ингибирование PHD путем введения окиси углерода, которая защищала миокард от ишемического поражения (Chin et al., 2007, Proc Natl Acad Sci. U.S.A., 104(12):5109-14), гипоксию в мозге, которая повышала устойчивость к ишемии (Bernaudin et al., 2002, J Cereb Blood Flow Metab., 22(4):393-403). Кроме того, ингибиторы PHD с малым размером молекулы защищают мозг в экспериментальных моделях инсульта (Siddiq et al., 2005, J Biol Chem., 280(50):41732-43). Более того, было показано, что активация HIF защищает сердце мыши, страдающей диабетом, где последствия обычно хуже (Natarajan et al., 2008, J Cardiovasc Pharmacol., 51(2):178-187). Тканепротективные эффекты можно также наблюдать при облитерирующем тромбангиите (болезнь Бюргера), симметричной гангрене (болезнь Рейно) и акроцианозе.
Пониженная зависимость от аэробного метаболизма с помощью цикла Кребса в митохондрии и повышенная зависимость от анаэробного гликолиза, вызванного ингибированием PHD, может оказывать благоприятное влияние на ткани с нормальным снабжением кислородом. Важно отметить, что ингибирование PHD, как было показано, повышает HIF в условиях нормального снабжения кислородом. Таким образом, ингибирование PHD вызывает псевдогипоксию, обусловленную гипоксическим откликом, инициированным через HIF, но насыщение тканей кислородом остается нормальным. Можно также ожидать, что перестройка метаболизма, вызванная ингибированием PHD, позволит реализовать способ лечения диабета, ожирения и связанных с ними расстройств, включая сопутствующие заболевания.
В целом, совокупность изменений экспрессии гена, вызванных ингибированием PHD, снижает количество энергии, производимой на единицу глюкозы, и будет стимулировать организм на сжигание большего количества жира для поддержания энергетического баланса. Механизмы интенсификации гликолиза рассматриваются выше. Другие исследования связывают гипоксический отклик с теми эффектами, которые, как ожидается, являются благотворными при лечении диабета и ожирения. Так, хорошо известно, что для уменьшения количества жира в организме применяются тренировки в условиях высокогорья (Armellini et al., 1997, Horm Metab Res., 29(9):458-61). Показано, что гипоксия и имитирующие гипоксию вещества, такие как десферриоксамин, предотвращают выделение адипоцита (Lin et al., 2006, J Biol Chem., 281(41):30678-83; Carrière et al., 2004, J Biol Chem., 279(39):40462-69). Этот эффект является обратимым по возвращении к нормальным условиям снабжения кислородом. Ингибирование активности PHD на начальных стадиях липогенеза подавляет образование новых адипоцитов (Floyd et al., 2007, J Cell Biochem., 101:1545-57). Гипоксия, хлорид кобальта и десферриоксамин повышают HIF и ингибируют транскрипцию ядерных гамма 2-PPAR (рецепторы, активирующие пролиферацию пероксисом) рецепторов гормона (Yun et al., 2002, Dev Cell., 2:331-41). Так как гамма 2-PPAR - это важный сигнал для выделения адипоцита, то следует ожидать, что ингибирование PHD будет подавлять выделение адипоцита. Было показано, что эти эффекты должны иметь место при участии HIF-регулируемого гена DEC1/Stra13 (Yun et al., см. выше).
Ингибиторы PHD с малым размером молекулы демонстрируют лечебное воздействие в животных моделях диабета и ожирения (Международная патентная заявка WO2004/052284, 24 июня 2004 г.; WO2004/052285, 24 июня 2004 г.). Эффекты, показанные для ингибиторов PHD на мышах с алиментарным ожирением, мышах db/db и крысах линии Zucker fa/fa, включали понижение следующего: концентрации глюкозы в крови, массы жира как в абдоминальном, так и в висцеральном скоплении жировой ткани, гемоглобина A1c, триглицеридов плазмы, массы тела, а также изменения биомаркеров установленного заболевания, таких как повышение уровней адреномедуллина и лептина. Лептин известен как продукт целевого гена HIF (Grosfeld et al., 2002, J Biol Chem., 277(45):42953-57). Продукты генов, участвующие в метаболизме жировых клеток, как было показано, должны регулироваться ингибированием PHD в зависимости от HIF (Международная патентная заявка WO2004/052285, см. выше). К таким продуктам относятся: аполипопротеин A-IV, ацил CoA тиоэстераза, карнитин ацетил трансфераза и инсулиноподобный фактор роста связывающего белка (IGFBP)-1.
Предполагается, что ингибиторы PHD должны быть терапевтически эффективны как стимуляторы васкулогенеза, развития кровеносных сосудов и артериогенеза. Эти процессы создают или восстанавливают ток крови к тканям и их насыщение кислородом в условиях ишемии и (или) гипоксии (Semenza et al., 2007, J Cell Biochem., 102:840-47; Semenza, 2007, Exp Physiol., 92(6):988-91). Было показано, что физические упражнения повышают HIF-1 и сосудистый эндотелиальный фактор роста в экспериментальных животных моделях и у людей (Gustafsson et al. 2001, Front Biosci., 6:D75-89) и, соответственно, количество кровеносных сосудов в скелетной мышце. VEGF (фактор роста васкулярного эндотелия) - хорошо известный продукт целевого гена HIF, являющимся основным фактором развития кровеносных сосудов (Liu et al., supra). Несмотря на то, что назначение различных форм активаторов рецептора VEGF является сильнодействующим стимулом для развития кровеносных сосудов, кровеносные сосуды, появляющиеся в результате этого потенциального способа лечения, являются неплотными. Считается, что это ограничивает возможность использования VEGF для лечения расстройств доставки кислорода. Повышенная экспрессия одного ангиогенного фактора может быть недостаточной для функциональной васкуляризации (новообразование кровеносных сосудов) (Semenza, 2007, см. выше). Потенциальные преимущества ингибирования PHD в сравнении с другими подобными способами ангиогенной терапии состоят в том, что это стимулирует контролируемую экспрессию множества ангиогенных факторов роста в зависимости от HIF, включая, помимо прочего, следующие: плацентный фактор роста (PLGF), ангиопоэтин-1 (ANGPT1), ангиопоэтин-2 (ANGPT2), бета-фактор роста тромбоцитарный (PDGFB) (Carmeliet, 2004, J Intern Med., 255:538-61; Kelly et al., 2003, Circ Res., 93:1074-81) и фактор роста стромальных клеток-1 (SDF-1) (Ceradini et al., 2004, Nat Med., 10(8):858-64). Экспрессия ангиопоэтина-1 в процессе развития кровеносных сосудов приводит к образованию плотных кровеносных сосудов, в отличие от кровеносных сосудов, образующихся при назначении только VEGF (Thurston et al., 1999, Science, 286:2511-14; Thurston et al., 2000, Nat Med., 6(4):460-3; Elson et al., 2001, Genes Dev., 15(19):2520-32). Было показано, что фактор роста стромальных клеток 1 (SDF-1) чрезвычайно важен для процесса притока предшественников эндотелиальных клеток к местам повреждения ткани. Экспрессия SDF-1 повышает адгезию, миграцию и хоминг циркулирующих CXCR4-позитивных клеток-предшественников к ишемической ткани. Более того, ингибирование SDF-1 в ишемической ткани или блокада CXCR4 на клетках, циркулирующих в периферической крови, предотвращает привлечение клеток-предшественников к местам повреждения (Ceradini et al., 2004, см. выше; Ceradini et al., 2005, Trends Cardiovasc Med., 15(2):57-63). Важно, что привлечение предшественников эндотелиальных клеток к местам повреждения у взрослых мышей снижается, и это компенсируется вмешательствами, которые повышают HIF на месте раны (Chang et al., 2007, Circulation, 116(24):2818-29). Ингибирование PHD дает преимущества не только за счет увеличения экспрессии ряда ангиогенных факторов, но также за счет координации их экспрессии в течение всего процесса развития кровеносных сосудов и привлечения предшественников эндотелиальных клеток к ишемической ткани.
Доказательство применимости ингибиторов PHD в проангиогенной терапии представлено в следующих исследованиях. Сверхсинтез HIF при участии аденовируса, как было показано, вызывает развитие кровеносных сосудов в неишемической ткани взрослого животного (Kelly et al., 2003, Circ Res., 93(11):1074-81) и свидетельствует о том, что лечение, повышающее HIF, например ингибирование PHD, будет вызывать развитие кровеносных сосудов. Было показано, что плацентный фактор роста (PLGF), также целевой ген HIF, играет важную роль в развитии кровеносных сосудов в ишемической ткани (Carmeliet, 2004, J Intern Med., 255(5):538-61; Luttun et al., 2002, Ann N Y Acad Sci., 979:80-93). Были продемонстрированы действенные проангиогенные эффекты лечения, которое повышает HIF, посредством сверхсинтеза HIF, в скелетной мышце (Pajusola et al., 2005, FASEB J., 19(10):1365-7; Vincent et al., 2000, Circulation, 102:2255-61) и в миокарде (Shyu et al., 2002, Cardiovasc Res., 54:576-83). Было также показано привлечение предшественников эндотелиальных клеток к ишемическому миокарду целевым геном HIF SDF-1 (Abbott et al., 2004, Circulation, 110(21):3300-05). Эти результаты подтверждают общую концепцию, суть которой состоит в том, что ингибиторы PHD будут эффективными для стимулирования развития кровеносных сосудов в регулировании ишемии тканей, в частности ишемии мышц. Предполагается, что терапевтическое развитие кровеносных сосудов, вызванное ингибиторами PHD, будет полезно для восстановления тока крови к тканям и, следовательно, для лечения заболеваний, включая, помимо прочего, следующие: стенокардию, ишемию и инфаркт миокарда, периферическую ишемическую болезнь, перемежающуюся хромоту, язву желудка и двенадцатиперстной кишки, неспецифический язвенный колит и воспалительное заболевание кишечника.
PHD и HIF играют главную роль в заживлении и регенерации тканей, в том числе в заживлении ран и язв. Последние исследования показали повышенную экспрессию всех трех PHD на местах ран у взрослых мышей и, как результат, уменьшение аккумулирования HIF (Chang et al., supra). Таким образом, повышение HIF у взрослых мышей путем назначения десферриоксамина повышает степень залечивания ран до уровня, наблюдаемого у молодых мышей. Аналогично, у мышей, страдающих диабетом, повышение HIF было ослаблено в сравнении с мышами того же помета без диабета (Mace et al., 2007, Wound Repair Regen., 15(5):636-45). Местное применение хлорида кобальта, имитатора гипоксии или сверхсинтез мышиного HIF, который ограничивает область разложения, зависящего от кислорода, и, таким образом, обеспечивает постоянно активную форму HIF, приводит к повышению HIF на месте раны, повышению экспрессии целевых генов HIF, таких как VEGF, Nos2 и Hmox1, и к ускорению заживления раны. Недавно было показано, что благоприятный эффект ингибирования PHD не ограничивается кожей и что ингибиторы PHD с малым размером молекулы дают положительный результат на моделях мышей с колитом (Robinson et al., 2008, Gastroenterology, 134(1):145-55).
Предполагается, что ингибирование PHD, приводящее к аккумулированию HIF, имеет по меньшей мере четыре механизма действия, каждый из которых вносит свой вклад в ускоренное и более полное заживление ран и язв: 1) защита ткани, подверженной опасности гипоксии и (или) ишемии, 2) стимулирование развития кровеносных сосудов для создания или восстановления надлежащего тока крови к месту поражения, 3) привлечение предшественников эндотелиальных клеток к местам поражения, 4) стимулирование выработки тех факторов роста, которые специфически стимулируют заживление и регенерацию.
Рекомбинантный человеческий фактор роста тромбоцитарный (PDGF) присутствует на рынке в виде бекаплермина (торговое название Regranex™) и одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для «Лечения диабетических невропатических язв нижних конечностей, которые выходят в подкожную основу или далее и снабжаются кровью в достаточной степени». Было показано, что бекаплермин эффективно ускоряет заживление ран у пациентов, страдающих диабетом (Steed, 2006, Plast Reconstr Surg., 117(7 Suppl):143S-149S; Nagai et al., 2002, Expert Opin Biol Ther., 2(2):211-8). Так как PDGF является целевым геном HIF (Schultz et al., 2006, Am J Physiol Heart Circ Physiol., 290(6):H2528-34; Yoshida et al., 2006, J Neurooncol., 76(1):13-21), то предполагается, что ингибирование PHD повысит выработку эндогенного PDGF и будет оказывать аналогичный или более благоприятный эффект на те, которые вырабатываются только с бекаплермином. Исследования на животных показали, что местное применение PDGF приводит к повышению количества ДНК, протеина и гидроксипролина, формированию более толстого слоя грануляционной и эпидермальной ткани, повышенному клеточному вторичному заселению мест повреждения. PDGF приводит в действие локальный эффект интенсификации образования новой соединительной ткани. Предполагается, что эффективность ингибирования PHD будет выше, чем эффективность ингибирования, вызванная бекаплермином из-за дополнительного тканепротективного и проангиогенного эффектов, опосредованных HIF.
Ожидается, что благоприятное воздействие ингибирования PHD распространится не только на ускорение заживления раны в коже и толстой кишке, но также на заживление других повреждений ткани, включая, помимо прочего, следующее: желудочно-кишечные язвы, реплантации трансплантата, ожоги, хронические язвы и обморожение.
Стволовые клетки и клетки-предшественники обнаружены в гипоксических нишах внутри тела, и гипоксия регулирует их дифференциацию и метаболический путь клетки (Simon et al., 2008, Nat Rev Mol Cell Biol., 9:285-96). Таким образом, ингибиторы PHD могут быть пригодны для поддержания стволовых клеток и клеток-предшественников в плюрипотентном состоянии и стимулирования дифференциации в направлении желательного типа клеток. Стволовые клетки могут быть полезны для культивирования и роста популяций стволовых клеток и могут удерживать клетки в плюрипотентном состоянии, в то время как гормоны и другие факторы вводятся в клетки для того, чтобы повлиять на дифференциацию и метаболический путь клетки.
Дальнейшее использование ингибиторов PHD в области лечения стволовыми клетками и клетками-предшественниками связано с использованием ингибиторов PHD для кондиционирования этих клеток, с тем чтобы они выдерживали процесс имплантации в организм и с тем чтобы генерировать соответствующий отклик организма, в результате чего имплантация стволовой клетки и клетки-предшественника станет практически осуществимой (Hu et al., 2008, J Thorac Cardiovasc Surg., 135(4):799-808). Точнее говоря, ингибиторы PHD могут способствовать интеграции стволовых клеток и привлечению соответствующего кровотока для поддержки стволовых клеток после их встраивания. Это образование кровеносного сосуда будет также выполнять функцию переноса гормонов и других факторов, высвобожденных этими клетками для остального организма.
Ингибиторы PHD также могут быть полезны при лечении инфекции (Peyssonnaux et al., 2005, J Invest Dermatol., 115(7):1806-15; Peyssonnaux et al., 2008 J Invest Dermatol., август 2008 г.; 128(8):1964-8). Было показано, что повышение HIF усиливает врожденную иммунную реакцию на инфекцию в фагоцитах и кератиноцитах. Фагоциты с увеличенным HIF демонстрируют повышенную бактерицидную активность, повышенное выделение окиси азота и повышенное производство антибактериального пептида кателицидин. Эти эффекты могут быть также полезны для лечения ожоговых инфекций.
Было также показано, что HIF участвует в процессе роста кости и срастания перелома (Pfander D et al., 2003 J Cell Sci., 116(Pt 9):1819-26., Wang et al., 2007 J Clin Invest., 17(6):1616-26.) и, следовательно, может использоваться для лечения или профилактики переломов. HIF стимулирует гликолиз, обеспечивающий энергией синтез внеклеточного матрикса эпифизарных хондроцитов в условиях гипоксии. HIF также играет важную роль в стимуляции выделения VEGF и развитии кровеносных сосудов в процессе срастания перелома. Рост кровеносных сосудов в растущую или срастающуюся кость может быть фактором, ограничивающим скорость процесса.
В литературе описаны некоторые молекулы малого размера c антагонистической активностью в отношении пролилгидроксилазы. К таким молекулам относятся помимо прочих некоторые имидазо[1,2-a]пиридин производные (Warshakoon et al., 2006, Bioorg Med Chem Lett., 16(21):5598-601), замещенные пиридин-производные (Warshakoon et al., 2006, Bioorg Med Chem Lett., 16(21):5616-20), некоторые пиразолопиридины (Warshakoon et al., 2006, Bioorg Med Chem Lett., 16(21):5687-90), некоторые бициклические гетероароматические N-замещенные производные глицина (Международная патентная заявка WO2007/103905, 13 сентября 2007 г.), соединения на основе хинолина (Международная патентная заявка WO2007/070359, 21 июня 2007 г.), некоторые барбитурат-N-замещенные производные глицина (Международная патентная заявка WO2007/150011, 27 декабря 2007 г.) и замещенные арил- и гетероарил-амидные (США, патентная заявка № US 2007/0299086, 27 декабря 2007 г.).
Некоторые производные бензоимидазола описаны в литературе. Например, LeCount et al., Journal of the Chemical Society, Perkin Transactions 1: Organic and Bio-Organic Chemistry (1972-1999) (1974), (2):297-301, Senga et al., Journal of Heterocyclic Chemistry (1975), 12(5):899-901, Kandeel et al., Polish Journal of Chemistry (1983), 57(1-3), 327-31, Povstyanoi et al., Ukrainskii Khimicheskii Zhurnal (Russian Edition) (1990), 56(10):1089-92, Singh et al., Indian Journal of Chemistry, Section B: Organic Chemistry Including Medicinal Chemistry, (1993) 32B(2):262-5, Lipunova et al., Mendeleev Communications (1996), (1):15-17, Lipunova et al., Russian Journal of Organic Chemistry (Translation of Zhurnal Organicheskoi, Khimii) (1997), 33(10):1476-86, бензоимидазол-пиразолы как промежуточные соединения для ингибиторов NHE-1 (WO9943663), N-гетероарилимидазолы как лекарственные препараты, действующие на психику (DE3824658). Кроме этого, 1-(1H-бензоимидазол-2-ил)-5-метил-1H-пиразол-4-карбоновая кислота (CAS № 1017666-26-0), этиловый эфир 1-(1H-бензоимидазол-2-ил)-5-гидрокси-1H-пиразол-4-карбоновой кислоты (CAS № 1006582-96-2), 1-(1H-бензоимидазол-2-ил-5-пиррол-1-ил-1H-пиразол-4-карбоновая кислота (CAS № 1017666-37-3) и 1-(1H-бензоимидазол-2-ил)-5-(2,5-диметилпиррол-1-ил)-1H-пиразол-4-карбоновая кислота (CAS № 1017666-50-0) имеются на рынке.
Тем не менее, до сих пор остается необходимость в сильнодействующих модуляторах пролилгидроксилазы с желательными фармацевтическими свойствами. Несмотря на изложенное выше, настоящее изобретение имеет целью новые производные бензоимидазола, пригодные для этой цели.
Краткое описание изобретения
Целью настоящего изобретения, в общем, являются соединения, представляющие собой ингибиторы PHD формулы (I),
где
n равно от 2 до 4
R1 независимо выбран из H, галогена, -C1-4алкила, -C3-8циклоалкил-C1-4пергалоалкила, трифтор-C1-4алкокси -OH, -NO2, -CN, CO2H, -OC1-4алкила, -SC1-4алкила, -S(C1-4алкил)-Rc, -S(O)2(C1-4алкил)-Rc, -S(O)-C1-4алкила, -SO2-C1-4алкила, -S-Rc, -S(O)-Rc, -SO2-Rc, -SO2-NH-Rd, -O-Rc, -CH2-O-Rc, -C(O)NH-Rc, -NRaRb, бензилокси, необязательно замещенного Rd, фенила или моноциклического гетероарила, необязательно замещенного Rd, -C3-8циклоалкила, необязательно содержащего O, S или N, причем упомянутый -C3-8циклоалкил необязательно замещен Rd, и две смежные R1 группы могут соединяться с образованием необязательно замещенного 3-8-членного кольца, необязательно содержащего один или несколько атомов O, S или N;
Ra и Rb каждый независимо представляет собой H, C1-4алкил, -C(O)C1-4алкил, -C(O)-Rc, -C(O)CH2-Re, C1-4алкил-Re, -SO2-Rc, -SO2-C1-4алкил, фенил, необязательно замещенный Rd, бензил, необязательно замещенный Rd, или моноциклическое гетероарильное кольцо, необязательно замещенное Rd; или же Ra и Rb вместе с атомом азота, с которым они соединены, могут образовывать необязательно замещенное моноциклическое гетероциклоалкильное кольцо, необязательно содержащее один или более атомов O, S или N;
Rc представляет собой -C3-8циклоалкил, фенил, необязательно замещенный Rd, бензил, необязательно замещенный Rd, или моноциклическое гетероарильное кольцо, необязательно замещенное Rd;
Rd независимо представляет собой -H, галоген, -OH, -C1-4алкил или -C1-4пергалогеналкил, трифтор C1-4алкокси, -OC1-4алкил, -O-фенил или -O-бензил;
Re представляет собой -C3-8гетероциклоалкил, необязательно содержащий один или более атомов O, S или N;
R2 и R3 оба представляют собой H, -CF3, или -CH3; и
каждый из Z представляет собой атом C или N, при условии, что не более чем два Z одновременно могут быть N; и
энантомеры, диастереомеры, рацематы этих соединений, или фармацевтически приемлемые соли этих соединений.
Настоящее изобретение включает изомерные формы соединений формулы (I) и их фармацевтически приемлемые соли, и ссылка здесь на одну из таких изомерных форм означает ссылку по меньшей мере на одну из таких изомерных форм. Специалист в данной области признает, что соединения в соответствии с данным изобретением могут существовать, например, в единственной изомерной форме, в то время как другие соединения могут существовать в форме региоизомерной смеси.
Настоящее изобретение также относится к фармацевтически приемлемым солям, фармацевтически приемлемым пролекарствам и фармацевтически активным метаболитам соединений формулы (I). В определенных предпочтительных вариантах осуществления соединение формулы (I) представляет собой соединение, выбираемое из разновидностей, описанных или проиллюстрированных в приведенном ниже подробном описании.
В следующем общем аспекте изобретение относится к лекарственным препаратам, каждый из которых включает: (a) эффективное количество соединения формулы (I) или фармацевтически приемлемую соль, фармацевтически приемлемое пролекарство или его фармацевтически активный метаболит; и (b) фармацевтически приемлемый наполнитель.
В другом общем аспекте изобретение направлено на способ лечения субъекта с имеющимся или диагностированным заболеванием, расстройством, или нарушением здоровья, обусловленными активностью энзима пролилгидроксилазы. Способ состоит в назначении пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы (I) или фармацевтически приемлемой соли, фармацевтически приемлемого пролекарства или его фармацевтически активного метаболита.
В определенных предпочтительных вариантах применения способа изобретения, заболевание, расстройство или нарушение здоровья выбирается из следующего: анемия, сосудистые расстройства, нарушения обмена веществ и заживление раны.
Дополнительные варианты реализации, особенности и достоинства изобретения будут очевидны из следующего подробного описания и практического осуществления изобретения.
Подробное описание
Настоящее изобретение может быть более полно оценено из нижеследующего описания, включающего глоссарий терминов и заключительные примеры. Для краткости цитируемые публикации, включая патенты, включены в настоящее описание посредством ссылки.
Термины «включающий», «содержащий», «состоящий из» используются в настоящем документе в их открытом, неограниченном значении.
Термин «алкил» относится к алкильной группе с прямой или разветвленной цепью, содержащей от 1 до 12 атомов углерода. Примеры алкильных групп включают метил (Me, который также может быть структурно обозначен символом, «/»), этил (Et), н-пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил (tBu), фенил, изофенил, трет-фенил, гексил, изогексил, и группы, которые в свете общепринятых знаний и учений, представленных здесь, будут считаться эквивалентными одному из вышеприведенных примеров.
Термин «пергалоалкил» относится к алкильной группе с прямой или разветвленной цепью, имеющей от 1 до 12 атомов в цепочке и атомы водорода, необязательно замещенные на атомы галогенов. Примеры пергалоалкильных групп включают трифторметил (CF3), дифторметил (CF2H), монофторметил (CH2F), пентафторэтил (CF2CF3), тетрафторэтил (CHFCF3), трифторэтил (CH2CF3) и группы, которые в свете общепринятых знаний и сведений, представленных в настоящем документе, могут считаться эквивалентными одному из вышеприведенных примеров.
Используемый в настоящей заявке термин «циклоалкил» означает насыщенный или частично насыщенный моноциклический, конденсированный полициклический или спиро-полициклический карбоцикл,