Окисленные соединения липидов и их применение
Иллюстрации
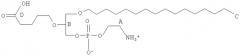
Показать всеИзобретение относится к новым соединениям структурной формулы (I) , которые могут быть использованы для лечения или профилактики заболеваний или нарушений, ассоциированных с воспалением. В формуле (I) каждый из A1, А2 и А3 независимо выбран из группы, состоящей из О и S, R1 представляет собой алкильную цепь длиной 2-28 атомов углерода, R2 выбран из группы, состоящей из (3-карбокси)пропила и (2-карбокси)этила, и R3 выбран из группы, состоящей из Н, С1-20ацила, фосфата, фосфохолина, фосфоэтаноламина, фосфоэтаноламин-N-глутаровой кислоты и фосфосерина. Изобретение также относится к фармацевтической композиции, содержащей указанные соединения, и к применению соединений для изготовления лекарственного средства, предназначенного для лечения или профилактики заболеваний или нарушений, ассоциированных с воспалением, или для снижения уровня цитокина, выбранного из группы, состоящей из интерлейкина-12 и интерлейкина-23. 15 н. и 45 з.п. ф-лы, 39 ил., 18 пр.
(I)
Реферат
ОБЛАСТЬ И ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение, в некоторых его вариантах, относится к новым окисленным липидам и способам, в которых используются окисленные липиды, для лечения или профилактики воспаления, ассоциированного с эндогенными окисленными липидами. Способы по настоящим вариантам могут быть использованы для лечения или профилактики заболеваний и нарушений, связанных с воспалением, таких как, например, атеросклероз и родственные нарушения, аутоиммунные заболевания или нарушения, а также пролиферативные заболевания или нарушения.
Ранее, окисленные фосфолипиды были описаны как эффективные для лечения состояний, таких как, например, сердечно-сосудистые заболевания, цереброваскулярные заболевания и воспалительные заболевания и нарушения.
Международная заявка на патент PCT/IL2004/000453 (Публикация 04/106486), настоящего патентообладателя, описывает окисленные липиды, которые могут быть использованы для профилактики и лечения воспалений, ассоциированных с эндогенными окисленными липидами. Пример такого соединения описан и известен как CI-201 (также называемый в данной области как VB-201).
Международная заявка на патент PCT/IL01/01080 (Публикация WO 02/41827), настоящего патентообладателя, описывает окисленные липиды, которые могут быть использованы для профилактики и лечения атеросклероза и родственных заболеваний.
Международная заявка на патент PCT/IL05/000735 (Публикация WO 06/006161), настоящего патентообладателя, описывает синтетические подходы, которые могут быть использованы для промышленного приготовления терапевтически эффективных окисленных фосфолипидов без применения колоночной хроматографии.
Дополнительный уровень техники включает Международную заявку на патент PCT/IL02/00005 (Публикация WO 02/053092) и PCT/IL08/000013 (Публикация WO 08/084472), принадлежащие настоящему патентообладателю.
Все указанные выше публикации включены в виде ссылки, как если бы они были изложены здесь полностью.
Все указанные выше публикации описывают этерифицированные окисленные липиды, которые содержат углеродный скелет, к которому присоединена алкильная цепь, при этом алкильная цепь является замещенной окисленной группой, и фосфат-содержащая группа. Алкильная цепь, которая является замещенной окисленной группой, предпочтительно присоединена к углеродному скелету эфирной связью (поэтому соединения называются «этерифицированными окисленными липидами»), поскольку такая связь наделяет соединения требуемыми фармакологическими свойствами, которые подробно описаны в упомянутых выше публикациях.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения разработали, успешно приготовили и протестировали новые окисленные фосфолипиды.
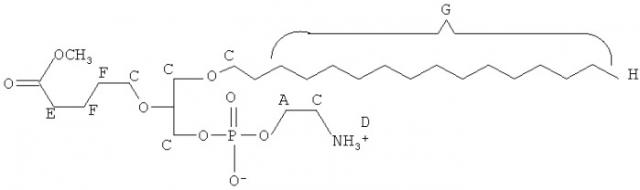
Согласно одному аспекту некоторых вариантов по настоящему изобретению, обеспечено соединение, имеющее формулу:
или его фармацевтически приемлемые соли, где:
(i) каждый A1, А2 и А3 независимо является выбранным из группы, состоящей из О и S.
(ii) R1 является выбранным из группы, состоящей из алкильной цепи длиной 2-28 атомов углерода, и
,
где Х представляет собой С1-25 цепь, Y является выбранным из группы, состоящей из , -ОН,-Н, алкила, алкокси, галогена, ацетокси и ароматических функциональных групп;и
Z является выбранным из группы, состоящей из:
, , , , и -OH,
где R' представляет собой С1-4 алкил; и
(iii) R2 является выбранным из группы, состоящей из (4-метилкарбокси)бутила, (3 -карбокси)пропила, (6-карбокси)гексанила, (2-карбокси)этила, 5,6-дигидроксигексанила, 5,5-диэтоксипентила и диметоксипентила; и
(iv) R3 является выбранным из группы, состоящей из Н, ацила, алкила, фосфата, фосфохолина, фосфоэтаноламина, фосфоэтаноламин-N-глутаровой кислоты, фосфосерина и фосфоинозитола.
Согласно одному аспекту некоторых вариантов по настоящему изобретению, обеспечено соединение, имеющее формулу:
или его фармацевтически приемлемые соли, где;
(i) каждый A1, A2 и А3 независимо является выбранным из группы, состоящей из О и S;
(ii) каждый R1 и R2 независимо является выбранным из группы, состоящей из алкильной цепи длиной 2-28 атомов углерода, и Y
при условии, что по меньшей мере один из R1 и R2 представляет собой Y
, где Х является С1-25 цепью, Y является выбранным из группы, состоящей из , -ОН, -Н, алкила, алкокси, галогена, ацетокси и ароматических функциональных групп; и
Z является выбранным из группы, состоящей из:
, , , , и -OH,
где R' представляет собой С1-4 алкил; и
(iii) Кз является выбранным из группы, состоящей из Н, фосфата, фосфоэтаноламина, фосфоэтаноламин-М-глутаровой кислоты и фосфосерина.
Согласно одному аспекту некоторых вариантов по настоящему изобретению, обеспечено соединение, имеющее формулу:
или его фармацевтически приемлемые соли, где:
(i) каждый A1, А2 и А3 независимо является выбранным из группы, состоящей из О и S;
(ii) R1 является выбранным из группы, состоящей из додецила, октадецила, октила, эйкозанила, цис-9-гексадеценила, (2-октил)додецила и (15-карбокси)пентадецила;
(iii) R2 является выбранным из группы, состоящей алкильной цепи длиной 2-28 атомов углерода, и
,
при условии, если R1 является отличным от (15-карбокси)пентадецила, то R2 представляет собой
где X представляет собой С1-25 цепь, Y является выбранным из группы, состоящей из
, -OH, -H, алкила, алкокси, галогена, ацетокси и ароматических функциональных групп; и
Z является выбранным из группы, состоящей из:
, , , , и -OH,
где R' представляет собой С1-4 алкил; и
(iv) R3 является выбранным из группы, состоящей из Н, ацила, алкила, фосфата, фосфохолина, фосфоэтаноламина, фосфоэтаноламин-Н-глутаровой кислоты, фосфосерина и фосфоинозитола.
Согласно одному аспекту некоторых вариантов по настоящему изобретению, обеспечено соединение, имеющее формулу:
или его фармацевтически приемлемые соли, где:
(i) A1 представляет собой S, и каждый А2 и А3 представляет собой О;
(ii) каждый R1 и R2 независимо является выбранным из группы, состоящей из алкильной цепи длиной 2-28 атомов углерода, и Y
при условии, что, по меньшей мере, один из R1 и R2 является , где Х представляет собой С1-25 цепь, Y является выбранным из группы, состоящей из:
, -ОН, -Н, алкила, алкокси, галогена, ацетокси и ароматических функциональных групп; и
Z является выбранным из группы, состоящей из:
, , , , и -OH,
где R' представляет собой С1-4 алкил; и
(iii) R3 является выбранным из группы, состоящей из Н, ацила, алкила, фосфата, фосфохолина, фосфоэтаноламина, фосфоэтаноламин-N-глутаровой кислоты, фосфосерина и фосфоинозитола.
Согласно одному аспекту некоторых вариантов по настоящему изобретению, обеспечено соединение, выбранное из группы, состоящей из следующих соединений:
1-гексадецил-2-(4-карбокси)бутил-глицеро-3-фосфат (CI-201-РА);
1-гексадепил-2-(4-метилкарбокси)бутил-глицеро-3-фосфоэтаноламин;
1-гексадецил-2-(4-метилкарбокси)бутил-глицеро-3-фосфохолин (CI-208);
1 -гексадецил-2-(4-карбокси)бутил-глицеро-3-фосфоэтаноламин (CI-202);
1-гексадецил-2-(3-карбокси)пропил-глицеро-3-фосфоэтаноламин (CI-206);
1 -гексадецил-2-(3-карбокси)пропил-глицеро-3-фосфохолин (CI-205);
1-гексадецил-2-(6-карбокси)гексанил-глицеро-3-фосфохолин(С1-203);
1-додецил-2-(4-карбокси)бутил-глицеро-3-фосфохолин (CI-209);
1-гексадецил-2-(4-карбокси)бутил-глицеро-3-фосфоэтаноламин-М-глутаровая
кислота (CI-210);
1-(15'-карбокси)пентадецил-2-(4-карбокси)бутил-глицеро-3 -фосфохолин (CI-213);
1-(15'-карбокси)пентадецил-2-(4-карбокси)бутил-глицеро-3 -фосфоэтаноламин (CI-214);
1-октадецил-2-(4-карбокси)бутил-глицеро-3-фосфохолин (CI-215);
1-октадецил-2-(4-карбокси)бутил-глицеро-3-фосфоэтаноламин (CI-216);
1-гексадецил-2-(2-карбокси)этил-глицеро-3-фосфохолин (CI-217);
1-8-гексадецил-2-(4-карбокси)бутил-глицеро-3-фосфохолин (1 -S-CI-201);
1-8-гексадецил-2-(4-карбокси)бутил-глицеро-3-фосфоэтаноламин(1-8-С1-202);
1-гексадецил-2-(5,6-дигидрокси)гексанил-глицеро-3-фосфохолин (di-OH);
1-(цис-9-гексадеценил)-2-(4-карбокси)бутил-глицеро-3-фосфохолин;
1-гексадецил-2-(4-карбокси)бутил-глицерин;
1-гексадецил-2-(5',5'-диэтоксипентил)глицеро-3-фосфохолин (diEtAc);
1-гексадецил-2-(5',5'-диметоксипентил)глицеро-3 -фосфохолин (diMeAc);
1-октил-2-(4-карбокси)бутил-глицеро-3-фосфохолин (CI-207);
1-октил-2-(4-карбокси)бутил-глицеро-3-фосфоэтаноламин;
1-эйкозанил-2-(4-карбокси)бутил-глицеро-3-фосфохолин (CI-219);
1-эйкозанил-2-(4-карбокси)бутил-глицеро-3-фосфоэтаноламин (CI-220);
1-(2-октил)додецил-2-(4-карбокси)бутил-глицеро-3-фосфохолин (VB-221);
1-(2-октил)додецил-2-(4-карбокси)бутил-глицеро-3-фосфоэтаноламин (VB-221); и
1 -гексадецил-2-(4-карбокси)бутил-глицеро-3-фосфосерин (VB-223). Согласно одному аспекту некоторых вариантов по настоящему изобретению, обеспечена фармацевтическая композиция, включающая, в качестве активного ингредиента, указанное соединение и фармацевтически приемлемый носитель.
Согласно одному аспекту некоторых вариантов по настоящему изобретению, обеспечен способ лечения или профилактики воспаления, ассоциированного с эндогенным окисленным липидом, при этом способ включает введение нуждающемуся субъекту терапевтически эффективного количества описанного здесь соединения, осуществляя тем самым лечение или профилактику воспаления, ассоциированного с эндогенным окисленным липидом у субъекта.
Согласно одному аспекту некоторых вариантов по настоящему изобретению, обеспечен способ снижения уровня цитокина, выбранного из группы, состоящей из интерлейкина-12 и интерлейкина-23, у субъекта, при этом способ включает введение субъекту эффективного количества описанного здесь соединения.
Согласно одному аспекту некоторых вариантов по настоящему изобретению, обеспечен способ лечения заболевания или нарушения, в котором снижение уровня цитокина, выбранного из группы, состоящей из интерлейкина-12 и интерлейкина-23, является предпочтительным, при этом способ включает введение нуждающемуся субъекту эффективного количества описанного здесь соединения.
Согласно одному аспекту некоторых вариантов по настоящему изобретению, обеспечено использование описанного здесь соединения в производстве лекарственных средств, предназначенных для лечения или профилактики воспаления, ассоциированного с эндогенным окисленным липидом.
Согласно одному аспекту некоторых вариантов по настоящему изобретению, обеспечено использование описанного здесь соединения в производстве лекарственных средств, предназначенных для снижения уровня цитокина, выбранного из группы, состоящей из интерлейкина-12 и интерлейкина-23, у субъекта.
Согласно одному аспекту некоторых вариантов по настоящему изобретению, обеспечено использование описанного здесь соединения в производстве лекарственных средств, предназначенных для лечения заболевания или нарушения, в котором снижение уровня цитокина, выбранного из группы, состоящей из интерлейкина-12 и интерлейкина-23, является предпочтительным.
Согласно некоторым вариантам изобретения, r) представляет собой алкильную цепь длиной 2-28 атомов углерода.
Согласно некоторым вариантам изобретения, описанное здесь соединение определено для использования в способе лечения или профилактики воспаления, ассоциированного с эндогенным окисленным липидом.
Согласно некоторым вариантам изобретения, описанное здесь соединение определено для использования в способе снижения уровня цитокина, выбранного из группы, состоящей из интерлейкина-12 и интерлейкина-23.
Согласно некоторым вариантам изобретения, описанное здесь соединение определено для использования в способе лечения заболевания или нарушения, в котором снижение уровня цитокина, выбранного из группы, состоящей из интерлейкина-12 и интерлейкина-23, является предпочтительным.
Согласно некоторым вариантам изобретения, фармацевтическая композиция упакована в упаковочный материал и идентифицирована оттиском в упаковочном материале или надписью, нанесенной на указанный упаковочный материал, как препарат, предназначенный для лечения или профилактики воспаления, ассоциированного с эндогенным окисленным липидом.
Согласно некоторым вариантам изобретения, фармацевтическая композиция упакована в упаковочный материал и идентифицирована оттиском в упаковочном материале или надписью, нанесенной на указанный упаковочный материал, как препарат, предназначенный для снижения уровня цитокина, выбранного из группы, состоящей из интерлейкина-12 и интерлейкина-23.
Согласно некоторым вариантам изобретения, фармацевтическая композиция упакована в упаковочный материал и идентифицирована оттиском в упаковочном материале или надписью, нанесенной на указанный упаковочный материал, как препарат, предназначенный для лечения заболевания или нарушения, в котором снижение уровня цитокина, выбранного из группы, состоящей из интерлейкина-12 и интерлейкина-23, является предпочтительным.
Согласно некоторым вариантам изобретения, воспаление ассоциировано с заболеванием или нарушением, выбранным из группы, состоящей из идиопатического воспалительного заболевания или нарушения, хронического воспалительного заболевания или нарушения, острого воспалительного заболевания или нарушения, аутоиммунного заболевания или нарушения, инфекционного заболевания или нарушения, воспалительного злокачественного заболевания или нарушения, воспалительного заболевания или нарушения, связанного с трансплантацией, воспалительного дегенеративного заболевания или нарушения, заболевания или нарушения, обусловленного гиперчувствительностью, воспалительного сердечнососудистого заболевания или нарушения, воспалительного цереброваскулярного заболевания или нарушения, заболевания или нарушения периферических сосудов, воспалительного заболевания или нарушения желез, воспалительного желудочно-кишечного заболевания или нарушения, воспалительного кожного заболевания или нарушения, воспалительного заболевания или нарушения печени, воспалительного неврологического заболевания или нарушения, воспалительного заболевания или нарушения костно-мышечной системы, воспалительного заболевания или нарушения почек, воспалительного заболевания или нарушения репродуктивной системы, воспалительного системного заболевания или нарушения, воспалительного заболевания или нарушения соединительной ткани, воспалительной опухоли, некроза, воспалительного заболевания или нарушения, связанного с имплантатом, воспалительного процесса, связанного со старением, заболевания или нарушения, обусловленного иммунодефицитом, а также воспалительного легочного заболевания или нарушения.
Если иное не оговорено, все технические и/или научные термины, использованные здесь, имеют то же самое значение, которое обычно понимается средним специалистом в данной области, к которой относится изобретение. Несмотря на то, что способы и материалы, аналогичные или эквивалентные приведенным в данном описании, могут использоваться при осуществлении на практике или проверке вариантов изобретения, ниже представлены примеры способов и/или материалов, описанных здесь. В случае возникновения противоречия необходимо обратиться к описанию изобретения, включающему определения терминов. Кроме того, материалы, способы и примеры носят только иллюстративный характер, и их не следует рассматривать как ограничивающие объем изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Некоторые варианты изобретения описаны здесь только в виде примера со ссылкой на прилагаемые чертежи. При подробном рассмотрении чертежей необходимо подчеркнуть, что отдельные детали приведены только в качестве примера и для иллюстрации вариантов изобретения. В данной связи, описание изобретения в сочетании с чертежами наглядно показывает опытным в данной области специалистам, каким образом можно осуществить на практике варианты данного изобретения.
На чертежах:
На Фиг.1 изображена диаграмма, показывающая продукцию IL 12/23 р40 клетками, обработанными разными дозами CI-202 (каждый столбик представляет 3 образца); Р<0.004 для каждой дозы по сравнению с контролем (0 мкг/мл);
На Фиг.2 изображена диаграмма, показывающая экспрессию мРНК IL 12/23 р40 в клетках, обработанных CI-201, CI-202 и фосфатидилхолином (PC), через 2, 3 и 4 часа после обработки;
На Фиг.3 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 10 или 20 мкг/мл (18.5 или 37 мкМ) CI-202, 10 или 20 мкг/мл (17 или 34 мкМ) CI-201, фосфатидилхолином (PC) и смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.4А и 4В изображены диаграммы, показывающие результаты отдельного эксперимента по тестированию токсичности разных доз CI-202;
На Фиг.5 изображена диаграмма, показывающая развитие МОГ-индуцированного экспериментального аутоиммунного энцефаломиелита у мышей, обработанных PBS или 4 мг/кг CI-202;
На Фиг.6 изображена диаграмма, показывающая развитие коллаген-индуцированного артрита у мышей, обработанных CI-202 (этаноламиновый аналог CI-201), и у контрольных мышей;
На Фиг.7 изображена диаграмма, показывающая продукцию IL 12/23 р40 клетками, обработанными разными дозами CI-203 (каждый столбик представляет 6 образцов), и Р величины по сравнению с контролем (0 мкг/мл);
На Фиг.8 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 1 или 20 мкг/мл (1.6 или 33 мкМ) (R)-CI-203 (R-CI-203) и рацемическим CI-203 (рац-CI-203), 1 или 20 мкг/мл (1.7 или 34 мкМ) (R)-CI-201 (R-CI-201) и (S)-CI-20l (S-CI-201), и 1 или 20 мкг/мл (1.3 или 26 мкМ) фосфатидилхолина (Ph.Ch.); ERK1/2 показана как контроль загрузки белка;
На Фиг.9А и 9В изображены диаграммы, показывающие результаты отдельного эксперимента по тестированию токсичности разных доз CI-203;
На Фиг.10 изображена диаграмма, показывающая продукцию IL 12/23 р40 клетками, обработанными разными дозами CI-209 (каждый столбик представляет 5 образцов), и Р величины (Р<0.008 для доз 10 и 20 мкг/мл, и Р<0.016 для доз 1, 2.5 и 5 мкг/мл) по сравнению с контролем (0 мкг/мл);
На Фиг.11 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 20 мкг/мл (38 мкМ) CI-209, CI-201 или фосфатидилхолином (PC), или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.12А и 12В изображены диаграммы, показывающие результаты отдельного эксперимента по тестированию токсичности разных доз CI-209;
На Фиг.13 изображена диаграмма, показывающая продукцию IL 12/23 р40 клетками, обработанными разными дозами CI-210 (каждый столбик представляет 4 образца), и Р величины (Р<0.029 для доз 10 и 20 мкг/мл и Р 0.057 для доз 2.5 и 5 мкг/мл) по сравнении с контролем (0 мкг/мл);
На Фиг.14 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 20 мкг/мл (31 мкМ) CI-210, CI-201 или фосфатидилхолином (PC), или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.15А и 15В изображены диаграммы, показывающие результаты отдельного эксперимента по тестированию токсичности разных доз CI-210;
На Фиг.16 изображена диаграмма, показывающая продукцию IL 12/23 р40 клетками, обработанными разными дозами CI-216 (каждый столбик представляет 4 образца), и Р величины по сравнению с контролем (0 мкг/мл);
На Фиг.17 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 10 или 20 мкг/мл (17 или 34 мкМ) CI-215 или фосфатидилхолином (PC), или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.18 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 10 или 20 мкг/мл (15 или 30 мкМ) CI-216, 10 или 20 мкг/мл (17 или 34 мкМ) CI-201, фосфатидилхолином (PC) или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.19 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 20 мкг/мл (38 мкМ) CI-206 или фосфатидилхолином (PC), или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.20 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 20 мкг/мл (35 мкМ) CI-205, CI-201 или фосфатидилхолином (PC), или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.21А и 21В изображены диаграммы, показывающие результаты отдельного эксперимента по тестированию токсичности разных доз CI-206;
На Фиг.22А и 22В изображены диаграммы, показывающие результаты отдельного эксперимента по тестированию токсичности разных доз CI-205;
На Фиг.23 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 20 мкг/мл (34 мкМ) CI-208, CI-201 или фосфатидилхолином (PC); α-тубулин (α-Туб) показан как контроль загрузки белка;
На Фиг.24А и 24В изображены диаграммы, показывающие результаты отдельного эксперимента по тестированию токсичности разных доз CI-208;
На Фиг.25А и 25В изображены диаграммы, показывающие результаты отдельного эксперимента по тестированию токсичности разных доз CI-213;
На Фиг.26А и 26В изображены диаграммы, показывающие результаты отдельного эксперимента по тестированию токсичности разных доз CI-214;
На Фиг.27 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 10 или 20 мкг/мл (18 или 36 мкМ) CI-217, 10 или 20 мкг/мл (17 или 34 мкМ) CI-201, фосфатидилхолином (PC) или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.28 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 10 или 20 мкг/мл (31 мкМ) CI-219 и 20 мкг/мл (34 мкМ) CI-201 или фосфатидилхолином (PC) или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.29 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 10 или 20 мкг/мл (34 мкМ) CI-220 и 20 мкг/мл (34 мкМ) CI-201 или фосфатидилхолином (PC), или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.30А и 30В изображены диаграммы, показывающие результаты отдельного эксперимента по тестированию токсичности разных доз CI-201-РА;
На Фиг.31 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 10 или 20 мкг/мл (17 или 34 мкМ) l-S-CI-201 (CI-S-201), 10 или 20 мкг/мл (17 или 34 мкМ) CI-201, фосфатидилхолином (PC) или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.32 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 10 или 20 мкг/мл (18 или 36 мкМ) l-S-CI-202 (CI-S-202), 10 или 20 мкг/мл (18.5 или 37 мкМ) CI-202, 10 или 20 мкг/мл (17 или 34 мкМ) CI-201, фосфатидилхолином (PC) или смесью PBS/1% этанол (раствор);
ERK1/2 показана как контроль загрузки белка;
На Фиг.33А и 33В изображены диаграммы, показывающие результаты отдельного эксперимента по тестированию токсичности разных доз di-OH;
На Фиг.34 изображена диаграмма, показывающая область атеросклеротических изменений у мышей, обработанных di-OH, и у контрольных мышей;
На Фиг.35 изображена диаграмма, показывающая область атеросклеротических изменений у мышей, обработанных diMeAc, и у контрольных мышей;
На Фиг.36А и 36В изображены диаграммы, показывающие результаты отдельного эксперимента по тестированию токсичности разных доз diEtAc;
На Фиг.37 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 1,5, 10 или 20 мкг/мл (1.7, 8.3, 16.7 или 33.3 мкМ) VB-223 или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.38 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 1, 5, 10 или 20 мкг/мл (1.6, 8, 16 или 32 мкМ) VB-221 или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка;
На Фиг.39 представлена фотография Вестерн-блот анализа, показывающая фосфотирозин (р-Тирозин) в образцах, обработанных 1, 5, 10 или 20 мкг/мл (1.7, 8.4,
16.8 или 33.6 мкМ) VB-222 или смесью PBS/1% этанол (раствор); ERK1/2 показана как контроль загрузки белка.
ОПИСАНИЕ КОНКРЕТНЫХ ВАРИАНТОВ ИЗОБРЕТЕНИЯ
Настоящее изобретение, в некоторых его вариантах, относится к новым окисленным липидам и способам, в которых используются окисленные липиды, для лечения или профилактики воспаления, ассоциированного с эндогенными окисленными липидами. Окисленные липиды, описанные здесь, могут применяться для лечения или профилактики заболеваний и нарушений, ассоциированных с воспалением, таких как, например, атеросклероз и родственные нарушения, аутоиммунные заболевания или нарушения, а также пролиферативные заболевания или нарушения.
Принципы и способы осуществления настоящего изобретения могут быть лучше поняты при обращении к фигурам и прилагаемым описаниям.
Прежде чем перейти к подробному объяснению, по меньшей мере, одного варианта изобретения, необходимо отметить, что изобретение не ограничивается подробной информацией, изложенной в последующем описании или проиллюстрированной Примерами. Возможны другие варианты изобретения, которые можно осуществить на практике или выполнить разными способами. Также, должно быть понятно, что фразеология и терминология, используемая здесь, служит для описания и не ограничивает объем изобретения.
Экспериментальные и клинические данные свидетельствуют о причинной роли окисленного LDL (ox LDL) и компонентов LDL в этиологии повышенной воспалительной реакции в случае атеросклероза. Была продемонстрирована как клеточная, так и гуморальная иммунная реактивность в отношении окисленного LDL, связанного с бляшкам, что позволяет предположить возникновение важного аутоиммунного компонента против окисленного LDL в процессе атерогенеза. Таким образом, против LDL, окисленного LDL и его компонентов были направлены многочисленные методы профилактики и лечения болезней сердца, сердечнососудистых заболеваний и заболеваний периферических сосудов.
Роль окисленных фосфолипидов в лечении воспаления является раскрытой, например, в Международной патентной заявке PCT/IL2004/000453 (Публикация WO 04/106486) и Американской заявке 11/528,657 (Публикация 2007-0099868) настоящего патентообладателя, обе из которых включены здесь в виде ссылки так, как если бы они были изложены здесь полностью.
CI-201 (также называемый здесь и в данной области как VB-201) является многообещающим окисленным фосфолипидом, который в настоящее время проходит расширенные клинические испытания по применению для лечения воспалительных состояний, таких как атеросклероз.
В попытке улучшить лечение воспаления, а также заболеваний и нарушений, ассоциированных с окисленными липидами, авторы настоящего изобретения приготовили новые окисленные фосфолипиды и структурно родственные соединения, которые демонстрируют улучшенное противовоспалительное действие и/или улучшенные фармакологические характеристики.
Улучшенное противовоспалительное действие может быть легко определено с помощью известных in vitro и in vivo моделей воспалительных процессов, а также может проявляться улучшенным терапевтическим действием на подлежащее лечению заболевание, как подробно описано далее. Улучшенные фармакологические характеристики включают улучшенную биостабильность, биодоступность, пониженную токсичность и, более того, улучшенную стабильность в процессе производства, составления и/или хранения. Данные характеристики могут быть также определены с помощью экспериментов, которые легко распознают опытные в данной области специалисты, и как подробно описано далее.
Как показано в последующем разделе «Примеры», при осуществлении настоящего изобретения на практике было действительно подтверждено, что новые разработанные окисленные липиды, описанные здесь, модулируют продукцию цитокина, ассоциированную с иммунной и/или воспалительной реакцией на эндогенный окисленный LDL, тем самым проявляя способность к снижению воспалительной реакции в воспалительных заболеваниях, таких как, но не ограничиваясь ими, атеросклероз и ревматоидный артрит.
Кроме того, как показано в последующем разделе «Примеры», новые разработанные окисленные липиды, описанные здесь, модулируют фосфорилирование тирозина аналогично CI-201, что свидетельствует о том, что данные новые разработанные окисленные липиды разделяют биологические эффекты (например, противовоспалительные действия), которые, как было ранее показано, проявлял CI-201.
Кроме того, как показано в последующем разделе «Примеры», описанные здесь соединения проявляют минимальную токсичность и проявляют биологические эффекты при дозах, при которых соединения являются в значительной степени не токсичными.
На Фиг.1 и 2 показано ингибирование иллюстративным соединением CI-202 продукции субъединицы р40 провоспалительных цитокинов, интерлейкина-12 и интерлейкина-23. На Фиг.3 показана модуляция фосфорилирования тирозина с помощью CI-202, аналогичная модуляции, проявляемой с помощью CI-201. На Фиг.4А и 4В показаны профили токсичности CI-202. На Фиг.5 показано, что CI-202 является терапевтически эффективным в мышиной модели аутоиммунного энцефаломиелита (экспериментальная модель человеческого множественного склероза и острого рассеянного энцефаломиелита). На Фиг.6 показано, что CI-202 является терапевтически эффективным в мышиной модели артрита.
На Фиг.7 показано ингибирование иллюстративным соединением CI-203 продукции субъединицы р40 провоспалительных цитокинов, интерлейкина-12 и интерлейкина-23. На Фиг.8 показана модуляция фосфорилирования тирозина с помощью CI-203, аналогичная модуляции, проявляемой с помощью CI-201. На Фиг.9А и 9В показаны профили токсичности CI-203.
На Фиг.10 показано ингибирование иллюстративным соединением CI-209 продукции субъединицы р40 провоспалительных цитокинов, интерлейкина-12 и интерлейкина-23. На Фиг.11 показана модуляция фосфорилирования тирозина с помощью CI-209. На Фиг.12А и 12В показаны профили токсичности CI-209.
На Фиг.13 показано ингибирование иллюстративным соединением CI-210 продукции субъединицы р40 провоспалительных цитокинов, интерлейкина-12 и интерлейкина-23. На Фиг.14 показана модуляция фосфорилирования тирозина с помощью CI-210. На Фиг.15А и 15В показаны профили токсичности CI-210.
На Фиг.16 показано ингибирование иллюстративным соединением CI-216 продукции субъединицы р40 провоспалительных цитокинов, интерлейкина-12 и интерлейкина-23. На Фиг.18 показана модуляция фосфорилирования тирозина с помощью CI-216, аналогичная модуляции, проявляемой с помощью CI-201.
На Фиг.17 показана модуляция фосфорилирования тирозина с помощью CI-215. На Фиг.19 показана модуляция фосфорилирования тирозина иллюстративным соединением CI-206. На Фиг.21А и 21В показаны профили токсичности CI-206.
На Фиг.20 показана модуляция фосфорилирования тирозина иллюстративным соединением CI-205, аналогичная модуляции, проявляемой с помощью CI-201. На Фиг.22А и 22В показаны профили токсичности CI-205.
На Фиг.23 показана модуляция фосфорилирования тирозина иллюстративным соединением CI-208, аналогичная модуляции, проявляемой с помощью CI-201. На Фиг.24А и 24В показаны профили токсичности CI-208.
На Фиг.25А и 25В, а также 26А и 26В показаны профили токсичности иллюстративных соединений CI-213 и CI-214, соответственно.
На Фиг.27 показана модуляция фосфорилирования тирозина иллюстративным соединением CI-217, аналогичная модуляции, проявляемой с помощью CI-201.
На Фиг.28 показана модуляция фосфорилирования тирозина иллюстративным соединением CI-219, аналогичная модуляции, проявляемой с помощью CI-201.
На Фиг.29 показана модуляция фосфорилирования тирозина иллюстративным соединением CI-220, аналогичная модуляции, проявляемой с помощью CI-201.
На Фиг.30А и 30В показаны профили токсичности иллюстративного соединения CI-201-РА.
На Фиг.31 показана модуляция фосфорилирования тирозина иллюстративным соединением 1-S-CI-201, аналогичная модуляции, проявляемой с помощью CI-201.
На Фиг.32 показана модуляция фосфорилирования тирозина иллюстративным соединением 1-S-CI-202, аналогичная модуляции, проявляемой с использованием CI-201.
На Фиг.34 показано, что иллюстративное соединение di-OH является терапевтически эффективным в мышиной модели атеросклероза. На Фиг.33А и 33В показаны профили токсичности di-OH.
На Фиг.35 показано, что иллюстративное соединение diMeAc является терапевтически эффективным в мышиной модели атеросклероза. На Фиг.36А и 36В показаны профили токсичности diEtAc, соединение тесно связано с diMeAc.
На Фиг.37-39 показана модуляция фосфорилирования тирозина иллюстративными соединениями VB-223, VB-221 и VB-222, соответственно.
Таким образом, было показано, что описанные здесь иллюстративные соединения являются биологически активными по результатам тестов in vitro, и было подтверждено, что некоторые соединения являются терапевтически эффективными in vivo. Свойства окисленного липида, которые не были тестированы in vivo, могут быть далее проверены на пригодных животных моделях, например таких, которые описаны здесь далее в разделе «Примеры», в Международной патентной заявке PCT/IL2004/000453 (Публикация WO 04/106486) и Американской патентной заявке 11/528,657 (Публикация 2007-0099868), и моделях, разработанных, как описано, например, в Singh et al.. Clinical Chemistry 51:12, 2252-2256 (2005), которая включена здесь полностью в виде ссылки, как если бы она была изложена здесь полностью.
Биостабильность окисленных липидов, описанных здесь, является улучшенной благодаря присутствию эфирных и/или сульфидных связей вместо сложноэфирных связей, присутствующих в большинстве липидов. Биостабильность обычно улучшает терапевтическое действие соединения. Биостабильность окисленных липидов можно определить, например, анализом их ферментативного расщепления фосфолипазой-С с использованием ELISA или измерением абсорбции.
Таким образом, описанные здесь окисленные липиды могут быть успешно признаны проявляющими улучшенное действие при лечении или профилактике воспаления, ассоциированного с эндогенными окисленными липидами, в отношении улучшенных терапевтических и/или фармакокинетических параметров.
Таким образом, согласно одному аспекту вариантов по настоящему изобретению, обеспечены новые окисленные липиды (например, окисленные фосфолипиды), как описано здесь.
Согласно одному иллюстративному варианту, окисленный липид представляет собой 1-гексадецил-2-(4-карбокси)бутил-глицеро-3-фосфат (также называемый здесь как «CI-201-PA»). Согласно одному иллюстративному варианту, окисленный липид представляет собой 1 -ге