Нуклеиновая кислота, обладающая активностью короткой интерферирующей рнк, вектор, содержащий данную нуклеиновую кислоту, функционально соединенную с последовательностями регуляции транскрипции, и способ их применения для подавления пролиферации клеток аднокарциномы поджелудочной железы человека
Иллюстрации
Показать всеИзобретение относится к молекулярной биологии, в частности к коротким интерферирующим РНК (siRNA), и может быть использовано в противоопухолевой терапии. На основе геномного анализа сконструированы последовательности siRNA против гена HIF1A человека с SEQ ID NO:1-2, siRNA против гена HSP8A человека с SEQ ID NO:3-4, siRNA против гена APEX1 человека с SEQ ID NO:5-6 и siRNA против гена CCND3 человека с SEQ ID NO:7-8, ассоциированных с пролиферацией клеток аденокарциномы поджелудочной железы человека. Использование полученных siRNA, в том числе в составе лентивирусного вектора, приводит к подавлению пролиферации клеток аденокарциномы поджелудочной железы человека и гибели опухоли. Изобретение позволяет добиться уровня подавления пролиферации до 65% при использовании siRNA к генам HIF1A и HSP8A, ассоциированным со стрессом и отвечающим за основные пролиферативные (CCND3) и репаративные (АРЕХ-1) пути деления клеток. 3 н.п. ф-лы, 10 ил., 2 пр.
Реферат
Область применения изобретения
Изобретение относится к молекулярной биологии, в частности к использованию механизма интерференции рибонуклеиновых кислот (РНК) за счет введения синтетических коротких двухцепочечных олигонуклеотидов: феномен, известный под названием эффекта малых интерферирующих РНК. Может использоваться для терапии рака поджелудочной железы с помощью РНК-интерференции.
Уровень техники
Рак поджелудочной железы (РПЖ) практически не поддается лечению; частота обнаружения в значительной степени коррелирует с летальностью данных больных. Одним из основных его видов - аденокарцинома протоков поджелудочной железы (PDAC, pancreatic ductal adenocarcinoma), остается одним из самых агрессивных типов злокачественных заболеваний, несмотря на многочисленные исследования в этой области и попытки найти способы лечения.
РНК-интерференция является эволюционно древним консервативным процессом, функционирующим в клетках животных и растений. Он обеспечивает защиту клеток от вирусной инвазии, блокируя трансляцию и обеспечивая целевую деградацию матричной РНК (мРНК) на этапе сборки рибосомы [Naqvi et al, Int J Biol Sci. 5, 97-117]. Возможность целевой деградации мРНК и последующее блокирование экспрессии требуемого гена открывают широкие перспективы для использования новых подходов в области терапии опухолевых заболеваний. SiRNA (small interfering RNA, малые интерферирующие РНК) представляют собой короткие двухцепочечные молекулы (до 30 пар оснований), являющиеся активной формой для запуска процесса РНК-интерференции [Elbashir et al. Nature. 411, 494-8]. РНК-интерференция, вызванная siRNA, оказывает посттранскрипционное подавление синтеза белков. В результате введения siRNA в клетки в условиях in vitro наблюдается 50-60%, реже 80-90% подавление экспрессии целевого гена [Gondi et al. J Cell Physiol. 2009, 220, 285-291; Takeshita F, T. Ochiya. Cancer Science. 2006, 97, 689-696]. В силу отсутствия предшественника у siRNA возможно создание искусственных siRNA к целевому белку.
В настоящее время существует два основных способа получения siRNA: синтез siRNA in vitro и введение плазмид, содержащих последовательности генов, необходимых для получения siRNA in vivo. Синтетическая siRNA используется для непосредственного введения в организм или в культуру клеток in vitro. РНК-интерференция с использованием экзогенных siRNA носит временный характер и никогда не обеспечивает 100% подавления экспрессии нужного гена. По разным данным только в единичных случаях можно достичь 80-95% эффекта. Но и этот эффект является кратковременным и требует дополнительных введений молекул siRNA [Paul et al. Nat Biotechnol. 2002, 20, 505-8]. С другой стороны, экспрессия этих молекул эндогенно позволяет добиться более длительного эффекта, что достигается путем генетической трансформации клеток. Исследования по РНК-интерференции клеток PDAC проведены для большого количества генов [Huang et al. Curr Pharm Des. 2011; 17(21):2221-2238].
Описание аналогов
He выявлено аналогов изобретения для терапии рака поджелудочной железы, находящихся на стадии клинических исследований.
Известно изобретение, где описывается возможность ингибирования активности белков STIP1 и ALDH1 А1 посредством блокирования экспрессии их генов. Белок STIP1 является адапторной молекулой, координирующей функциональную активность таких шаперонов, как белки теплового шока HSP10 и HSP90, через регуляцию АТФ-азной активности и конформации шаперонов в субстрат-связанном и свободном состояниях. Белок ALDH1 А1 принадлежит к белкам семейства альдегидодегидрогеназ (WO 2009109952).
Известна композиция на основе ингибиторов АРЕХ1, которые могут быть полезны для диагностики и, возможно, лечения рака (WO 2012148889).
Известна композиция, в состав которой входят антитела к APEX1/Ref-1 для диагностики рака мочевого пузыря (WO 2012077983).
Известно изобретение, в котором описывается возможность использования siRNA к АРЕХ1 в составе лекарственного средства для лечения рака и одновременного анализа повреждений системы репарации АРЕХ1 (KR 20110066469).
Известно изобретение, близкое к описываемому, где используется рекомбинантный аденовирусный вектор со встроенной siRNA, который эффективно предотвращает экспрессию гена АРЕХ1 и эффективно увеличивает чувствительность радиотерапии и химиотерапии опухолевых клеток (CN 101186930).
Известно изобретение, наиболее близкое к описываемому. В нем предлагается использовать siRNA к АРЕХ1, а также циклин-зависимым киназам 3 (CDK3), которые участвуют в регуляции клеточного цикла и пролиферации, с целью лечения рака и других заболеваний клеточной пролиферации (WO 2004007754).
Известно изобретение, близкое к описываемому изобретению, в котором заявлено, что в качестве противоопухолевого агента возможно использовать siRNA для подавления фактора гипоксии HIF1A с целью подавления пролиферации клеток рака и метастазов. Для доставки siRNA в изобретении используют плазмиду с аденовирусным, ретровирусным векторами, а также вирусным вектором коровьей оспы (KR 20120081936).
Известно изобретение, где показана возможность ингибирования активности HIF1A посредством влияния на экспрессию генов с помощью siRNA для эффективного лечения, профилактики или уменьшения роста опухоли (US 2009192104).
Известны изобретения, в которых в качестве активного ингредиента для ингибирования активности HIF1A используют рапонтингенин и цетуксимаб в сочетании с аналогами антиангиогенных гормонов щитовидной железы, таких как тетрак или симистор (KR 20120041390, US 2010255108).
Известно изобретение, в котором снижение экспрессии HIF1A вызвано применением олигомерных компонентов из 12-14 нуклеотидов к мРНК фактора гипоксии, что может использоваться для лечения гиперпролиферативных заболеваний, таких как рак (WO 2009043759).
Не выявлены патенты, описывающие конструкции для РНК-интерференции циклина D3 и HSP8A для терапии рака; не выявлено патентных документов, в которых используются предлагаемые подходы мультиплексной РНК-интерференции генов CCND3, АРЕХ1, HIF1A, HSP8A для терапии рака поджелудочной железы.
В предлагаемом изобретении показана возможность подавления с помощью РНК-интерференции нескольких генов из разных сигнальных путей клетки, что приводит к усилению противоопухолевого эффекта. Из известных генов, для которых показана роль в патогенезе PDAC, взяты четыре гена, которые могут потенциально взаимодействовать и усиливать действие друг друга. Это гены, кодирующие белки теплового шока 70 кДа (HSP8A) [Powers et al. Cancer Cell, 2008; 14:250-262]; фактор гипоксии I типа (HIF1A) [Akakura et al. 2001; 61:6548-54; Chen et al. J. Biol. Chem., 2003; 278:13595-8.]; циклин D3 (CCND3) [Al-Aynati et al. Clin Cancer Res. 2004 Oct 1; 10(19):6598-605; Ito et al. Anticancer Res. 2001; 21:1043-1048; Lapenna, S. & Giordano, Drug Discov. 2009; 8, 547-566] и APEX нуклеазу 1 (APEX1) [Tell et al. Antioxid Redox Signal 2009; 11:601-620; Cardoso et al. PLoS One. 2012; 7(10):e47462].
Изобретение решает задачу подавления экспрессии генов, ассоциированных с пролиферацией клеток аденокарциномы поджелудочной железы человека, что приводит к подавлению их пролиферации и гибели опухоли.
Поставленная задача решается за счет применения нуклеиновых кислот, обладающих активностью малых интерферирующих РНК к генам CCDN3, АРЕХ1, HIF1A, HSP8A (см. перечень последовательностей, SEQ ID №1-8). Для использования данных последовательностей и их комбинаций в терапии рака поджелудочной железы последовательности клонированы в вектора для получения лентивирусов, кодирующих короткие шпилечные структуры (shRNA) соответствующих siRNA, которые нарабатываются эндогенно при заражении опухолевых клеток лентивирусами. Соответствующие лентивирусы получены в клетках-паковщиках НЕК-293Т (фиг.8). Работы по тестированию проведены в культурах in vitro на линиях клеток PDAC: AsPC-1, MiaPaCa и контрольных клетках кератиноцитов человека НаСаТ. Новизна способа применения заключается в комбинировании siRNA или лентивирусных векторов, кодирующих соответствующие shRNA к генам, ассоциированным со стрессом, таким как HIF1A и HSP8A, с генами, отвечающими за основные пролиферативные (CCND3) и репаративные (АРЕХ-1) пути деления клеток.
Техническим результатом является подавление экспрессии данных генов в клетках аденокарциномы поджелудочной железы человека (фиг.1-7) и подавление пролиферации клеток аденокарциномы поджелудочной железы человека при использовании одиночных лентивирусов, а также синергический эффект при использовании их комбинаций (до 65%) (фиг.9-10). Эффект не является специфичным для рака поджелудочной железы. Действие данных последовательностей РНК универсально для всех быстро пролиферирующих клеток, например на клетки кератиноцитов человека НаСаТ, находящихся в состоянии стресса, что характерно для всех раковых клеток.
Изобретение иллюстрируют следующие графические материалы:
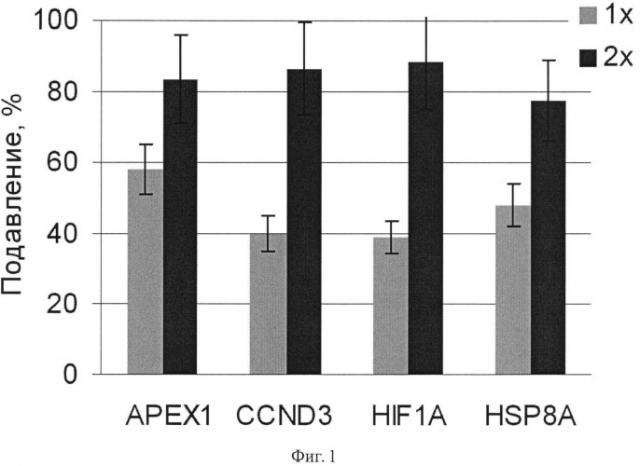
Фиг.1. Подавление экспрессии генов АРЕХ1, CCND3, HIF-1a и HSP8A в клетках аденокарциномы поджелудочной железы человека ВхРС-3 в результате 48 ч РНК интерференции дцРНК к соответствующим генам. Интерференцию осуществляют дцРНК генов однократно (1х) или двухкратно (2х) на 0 и 24 ч. Данные приведены в виде доли от контроля. В контроле трансфекцию проводили несмысловой РНК, меченной флуоресцентным красителем.
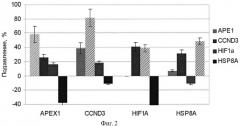
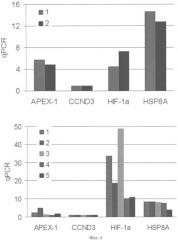
Фиг.2. Подавление экспрессии генов АРЕХ1, CCND3, HIF1A и HSP8A в клетках аденокарциномы поджелудочной железы человека ВхРС-3 в результате 48 ч РНК интерференции дцРНК к соответствующим генам. Трансфекцию проводят однократно. По оси абсцисс указаны гены, анализ экспрессии которых проводили методом кПЦР. Интерференцию осуществляли дцРНК к генам, указанным на вкладке. Уровень подавления целевого гена указан штриховкой. В контроле трансфекцию проводили несмысловой РНК, меченной флуоресцентным красителем.
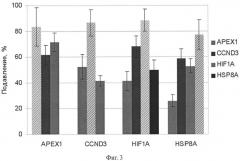
Фиг.3. Подавление экспрессии генов АРЕХ1, CCND3, HIF1A и HSP8A в клетках аденокарциномы поджелудочной железы человека ВхРС-3 в результате 48 ч РНК интерференции дцРНК к соответствующим генам. Трансфекция проведена два раза с интервалом в 24 ч. По оси абсцисс указаны гены, анализ экспрессии которых проводили методом количественной полимеразной цепной реакции. Интерференцию осуществляли дцРНК генов, указанных на вкладке. Уровень подавления целевого гена указан штриховкой. В контроле трансфекцию проводили несмысловой РНК, меченной флуоресцентным красителем.
Фиг.4. Сравнительная экспрессия генов APEX-1, CCND3, HIF1A, HSP8A в клетках аденокарциномы поджелудочной железы AsPC-1 (верхнее окно) и ВхРС-3 (нижнее окно). Результаты приведены в виде относительных единиц, нормированных на экспрессию актина. Приведены данные по 2-м и 5-ти экспериментам для линий AsPC-1 и ВхРС-3 соответственно.
Фиг.5. Подавление экспрессии генов АРЕХ1 и CCND3 в клетках аденокарциномы поджелудочной железы человека ВхРС-3 в результате 48 ч РНК интерференции комбинациями дцРНК к соответствующим генам. Трансфекция проведена однократно. По оси абсцисс указаны гены, анализ экспрессии которых проводили методом количественной полимеразной цепной реакции. Уровень подавления экспрессии целевых генов специфическим дцРНК указан косой штриховкой. Интерференцию осуществляли комбинациями дцРНК генов, указанных на вкладке, где А - АРЕХ-1; С - CCND3; HI - HIF1A; HS - HSP8A. Уровень подавления экспрессии парой дцРНК, в которую входит смысловая для данного гена последовательность, отмечен прямой штриховкой. Достоверный эффект (р<0.05) дополнительного подавления отмечен звездочкой, отсутствие эффекта отмечено «X».
Фиг.6. Подавление экспрессии генов HIF1A и HSP8A в клетках аденокарциномы поджелудочной железы человека ВхРС-3 в результате 48 ч РНК интерференции комбинациями дцРНК к соответствующим генам. Обозначения см. фиг.4.
Фиг.7. Подавление экспрессии целевых генов при мультиплексной РНК интерференции генов АРЕХ1 (A), CCND3 (С), HIF1A (HI) и HSP8 (HS). Подавление экспрессии гена АРЕХ-1 (верхний левый рисунок), CCND3 (верхний правый рисунок), HIF1A (нижний левый рисунок) и HSP8A (нижний правый рисунок) при интерференции отдельными siRNA (серые столбики) и комбинациями siRNA (черные столбики). Достоверное усиление эффекта за счет мультиплексной интерференции указано звездочкой (р<0.05).
Фиг.8. Эффективность трансдукции вирусами, содержащими shRNA генов АРЕХ-1 (А); CCND3 (Б); HIF1A (В) и HSP8A (Г), клеток MiaPaCa. Использовали надосадочные жидкости трансфецированных клеток НЕК-293Т на 20, 48, 72 и 96 часов после трансфекции.
Фиг.9. Подавление пролиферации линии панкреатических клеток AsPC-1 вирусами к генам АРЕХ-1, CCND3, HIF1A, HSP8A и их сочетаниями. Обозначения генов аналогично фиг.5-8.
Фиг.10. Подавление пролиферации линии кератиноцитов человека НаСаТ вирусами к генам АРЕХ-1, CCND3, HIF1A, HSP8A и их сочетаниями. Обозначения генов аналогично фиг.5-9.
Осуществление изобретения
Изобретение иллюстрируют следующие примеры
1. РНК интерференция генов HSP8A, HIF1A, CCND3 и АРЕХ1 в клетках поджелудочной железы
Оценка эффективности подавления экспрессии генов сконструированными siRNA
Оценку экспрессии целевых генов при использовании отдельных дцРНК siRNA или их комбинаций к разным генам-мишеням проводят методом количественной ПЦР «в реальном времени» (кПЦР). Для этого сконструированные и синтезированные пары одноцепочечных последовательностей (SEQ ID №1-8) смешивают 1/1, инкубируют в течение 10 мин при 70°C для получения активных двухцепочечных РНК (дцРНК). Для анализа экспрессии генов используют клетки линий аденокарциномы поджелудочной железы ВхРС-3 (CRL-1687) и AsPC-1 (CRL-1682). Клетки культивируют в стандартных условиях на среде DMEM с 7% фетальной телячьей сыворотки, пенициллин/стрептомицин/глутамин добавками (полная питательная среда, ППС) (все реактивы из ПанЭко, Москва, Россия) во флаконах Costar (ПанЭко, Москва, Россия). Перед экспериментом клетки снимают с пластика раствором трипсина/ЭДТА (ПанЭко, Москва, Россия), подсчитывают концентрацию, переводят в ППС без антибиотиков и рассевают в 24-луночные планшеты по 300 тысяч на лунку. Клетки выращивают ночь. Трансфекцию дцРНК проводят с помощью агента ScreenFect (InCella, дистрибьютор Русбиолинк, Москва, Россия) по протоколу производителя. Для анализа эффективности трансфекции используют флуоресцентно меченые несмысловые дцРНК. Трансфекцию проводят однократно отдельными дцРНК или их комбинациями. Клетки с дцРНК инкубируют 48 часов, после чего из клеток выделяют тотальную РНК. Выделение РНК и обработка РНК ДНКазой RQ1.
Через 48 ч после посева клетки отмывают средой без сыворотки и выделяют РНК из образцов, используя реагент Trizol (Invitrogen), следуя инструкциям изготовителя. Для удаления примесей геномной ДНК тотальную РНК обрабатывают ДНКазой RQ1 (Promega) по инструкции изготовителя. Обработанную РНК используют в синтезе первой цепи.
Синтез первой цепи
Синтез первой цепи с полученных образцов РНК осуществляют с помощью набора Revert Aid (Thermo), следуя инструкциям изготовителя. В качестве затравки для синтеза используют гексамеры со случайной последовательностью. 0,5-1 мкг тотальной РНК инкубируют 10 мин с гексамерами и смесью четырех дезоксинуклеозидтрифосфатов на льду. К смеси добавляют буфер для обратной транскриптазы и обратную транскриптазу и инкубируют 10 мин при +25°C и далее 30 мин при +50°C. Для остановки реакции смесь прогревают 10 мин при 85°C. Полученную первую цепь используют далее в качестве матрицы в кПЦР.
ПЦР в «реальном времени» (кПЦР)
Для проведения кПЦР используют праймеры (перечень последовательностей, SEQ ID №9-18). В качестве референсного гена используют ген β-актина. кПЦР для каждой матрицы и соответствующего праймера проводят в 2 повторах. Кроме того, в каждой ПЦР для всех используемых матриц проводят реакции с праймерами на референсный ген (для нормализации уровня мРНК генов-мишеней), и для каждого праймера проводят контрольную реакцию, содержащую воду вместо матрицы. Для проведения кПЦР используют реактивы производства компании Синтол, Москва. В 1,5 мл пробирке смешивают воду и 2,5х реакционную смесь, содержащую 2,5х ПЦР буфер (KCl, Трис-HCl pH 8,8, 6,25 мМ MgCl2), Taq ДНК-полимеразу, смесь четырех дезоксинуклеозидтрифосфатов, глицерин, Tween-20, интеркалирующий краситель EvaGreenI и пассивный референсный краситель ROX. Далее общую смесь разделяют на необходимое число частей, соответствующих количеству праймеров к генам-мишеням плюс референсный ген, и к каждой части добавляют отдельную пару праймеров. Далее каждую часть делят на аликвоты, количество которых соответствует числу анализируемых образцов кДНК для данной пары праймеров плюс одна контрольная аликвота, куда вместо матрицы добавляют воду. После добавления матриц или воды аликвоты разделяют на два повтора и вносят в лунки планшета для ПЦР.
Готовые пробы помещают в прибор CFX96 (Bio-Rad), реакции проводят, используя следующую программу для проведения кПЦР (красители: EvaGreenl/ROX): 95°C - 300 сек, 1 цикл; 60°C - 40 сек, 95°C - 15 сек, 50 циклов.
Для подтверждения гомогенности продукта проводят реакцию плавления полученных фрагментов.
При трансфекции клеток целевыми дцРНК для всех выбранных последовательностей siRNA наблюдают снижение экспрессии целевого гена, уровень снижения экспрессии зависит от варианта применения siRNA. Эффект РНК-интерференции усиливается при двукратной трансфекции целевыми siRNA и при мультиплексной трансфекции siRNA к разным генам (фиг.1-7).
2. Получение shRNA в лентивирусах и оценка способности данных RNA подавлять пролиферацию раковых клеток
Получение лентивирусов, содержащих последовательности siRNA генов АРЕХ-1, CCND3, HIF1A и HSP8A
Для получения терапевтических препаратов последовательности siRNA (SEQ ID №1-8) клонируют в виде шпилечных структур shRNA в вектор pLVneo стандартными методами. В плазмиду дополнительно вводят ген, кодирующий зеленый флуоресцентный белок (GFP) для визуализации трансфекции и трансдукции. Полученные плазмиды используют для получения лентивирусных частиц с использованием плазмид-паковщиков везикулярного стоматита VSV и цитомегаловируса CMV. Вирусные частицы нарабатывают в клетках НЕК-293Т. Наличие и титры вирусов определяют по эффективности трансдукции клеток MiaPaCa полученными вирусами. Показано, что вирусы, содержащие CCND3 и HIF1A, нарабатываются в течение 48-72 ч; вирусы, содержащие АРЕХ-1 и HSP8A, несколько позже с пиком на 96 ч (Фиг.8).
Влияние РНК интерференции на пролиферацию клеток поджелудочной железы
Эксперимент проводят на клеточных линиях аденокарциномы поджелудочной железы AsPC-1 и на клетках кератиноцитов человека НаСаТ. Клетки культивируют во флаконах в полной питательной среде DMEM с антибиотиками, 7% фетальной сыворотки теленка, L-глутамином и 2-меркаптоэтанолом (все из ПанЭко, Москва, Россия). Перед экспериментом клетки отделяют от планшета трипсином, подсчитывают и переносят в 96-луночные планшеты в полной питательной среде по 15 тыс. клеток на лунку; к клеткам добавляют полибрин в конечной концентрации 8 мкг/мл для улучшения адгезии вирусов к клеткам. До внесения клеток на планшеты наносят вирусы (по 25 мл на лунку) или их смеси в 100 мкл, а затем разносят клетки. Инкубацию проводят в течение 72 часов в СО2 инкубаторе при 37°C. Выживание клеток определяют с помощью МТТ-теста. На последние 3 часа инкубирования в каждую лунку вносят по 10 мкл раствора МТТ (5 мг/мл, Sigma). По окончанию инкубирования культуральную жидкость удаляют переворотом планшета и вносят по 100 мкл диметилсульфоксида для растворения кристаллов формазана, образованного в результате восстановления МТТ живыми клетками. Измерение оптической плотности содержимого каждой лунки проводят на приборе Multiscan FC (Thermo Fisher Scientific, USA) при длине волны 540 нм. Выживание клеток оценивают по оптической плотности раствора формазана. Как для клеток панкреатической линии AsPC-1, так и для клеток линии кератиноцитов НаСаТ наблюдается эффект усиления действия вирусов при их сочетании (Фиг.9-10).
Перечень последовательностей
SEQ ID №1
5′-UGUGUCCUUAAACCGGUUGdTdT-3′ - прямая siRNA к гену HIF1A
SEQ ID №2
5′-CAACCGGUUUAAGGACACAdTdT-3 - обратная siRNA к гену HIF1A
SEQ ID№3
5′-GAUGAAGGAAAUUGCAGAAdTdT-3′ - прямая siRNA к гену HSP8A
SEQ ID №4
5′-UUCUGCAAUUUCCUUCAUCdTdT-3′ - обратная siRNA к гену HSP8A
SEQ ID №5
5′-GUCUGGUACGACUGGAGUACC-3′ - прямая siRNA к гену АРЕХ1
SEQ ID №6
5′-UACUCCAGUCGUACCAGACCU-3′ - обратная siRNA к гену АРЕХ1
SEQ ID №7
5′-GACCAGCACUCCUACAGAUdTdT-3′ - прямая siRNA к гену CCND3
SEQ ID №8
5′-AUCUGUAGGAGUGCUGGUCdTdT-3′ - обратная siRNA к гену CCND3
SEQ ID №9
5′TTCACCTGAGCCTAATAGTCC3′ - прямой праймер к гену HIF1A
SEQ ID №10
5′CAAGTCTAAATCTGTGTCCTGAG3′ - обратный праймер к гену HIF1A
SEQ ID №11
5′CTTTATGGTGGTGAATGATGCT3′ - прямой праймер к гену HSP8A
SEQ ID №12
5′GGTAACAGTCTTCCCAAGGT3′ - обратный праймер к гену HSP8A
SEQ ГО №13
5′CTTACGGCATAGGCGATGAG3′ - прямой праймер к гену АРЕХ1
SEQ ID №14
5′TACTCCAGTCGTACCAGACC3′ - обратный праймер к гену АРЕХ1
SEQ ID №15
5′GATTTCCTGGCCTTCATTCTG3′ - прямой праймер к гену CCND3
SEQ ID №16
5′GGCAAAGGTATAATCTGTAGCAC - обратный праймер к гену CCND3
SEQ ID №17
5′CACCACACCTTCTACAATGAG3′ - прямой праймер к гену B-actin
SEQ ID №18
5′GTCTCAAACATGATCTGGGTC3′ - обратный праймер к гену B-actin
1. Нуклеиновая кислота для подавления пролиферации клеток аденокарциномы поджелудочной железы человека, характеризующаяся нуклеотидной последовательностью, выбранной из SEQ ID №:1-8.
2. Лентивирусный вектор, содержащий по крайней мере одну нуклеиновую кислоту по п.1, функционально соединенную с последовательностями регуляции транскрипции, для подавления пролиферации клеток аденокарциномы поджелудочной железы человека.
3. Способ подавления пролиферации клеток аденокарциномы поджелудочной железы человека по меньшей мере одной нуклеиновой кислотой по п.1 или по меньшей мере одним вектором по п.2.