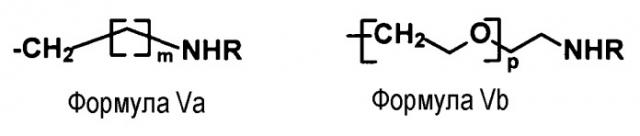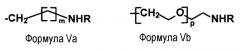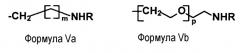Способы и композиции, относящиеся к синтетическим бета-1,6-глюкозаминолигосахаридам
Иллюстрации
Показать всеИзобретение относится к эффективным для лечения и профилактики инфекционных заболеваний конъюгатам олигосахарид-носителям, содержащим олигосахарид, конъюгированный с носителем через линкер формул VIIIa или VIIIb:
где n больше 1, m выбран из 1-10, p выбран из 1-20 и R представляет собой H или алкил, линкер связан с атомом кислорода олигосахарида через концевую CH2 группу, и линкер связан через концевую CO группу с аминогруппой соединения носителя посредством амидной связи, олигосахарид является β-1-6 связанным глюкозамином, и носитель является пептидом, белком, полисахаридом, нуклеиновой кислотой, липидом или столбнячным анатоксином. Предложены новые конъюгаты, эффективные для стимуляции иммунного ответа, и способ их получения. 9 н. и 12 з.п. ф-лы, 12 пр., 23 ил., 1 табл.
Реферат
Родственные заявки
По настоящей заявке испрашивается приоритет предварительных заявок на патенты США 61/135493 и 61/208155, поданных 21 июля 2008 года и 20 февраля 2009 года, соответственно, все содержание которых включено в настоящую заявку путем ссылки.
Правительственная поддержка
Настоящее изобретение было частично поддержано грантом Национального Института Здравоохранения США RO1A1046706. Правительство США обладает правами на изобретение.
Область техники, к которой относится изобретение
Изобретение относится к композициям и способам, относящимся к синтетическим олиго-β-(1→6)-2-амино-2-дезокси-D-глюкопиранозидам, которые в настоящей заявке взаимозаменяемо упоминаются как олиго-β-(1→6)-D-глюкозамины или олигоглюкозамины.
Уровень техники
Стафилококки (Staphylococci) представляют собой грамположительные бактерии, которые обычно населяют и колонизируют кожу и слизистые оболочки человека. Если кожа или слизистая оболочка повреждаются при хирургической операции или другой травме, то стафилококки могут получить доступ к внутренним тканям, что приводит к развитию инфекции. Если стафилококки пролиферируют локально или попадают в лимфатическую или кровеносную систему, то могут развиваться тяжелые инфекционные осложнения, связанные со стафилококковой бактериемией. Указанные осложнения включают септический шок, эндокардит, артрит, остеомиелит, пневмонию и абсцессы в различных органах.
Стафилококки включают как коагулаза-положительные организмы, которые продуцируют свободную коагулазу, так и коагулаза-отрицательные организмы, которые не продуцируют свободную коагулазу. Золотистый стафилококк (Staphylococcus aureus) является наиболее распространенной коагулаза-положительной формой стафилококков. S.aureus обычно вызывает инфекцию в локальном участке, экстраваскулярно или интраваскулярно, которая, в конечном счете, может привести к бактериемии. S.aureus также является основной причиной острого остеомиелита и вызывает инфекционные стафилококковые пневмонии. Кроме того, S.aureus является причиной приблизительно 1-9% случаев бактериального менингита и 10-15% абсцессов мозга.
Существует по меньшей мере тридцать один известный вид коагулаза-отрицательных стафилококков, включая S.epidermidis, S.saprophyticus, S.hominis, S.warneri, S.haemolyticus, S.saprophiticus, S.cohnii, S.xylosus, S.simulans и S.capitis. S.epidermidis является наиболее частым инфекционным агентом, связанным с внутривенными катетерами, и наиболее часто выделяется при первичных госпитальных бактериемиях. S.epidermidis также связан с эндокардитом искусственного клапана.
Стафилококк также является распространенным источником бактериальной инфекции у животных. Например, стафилококковый мастит является обычной проблемой у жвачных животных, таких как рогатый скот, овцы и козы. Болезнь обычно лечат антибиотиками с целью устранить инфекцию, однако подобная терапия является дорогостоящей процедурой и в то же время приводит к потере производства молока. Наиболее эффективными вакцинами, известными на настоящее время, являются живые, интактные вакцины S.aureus, которые вводят подкожно. Однако введение живых вакцин связано с риском инфекции. По этой причине многие исследователи пытались получить инактивированные вакцины S.aureus и/или выделить капсулярные полисахариды или компоненты клеточной стенки, которые будут вызывать иммунитет к S.aureus.
Соединения-носители иногда применяются в вакцинах для усиления иммунного ответа на антиген. Например, носитель в некоторых вакцинах может применяться для стимуляции хелперных T-клеток в ответ на антигенную молекулу. Антигенные молекулы, которые являются природными веществами или фрагментами природных веществ, в некоторых случаях менее удобны и с меньшей легкостью поддаются манипуляциям и/или конъюгированию с другими соединениями, такими как, например, соединения-носители, и это может уменьшать терапевтический эффект таких вакцин.
Сущность изобретения
Изобретение относится к новым способам и соединениям для получения антигенных композиций, таких как, но ими не ограничиваясь, вакцины. В частности, изобретение относится к новым способам модификации олигосахаридных антигенов. Указанные способы включают контролируемый синтез олигосахарида, (a) состоящего из моносахаридных мономеров в определенном порядке и (b) конъюгированного с соединением-носителем. Полученные в результате конъюгаты способны лучше стимулировать (либо посредством индукции, либо усиления) иммунный ответ в отношении целевого микробного полисахаридного антигена. Как описано в настоящей заявке, такие иммунные ответы полезны при лечении и/или профилактике различных инфекций, включая, но ими не ограничиваясь, стафилококковые инфекции.
Различные аспекты изобретения относятся к конкретным линкерам (или сшивающим агентам, или спейсерам, или сшивающим реагентам, причем указанные термины взаимозаменяемо используются в настоящей заявке), а также к их применению в синтезе конъюгатов. Особый интерес представляют конъюгаты олигосахаридов и различных соединений-носителей. Указанные олигосахариды включают олиго-β-(1→6)-D-глюкозамин (связанный глюкозамин, как указано в настоящей заявке), который состоит из глюкозаминовых мономеров, соединенных друг с другом β-(1→6) связью. Один или несколько различных мономеров, которые составляют связанный глюкозамин, могут быть N-ацетилированы. Таким образом, мономерами могут быть D-глюкозаминовые или N-ацетил-D-глюкозаминовые мономеры, при этом связанный глюкозамин может включать определенную последовательность из одного или обоих типов данных мономеров (или моносахаридов, поскольку указанные термины используются в настоящей заявке взаимозаменяемо). Олигоглюкозамины по изобретению также включают спейсеры, которые имеют тиолсодержащие группы на своих "восстанавливающих" концах. Спейсер используется для связывания олигоглюкозаминов с носителями. Носители могут состоять из аминокислот (например, пептиды или белки), хотя они не ограничиваются этим.
Таким образом, в одном аспекте изобретение относится к соединению формулы I:
Формула I
где X является любым атомом или группой, Y является защитной группой серы и n больше 1. В одном варианте осуществления Y является ацильной группой. В другом варианте осуществления Y является ацетильной группой, при этом соединение имеет структуру формулы II:
Формула II
где Ac является ацетильной группой.
В другом варианте осуществления соединение является активированным сложным эфиром формулы I. В другом варианте осуществления соединение является циано, азидо или галогенпроизводным активированного сложного эфира формулы I. В другом варианте осуществления соединение имеет структуру формулы III:
Формула III
где Ac является ацетильной группой, и соединение называется N-гидроксисукцинимидил-4-ацетилсульфанилбутиратом. В другом варианте осуществления соединение имеет структуру формулы IV:
Формула IV
где Ac является ацетильной группой, и соединение называется N-нитрофенил-4-ацетилсульфанилбутиратом.
В другом аспекте изобретение относится к способу синтеза N-гидроксисукцинимидил-4-ацетилсульфанилбутирата (формула III), включающему реакцию 4-ацетилсульфанилмасляной кислоты (формула V):
Формула V
с N-гидроксисукцинимидилтрифторацетатом (CF3COOSu) с получением N-гидроксисукцинимидил-4-ацетилсульфанилбутирата (формула III).
В другом аспекте изобретение относится к способу синтеза N-нитрофенил-4-ацетилсульфанилбутирата (IV), включающему реакцию 4-ацетилсульфанилмасляной кислоты (формула V):
Формула V
с N-нитрофенилтрифторацетатом (CF3COOpNp) с получением N-нитрофенил-4-ацетилсульфанилбутирата (формула IV).
В другом аспекте изобретение относится к способу синтеза олигосахарида, конъюгированного с носителем, включающему реакцию олигосахарида (a) во-первых, с соединением, имеющим структуру формулы Va или Vb:
где m является числом, выбранным из 1-10, p является числом, выбранным из 1-20, а R представляет собой H или алкильную группу, (b) во-вторых, с соединением формулы I, II, III или IV и (c) в-третьих, с носителем, где олигосахарид представляет собой β-1-6 связанный глюкозамин.
В еще одном аспекте изобретение относится к композиции, содержащей олигосахарид, несущий O-связанный линкер, где линкер включает:
Формула VI
В одном варианте осуществления олигосахарид представляет собой β-1-6 связанный глюкозамин. В другом варианте осуществления длина олигосахарида составляет 2-20 мономеров. В другом варианте осуществления длина олигонуклеотида составляет 5-11 мономеров. В еще одном варианте осуществления длина олигосахарида составляет 7, 9 или 11 мономеров.
В одном варианте осуществления олигосахарид ацетилирован на 0% или ацетилирован на 100%. В другом варианте осуществления олигосахарид ацетилирован на 0-40%.
В еще одном аспекте изобретение относится к композиции, содержащей конъюгат олигосахарид-носитель, содержащий олигосахарид, конъюгированный с носителем через линкер, который представляет собой:
Формула VIIIa
Формула VIIIb
где линкер является O-связанным с олигосахаридом и N-связанным с носителем.
В еще одном аспекте изобретение относится к способу синтеза конъюгата олигосахарид-носитель, включающему реакцию олигосахарида, конъюгированного с линкером формулы IXa или IXb:
Формула IXa
Формула IXb,
с носителем, имеющим аминогруппу, модифицированную в результате реакции с соединением формулы:
Формула X
с получением олигосахарида, конъюгированного с соединением-носителем через линкер, имеющий структуру формулы VIIIa или VIIIb.
В одном варианте осуществления носитель является пептидом. В другом варианте осуществления носитель является белком. Примером носителя является столбнячный анатоксин.
В одном варианте осуществления олигосахарид представляет собой β-1-6 связанный глюкозамин.
В одном варианте осуществления композиция имеет соотношение олигосахарида к носителю 1:1, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1, 8:1, 9:1, 10:1, 20:1, 30:1, 40:1, 50:1, 60:1, 70:1, 80:1, 90:1 или 100:1.
В некоторых вариантах осуществления длина олигосахарида составляет 2-20 мономеров, 5-11 мономеров или 5, 7, 9 или 11 мономеров.
В одном варианте осуществления олигосахарид ацетилирован на 100%. В другом варианте осуществления олигосахарид ацетилирован на 0%. В еще одном варианте осуществления олигосахарид ацетилирован на 0-40%.
В некоторых вариантах осуществления композиция дополнительно содержит фармацевтически приемлемый носитель, адъювант и/или антибактериальное средство.
В другом аспекте изобретение относится к способу стимуляции иммунного ответа у субъекта, включающему введение субъекту, нуждающемуся в этом, конъюгата олигосахарид-носитель, описанного выше, или конъюгата олигосахарид-носитель, синтезированного способом, описанным выше, в количестве, эффективном для стимуляции иммунного ответа у субъекта.
В одном варианте осуществления субъект является человеком. В другом варианте осуществления субъект не является человеком.
В другом варианте осуществления способ дополнительно включает выделение антител или антителопродуцирующих клеток у субъекта.
В другом варианте осуществления способ дополнительно включает введение субъекту адъюванта. В другом варианте осуществления способ дополнительно включает введение субъекту антибактериального средства.
В еще одном аспекте изобретение относится к способу лечения или профилактики инфекции у субъекта, включающему введение субъекту, имеющему инфекцию или подверженному риску ее развития, эффективного для индукции иммунного ответа количества конъюгата олигосахарид-носитель, описанного выше, или конъюгата олигосахарид-носитель, синтезированного способом, описанным выше, где инфекция вызвана видом бактерии, которая продуцирует или способна продуцировать PNAG.
В одном варианте осуществления инфекция является инфекцией Staphylococcus. В соответствующем варианте осуществления инфекция Staphylococcus является инфекцией Staphylococcus aureus. В другом соответствующем варианте осуществления инфекция Staphylococcus является инфекцией Staphylococcus epidermidis. В одном варианте осуществления субъект подвергается риску воздействия Staphylococcus. В другом варианте осуществления субъект подвергся воздействию Staphylococcus.
В других вариантах осуществления инфекция является инфекцией E.coli, инфекцией Y.pestis, инфекцией Y.entercolitica, инфекцией Y.pseudotuberculosis, инфекцией Aggregatibacter actinomycetemcomitans, инфекцией Actinobacillus pleuropneumoniae, инфекцией Bordetella pertussis, инфекцией B.parapertussis, инфекцией B.bronchiseptica, инфекцией Acinetobacter, инфекцией Burkholderia, например, Burkholderia cenocepacia, инфекцией Stenatrophomonas maltophilia, инфекцией Shigella или инфекцией Klebsiella, такой как Klebsiella pneumoniae.
В некоторых вариантах осуществления конъюгат олигосахарид-носитель вводят с адъювантом и/или антибактериальным средством.
В еще одном аспекте изобретение относится к способу получения антител, включающему введение субъекту эффективного для продукции антител, специфичных к нативному PNAG, количества конъюгата олигосахарид-носитель, описанного выше, или конъюгата олигосахарид-носитель, синтезированного способом, описанным выше, и выделение антитела у субъекта.
В другом аспекте изобретение относится к способу получения моноклональных антител, включающему введение субъекту эффективного для продукции антител, специфичных к нативному PNAG, количества конъюгата олигосахарид-носитель, описанного выше, или конъюгата олигосахарид-носитель, синтезированного способом, описанным выше, сбор антителопродуцирующих клеток у субъекта, слияние антителопродуцирующих клеток, полученных у субъекта, с клетками миеломы и сбор антитела, продуцируемого из слитого субклона.
В одном варианте осуществления антитела являются поликлональными антителами. В одном варианте осуществления субъектом является кролик. В другом варианте осуществления субъектом является человек.
Следует понимать, что все комбинации предыдущих принципов и дополнительных принципов, описываемых более подробно ниже (при условии, что такие понятия не являются взаимно исключающими), рассматриваются как часть предмета изобретения, раскрытого в настоящей заявке. В частности, все комбинации заявленных объектов, приведенных в конце настоящего описания, рассматриваются как часть предмета изобретения, раскрытого в настоящей заявке. Необходимо также понимать, что терминология, прямо применяемая в настоящей заявке, которая также может присутствовать в любом описании, включенном путем ссылки, должна соответствовать значению, наиболее соответствующему конкретным принципам, раскрытым в настоящей заявке.
Краткое описание фигур
Фиг.1A и B представляют собой графики, на которых показано связывание антисывороток, индуцированных против неацетилированного нонаглюкозамина (9GlcNH2), с PNAG (A) или dPNAG (B) из S.aureus.
Фиг.2A и B представляют собой графики, на которых показано связывание антисывороток, индуцированных против полностью ацетилированного нонаглюкозамина (9GlcNAc), с PNAG или dPNAG из S.aureus.
Фиг.3A и B представляют собой графики, на которых показано связывание антисывороток, индуцированных против конъюгированного 9GlcNAc или 9GlcNH2, с 11GlcNAc или 11GlcNH2.
Фиг.4 представляет собой график, на котором показана гибель бактерий S.aureus штамма MN8 под действием антисывороток, индуцированных у двух кроликов, один из которых получал конъюгат 9GlcNH2-TT, а второй получал конъюгат 9GlcNAc-TT, при этом антисыворотку забирали через 2 недели после последней инъекции вакцины.
Фиг.5 представляет собой график, на котором показана гибель бактерий S.aureus штамма MN8 под действием антисывороток, индуцированных у двух кроликов, один из которых получал конъюгат 9GlcNH2-TT, а второй получал конъюгат 9GlcNAc-TT, при этом антисыворотку забирали через 4 недели после последней инъекции вакцины, а также, для сравнения, показана гибель тех же бактерий под действием антисыворотки, индуцированной к конъюгированной вакцине, состоящей из молекулы dPNAG (примерно 100 кДа), конъюгированной со столбнячным анатоксином (TT) и далее обозначенной (051).
Фиг.6-8 представляют собой графики, на которых сравнивается гибель штаммов S.aureus (фиг.6 и 8, LAC (NT, USA300); фиг.7, SF8300 (NT, USA300)) под действием антисывороток кролика (забор 1) к полностью ацетилированному или неацетилированному 9-меру олигоглюкозамину (9GlcNH2), конъюгированному с TT (9GlcNH2-TT). Для сравнения показана гибель тех же бактерий под действием антисыворотки, индуцированной к конъюгированной вакцине, состоящей из молекулы dPNAG (примерно 100 кДа), конъюгированной со столбнячным анатоксином (TT) и далее обозначенной (051).
Фиг.9-16 представляют собой графики, на которых сравнивается гибель штаммов S.aureus (фиг.9, MN8 (капсулярный полисахарид (CP) 8); фиг.10, LAC (нетипируемый (NT), USA300)); фиг.11, SF8300 (NT, USA300)); фиг.12, Newman (CP5); фиг.13, PS80; фиг.14, Reynolds (CP5); фиг.15, Reynolds (нетипируемый); фиг.16, Reynolds (CP8)) под действием антисыворотки кролика (обозначенной "забор 2") к полностью ацетилированному или неацетилированному 9-меру олигоглюкозамину, конъюгированному с TT. Для сравнения показана гибель тех же бактерий под действием антисыворотки, индуцированной к конъюгированной вакцине, состоящей из молекулы dPNAG (примерно 100 кДа), конъюгированной со столбнячным анатоксином (TT) и далее обозначенной (051).
Фиг.16A представляет собой график, на котором показана гибель двух PNAG-положительных (E.coli J и E.coli P), но не PNAG-отрицательного (E.coli H), штаммов E.coli под действием антисывороток кролика к 9GlcNH2-TT, полученных через 6 недель после последней иммунизации.
Фиг.17, 18 и 19 представляют собой графики, на которых показаны результаты исследования in vivo, которое относится к профилактике кожного абсцесса, вызванного инфекцией S.aureus, после иммунизации антисывороткой, индуцированной против неацетилированного 9-мера олигоглюкозамина, конъюгированного с TT (9GlcNH2-TT, забор 2), и введенной мышам за 24 часа до заражения 2×104 (фиг.18), 2×105 (фиг.19) или 2×106 (фиг.20) КОЕ штамма S.aureus LAC.
На фиг.20 показано обобщение результатов, представленных на фиг.17-19.
Фиг.21, 22 и 23 представляют собой графики, на которых показаны результаты исследований in vivo, которые относятся к профилактике кожного абсцесса, вызванного инфекцией S.aureus, после иммунизации антисывороткой, индуцированной против неацетилированного 9-мера олигоглюкозамина и введенной мышам до заражения 1×106 КОЕ S.aureus MN8 (фиг.21), 4×106 КОЕ S.aureus Newman (фиг.22) и 4×106 КОЕ S.aureus NewmanΔica и 1,5×106 КОЕ S.aureus MN8Δica (фиг.23).
Подробное описание изобретения
Изобретение в целом относится к синтезу и применению олигосахаридного конъюгата. Изобретение относится к способам синтеза de novo и композициям, применяемым в них для получения новых композиций. Указанные способы синтеза облегчают модификацию олигосахарида или полисахарида, которая была бы невозможна при использовании природных полисахаридных антигенов.
Изобретение относится, среди прочего, к способам получения олиго-β-(1→6)-D-глюкозаминолигосахаридов или полисахаридов, имеющих определенный порядок мономеров, способам конъюгирования таких олигосахаридов или полисахаридов с линкерами для последующего конъюгирования с соединениями-носителями, способам получения конъюгатов олигосахарид-носитель или конъюгатов полисахарид-носитель, а также композициям указанных различных соединений. Изобретение также относится к различным новым линкерам, которые неожиданно являются более полезными, чем ранее известные линкеры, в указанных способах получения. Полученный в результате конъюгат олигосахарид-носитель является пригодным для стимуляции иммунного ответа in vivo у человека и субъектов, не являющихся человеком, включая получение антител непосредственно к олигосахаридам и к соответствующим природным антигенам PNAG и dPNAG.
Антигены PNAG и dPNAG более подробно описаны в опубликованной заявке PCT WO 2004/043405. В кратком изложении, PNAG относится к поли-N-ацетилглюкозамину, который является поверхностным полисахаридом, продуцируемым различными видами бактерий, включая, но ими не ограничиваясь, стафилококки, такие как S.aureus и S.epidermis. PNAG существует в природе как в высоко, так и в недостаточно ацетилированных формах. "Высокоацетилированная" форма PNAG представляет собой PNAG, имеющий более 50% ацетатного замещения. Недостаточно ацетилированные формы PNAG (именуемые в настоящей заявке как dPNAG) могут иметь 0-40% ацетилирования. (См. формулу VII, где R1 обозначает положение ацетильной группы, если таковая присутствует). Нативный PNAG представляет собой смесь форм PNAG с различными степенями ацетилирования. Нативный PNAG может включать dPNAG в смеси с ацетилированными в более высокой степени формами PNAG. PNAG или dPNAG могут состоять из сотен или тысяч, или большего количества глюкозаминовых звеньев (или мономеров).
Олигосахариды по изобретению, как предполагается, имитируют области PNAG или dPNAG. Таким образом, в случае применения in vivo, конъюгат олигосахарид-носитель индуцирует иммунные ответы, направленные к областям олигосахарида, которые являются подобными или идентичными PNAG и/или dPNAG, и поэтому такие иммунные ответы эффективны против таких видов бактерий, которые продуцируют или способны продуцировать PNAG и/или dPNAG.
В некоторых аспектах изобретения олигосахариды состоят только из D-глюкозаминовых или только из N-ацетил-D-глюкозаминовых звеньев, или из обоих типов указанных мономеров в определенном отношении и порядке. Отношение и порядок служат для имитации, в некоторых вариантах осуществления, отношений и порядков, присутствующих в нативном PNAG. Олигосахариды подвергают манипуляциям согласно изобретению для включения спейсера (или линкера, поскольку данные термины используются в настоящей заявке взаимозаменяемо), содержащего тиольные группы на своем конце (например, на восстанавливающем конце).
Получение олигосахаридов, содержащих аминогруппы, таких как связанные глюкозаминолигосахариды (или олигоглюкозамины, поскольку данные термины используются в настоящей заявке взаимозаменяемо), подходящих для конъюгирования с одним или несколькими носителями, является затруднительным в данной области. Частично это обусловлено тем, что стереоспецифичный синтез связанного глюкозамина требует использования участвующих, но временных, ацильных N-защитных групп (так называемых "участвующих" групп) в гликозильных донорах для образования необходимой β-гликозидной связи между мономерами. N-фталоильная, N-трихлорэтоксикарбонильная и некоторые другие группы подходят в качестве участвующих групп. Некоторые другие участвующие группы, однако менее подходящие, включают N-ацетильные участвующие группы, которые присутствуют в некоторых олигосахаридах, рассматриваемых в рамках изобретения. В качестве примера, N-ацетилированные гликозильные доноры обладают низкой реакционной способностью и дают только скромные выходы продуктов гликозилирования. Кроме того, присутствие N-ацетильных групп в гликозильном доноре усложняет реакцию гликозилирования вследствие образования оксазолина в качестве промежуточного продукта, миграции N-ацетильных групп и других нежелательных химических реакций.
В отношении связанных глюкозаминов, их структура, а более конкретно, количество аминогрупп, которые они содержат, требует введения линкера перед полным освобождением аминогрупп. Удаление вышеуказанной временной N-защитной группы с получением свободного олигосахарида проводят в основных условиях. Наиболее эффективным реагентом для удаления N-фталоильной участвующей группы является гидразингидрат в кипящем этаноле. Указанный реагент также эффективно удаляет O-ацильные защитные группы, включая ацетильные и бензоильные группы, которые могут содержаться в целевом олигосахариде.
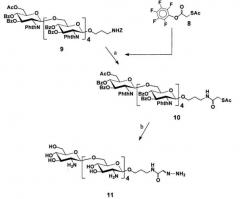
Коммерчески доступные линкеры, которые использовали для присоединения аминосодержащих лигандов к белкам, представляли собой пентафторфенил-S-ацетилтиогликолят (химическая структура 8, показанная в примерах) и N-гидроксисукцинимидил-3-ацетилсульфанилпропионат (химическая структура 12, показанная в примерах). Указанные сшивающие реагенты могут быть использованы для введения в олигосахарид тиольной группы; однако, как более подробно описано в примерах, оба реагента нестабильны в условиях удаления фталоильных групп. В примере 5 показано, что линкер на основе тиогликолевой кислоты подвергается окислительной перегруппировке, а в примере 6 показано, что производное 3-меркаптопропионовой кислоты дает сложную смесь побочных продуктов. Оба преобразования приводят к потере необходимой тиольной функциональной группы.
Таким образом, изобретение частично основано на открытии и применении класса линкеров, которые являются эффективными и превосходят ранее известные линкеры при конъюгировании олигосахаридов (включая их аминосодержащие варианты) с носителем, таким как белок. Данный класс линкеров определяется как производные ω-ацетилсульфанилкарбоновой кислоты формулы I (где n>1).
Формула I
Данный класс линкеров обеспечивает эффективное N-ацилирование в процессе присоединения к олигосахариду. Линкером может быть активированный сложный эфир формулы I или его циано, азидо или галогенпроизводное. Линкером может быть другое производное формулы I, если такое производное является активным в качестве ацилирующего агента и, таким образом, подходит для присоединения к олигосахаридам по настоящему изобретению. Y представляет собой временную защитную группу атомов серы, которая известна в данной области и которая включает ацильные и ацетильные группы. Удаление группы Y освобождает SH группу, которая необходима для присоединения олигосахарида к носителю. X представляет собой любую уходящую группу, которая обеспечивает необходимую ацилирующую способность соединению формулы I.
Следует понимать, что любой из классов линкеров, предоставляемых изобретением, может быть использован для конъюгирования олигосахаридов с соединениями-носителями.
В качестве примера, один класс линкеров может включать структуру формулы II (где n>1):
Формула II
В качестве другого примера, другой класс линкеров может включать N-гидроксисукцинимидильные производные. Примером такого линкера, описанного в примерах 1 и 3, является N-гидроксисукцинимидил-4-ацетилсульфанилбутират (соединение 2 на схеме 1, примеры 1 и 3). Данный линкер имеет следующую структуру формулы III:
Формула III
Данный линкер стабилен в условиях полного снятия защитных групп углеводов, таких олигосахариды и полисахариды.
Другим примером активированного сложного эфира является N-нитрофенил-4-ацетилсульфанилбутират (соединение 3, примеры 2 и 3). Данное соединение имеет следующую структуру формулы IV:
Формула IV
(N-нитрофенил-4-ацетилсульфанилбутират).
Изобретение относится к способу синтеза N-гидроксисукцинимидил-4-ацетилсульфанилбутирата (формула III). Указанный способ включает реакцию 4-ацетилсульфанилмасляной кислоты (формула V):
Формула V
с N-гидроксисукцинимидилтрифторацетатом (CF3COOSu) с получением N-гидроксисукцинимидил-4-ацетилсульфанилбутирата (формула III).
Изобретение дополнительно относится к способу синтеза N-нитрофенил-4-ацетилсульфанилбутирата (формула IV). Указанный способ включает реакцию 4-ацетилсульфанилмасляной кислоты (формула V):
Формула V
с N-нитрофенилтрифторацетатом (CF3COOpNp) с получением N-нитрофенил-4-ацетилсульфанилбутирата (формула IV).
Указанные способы синтеза более подробно описаны в примерах.
Изобретение также относится к композициям, содержащим олигосахарид, включающий линкер, конъюгированный с О1-атомом глюкозаминового звена на "восстанавливающем конце" олигосахарида. Указанный О1-конъюгированный линкер используется для присоединения SH-содержащего линкера посредством реакции с соединением формулы I. О1-конъюгированный линкер имеет структуру формулы Va (ниже), содержащую аминоалкильные группы и где m может изменяться от 1 до 10, а R может представлять собой H или простую алкильную группу (например, метильную или этильную группу). Альтернативно, О1-конъюгированный линкер может иметь структуру формулы Vb (ниже), где p может изменяться от 1 до 20, а R является таким же, как в формуле Va.
Конъюгаты олигосахаридов по настоящему изобретению, таким образом, могут быть синтезированы путем сочетания соединений формулы Va или Vb с соединением формулы I. Преобразование и последующее удаление временной S-защитной группы (пример 8) или восстановление соответствующего промежуточного дисульфида (пример 7) приводят к получению конечной связывающей группы, используемой при конъюгировании олигосахаридов с соединением-носителем. Такие конечные связывающие группы описаны в примерах 7 и 8 и имеют структуру формулы VI:
Формула VI.
Олигосахарид может содержать 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 30, 40, 50, 60, 70, 80, 90 или 100 моносахаридных мономеров. В некоторых важных вариантах осуществления олигосахарид содержит 5 или более мономеров, включая 5, 7, 9 или 11 мономеров. В некоторых вариантах осуществления олигосахарид содержит 2-20 мономеров или 3-20 мономеров, или 4-20 мономеров, или 5-20 мономеров.
В некоторых важных вариантах осуществления мономером является глюкозамин, а олигосахаридом является связанный глюкозамин. Структура глюкозаминового мономера (присутствующего в связанном глюкозамине) является следующей:
Формула VII
где R1 представляет собой H в случае глюкозаминовых звеньев со "свободной" аминогруппой или R1 представляет собой ацетильную группу (COCH3) в случае N-ацетилированных глюкозаминовых звеньев. Указанные звенья связаны через β-(1→6)-связи. Может быть связано любое число глюкозаминовых звеньев, включая 2, 3, 4, 5, 6, 7, 8, 9, 10, 50 или более звеньев, вплоть до 100 звеньев (замещенных ацетильными группами или незамещенных).
Степень N-ацетилирования в соединениях формулы VII может изменяться. Она может варьировать от 0-50% N-ацетилирования (т.е. 0-50% R1 являются ацетильными группами), включая 0-40% N-ацетилирование. В некоторых вариантах осуществления β-(1→6) связанный глюкозамин является N-ацетилированным менее чем на 50%, менее чем на 40%, менее чем на 30%, менее чем на 20%, менее чем на 10% или менее чем на 5%. В некоторых важных вариантах осуществления уровень N-ацетилирования и положение ацетильных групп в олигосахариде известны исходя из способа синтеза. Таким образом, олигосахарид может быть синтезирован с упорядоченным расположением глюкозаминовых звеньев, содержащих или не содержащих N-ацетильные группы. В примерах предложены способы получения олигосахаридов, имеющих определенные и упорядоченные ацетильные замещения. Кроме того, может быть приведена ссылка на Gening et al. Carbohydrate Research 2007 342:567-575, Gening et al. Russian J Bioorganic Chem 2006 32(4):389-399, Yang and Du Carbohydrate Research 2003 338:495-502, Yang et al. Carbohydrate Research 2003 338:1313-1318, and Fridman et al. Organic Letters 2002 4(2):281-283.
Изобретение также относится к композиции, содержащей конъюгат олигосахарид-носитель, включающий олигосахарид, конъюгированный с соединением-носителем через линкер формулы VIIIa или VIIIb.
Формула VIIIa
Формула VIIIb
где линкер является O-связанным с олигосахаридом и N-связанным с соединением-носителем.
Изобретение дополнительно относится к способу синтеза конъюгата олигосахарид-носитель путем реакции конъюгатов олигосахарида, содержащих линкеры с концевыми SH-группами, такие как линкеры, которые имеют структуры формулы IXa или IXb:
Формула IXa
Формула IXb
(в случае соединений из примеров 7 и 8)
с соединением-носителем, в котором концевые аминогруппы модифицированы путем присоединения соединения формулы X:
Формула X
с получением олигосахарида, конъюгированного с соединением-носителем через линкер, имеющий структуру формулы VIIIa или VIIIb.
В некоторых вариантах осуществления линкер формулы VIIIa или VIIIb связан через свою концевую CH2-группу с О1-атомом глюкозаминового звена на "восстанавливающем конце" олигосахарида. Такую связь называют O-связью, а олигосахарид именуют как O-связанный с линкером.
В некоторых вариантах осуществления линкер формулы VIIIa или VIIIb связан через концевую группу CO с аминогруппой в соединении-носителе амидной связью. Такую связь называют N-связью, а носитель именуют как N-связанный с линкером.
При получении конъюгатов носителя, содержащего аминогруппу, и олигоглюкозаминов, имеющих линкер с концевой SH-группой, как описано выше и в примерах 8 и 9, можно использовать реагент SBAP. Однако в изобретении рассматривают использование других реагентов, подходящих для связывания носителя, содержащего аминогруппу, и олигосахаридов с концевой SH-группой (в частности, как описано G. Hermanson "Bioconjugate Techniques", 2nd Edition, Academic Press, 2008).
Соединение-носитель
"Соединение-носитель" (или носитель, поскольку данные термины используются в настоящей заявке взаимозаменяемо), используемое в настоящей заявке, представляет собой соединение, которое конъюгировано с олигосахаридом при помощи линкера по изобретению. Как правило, соединением-носителем является такое соединение, которое усиливает иммунный ответ против олигосахаридного лиганда.
Соединения-носители включают, но не ограничиваются ими, белки, пептиды, полисахариды, нуклеиновые кислоты или другие полимеры, липиды и малые олигомерные молекулы, особенно дендримеры. В некоторых вариантах осуществления соединение-носитель может быть природным или может быть получено из природного вещества. Белки включают, например, белки плазмы крови, такие как сывороточный альбумин, иммуноглобулины, аполипопротеины и трансферрин; бактериальные полипептиды, такие как столбнячный анатоксин (TT), TRPLE, β-галактозидазу, полипептиды, такие как белок gD герпеса, аллергены, токсоид дифтерии, флагеллин salmonella, пилин hemophilus, мембранные белки 15 кДа, 28-30 кДа и 40 кДа hemophilus, термолабильный энтеротоксин ltb Escherichia coli, токсин холеры, а также вирусные белки, включая VP ротавируса и белки f и g респираторно-синцитиального вируса. Носители, применимые в изобретении, включают любой белок, который безопасен для введения млекопитающим и который необязательно является иммунологически эффективным белком-носителем. Таким образом, в некоторых вариантах осуществления соединение-носитель может само по себе быть иммуногенным. Примеры включают соединения, которые были использованы в вакцинах или в качестве вакцин против видов бактерий, таких как, но ими не ограничиваясь, виды, перечисленные в настоящей заявке.
Соединения-носители, которые особенно пригод