Оксииндольные производные, обладающие агонистической активностью в отношении мотилинового рецептора
Иллюстрации
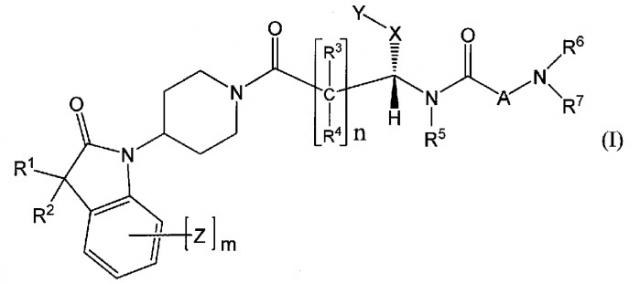
Показать всеГруппа изобретений относится к новым оксииндольным производным формулы (I) или их фармацевтически приемлемым солям, фармацевтическим композициям на их основе и их применению для лечения различных расстройств, которые опосредованы через мотилиновый рецептор (GPR38). В общей формуле I R1 означает водород, C1-С4алкил или C3-С7циклоалкил; R2 означает C1-С4алкил или C3-С7циклоалкил; или R1 и R2 вместе с атомами, с которыми они связаны, образуют 3-6-членное кольцо, которое может содержать кислород; R3 и R4 означают водород или C1-С4алкил; R5 означает водород или C1-С4алкил; R6 и R7 означают водород, C1-С4алкил или C1-С4алкокси C1-С4алкил; или R6 и R7 вместе с атом азота, с которым они связаны, образуют 4-6-членное кольцо, которое может содержать азот или кислород, при этом 4-6-членное кольцо необязательно замещено 1-4 заместителями, выбранными из группы, состоящей из C1-С4алкила, амино, C1-С4алкиламино и ди(C1-С4алкил)амино; A означает
где p, q и r независимо имеют значение 0, 1 или 2; R8 и R9 означают водород или C1-С6алкил; где алкил необязательно замещен гидрокси, C1-С4алкилом, амино, C1-С4алкиламино и ди(C1-С4алкил) амино; или R8 и R9 могут быть объединены друг с другом с образованием C3-C7-членного кольца; или R8 и R9 независимо могут быть объединены с одной иди обеими R8 и R9 группами с образованием алкиленовых мостиков между концевым азотом и алкильной частью R8 или R9 групп, при этом мостик содержит от 1 до 5 атомов углерода; указанный мостик необязательно замещен 1-4 C1-C4 алкильными группами; W означает N-R10, указанный R10 означает водород или C1-С4алкил; X означает C0-С4алкилен или C0-С4алкилен-K-C0-С4алкилен, где K означает -O- и где алкилен необязательно замещен C1-С4алкилом; Y означает водород или 5-10-членное кольцо; указанное кольцо необязательно замещено гидрокси, галогеном, галоген C1-С4алкилом, C1-С4алкилом или C1-С4алкокси, причем когда X означает C0, то Y не означает водород; Z означает галоген или C1-С4алкил; m имеет значение 0, 1, 2, 3 или 4; n имеет значение 0, 1 или 2. 5 н. и 5 з.п. ф-лы, 15 табл., 99 пр.
Реферат
Область изобретения
Группа изобретений относится к новым оксииндольным производным формулы (I) или их фармацевтически приемлемым солям, способам их получения, фармацевтическим композициям, содержащим такие соединения, и их применению для лечения различных расстройств, которые опосредованы через мотилиновый рецептор (GPR38).
Предпосылки изобретения
GPR38 представляет собой 7-трансмембранный связанный с G-белком рецептор с высоким сродством в отношении пептида мотилина [Feighner et al., Science 1999, 284, 2184], что позволяет предположить, что эндогенный мотилин проявляет всю или бóльшую часть своей активности через этот рецептор.
Мотилин представляет собой состоящий из 22 аминокислот пептид, обнаруженный в больших количествах в эндокрино-подобных клетках желудочно-кишечного (GI) тракта, и особенно в области двенадцатиперстной кишки-тощей кишки. Известно, что при голодании этот пептид связан с началом Фазы III активности мигрирующего комплекса в желудке [Boivin et al., Dig. Dis. Sci. 1992, 37, 1562], что говорит о роли в механизмах прокинетической активности. Мотилин также высвобождается из кишечника в процессе питания, мнимого кормления, растяжения желудка или при пероральном или внутривенном введении питательных веществ [Christofides et al., Gut 1979, 20, 102; Bormans et al., Scand. J. Gastroenterol. 1987, 22, 781], что говорит о дополнительных ролях этого пептида в модуляции характера перистальтики в процессе питания.
Давно известно, что у животных или человека мотилин усиливает GI перистальтику и способствует опорожнению желудка и прохождению через кишечник в анальном направлении как в условиях голодания, так и насыщения. Считают, что эта активность проявляется преимущественно за счет способствования, по меньшей мере, холинергической возбудительной функции кишечника [Van Assche et al., Eur. J. Pharmacol. 1997, 337, 267], возможно также с вовлечением активации блуждающего нерва [Mathis & Malbert, Am. J. Physiol. 1998, 274, G80]. Кроме того, более высокие концентрации мотилина непосредственно вызывают небольшое сокращение мышц [Van Assche et al., Eur. J. Pharmacol. 1997, 337, 267].
Было показано, что антибиотик эритромицин имитирует GI активность мотилина в дополнение к его ранее описанным антибиотическим свойствам [см. Peeters, Problems of the Gastrointestinal Tract, Anaesthesia Ed., Herbert MK et al. Springer-Verlag, Berlin, Heidelberg 1999, pp 39-51]. Недавно было показано, что эритромицин активирует GPR38 рецептор, что подтверждает его способность имитировать функцию мотилина [Carreras et al., Analyt. Biochem. 2002, 300, 146]. Кроме того, доступность этого непептидного агониста мотилинового рецептора позволила осуществить, по меньшей мере, некоторые клинические исследования для определения клинического потенциала агонистов мотилинового рецептора. Эти исследования убедительно продемонстрировали способность усиливать опорожнение желудка в различных условиях, связанных с гастропарезом, таких как функциональная диспепсия и диабетический гастропарез. Кроме того, было показано, что у человека эритромицин повышает давление в нижнем эзофагеальном сфинктере, что, вместе с усилением опорожнения желудка, говорит о роли в лечении гастроэзофагеального рефлюкса (GERD). Наконец, эритромицин используется для промотирования пропульсивной активности кишечника, находя клиническое применение в лечении псевдообструкции и состояний с нарушенной перистальтикой толстой кишки [Peeters, Problems of the Gastrointestinal Tract, Anaesthesia Ed., Herbert MK et al. Springer-Verlag, Berlin, Heidelberg 1999, pp 39-51].
Следовательно, ожидают, что агонисты на GPR38 рецепторе будут имитировать активность мотилина или других веществ, действующих на этом рецепторе, таких как эритромицин, и найдут клиническое применение в лечении расстройств GI, связанных с гипокинезией, в частности функциональных кишечных расстройств, таких как GERD, функциональная диспепсия (FD) и синдром раздраженной толстой кишки (IBS). Соединения также будут полезными для лечения других GI состояний, причина которых известна и при которых GI перистальтика понижена. Такие состояния включают запор, вызванный различными заболеваниями, такими как связанные с невропатией, и/или введением других лекарственных средств, псевдообструкция кишечника, паралитическая непроходимость кишечника после хирургической операции или некоторых других манипуляций, желудочный стаз или гипокинезия, вызванная различными заболеваниями, такими как диабет, и/или введением других лекарственных средств, или возникающая у пациентов с энтеральным кормлением. Интересно, что способность мотилина или эритромицина активировать блуждающий нерв, связь этого нерва с изменениями пищевого поведения [например, Furness et al., Auton. Neurosci. 2001, 92, 28] и хромосомальная локализация GPR38 [based on Ensembl: 13q21.1 (58.46-59.46 Mb)] в маркерах (D13S257-13q14.11 до D13S258 на 13q21.33) локуса, связанного с ожирением [Feitosa et al., Am. J. Hum. Genet. 2002, 70, 72], также говорит о том, что агонисты, активные на GPR38 рецепторе, помимо промотирования GI перистальтики, будут способствовать пищевому поведению, по меньшей мере, у тех пациентов, у которых имеет место некоторое подавление аппетита или кахексия. Такая активность указывает на то, что агонисты на этом рецепторе найдут клиническое применение в лечении симптомов, связанных, например, с лечением рака или вызванных развитием рака.
Помимо способности агонистов мотилинового рецептора промотировать GI перистальтику, связь полиморфизма гена мотилина с болезнью Крона [Annese et al., Dig. Dis. ScL 1998, 43, 715-710] и изменения плотности мотилинового рецептора при колите [Depoortere et al., Neurogastroenterol. Motil. 2001, 13, 55] предполагают возможность применения агонистов мотилинового рецептора для лечения воспалительных состояний кишечника в целом.
Наконец, GPR38 также обнаружен в областях вне GI тракта. Эти области включают гипофиз, жировую ткань, мочевой пузырь и некоторые области головного мозга. Это предполагает клиническое применение для промотирования функции гипофиза, такой как высвобождение веществ, способствующих секреции гормона роста, присутствие в жировой ткани также говорит о роли в контроле массы тела, а присутствие в мочевом пузыре говорит о роли агонистов на этом рецепторе в лечении недержания мочи. Присутствие GPR38 в головном мозге подтверждает применение при расстройствах GI и нарушениях питания, указанных выше, но, кроме того, говорит о том, что рецептор вовлечен в больший спектр функций блуждающего нерва-гипоталамуса.
WO 9410185, EP 838469, WO 9823629, DE 19805822 и US 6165985 заявляют производные эритромицина, нацеленные на GPR38, для применения при расстройствах, связанных с GI перистальтикой. WO 9921846, WO 0185694, WO 0168620, WO 0168621 и WO 0168622 раскрывают ряд малых молекул-антагонистов GPR38 рецептора. JP 07138284 и EP 807639 раскрывают пептидные агонисты. JP 09249620, WO 02092592, WO 05027637, US 2005065156 и Li et al., (2004, Journal of Medicinal Chemistry, 47(7) p1704-1708) раскрывают ряд малых молекул-агонистов. WO 05012331 и WO 05012332 раскрывают макроциклические соединения, которые являются агонистами или антагонистами мотилиновых или грелиновых рецепторов млекопитающих. WO 06127252 раскрывает производные эритромицина.
Краткое описание изобретения
Техническая задача
Существует необходимость в обеспечении агонистов мотилина, которые могут быть хорошим лекарственным средством. Они должны хорошо абсорбироваться из GI тракта, быть метаболически стабильными и обладать привлекательными фармакокинетическими свойствами. Они не должны быть токсичными. Кроме того, идеальный кандидат для использования в качестве лекарственного средства должен существовать в физической форме, которая является стабильной, негигроскопичной и легко формулируемой в композицию. В частности, желательно, чтобы соединения могли сильно связываться с мотилиновым рецептором и демонстрировать функциональную активность в качестве агонистов. Настоящее изобретение обеспечивает новые соединения, которые обладают отличной агонистической активностью в отношении мотилина.
Решение задачи
WO 08/000729, WO 07/007018 и WO 07/012479 раскрывают ряд малых молекул-агонистов.
Соединения по настоящему изобретению структурно отличаются от известных соединений, раскрытых в указанных документах предшествующего уровня техники, присутствием оксииндола.
Кроме того, WO 96/13265 формально раскрывает оксииндольные соединения. Однако соединения представляют собой вещества, способствующие секреции гормона роста, которые отличаются от агонистов мотилина. Кроме того, все раскрытые соединения по настоящему изобретению, как считают, вводят D-аминокислоту в молекулы, тогда как соединения по настоящему изобретению отличаются тем, что они вводят L- (альфа-, бета- или гамма-) аминокислоту в молекулы.
WO 96/13265 раскрывает соединения, которые не содержат L-аминокислотную группу и не обладают активностью агонистов мотилина.
Был обнаружен структурно новый класс соединений с аминокислотной группой L-типа в молекулах, который обеспечивает получение агонистов мотилинового рецептора (GPR38).
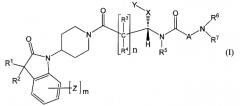
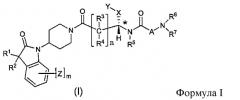
Настоящее изобретение поэтому обеспечивает соединения формулы (I) и их соли:
[Химическая формула 1]
где
R1 и R2 независимо выбраны из группы, включающей водород, C1-C4 алкил и C3-C7 циклоалкил; или альтернативно, R1 и R2, вместе с атомами, с которыми они связаны, образуют 3-6-членное кольцо, которое может содержать кислород; указанное кольцо необязательно замещено 1-4 заместителями, независимо выбранными из группы, включающей галоген, гидрокси, C1-C4 алкил и C1-C4 алкокси;
R3 и R4 независимо представляют собой водород или C1-C4 алкил;
R5 представляет собой водород, C1-C4 алкил, или C1-C4 алкокси C1-C4 алкил; из них, водород или C1-C4 алкил является предпочтительным для R5;
R6 и R7 независимо выбраны из водорода, C1-C4 алкила, гидрокси C1-C4 алкила, C1-C4 алкокси C1-C4 алкила, амино C1-C4 алкила, C1-C4 алкиламино C1-C4 алкила, ди(C1-C4 алкил)амино C1-C4 алкила, насыщенного гетероциклила и насыщенного гетероциклил C1-C4 алкила; указанный насыщенный гетероциклил и алкил могут содержать независимо от 1 до 4 C1-C4 алкильных групп; или альтернативно, R6 и R7 вместе с атом азота, с которым они связаны, образуют 4-6-членное кольцо, которое может содержать азот или кислород, где указанное 4-6-членное кольцо необязательно замещено 1-4 заместителями, независимо выбранными из группы, включающей гидрокси, C1-C4 алкил, C1-C4 алкокси, C3-C7 циклоалкил, амино, C1-C4 алкиламино и ди(C1-C4 алкил)амино;
A представляет собой
[Химическая формула 2]
где p, q и r независимо имеют значение 0, 1, 2 или 3;
R8 и R9 независимо представляет собой водород, C1-C6 алкил или C3-C7 циклоалкил; указанный алкил и циклоалкил необязательно замещены гидрокси, C1-C4 алкилом, амино, C1-C4 алкиламино и ди(C1-C4 алкил)амино; или R8 и R9 могут быть объединены друг с другом с образованием C3-C7-членного кольца, которое может содержать кислород; или R8 и R9 независимо могут быть объединены с одной или обеими R8 и R9 группами с образованием алкиленовых мостиков между концевым азотом и алкильной частью R8 или R9 групп, где мостик содержит от 1 до 5 атомов углерода и может содержать азот или кислород; указанный мостик необязательно замещен 1-4 заместителями, независимо выбранными из группы, включающей галоген, гидрокси, C1-C4 алкил, галоген C1-C4 алкил и C1-C4 алкокси;
W представляет собой N-R10, указанный R10 представляет собой водород или C1-C4 алкил;
X представляет собой C0-C4 алкилен или C0-C4 алкилен-K-C0-C4 алкилен, где K представляет собой -O-, -NH-, NR9-, -S-, -SO-, -SO2-, -CO-, -OCO-, -C(O)O-, -CR11=CR12-,
[Химическая формула 3]
-С≡С-,
-NR11CO-, или -CONR11-; указанный алкилен необязательно замещен C1-C4 алкилом, гидрокси C1-C4 алкилом, амино C1-C4 алкилом, C1-C4 алкиламино C1-C4 алкилом, ди(C1-C4)алкиламино C1-C4 алкилом или C1-C4 алкокси C1-C4 алкилом; из них, -O-, -NH- или NR9- является предпочтительным для K; из них, указанный алкилен, необязательно замещенный C1-C4 алкилом, гидрокси C1-C4 алкилом или C1-C4 алкокси C1-C4 алкилом, является предпочтительным;
R11 представляет собой водород или C1-C4 алкил;
Y представляет собой водород, галоген или 5-10-членное кольцо; указанное кольцо необязательно замещено гидрокси, галогеном, галоген C1-C4 алкилом, C1-C4 алкилом, гидрокси C1-C4 алкилом, амино C1-C4 алкилом, C1-C4 алкокси или C1-C4 алкокси C1-C4 алкилом; из них, водород или 5-10-членное кольцо является предпочтительным для Y; из них, указанное кольцо, необязательно замещенное гидрокси, галогеном, галоген C1-C4 алкилом, C1-C4 алкилом, гидрокси C1-C4 алкилом, C1-C4 алкокси или C1-C4 алкокси C1-C4 алкилом, является предпочтительным;
Z представляет собой галоген, C1-C4 алкил, C1-C4 алкокси или гидрокси;
m имеет значение 0, 1, 2, 3 или 4; из них, 0, 1 или 2 является предпочтительным для m;
n имеет значение 0, 1 или 2; из них, 0 или 1 является предпочтительным для n.
Также настоящее изобретение обеспечивает применение соединения формулы (I) или его фармацевтически приемлемой соли, каждого как оно описано в настоящей заявке, для получения лекарственного средства для лечения состояния, опосредованного активностью мотилинового рецептора, в частности мотилиновой агонистической активностью.
Предпочтительно, настоящее изобретение также обеспечивает применение соединения формулы (I) или его фармацевтически приемлемой соли, каждого как он описан в настоящей заявке, для получения лекарственного средства для лечения заболеваний, выбранных из связанных с мотилином заболеваний.
Также настоящее изобретение обеспечивает фармацевтическую композицию, включающую соединение формулы (I) или его фармацевтически приемлемую соль, каждого как оно описано в настоящей заявке, вместе с фармацевтически приемлемым носителем для указанного соединения.
Также, настоящее изобретение обеспечивает фармацевтическую композицию, включающую соединение формулы (I) или его фармацевтически приемлемую соль, каждого как оно описано в настоящей заявке, вместе с фармацевтически приемлемым носителем для указанного соединения, и другое фармакологически активное вещество.
Кроме того, настоящее изобретение обеспечивает способ лечения состояния, опосредованного активностью мотилинового рецептора, у субъекта-млекопитающего, который включает введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, каждого как он описан в настоящей заявке.
Примеры состояний, опосредованных активностью мотилинового рецептора, включают, но не ограничиваются этим, связанные с мотилином заболевания. Соединения по настоящему изобретению демонстрируют агонистическую активность в отношении мотилинового рецептора. Соединения по настоящему изобретению могут демонстрировать меньшую токсичность, хорошую абсорбцию, распределение, хорошую растворимость, меньшее сродство связывания с белком, отличным от мотилинового рецептора, меньшее взаимодействие лекарственное средство-лекарственное средство и хорошую метаболическую стабильность.
Преимущества настоящего изобретения
Фактически, в настоящем изобретении подтверждено, что, когда аминокислотную группу L-типа замещают D-аминокислотой, агонистическая активность в отношении мотилина существенно снижается. Как показано в таблице в экспериментальной части, на функциональньную активность в отношении мотилинового рецептора влияет абсолютная конфигурация аминокислотной линкерной группы, которая отличается не менее чем в 100-10000 раз между соединением с L-аминокислотной группой и соответствующими соединениями с D-аминокислотной группой.
Описание вариантов воплощения
Как он используется в настоящей заявке, термин "алкил", в качестве группы или части группы, например, алкокси или гидроксиалкил, относится к линейной или разветвленной алкильной группе во всех изомерных формах. Термин "C1-C4 алкил" относится к алкильной группе, определенной выше, содержащей, по меньшей мере, 1 и максимально 4 атомов углерода. Примеры таких алкильных групп включают метил, этил, пропил, изопропил, н-бутил, изобутил, втор-бутил или трет-бутил. Примеры таких алкоксигрупп включают метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси и трет-бутокси.
Термин "циклоалкил", как используется в настоящей заявке, предпочтительно означает циклоалкильную группу, содержащую 3-7 атомов углерода, и примеры включают циклопропил, циклобутил, циклопентил и циклогексил, циклогептил.
Термин "галоген" относится к фтору (F), хлору (Cl), брому (Br) или иоду (I), и термин "гало" относится к галогену: фтору (-F), хлору (-Cl), брому (-Br) и иоду (-I).
Термин "гетероциклил" означает 5- или 6-членное кольцо, которое включает один или несколько гетероатомов, выбранных из азота, кислорода и серы. Примеры таких гетероциклильных групп включают пирролидинил, пиперидинил, пиперазинил и морфолинил.
В соединениях формулы (I) присутствует хиральный атом углерода, присоединенный к X, и поэтому соединения формулы (I) в плоскостной структуре существуют в виде стереоизомеров. Настоящее изобретение характеризуется тем, что содержит один оптический изомер стереоизомерных форм вокруг атома углерода, связанного с X, в соединениях формулы (I), что показано пунктирной линией C-X связи. Предполагаемые стереоизомерные формы можно разделить или отделить друг от друга традиционными способами, или любой определенный изомер можно получить путем традиционного стереоселективного или асимметрического синтеза.
В некоторых соединениях формулы (I) могут присутствовать несколько хиральных атомов углерода, отличных от атома углерода, связанного с X. В таких случаях, соединения формулы (I) существуют в виде стереоизомеров. Настоящее изобретение охватывает все оптические изомеры, такие как стереоизомерные формы соединений формулы (I), включая энантиомеры, диастереоизомеры и их смеси, такие как рацематы. Разные стереоизомерные формы можно разделить или отделить друг от друга традиционными способами, или любой определенный изомер можно получить путем традиционного стереоселективного или асимметрического синтеза.
Некоторые соединения в настоящей заявке могут существовать в различных таутомерных формах, и должно быть понятно, что настоящее изобретение охватывает все такие таутомерные формы.
Подходящими соединениями по настоящему изобретению являются следующие:
(R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)пиперидин-3-карбоксамид;
(S)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)пиперидин-2-карбоксамид;
(S)-2-амино-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3,3-диметилбутанамид;
(S)-2-(1-аминоциклобутил)-N-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)ацетамид;
(S)-1-(аминометил)-N-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)циклопропанкарбоксамид;
(S)-N-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)азетидин-3-карбоксамид;
(S)-N-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)пиперидин-4-карбоксамид;
(S)-2-(1-аминоциклопентил)-N-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)ацетамид;
(S)-N-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-метил-3-(метиламино)бутанамид;
(S)-3-(циклопентиламино)-N-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)пропанамид;
(S)-N-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-((2-метоксиэтил)(метил)амино)пропанамид;
(S)-N-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-2-(пирролидин-1-ил)ацетамид;
(R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-1-метилпиперидин-3-карбоксамид;
(1S,3R)-N-((S)-3-(4-хлорфенил)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксопропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-3-(2-(трифторметил)фенил)пропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-3-циклогексил-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксопропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-3-(нафталин-1-ил)-1-оксопропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-3-(2-хлорфенил)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксопропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-3-o-толилпропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-3-(4-фторфенил)-1-оксопропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-3-(3-фторфенил)-1-оксопропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-3-(3-хлорфенил)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксопропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-3-фенилпропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-3-(3-метоксифенил)-1-оксопропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-3-(2-фторфенил)-1-оксопропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-4-метил-1-оксопентан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-3-(1H-индол-3-ил)-1-оксопропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-3-(3-(трифторметил)фенил)пропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-3-(4-(трифторметил)фенил)пропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-3-(4-метоксифенил)-1-оксопропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-3-феноксипропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-3-(2-хлорфенокси)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксопропан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(1S,3R)-N-((S)-4-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-4-оксо-1-фенилбутан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(R)-N-((S)-1-(4-(5-фтор-3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)пиперидин-3-карбоксамид;
(1S,3R)-N-((S)-1-(4-(5-фтор-3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-(метиламино)циклопентанкарбоксамид;
(S)-N-(1-(4-(5-фтор-3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-метил-3-(метиламино)бутанамид;
(S)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-(метиламино)пирролидин-1-карбоксамид;
1-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-((S)-пирролидин-2-илметил)мочевина;
1-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-((R)-пиперидин-3-ил)мочевина;
3-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-1-метил-1-((S)-пирролидин-2-илметил)мочевина;
1-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-((R)-пирролидин-2-илметил)мочевина;
1-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-((R)-пирролидин-3-ил)мочевина;
1-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-((R)-пирролидин-3-илметил)мочевина;
(R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-метилпиперазин-1-карбоксамид;
(S)-1-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-(4-этилпиперидин-4-ил)мочевина;
(S)-1-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-(4-метилпиперидин-4-ил)мочевина;
1-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-((S)-пирролидин-3-ил)мочевина;
1-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-((S)-пиперидин-2-илметил)мочевина;
1-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-((R)-пиперидин-3-илметил)мочевина;
(S)-1-(2-амино-2-метилпропил)-3-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)мочевина;
(S)-3-(циклопропил(метил)амино)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)пирролидин-1-карбоксамид;
(S)-1-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-(2-(пирролидин-1-ил)этил)мочевина;
(S)-1-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-(2-(диметиламино)этил)мочевина;
(S)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-(диметиламино)пирролидин-1-карбоксамид;
1-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-(((S)-1-метилпирролидин-2-ил)метил)мочевина;
(S)-1-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-(1,4-диметилпиперидин-4-ил)мочевина;
(S)-N-((S)-1-(4-(5-фтор-3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-(метиламино)пирролидин-1-карбоксамид;
1-((S)-1-(4-(5-фтор-3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-((S)-пирролидин-2-илметил)мочевина;
(S)-1-(1-(4-(5-фтор-3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-4-фенилбутан-2-ил)-3-(4-метилпиперидин-4-ил)мочевина;
(S)-N-(1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-3-(2-(трифторметил)фенил)пропан-2-ил)пиперидин-4-карбоксамид;
(S)-N-(3-(2-хлорфенил)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксопропан-2-ил)пиперидин-4-карбоксамид;
(S)-N-(3-(4-хлорфенил)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксопропан-2-ил)пиперидин-4-карбоксамид;
(R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-3-фенилпропан-2-ил)пиперидин-3-карбоксамид;
(R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-3-(2-фторфенил)-1-оксопропан-2-ил)пиперидин-3-карбоксамид;
(R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-3-(3-фторфенил)-1-оксопропан-2-ил)пиперидин-3-карбоксамид;
(R)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-3-(2-(трифторметил)фенил)пропан-2-ил)пиперидин-3-карбоксамид;
(R)-N-((S)-3-(2-хлорфенил)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксопропан-2-ил)пиперидин-3-карбоксамид;
(R)-N-((S)-3-(4-хлорфенил)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксопропан-2-ил)пиперидин-3-карбоксамид;
(S)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-3-(3-фторфенил)-1-оксопропан-2-ил)-3-(метиламино)пирролидин-1-карбоксамид;
(S)-N-((S)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксо-3-(2-(трифторметил)фенил)пропан-2-ил)-3-(метиламино)пирролидин-1-карбоксамид;
(S)-N-((S)-3-(2-хлорфенил)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксопропан-2-ил)-3-(метиламино)пирролидин-1-карбоксамид;
(S)-N-((S)-3-(4-хлорфенил)-1-(4-(3,3-диметил-2-оксоиндолин-1-ил)пиперидин-1-ил)-1-оксопропан-2-ил)-3-(метиламино)пирролидин-1-карбоксамид;
и их соли.
В объем "соединений по настоящему изобретению" включены все соли, сольваты, гидраты, комплексы, полиморфы, пролекарства, радиоактивно меченные производные, стереоизомеры и оптические изомеры соединений формулы (I).
Соединения формулы (I) могут образовывать кислотно-аддитивные соли. Должно быть понятно, что для использования в медицине соли соединений формулы (I) должны быть фармацевтически приемлемыми. Подходящие фармацевтически приемлемые соли должны быть очевидны для специалистов в данной области, и включают соли, описанные в J. Pharm. ScL, 1977, 66, 1-19, такие как кислотно-аддитивные соли, образованные с неорганическими кислотами, например с хлористоводородной, бромистоводородной, серной, азотной или фосфорной кислотой; и с органическими кислотами, например янтарной, малеиновой, муравьиной, уксусной, трифторуксусной, пропионовой, фумаровой, лимонной, винной, бензойной, п-толуолсульфоновой, метансульфоновой или нафталинсульфоновой кислотой. Некоторые соединения формулы (I) могут образовывать кислотно-аддитивные соли с одним или несколькими эквивалентами кислоты. Объем настоящего изобретения включает все возможные стехиометрические и нестехиометрические формы. Кроме того, некоторые соединения, содержащие кислотную функцию, такую как карбокси, можно выделить в форме их неорганической соли, в которой противоион может быть выбран из натрия, калия, лития, кальция, магния и т.п., а также из органических оснований.
Соединения формулы (I) и их соли можно получить в кристаллической или некристаллической форме, и, в случае кристаллической формы, они необязательно могут быть гидратированы или сольватированы. В объем настоящего изобретения включены стехиометрические гидраты или сольваты, а также соединения, содержащие различные количества воды и/или растворителя.
Соли и сольваты, содержащие не являющиеся фармацевтически приемлемыми противоионы или ассоциированные растворители, включены в объем настоящего изобретения, например, для использования в качестве промежуточных соединений в получении других соединений формулы (I) и их фармацевтически приемлемых солей.
Кроме того, соединения формулы (I) можно вводить в виде пролекарств. Как это используется в настоящей заявке, "пролекарство" соединения формулы (I) представляет собой функциональное производное соединения, которое, при введении пациенту, в конечном счете высвобождает соединение формулы (I) in vivo. Введение соединения формулы (I) в виде пролекарства может позволить квалифицированному специалисту осуществить одно или несколько из следующих: (a) модифицировать начало действия соединения in vivo; (b) модифицировать продолжительность действия соединения in vivo; (c) модифицировать транспортирование или дистрибуцию соединения in vivo; (d) модифицировать растворимость соединения in vivo; и (e) преодолеть побочный эффект или другое затруднение, связанное с соединением. Типичные функциональные производные, используемые для получения пролекарств, включают модификации соединения, которые химически или ферментативно расщепляются in vivo. Такие модификации, которые включают получение фосфатов, амидов, сложных эфиров, тиоэфиров, карбонатов и карбаматов, хорошо известны специалистам в данной области.
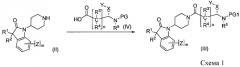
Настоящее изобретение также включает изотопно-меченные соединения, которые идентичны соединениям, описанным в настоящей заявке, но отличаются тем, что один или несколько атомов замещены атомом, имеющим атомную массу или массовое число, отличное от атомной массы или массового числа, обычно существующих в природе. Примеры изотопов, которые могут быть включены в соединения по настоящему изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора, иода и хлора, такие как 3H, 11C, 14C, 18F, 123I и 125I. Соединения по настоящему изобретению, которые содержат указанные выше изотопы и/или другие изотопы других атомов, включены в объем настоящего изобретения. Изотопно-меченные соединения по настоящему изобретению, например, соединения, в которые включены радиоактивные изотопы, такие как 3H, 14C, являются полезными в анализах распределения лекарственного средства и/или тканевого субстрата. Изотопы трития, т.е. 3H, и углерода-14, т.е. 14C, являются особенно предпочтительными из-за простоты их получения и возможности детекции. 11C и 18F изотопы являются особенно полезными в PET (позитрон-эмиссионная томография), а 125I изотопы являются особенно полезными в SPECT (однофотонная эмиссионная компьютерная томография), все они являются полезными для методов визуального исследования головного мозга. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий, т.е. 2H, может обеспечить некоторые терапевтические преимущества в результате большей метаболической стабильности, например больший период полураспада in vivo или потребность в меньших дозах, следовательно, могут быть предпочтительными в некоторых обстоятельствах. Изотопно-меченные соединения по настоящему изобретению, как правило, можно получить путем осуществления процедур, раскрытых на Схемах и/или в Примерах ниже, с последующим замещением реагента, который не является изотопно-меченным, изотопно-меченным реагентом.
Активность и эффективность соединений по настоящему изобретению в отношении GPR38 можно определить при помощи анализа репортера, осуществляемого на человеческом клонированном рецепторе, как описано в настоящей заявке. Соединения формулы (I) продемонстрировали агонистическую активность на GPR38 рецепторе при использовании функционального анализа, описанного в настоящей заявке.
Поэтому соединения формулы (I) и их фармацевтически приемлемые соли являются полезными для лечения состояний или расстройств, которые опосредованы через GPR38 рецептор. В частности, соединения формулы (I) и их фармацевтически приемлемые соли являются полезными для лечения некоторых расстройств GI, таких как гастроэзофагеальный рефлюкс, функциональная диспепсия, синдром раздраженной толстой кишки, запор, псевдообструкция кишечника, паралитическая непроходимость кишечника после хирургической операции или других манипуляций, рвота, желудочный стаз или гипокинезия, вызванная различными заболеваниями, такими как диабет, и/или введением других лекарственных средств, или возникающая у пациентов с энтеральным кормлением, болезнь Крона, колит, кахексию, связанную с прогрессирующими заболеваниями, такими как рак, и/или их лечением, и других расстройств, таких как недержание (далее указаны как "Расстройства по настоящему изобретению").
Должно быть понятно, что "лечение", как это используется в настоящей заявке, включает профилактику, а также облегчение выявленных симптомов.
Таким образом, настоящее изобретение также обеспечивает соединения формулы (I) и их фармацевтически приемлемые соли для использования в качестве терапевтических средств, в частности, для лечения состояний или расстройств, опосредованных через GPR38 рецептор. В частности, настоящее изобретение обеспечивает соединения формулы (I) и их фармацевтически приемлемые соли для использования в качестве терапевтических средств для лечения "Расстройств по настоящему изобретению".
Настоящее изобретение, кроме того, обеспечивает способ лечения состояний или расстройств у млекопитающих, включая человека, которые могут быть опосредованы через GPR38 рецептор, который включает введение страдающему таким расстройством субъекту терапевтически надежного и эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
В другом аспекте, настоящее изобретение обеспечивает применение соединений формулы (I) и их фармацевтически приемлемых солей для получения лекарственного средства для применения в лечении состояний или расстройств, опосредованных через GPR38 рецептор.
Для применения соединений формулы (I) и их фармацевтически приемлемых солей в терапии, их обычно следует сформулировать в фармацевтическую композицию в соответствии со стандартной фармацевтической практикой. Настоящее изобретение также обеспечивает фармацевтическую композицию, которая включает соединение формулы (I) или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или эксципиент.
В следующем аспекте, настоящее изобретение обеспечивает способ получения фармацевтической композиции, который включает смешивание соединения формулы (I) или его фармацевтически приемлемой соли и фармацевтически приемлемого носителя или эксципиента.
Фармацевтическая композиция по настоящему изобретению, которую можно получить путем смешивания, подходящим при температуре окружающей среды и атмосферном давлении, обычно адап