Способ получения ультрадисперсных порошков карбонатов
Иллюстрации
Показать всеИзобретение может быть использовано в химической промышленности. Способ получения ультрадисперсных порошков карбонатов включает карбонизацию водной суспензии исходного сырья в условиях повышения давления двуокиси углерода при одновременной гомогенизации суспензии. В качестве исходного сырья используют грубодисперсные порошки соответствующих природных карбонатов железа, или кальция, или магния, или кальция-магния, или кальция-железа-магния. Процесс карбонизации ведут при температуре 6-20°C и кратковременном до 1 с повышении давления от 2,6 до 3,0 МПа. Раствор неустойчивых гидрокарбонатов сливают, фильтруют и подвергают тепловой обработке при температуре 105°C. Изобретение позволяет упростить получение ультрадисперсных карбонатов. 1 ил., 4 пр.
Реферат
Изобретение относится к химической технологии неорганических материалов, а именно к способам получения ультрадисперсных порошков карбонатов и может быть использовано в химической промышленности для получения металлов.
Карбонаты - нормальные соли угольной кислоты Н2СО3, широко применяются в химической промышленности, а также используются как сырье для получения металлов, например, FeCO3, ZnCO3 и др {Глинка Н.Л. Общая химия. - М.: Химия, 1965).
Известен способ высокоскоростного получения осажденного карбоната кальция с проведением процесса карбонизации при повышенных давлениях. При этом процесс карбонизации водной суспензии гидрооксида кальция Са(ОН)2 или оксида кальция СаО проводится в сосуде высокого давления с механической активацией и внутренним барботажем двуокиси углерода СО2 (Заявка WO 01/07365 А1 от 01.02.2001).
Однако данный способ требует предварительного получения исходных реагентов Са(ОН)2 и СаО из природного сырья и повышенного расхода двуокиси углерода СО2, что значительно увеличивает себестоимость конечного продукта и усложняет технологию процесса.
Наиболее близким к предлагаемому изобретению является автоклавный способ получения ультрадисперсных порошков карбонатов, включающий карбонизацию водной суспензии порошков природных карбонатов с размером частиц 100 мкм в условиях избыточного давления двуокиси углерода от 0,8 до 2,5 МПа и температуре (4-50°C) при одновременном механическом перемешивании суспензии (патент RU 2374176 от 04.04.2006).
Данный способ требует создания избыточного давления СО2 в автоклаве, что влечет за собой неоправданные потери углекислого газа при сбросе давления и небезопасно для людей в случае промышленного применения способа.
Новая техническая задача - упрощение технологии, повышение безопасности и экономичности способа.
Для решения поставленной задачи в способе получения ультрадисперсных порошков карбонатов путем карбонизации водной суспензии исходного сырья в условиях повышения давления двуокиси углерода при одновременной гомогенизации суспензии используют грубодисперсные порошки соответствующих природных карбонатов железа, или кальция, или магния, или кальция-магния, или кальция-железа-магния, процесс карбонизации ведут при температуре 6-20°C и кратковременного до 1 сек повышения давления от 2,6 до 3,0 МПа, далее раствор неустойчивых гидрокарбонатов сливают, фильтруют и подвергают тепловой обработке при температуре 105°C.
Способ осуществляют следующим образом
Для получения ультрадисперсных порошков карбонатов металлов (железа, кальция, магния, кальция-магния, кальция-железа-магния) путем карбонизации водной суспензии исходного сырья в условиях кратковременного повышения давления двуокиси углерода при одновременной гомогенизации суспензии в качестве исходного сырья используют грубодисперсные порошки соответствующих природных карбонатов. Для получения карбоната железа используют сидерит, для получения карбоната кальция - известняк, для получения карбоната магния - магнезит, для получения карбоната кальция-магния - доломит, для получения карбоната кальция-железа-магния - анкерит с размером частиц в пределах 100 мкм, процесс карбонизации ведут при температуре 6-20°C и кратковременном повышении давления в реакционной зоне от 2,6 до 3 МПа, далее полученный раствор неустойчивых гидрокарбонатов сливают, фильтруют и подвергают тепловой обработке при температуре 105°C.
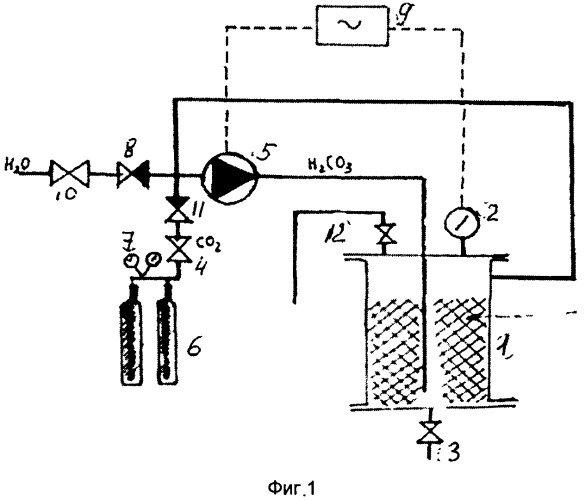
На фиг. 1 изображено устройство для получения ультрадисперсных порошков металлов. Оно включает герметичный бак-реактор (1), оснащенный электроконтактным манометром (2), сливным патрубком с вентилем (3) и патрубком контроля заполнения системы водой с вентилем (4). Герметичный бак-реактор (1) трубопроводом соединен со входом центробежного насоса (5), на который из баллона с углекислым газом (6) через редуктор (7) поступает углекислый газ под давлением 0,15 МПа. На вход центробежного насоса (5) через трубопровод с обратным клапаном (8) поступает вода. В бак-реактор (1) засыпают исходный карбонат с размером частиц не менее 100 мкм. Электроконтактный манометр (2) через блок автоматики (9) управляет включением-выключением центробежного насоса (5).
Устройство работает следующим образом. На 2/3 высоты герметичного бака-реактор (1) засыпают исходный карбонат и через вентиль (10) и обратный клапан (8) подают воду. Когда система заполнится водой, включают центробежный насос (5). На редукторе (7) баллона с углекислым газом (6) выставляют давление 0,15 МПа и углекислый газ через вентиль (4) и обратный клапан (11) подают на центробежный насос (5). Начинается образование угольной кислоты Н2СО3 и перевод исходного карбоната в соответствующий гидрокарбонат. Процесс растворения исходного карбоната контролируется электроконтактным манометром (2), установленным на герметичном баке-реакторе (1). Во время реакции растворения карбонатов и переводе их в гидрокарбонатную форму давление на электроконтактном манометре (2) будет равняться нулю. Когда весь исходный карбонат прореагирует с угольной кислотой Н2СО3 и преобразуется в соответствующий гидрокарбонат, давление на электроконтактном манометре (2) поднимется до уровня входного давления, выставленного на редукторе (7), и через блок автоматики (9) выключает центробежный насос (5). После чего перекрывают вентили (10) и (4) подачи воды и углекислого газа, а на сливном патрубке открывают вентиль (3) и раствор соответствующего гидрокарбоната сливают из герметичного бака-реактора (1). Полученные таким образом растворы гидрокарбонатов, например Fe(НСО3)2, или Mg(HCP3)2, или xCa(HCP3)2yMg(HCO3)2, или хСа(НСО3)2yFe(НСО3)2 z Mg(HCO3)2, являются неустойчивыми при атмосферном давлении и разлагаются на карбонаты при температуре 105°С, образуя при разложении гидрокарбонатов ультрадисперсные порошки карбонатов, соответственно FeCO3, MgCO3, (Ca,Mg)[CO3]2, Ca(Fe,Mg)[CO3]2, причем размер частиц в полученных порошках не превышает 50 нм (Ничуговский Г.Ф. Определение влажности химических веществ. - Л.: Химия, 1977). При этом динамика процесса испарения влаги из растворов гидрокарбонатов противодействует образованию наноразмерных агрегатов конечных карбонатов.
Пример 1
В 5-литровый герметичный бак-реактор (2) на 2/3 объема засыпается грубодисперсный порошок сидерита FeCO3 с размером частиц в пределах 100 мкм. Затем в систему подается вода с температурой 6-20°С. Когда из патрубка контроля заполнения системы водой потечет вода, перекрывается вентиль подачи воды (10) и вентиль контроля заполнения системы водой (12). После этого в систему из баллона (6) подается углекислый газ с выставленным на редукторе (7) давлением 0,15 МПа и включается центробежный насос (5). Образующаяся при прокачке центробежным насосом (5) воды через герметичный бак-реактор (1) суспензия исходного порошка сидерита смешивается с подаваемым в систему углекислым газом. По трубопроводу" поступает в центробежный насос (5), где между лопастями крыльчатки и корпусом насоса подвергается кратковременному воздействию высокого давления (до 15 МПа), в результате чего из воды а углекислого газа образуется угольная кислота Н2СО3, при этом протекает процесс превращения нерастворимого карбоната железа FeCO3 в хорошо растворимый гидрокарбонат сидерита Fe(НСО3)2 по схеме:
После растворения всего порошка карбоната железа FeCO3 и перехода его в гидрокарбонат Fe(НСО3) 2 давление CO2 в баке-реакторе (1) повышается до значения давления, выставленного на редукторе (5), и контакты электроконтактного манометра (2) через блок автоматики (9) выключают центробежный насос (5). Образовавшийся в баке-реакторе (1) гидрокарбонат железа Fe(НСО3)2 выпускается вентилем (3) сливного патрубка через фильтр. Осевшая на фильтре пульпа гидрокарбоната железа подвергается прогреву до 105°С, в результате чего образуется ультрадисперсный порошок вторичного карбоната железа FeCO3 по схеме:
Полученный порошок вторичного карбоната железа, образовавшийся при тепловой обработке гидрокарбоната железа, имеет размер частиц не более 50 нм, на основании чего можно сделать вывод, что данное устройство обеспечивает получение ультрадисперсного карбоната железа из природного сидерита, используя при этом стехиометрически необходимое количество углекислого газа. Избыток воды и растворенного в ней углекислого газа, оставшийся после фильтрации, можно использовать повторно, что позволит сократить расход улекислого газа.
Пример 2
В 5-литровый герметичный бак-реактор (1) на 2/3 объема засыпается грубо дисперсный порошок карбоната кальция СаСО3 с размером частиц в пределах 100 мкм. Затем в систему подается вода с температурой 6-20°С. Когда из патрубка контроля заполнения системы водой потечет вода, перекрывается вентиль подачи воды (10) и вентиль контроля заполнения системы водой (12). После этого в систему из баллона (6) подается углекислый газ с выставленным на редукторе (7) давлением 0,15 МПа и включается центробежный насос (5). Образующаяся при прокачке центробежным насосом (5) воды через герметичный бак-реактор (1) суспензия исходного порошка известняка, смешиваясь с подаваемым в систему углекислым газом, по трубопроводу поступает в центробежный насос (5), где между лопастями крыльчатки и корпусом насоса подвергается кратковременному воздействию высокого давления (до 3 МПа) в результате чего из воды и углекислого газа образуется угольная кислота Н2СО3, при этом протекает процесс превращения нерастворимого карбоната кальция СаСО3 в хорошо растворимый гидрокарбонат кальция Са(НСО3)2 по схеме:
После растворения всего порошка карбоната кальция СаСО3 и перехода его в гидрокарбонат Са(НСО3) давление CO2 в баке-реакторе (2) повышается до значения давления, выставленного на редукторе (5), и контакты электроконтактного манометра (3) через блок автоматики (11) выключают центробежный насос (1). Образовавшийся в баке-реакторе (2) гидрокарбонат кальция Са(НСО3)2 выпускается вентилем (8) сливного патрубка через фильтр. Осевшая на фильтре пульпа гидрокарбоната подвергается прогреву до 105°С, в результате чего образуется ультрадисперсный порошок вторичного карбоната кальция по схеме:
Полученный порошок вторичного карбоната кальция, образовавшийся при тепловой обработке гидрокарбоната, имеет размер частиц не более 50 нм, на основании чего можно сделать вывод, что данное устройство обеспечивает получение ультрадисперсного карбоната кальция из природного известняка, используя при этом стехиометрически необходимое количество углекислого газа. Избыток воды и растворенного в ней углекислого газа, оставшиеся после фильтрации, можно использовать повторно, что позволит сократить расход углекислого газа.
Пример 3
В 5-литровый герметичный бак-реактор (1) на 2/3 объема засыпается грубодисперсный порошок карбоната магния MgCO: с размером частиц в пределах 100 мкм. Затем в систему подается вода температурой 6-20°С. Когда из патрубка контроля заполнения системы водой потечет вода, перекрывается вентиль подачи воды (10) и вентиль контроля заполнения системы водой (12). После этого в систему из баллона (6) подается углекислый газ с выставленным на редукторе (5) давлением 0,15 МПа и включается центробежный насос (1). Образующаяся при прокачке через центробежный насос (5) воды через герметичный бак-реактор (1) суспензия исходного порошка магнезита, смешиваясь с подаваемым в систему углекислым газом, по трубопроводу поступает в центробежный насос (5), где между лопастями крыльчатки и корпусом насоса подвергается кратковременному воздействию высокого давления (до 1 МПа), в результате чего из воды и углекислого газа образуется угольная кислота Н2СО3, при этом протекает процесс нерастворимого карбоната магния MgCO3 в хорошо растворимый гидрокарбонат магния Mg(HC03)r по схеме:
После растворения всего порошка карбоната магния MgCO3 и перехода его в гидрокарбонат магния Mg(HCO3)2 давление СО в баке-реакторе (1) до значения давления, выставленного на редукторе (7), и контакты электроконтактного манометра (2) через блок автоматики (9) выключают центробежный насос (5). Образовавшийся в баке-реакторе гидрокарбонат магния Mg(HCO3)2 выпускается вентилем (3) сливного патрубка через фильтр. Осевшая на фильтре пульпа гидрокарбоната магния Mg(HCO3)2 подвергается прогреву до 105°С, в результате чего образуется ультрадисперсный порошок вторичного карбоната магния MgCO3 по схеме:
Полученный порошок вторичного карбоната магния, образовавшийся при тепловой обработке гидрокарбоната, имеет размер частиц не более 50 нм, на основании чего можно сделать вывод, что данное устройство обеспечивает получение ультрадисперсного карбоната магния из природного магнезита, используя при этом стехиометрически необходимое количество углекислого газа. Избыток воды и растворенный в ней углекислый газ, оставшиеся после фильтрации, можно использовать повторно, что позволит сократить расход углекислого газа.
Пример 4
В 5-литровый герметичный бак-реактор (1) на 2/3 объема засыпается грубодисперсный порошок природного доломита CaMg(CO3)2 с размером частиц в пределах 100 мкм. Затем в систему подается вода температурой 6-20°С. Когда из патрубка контроля заполнения системы водой потечет вода, перекрывается вентиль подачи воды (10) и вентиль контроля заполнения системы водой (12). После этого в систему из баллона (6) подается углекислый газ с выставленным на редукторе (7) давлением 0,15 МПа и включается центробежный насос (5). Образующаяся при прокачке центробежным насосом (5) воды через герметичный бак-реактор (1) суспензия исходного порошка доломита, смешиваясь с подаваемым в систему углекислым газом, по трубопроводу поступает в центробежный насос (5), где между лопастями крыльчатки и корпусом насоса подвергается кратковременному воздействию высокого давления до 3 МПа, в результате чего из воды и углекислого газа образуется угольная кислота H2CO3, при этом протекает процесс превращения нерастворимого доломита в хорошо растворимые гидрокарбонаты доломита Са(НСО3)2 и Mg(HCO3)2 по схеме:
После растворения всего порошка исходного доломита и перехода его в гидрокарбонаты Са(НСО3)2 и Mg(HCO3)2 давление CO2 в герметичном баке-реакторе (2) повышается до давления, выставленного на редукторе 15), и контакты электроконтактного манометра (3) через блок автоматики (11) выключают центробежный насос (1). Образовавшиеся в герметичном баке-реакторе гидрокарбонаты доломита выпускаются вентилем (3) сливного патрубка через фильтр. Осевшая на фильтре пульпа гидрокарбонатов доломита подвергается прогреву до 105°C, в результате чего образуется ультрадисперсный порошок вторичного доломита по схеме:
Полученный порошок вторичных карбонатов кальция-магния, образовавшийся при тепловой обработке гидрокарбонатов, имеет размер частиц не более 50 нм, на основании чего можно сделать вывод, что устройство обеспечивает получение ультрадисперсных карбонатов кальция-магния из природных доломитов, используя при этом стехиометрически необходимое количество углекислого газа. Избыток воды и растворенного в ней углекислого газа, оставшийся после фильтрации, можно использовать повторно, что позволит сократить расход углекислого газа.
По аналогии с вышеприведенными примерами происходят и основные реакции превращения с грубодисперсным порошком (размер частиц более 100 мкм) анкерита Ca(Fe,Mg)[CO3]2, в результате которых образуются растворы гидрокарбонатов, из которых получается ультрадисперсный порошок вторичного анкерита с размером частиц не более 50 нм.
Теоретические и экспериментальные исследования по эффективности предлагаемого устройства включали его теоретическое обоснование и экспериментальную отработку процесса получения ультрадисперсных порошков сидерита, или магнезита, или кальцита, или доломита, или анкерита при варьировании давления, температуры воды и дисперсности исходных порошков. Результаты отработки позволили выбрать оптимальные параметры процесса - размеры частиц исходных порошков в пределах 100 мкм, давление подачи СО2 в систему 0,15 МПа, рабочее давление в корпусе насоса 0,8-1 МПа, температура воды 6-10°C. Указанные значения параметров процесса являются наиболее рациональными при проведении процесса получения насыщенных гидрокарбонатов Fe(HCO3)2, или Mg(HCO3)2, или Са(НСО3)2, или xCa(НСО3)2 yMg(HCO3)2, или xCa(НСО3)2′ yFe(HCO3)2′ zMg(HCO3)2 с последующим их тепловым разложением на вторичные ультрадисперсные порошки карбонатов, или FeCO3, или MgCO3, или СаСО3, или (Ca,Mg)[CO3]2, или Ca(Fe,Mg)[CO3]2 с заданными техническими характеристиками.
Процесс разложения исходных карбонатов происходит в корпусе центробежного насоса между лопастями крыльчатки и корпусом насоса, где возникает кратковременное до 1 сек повышенное давление 2,6-3,0 МПа, а из воды и углекислого газа образуется угольная кислота.
Диапазон рабочих температур 6-20°С соответствует диапазону максимальной растворимости двуокиси углерода в воде.
Выбранный размер частиц порошков исходных карбонатов - в пределах 100 мкм является оптимальным, так как обеспечивает прохождение реакции разложения карбонатов в корпусе центробежного насоса.
При соблюдении указанных диапазонов давления и температуры водная суспензия порошков исходных карбонатов между лопастями крыльчатки и корпусом центробежного насоса полностью разлагается в гидрокарбонаты, что обеспечивает максимальное сокращение времени проведения процесса.
В указанных диапазонах давления и температуры между лопастями крыльчатки и корпусом центробежного насоса происходит мгновенное растворение углекислого газа в воде с образованием угольной кислоты и растворением порошков исходных карбонатов, что обуславливается хемосорбцией (Адам Н.К. Физика и химия поверхностей. - М.-Л.: Гостехиздат, 1947; Кузнецов В.Д. Кристаллы и кристаллизация. - М: ГИТТЛ, 1954) двуокиси углерода с образованием гидрокарбонатов по следующим схемам:
В результате протекания процесса двуокись углерода связывается суспензией в необходимом для протекания реакции количестве. Степень превращения исходного материала в гидрокарбонат по указанной реакции в данном устройстве составляет 95-98%. При сливе насыщенных растворов гидрокарбонатов из устройства, фильтровании растворов гидрокарбонатов и последующей тепловой обработке они разлагаются на вторичные карбонаты. При температуре 105°С происходит образование карбонатов указанных металлов и их комплексов из водных растворов их гидрокарбонатов, в результате чего образуется большое количество центров кристаллизации, которые не имеют условий для своего роста и определяют конечный размер частиц получаемых вторичных карбонатов железа, магния, кальция, кальция-магния, кальция-железа-магния, что и обуславливает их повышенную по сравнению с исходным сырьем дисперсность.
Таким образом, применение предлагаемого устройства позволяет получать из грубодисперсных порошков природных минералов ультрадисперсные порошки карбонатов железа с размером частиц определенного размера - FeCO3, магния - MgCO3, кальция - СаСО3, кальция-магния - xCaCO3 yMgCO3, кальция-железа-магния - Ca(Fe,Mg)[CO3]]2 при значительном снижении двуокиси углерода, воды и поэтому способствует уменьшению его общей себестоимости по сравнению с существующими технологиями.
Способ получения ультрадисперсных порошков карбонатов путем карбонизации водной суспензии исходного сырья в условиях повышения давления двуокиси углерода при одновременной гомогенизации суспензии, отличающийся тем, что используют грубодисперсные порошки соответствующих природных карбонатов железа, или кальция, или магния, или кальция-магния, или кальция-железа-магния, процесс карбонизации ведут при температуре 6-20°C и кратковременном до 1 с повышении давления от 2,6 до 3,0 МПа, далее раствор неустойчивых гидрокарбонатов сливают, фильтруют и подвергают тепловой обработке при температуре 105°C.