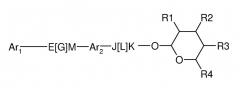Пестицидные композиции
Иллюстрации
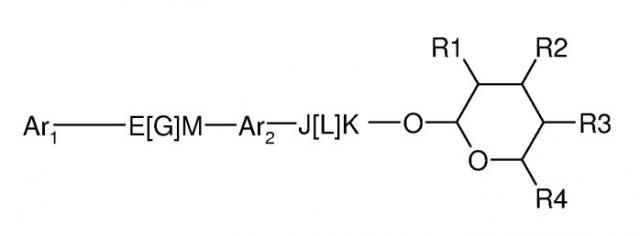
Показать всеИзобретение относится к новым соединениям-производным тетрагидропирана следующей формулы, где (a) Ar1 представляет собой замещенный фенил, причем указанный замещенный фенил имеет один или более заместителей, независимо выбранных из H, C1-C6 галогеналкил, C1-C6 алкокси, C1-C6 галогеналкокси, C(=O)H, C1-C6 (гидрокси)галогеналкил; (b) E представляет собой N, C или CR5;(c) G представляет собой двойную или тройную связь; (d) M представляет собой N, C или CR5 (при условии, что когда Е представляет собой атом азота "N", тогда M представляет собой атом азота "N"; когда E представляет собой атом углерода "С", тогда М представляет собой атом углерода "C"; и когда E представляет собой "CR5", тогда M представляет собой "CR5"); (e) Ar2 представляет собой фенил; (f) J представляет собой NR5 или CR5; (g) L представляет собой одинарную или двойную связь; (h) K представляет собой C=O или N; (i) R1 представляет собой C1-C6 алкокси; (j) R2 представляет собой C1-C6 алкокси; (k) R3 представляет собой C1-C6 алкокси; (l) R4 представляет собой C1-C6 алкил; (m) R5 представляет собой Н, или их пестицидно приемлемым кислотно-аддитивным солям, которые обладают пестицидной активностью, а также к использованию этих соединений в способе борьбы с сельскохозяйственными вредителями. 2 н. и 6 з.п. ф-лы, 4 табл., 12 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОББРЕТЕНИЕ
Данная заявка утверждает преимущество Предварительной Заявки на Патент США Сер. № 61/151549, заявленной 11 февраля 2009 года, содержание которой во всей полноте введено в данное описание в виде ссылки. Изобретение, раскрытое в данном документе, относится к технической области пестицидов и их применения для борьбы с сельскохозяйственными вредителями.
УРОВЕНЬ ТЕХНИКИ
Сельскохозяйственные вредители ежегодно вызывают миллионы человеческих смертей во всем мире. Кроме того, существует более десяти тысяч разновидностей сельскохозяйственных вредителей, которые вызывают потери в сельском хозяйстве. Указанные сельскохозяйственные потери каждый год составляют миллиарды долларов США. Термиты вызывают повреждения различных структур, таких как дома. Указанные повреждения, вызванные термитами, каждый год составляют миллиарды долларов США. И наконец, множество вредителей пищевых продуктов, которые подлежат хранению, поедают и портят находящиеся на хранении продукты питания. Указанные потери продуктов питания, находящихся на хранении, каждый год составляют миллиарды долларов США, но что более важно, лишают людей необходимой пищи.
Существует острая потребность в новых пестицидах. Насекомые вырабатывают резистентность к пестицидам, используемым в настоящее время. Сотни видов насекомых являются резистентными к одному или нескольким пестицидам. Хорошо известно развитие резистентности к некоторым ранее разработанным пестицидам, таким как ДДТ, карбаматы и органические фосфаты. Однако резистентность развилась даже к некоторым более новым пестицидам. Поэтому есть потребность в новых пестицидах и, в особенности, в пестицидах, которые обладают новыми механизмами действия.
ЗАМЕСТИТЕЛИ (НЕИСЧЕРПЫВАЮЩИЙ ПЕРЕЧЕНЬ)
Представленный перечень примеров заместителей не является (за исключением галогенов) исчерпывающим и не должен рассматриваться как ограничение изобретения, раскрытого в данном документе.
Термин «алкенил» означает ациклический ненасыщенный (содержащий, по меньшей мере, одну двойную углерод-углеродную связь) разветвленный или неразветвленный заместитель, содержащий атомы углерода и водорода, например винил, аллил, бутенил, пентенил, гексенил, гептенил, октенил, ноненил и деценил.
Термин «алкенилокси» означает алкенил, дополнительно содержащий одинарную углерод-кислородную связь, например аллилокси, бутенилокси, пентенилокси, гексенилокси, гептенилокси, октенилокси, ноненилокси и деценилокси.
Термин «алкокси» означает алкил, дополнительно содержащий одинарную углерод-кислородную связь, например метокси, этокси, пропокси, изопропокси, 1-бутокси, 2-бутокси, изобутокси, трет-бутокси, пентокси, 2-метилбутокси, 1,1-диметилпропокси, гексокси, гептокси, октокси, нонокси и декокси.
Термин «алкокси» означает ациклический насыщенный разветвленный или неразветвленный заместитель, содержащий атомы углерода и водорода, например метил, этил, пропил, изопропил, 1-бутил, 2-бутил, изобутил, трет-бутил, пентил, 2-метилбутил, 1,1-диметилпропил, гексил, гептил, октил, нонил и децил.
Термин «алкинил» означает ациклический ненасыщенный (содержащий по меньшей мере одну тройную углерод-углеродную связь и любое количество двойных связей) разветвленный или неразветвленный заместитель, содержащий атомы углерода и водорода, например этинил, пропаргил, бутинил, пентинил, гексинил, гептинил, октинил, нонинил и децинил.
Термин «галоген» означает фтор, хлор, бром и йод.
Термин «галогеналкокси» означает галогеналкил, дополнительно содержащий одинарную углерод-кислородную связь, например фторметокси, дифторметокси и трифторметокси, 2-фторэтокси, 1,1,2,2,2-пентафторэтокси, 1,1,2,2-тетрафтор-2-бромэтокси и 1,1,2,2-тетрафторэтокси.
Термин «галогеналкил» означает алкил, дополнительно содержащий от одного до максимально возможного количества одинаковых или различающихся атомов галогенов, например фторметил, дифторметил, трифторметил, 2-фторэтил, 2,2,2-трифторэтил, хлорметил, трихлорметил и 1,1,2,2-тетрафторэтил.
Термин «галогенфенилокси» означает фенилокси, содержащий один или нексколько одинаковых или различающихся атомов галогенов.
Термин «гидроксиалкил» означает алкил, содержащий одну или несколько гидроксильных групп.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Соединения согласно настоящему изобретению соответствуют следующей формуле:
где
(а) Ar1 представляет собой
(1) фуранил, фенил, пиридазинил, пиридил, пиримидинил, тиенил или
(2) замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил или замещенный тиенил,
где указанные замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил и замещенный тиенил содержат один или несколько заместителей, независимо выбранных из группы, включающей H, F, Cl, Br, I, CN, NO2, C1-C6 алкил, C1-C6 галогеналкил, С1-C6 гидроксиалкил, C3-C6 циклоалкил, C3-C6 галогенциклоалкил, C3-C6 гидроксициклоалкил, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C3-C6 гидроксициклоалкокси, С1-C6 алкокси, С1-C6 галогеналкокси, C2-C6 алкенил, C2-C6 алкинил, S(=O)n(C1-C6 алкил), S(=O)n(С1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=О)H, C(=О)NRxRy, (С1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), С(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (С1-C6 алкил)O(С1-C6 алкил), (С1-C6 алкил)S(С1-C6 алкил), (C1-C6 галогеналкил)O(С1-C6 галогеналкил)O, C1-C6 (гидрокси)галогеналкил, C(=O)(С1-C6 алкил)C(=O)O(С1-C6 алкил), фенил, фенокси, замещенный фенил и замещенный фенокси (где указанный замещенный фенил и замещенный фенокси содержит один или несколько заместителей, независимо выбранных из группы, включающей H, F, Cl, Br, I, CN, NO2, С1-C6 алкил, С1-C6 галогеналкил, C1-C6 гидроксиалкил, C3-C6 циклоалкил, C3-C6 галогенциклоалкил, C3-C6 гидроксициклоалкил, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C3-C6 гидроксициклоалкокси, С1-C6 алкокси, С1-C6 галогеналкокси, C2-C6 алкенил, C2-C6 алкинил, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(С1-C6 алкил), OSO2(С1-C6 галогеналкил), C(=О)H, C(=О)NRxRy, (С1-C6 алкил)NRxRy, С(=O)(C1-C6 алкил), С(=O)O(C1-C6 алкил), С(=O)(C1-C6 галогеналкил), С(=O)O(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (С1-C6 алкил)O(С1-C6 алкил), (С1-C6 алкил)S(С1-C6 алкил), С(=O)(C1-C6 алкил)C(=O)O(С1-C6 алкил)фенил и фенокси);
(b) E представляет собой N, C или CR5;
(c) G представляет собой двойную или тройную связь;
(d) M представляет собой N, C или CR5 (при условии, что когда E представляет собой атом азота “N”, тогда M представляет собой атом азота “N”; когда E представляет собой атом углерода “C”, тогда M представляет собой атом углерода “C”; и когда E представляет собой “CR5”, тогда M представляет собой “CR5”);
(c) Ar2 представляет собой
(1) фуранил, фенил, пиридазинил, пиридил, пиримидинил, тиенил или
(2) замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил или замещенный тиенил,
где указанные замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил и замещенный тиенил содержат один или несколько заместителей, независимо выбранных из группы, включающей H, F, Cl, Br, I, CN, NO2, C1-C6 алкил, C1-C6 галогеналкил, С1-C6 гидроксиалкил, C3-C6 циклоалкил, C3-C6 галогенциклоалкил, C3-C6 гидроксициклоалкил, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C3-C6 гидроксициклоалкокси, С1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенил, C2-C6 алкинил, S(=O)n(C1-C6 алкил), S(=O)n(С1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=О)H, C(=О)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), С(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), (C1-C6 галогеналкил)O(C1-C6 галогеналкил)O, C1-C6 (гидрокси)(галоген)алкил, C(=О)(С1-C6 алкил)C(=O)O(С1-C6 алкил), фенил, фенокси, замещенный фенил и замещенный фенокси (где указанные замещенный фенил и замещенный фенокси содержат один или несколько заместителей, независимо выбранных из группы, включающей H, F, Cl, Br, I, CN, NO2, C1-C6 алкил, C1-C6 галогеналкил, C1-C6 гидроксиалкил, C3-C6 циклоалкил, C3-C6 галогенциклоалкил, C3-C6 гидроксициклоалкил, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C3-C6 гидроксициклоалкокси, С1-C6 алкокси, С1-C6 галогеналкокси, C2-C6 алкенил, C2-C6 алкинил, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=О)H, C(=О)NRxRy, (С1-C6 алкил)NRxRy, С(=O)(C1-C6 алкил), С(=O)O(C1-C6 алкил), С(=O)(C1-C6 галогеналкил), С(=O)O(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (С1-C6 алкил)O(С1-C6 алкил), (С1-C6 алкил)S(С1-C6 алкил), С(=O)(C1-C6 алкил)C(=O)O(С1-C6 алкил)фенил и фенокси);
(d) J представляет собой O, N, NR5, CR5 или C=O;
(e) L представляет собой одинарную или двойную связь;
(f) K представляет собой CR5, C=O, N, NR5 или C=S;
(g) R1 представляет собой H, OH, F, Cl, Br, I, оксо, C1-C6 алкил, C1-C6 галогеналкил, C1-C6 алкокси, C3-C6 циклоалкокси, C1-C6 галогеналкокси, C2-C6 алкенилокси, (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)O(С1-C6 алкокси), OC(=O)(C1-C6 алкил), OC(=O)(C3-C6 циклоалкил), OC(=O)(C1-C6 галогеналкил), OC(=O)(C2-C6 алкенил) или NRxRy;
(h) R2 представляет собой H, F, Cl, Br, I, оксо, C1-C6 алкил, C1-C6 галогеналкил, C1-C6 алкокси, C3-C6 циклоалкокси, C1-C6 галогеналкокси, C2-C6 алкенилокси, (C1-C6 алкил)O(С1-C6 алкил), (C1-C6 алкил)O(С1-C6 алкокси), OC(=O)(C1-C6 алкил), OC(=O)(C3-C6 циклоалкил), OC(=O)(C1-C6 галогеналкил), OC(=O)(C2-C6 алкенил) или NRxRy;
(i) R3 представляет собой H, OH, F, Cl, Br, I, оксо, C1-C6 алкил, C1-C6 галогеналкил, C1-C6 алкокси, C3-C6 циклоалкокси, C1-C6 галогеналкокси, C2-C6 алкенилокси, (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)O(C1-C6 алкокси), OC(=O)(C1-C6 алкил), OC(=O)(C3-C6 циклоалкил), OC(=O)(C1-C6 галогеналкил), OC(=O)(C2-C6 алкенил) или NRxRy;
(j) R4 представляет собой H, С1-C6 алкил, С1-C6 галогеналкил, С1-C6 алкокси, С1-C6 галогеналкокси, C2-C6 алкенилокси, (С1-C6 алкил)O(С1-C6 алкил);
(k) R5 представляет собой (каждый независимо) H, C1-C6 алкил, C1-C6 галогеналкил, C3-C6 циклоалкил или C3-C6 галогенциклоалкил; и
(l) Rx и Ry независимо выбраны из группы, включающей H, С1-C6 алкил, С1-C6 галогеналкил, С1-C6 гидроксиалкил, C3-C6 циклоалкил, C3-C6 галогенциклоалкил, C3-C6 гидроксициклоалкил, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C3-C6 гидроксициклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенил, C2-C6 алкинил, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(С1-C6 алкил), OSO2(С1-C6 галогеналкил), C(=О)H, C(=О)OH, C(=O)(C1-C6 алкил), С(=O)O(C1-C6 алкил), С(=O)(C1-C6 галогеналкил), С(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(С1-C6 алкил), (C1-C6 алкил)S(С1-C6 алкил), C(=О)(C1-C6 алкил)C(=O)O(С1-C6 алкил), фенил и фенокси.
В другом варианте осуществления изобретения:
Ar1 представляет собой замещенный фенил, где указанный замещенный фенил содержит один или несколько заместителей, независимо выбранных из группы, включающей С1-C6 галогеналкил, С1-C6 алкокси, С1-C6 галогеналкокси, С(=O)(C1-C6 алкил), (С1-C6 галогеналкил)O(С1-C6 галогеналкил)O и С1-C6 (гидрокси)галогеналкил.
В еще одном варианте осуществления изобретения:
Ar1 представляет собой замещенный фенил, где указанный замещенный фенил содержит один или несколько заместителей, независимо выбранных из группы, включающей С1-C6 галогеналкил, С1-C6 алкокси, С1-C6 галогеналкокси и (C1-C6 галогеналкил)O(C1-C6 галогеналкил)O.
В еще одном варианте осуществления изобретения Ar2 представляет собой фенил.
В еще одном варианте осуществления изобретения J представляет собой N, NR5 или CR5.
В еще одном варианте осуществления изобретения K представляет собой C=O или N.
В еще одном варианте осуществления изобретения R1, R2 и R3 (каждый независимо) представляет собой С1-C6 алкокси.
В еще одном варианте осуществления изобретения R4 представляет собой С1-C6 алкил.
В другом варианте осуществления изобретения R5 представляет собой H.
Наряду с описанными вариантами осуществления изобретения возможны и другие варианты осуществления изобретения и их сочетания.
ПОЛУЧЕНИЕ ПИРАНОЗНЫХ ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ
Для получения соединений согласно настоящему изобретению может использоваться широкий спектр пираноз (в различных структурных формах, например, D- и L-). Например, могут использоваться пиранозы, выбранные из следующего перечня, который не является исчерпывающим: рибоза, аробиноза, ксилоза, ликсоза, рибулоза, ксилулоза, аллоза, альтроза, глюкоза, манноза, гулоза, идоза, галактоза, талоза, псикоза, фруктоза, сорбоза, тагатоза, фукоза, микароза, квиновоза, олеандроза, рамноза и паратоза. В большинстве примеров, представленных ниже, для получения промежуточных пиразоз использовалась L-рамноза.
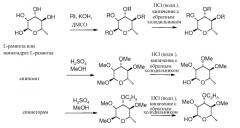
Обычно пиранозы, используемые в качестве промежуточных продуктов, могут быть получены следующим образом (с использованием, например, L-рамнозы). О-алкилированные производные рамнозы могут быть получены из коммерчески доступной L-рамнозы или гидрата L-рамнозы с использованием алкилйодида и порошкообразного гидроксида калия (КОН) в сухом диметилсульфоксиде (ДМСО) при температуре в интервале от 5°С до 15°С. Полностью алкилированный продукт затем выделяется экстракцией ДМСО раствора гексанами с последующим концентрированием гексанового слоя в вакууме. Полученный промежуточный алкилпиранозид затем подвергается обработке непосредственно водной соляной кислотой (HCl) или другой водной кислотой, которая образует свободный гидроксисахар обычно в виде смеси α и β аномеров.
Альтернативно, пералкилированная L-рамноза может быть выделена гидролизом спиносада или другого три-(О-алкил)рамнозилированного натурального продукта с использованием условий, аналогичных условиям, описанным для выделения метилолеандросида из авермектина В2 (Loewe et al. J. Org. Chem. 1994, 59, 7870). Таким образом, обработка технического спиносада избытком концентрированной серной кислоты в сухом метиловом спирте (МеОН) приводит к гидролизу рамнозного сахара и превращению его в метилпиранозид. Чистый метилпиранозид далее может удаляться из реакционной среды полной экстракцией гексанами или другим углеводородным растворителем. После этого чистый рамнопиранозид может выделяться с примерно 65-75% выходом отгонкой из сырого жидкого продукта в вакууме.
3-О-этил-2,4-ди-О-метилрамноза может быть получена аналогичным образом исходя из спинеторама. Другие алкилированные производные могут быть получены аналогично исходя из подходящим образом функционализированных спиносоидных производных, полученных из спиносинового фактора, который содержит одну или несколько свободных гидроксильных групп, присоединенных к рамнозе, (например, спиносина J) в условиях, описанных в Патенте США 6001981 (DeAmicis et al., 1999).
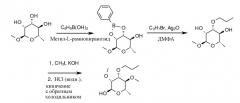
Рамнозный предшественник, селективно алкилированный заместителем большой молекулярной массы в С3 положении, был описан (см., например, Pozsgay et al. Can. J. Chem. 1987, 65, 2764). Альтернативный способ получения, в котором не применяется оловосодержащий реагент, описан ниже. Взаимодействие метилпиранозида L-рамнозы с одним эквивалентом фенилбороновой кислоты в условиях, которые позволяют удалять воду, приводят к образованию боронового ацеталя. Обработка полученного ацеталя алкилйодидом и оксидом серебра в полярном апротонном растворителе, таком как N,N-диметилформамид (ДМФА), при температуре в интервале от 0°С до 110°С приводит к селективному алкилированию при С3-ОН, давая 3-О-алкилметилпиранозид. Полученный продукт далее может дополнительно метилироваться в положениях 2-ОН и 4-ОН с использованием метилйодида в условиях, описанных выше. Полностью алкилированная рамноза затем может подвергаться гидролизу как описано выше с получением 2,4-ди-О-метил-3-О-алкил-L-рамнозы.
Иллюстрации получения таких промежуточных пираноз представлены в примерах.
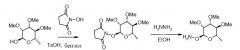
Могут быть получены и промежуточные гидроксиаминопиранозы. Например, они могут быть получены из соответствующего производного рамнозы и N-гидроксисукцинимида (NHS) в условиях, при которых образующаяся вода удаляется азеотропно для получения N-сукцинимидоилгидроксиаминного аддукта. В одном варианте осуществления изобретения эти условия включают объединение рамнозы и NHS в толуоле или бензоле, добавление каталитического количества кислоты, такой как п-толуолсульфоновая кислота (TsOH), и нагревание до температуры кипения с обратным холодильником в аппарате, снабженном ловушкой Дина-Старка. Превращение в свободный гидроксиаминный промежуточный продукт проводится обработкой сукцинимидоильного аддукта избытком гидразингидрата или безводного гидразина в спиртовом растворителе, таком как МеОН или этиловый спирт (EtOH). Последующее взаимодействие О-рамнозилгидроксиламина с альдегидом или кетоном с использованием EtOH или другого растворителя, представляющего собой низший спирт, при температуре в интервале от температуры окружающей среды до температуры образования флегмы приводит к получению О-рамнозилоксима.
ПОЛУЧЕНИЕ ПРОМЕЖУТОЧНЫХ ДИАРИЛЬНЫХ ПРОИЗВОДНЫХ
Соединения согласно настоящему изобретению получают связыванием описанных выше пираноз с диарильным промежуточным продуктом Ar1-E[G]M-Ar2 с использованием агента ковалентного связывания J[L]KQ (определенного выше). Для получения соединений согласно настоящему изобретению может применяться широкий спектр диарильных предшественников при условии, что они содержат подходящую функциональную группу на Ar2, к которой пиранозный промежуточный продукт может присоединяться для получения агента ковалентного связывания. Подходящие функциональные группы включают аминогруппу, оксоалкильную группу, формильную группу или группу карбоновой кислоты. Указанные промежуточные продукты могут быть получены способами, описанными ранее в химической литературе. Некоторые из этих способов представлены далее.
ПОЛУЧЕНИЕ ОКСИМ-СВЯЗАННЫХ СОЕДИНЕНИЙ
Оксим-связанные соединения могут быть получены из соответствующих арилальдегидов или кетонов взаимодействием с соответствующим 2-гидроксиаминосахаром в органическом растворителе, таком как МеОН или EtOH, при температуре в интервале от 0 до 100°С.
ПОЛУЧЕНИЕ КАРБАМАТ-СВЯЗАННЫХ СОЕДИНЕНИЙ
Карбамат- или тиокарбамат-связанные соединения могут быть получены из соответствующих ариламинов посредством превращения в изоцианат, изотиоцианат или п-нитрофенилкарбамат с последующей обработкой подходящим -ROH и органическим либо неорганическим основанием в подходящем растворителе, таком как тетрагидрофуран (ТГФ), при температуре в интервале от 0 до 100°С:
В этих реакциях α-конфигурация при С1 рамнозного фрагмента является обычно основным продуктом, хотя также образуется незначительное количество β-аномера. Два эти изомера могут разделяться хроматографически или они могут использоваться в виде смеси.
Получение соединений согласно настоящему изобретению может осуществляться посредством синтеза подходящего промежуточного продукта, содержащего функциональную кислотную, альдегидную, кетоновую или аминогруппу для присоединения к промежуточной пиранозе.
ПРИМЕРЫ
Данные примеры представлены для иллюстрации и не должны рассматриваться как ограничение изобретения, раскрытого в данном документе.
ПРИМЕР 1: Получение (3R,4R,5S,6S)-2,3,4,5-тетраметокси-6-метилтетрагидропирана (соединение Е-1)
Раствор гидрата L-рамнозы (40 граммов (г), 0,22 моль (моль)) в сухом диметилсульфоксиде (ДМСО; 450 миллилитров (мл)) загружают в 3-горлую круглодонную объемом 2 литра (л) и механически перемешивают, добавляя одной порцией порошкообразный гидроксид калия (KOH; 75 г, 1,34 моль). К полученному раствору добавляют йодметан (187 г, 1,32 моль) таким образом, чтобы температура раствора оставалась ниже 30°C. Для поддержания указанной температуры используют баню со смесью сухой лед/ацетон. После завершения добавления (примерно в течение 2 часов) раствор перемешивают в течение дополнительных 3 часов, и затем смесь оставляют на ночь при комнатной температуре. После этого полученный прозрачный раствор экстрагируют гексанами (4×500 мл), объединенную гексановую фракцию промывают раствором соли, сушат и выпаривают растворитель, получая раствор светло-оранжевого цвета (44 г, 92%). Перегонка приводит к получению 40 г бесцветного масла, т.кип. 150°C (0,5 мм Hg = 66,66 Па).
ПРИМЕР 2: Получение (3R,4R,5S,6S)-3,4,5-триметокси-6-метилтетрагидропиран-2-ол (соединение E-2)
Раствор соединения E-I (35,7 г, 0,162 моль) в 2N соляной кислоте (HCl; 300 мл) нагревают до 98°C и выдерживают при указанной температуре в течение 5 часов, затем охлаждают до комнатной температуры и экстрагируют дихлорметаном (CH2Cl2; 4×170 мл). Объединенные экстракты сушат над сульфатом магния (MgSO4) и обесцвечивают древесным углем. Упаривание раствора приводит к получению указанного в заголовке соединения (24,7 г, 74%) в виде вязкого масла. Часть сырого продукта (960 миллиграммов (мг)) подвергают вакуумной перегонке с использованием аппарата Кугельроха (Kuhgelrohr), собирая 890 мг при 145-155°C (1-2 мм = 133,32-266,64 Па).
ПРИМЕР 3: Получение (3R,4R,5S,6S)-4-этокси-2,3,5-триметокси-6-метилтетрагидропирана (соединение E-3)
К раствору метилового спирта (2,5 литра (л)) в колбе Эрленмейера (Erlenmeyer) объемом 4 л при перемешивании медленно добавляют серную кислоту (H2SO4, 98%; 300 мл, 5,6 моль). После охлаждения раствора до температуры окружающей среды к раствору добавляют 3'-OEt-спиносин J/L (350 г, 0,47 моль) (полученный в соответствии с методикой, описанной в Патенте США № 6001981, DeAmicis et al., 1999) и полученный раствор кипятят с обратным холодильником в течение 6 часов. Охлажденный раствор переносят в делительную волонку объемом 4 л и экстрагируют гексанами (3×1 л). Объединенную органическую фракцию сушат и концентрируют в вакууме, затем перегоняют с использованием аппарата Кугельроха, получая бесцветное масло (65 г, 60%), т. кип. 165°C (10 мторр = 1,333 Па).
ПРИМЕР 4: Получение (2R,3R,4R,5R,6S)-2,3,5-триметокси-6-метил-4-пропокситетрагидропирана (соединение E-5)
Стадия 1. (2R,3R,4R,5R,65)-2-Метокси-6-метил-4-пропокситетрагидропиран-3,5-диол. В соответствии с методикой, описанной в публикации Oshima et al., Tetrahedron Lett. 1997, 38, 5001, для получения 3,4-боронатного эфира метил-α-L-фукопиранозида метил-OC-L-рамнопиранозид превращают в 2,3-боронатный эфир. Сырой эфир (10,0 г, 37,7 миллимоль (ммоль)) растворяют в толуоле (150 мл) и обрабатывают йодпропаном (8,0 г, 47 ммоль), оксидом серебра (21,8 г, 94,3 ммоль) и триэтиламином (4,77 г, 47,1 ммоль). Раствор нагревают до 100°C и перемешивают в течение ночи (16 часов). После охлаждения и фильтрации раствор концентрируют до вязкого масла и очищают хроматографией (силикагель, элюирование с градиентом: (EtOAc)-гексан), получая 5,9 г чистого продукта.
Стадия 2. Продукт, полученный на стадии 1, метилируют с использованием MeI и KOH в условиях, описанных в примере 1, для получения соединения E-5.
Промежуточные пиранозы, представленные в таблице 1, получают способами, описанными выше и представленными в примерах 1-4.
Пример получения промежуточной 2-O-сукцинимидоилпиранозы описан ниже.
ПРИМЕР 5: Получение 1-(2S,3R,4R,5S,6S)-3,4,5-триметокси-6-метилтетрагидропиран-2-илокси)пирролидин-2,5-диона (соединение E-23)
К раствору 2,3,4-три-O-метил-L-рамнозы (6,5 г, 31,5 ммоль) и N-гидроксисукцинимида (5,4 г, 47 ммоль) в бензоле (50 мл) при перемешивании добавляют п-толуолсульфоновую кислоту (50 мг, кат.). Раствор нагревают до температуры образования флегмы и собирают воду (H2O), используя ловушку Дина-Старка. Спустя 4 часа раствор охлаждают и верхний толуоловый слой отделяют от небольшого количества нерастворимой смолы. Органический слой промывают насыщенным раствором гидрокарбоната натрия (NaHCO3; 20 мл), затем сушат над MgSO4 и упаривают до твердого остатка. Перекристаллизация из смеси эфир (Et2O)-гексаны приводит к получению указанного в заголовке соединения (4,95 г, 52%) в виде твердого не совсем белого вещества.
ПРИМЕР 6: Получение 1-(2S,3R,4R,5S,6S)-5-гидрокси-3,4-диметокси-6-метилтетрагидропиран-2-илокси)пирролидин-2,5-диона (соединение E-24)
Раствор (2R,3R,4R,5S,6S)-5-бензилокси-3,4-диметокси-6-метилтетрагидропиран-2-ола (полученного в соответствии с методикой, описанной в публикации Wu et al., Carbohydr. Res. 1998, 306, 493; 10,5 г, 26,6 ммоль), N-гидроксисукцинимида (5,0 г, 50 ммоль) и TsOH (250 мг, кат.) в бензоле (100 мл) кипятят с обратным холодильником в течение 24 часов с удалением H2O, используя ловушку Дина-Старка. Раствор коричневого цвета охлаждают, фильтруют, промывают насыщенным раствором NaHCO3 и концентрируют. Смолистое масло очищают хроматографией (силикагель, элюирование: гексаны-ацетон 70:30). После этого чистый O-сукцинимид (7,5 г, 14,5 ммоль) переносят в аппарат гидрогенизации Парра объемом 500 мл и подвергают дебензилированию с использованием Pd(OH)2/C (0,95 г) в EtOH (75 мл). Через раствор в течение 24 часов пропускают водород под давлением 19 фунтов/кв.дюйм (131,005 кПа), затем раствор фильтруют и упаривают до твердого остатка, который затем перекристаллизовывают из EtOH, получая продукт в виде твердого белого вещества (3,25 г).
Промежуточные O-сукцинимидипиранозы, представленные в таблице 2, были получены способами, которые описаны выше и проиллюстрированы в примерах 5 и 6.
Пример получения промежуточных 2-гидроксиламинопираноз из соответствующих промежуточных O-сукцинимидоилпираноз описан далее.
ПРИМЕР 7: Получение О-((2S,3R,4R,5S,6S)-3,4,5-триметокси-6-метилтетрагидропиран-2-ил)гидроксиламина (соединение E-30)
Е-23, производное 2,3,4-три-O-метил-N-сукцинимидилрамнозы (0,50 г, 1,65 ммоль), полученное в соответствии с методикой примера 5, растворяют в абсолютном EtOH (5 мл) и обрабатывают избытком гидразингидрата (0,4 г, 8 ммоль). Раствор перемешивают при температуре окружающей среды в течение 60 минут (мин), в процессе чего образуется объемный белый осадок. Добавляют дополнительное количество EtOH (5 мл) и раствор перемешивают при температуре окружающей среды в течение ночи. Раствор фильтруют и концентрируют, затем очищают хроматографией (элюирование: 100% EtOAc), получая 265 мг (74% выход) гидроксиламина в виде твердого кристаллического вещества.
Промежуточные пиранозы, представленные в таблице 3, получают способами, которые описаны выше, как показано в примере 7.
ПРИМЕР 8: Получение 4-[(Е)-2-(4-трифторметоксифенил)винил]бензальдегида O-((2S,3R,4R,5S,6S)-3,5-диметокси-6-метил-4-пропокситетрагидропиран-2-ил)оксима (соединение 1)
Стадия 1. 4-[(Е)-2-(4-трифторметоксифенил)винил]бензонитрил. В круглодонную колбу, через которую пропущен поток азота, добавляют трехосновный фосфат калия (617 мг, 2,9 ммоль) в диметил ацетамиде (DMA; 2 мл), 4-трифторметоксибромбензол (500 мг, 2,1 ммоль) и 4-циановинилбензол (322 мг, 2,5 ммоль) с последующим добавлением ацетата палладия (23 мг, 5 моль%). Раствор нагревают до 140°C и выдерживают при указанной температуре с перемешиванием в течение 12 часов. После этого раствору дают возможность охладиться до комнатной температуры, раствор выливают в H2O, экстрагируют EtOAc и промывают раствором соли. Объединенные органические слои сушат над MgSO4, фильтруют и концентрируют. Сырой продукт очищают колоночной хроматографией (элюирование: EtOAc в гексанах, 0-75%), получая твердый продукт желтого цвета (543 мг, 90%), который очищают газовой хроматографией/масс-спектральным (ГХ-МС) анализом. Полученный продукт используют в следующей стадии без дополнительной очистки.
Стадия 2. 4-[(Е)-2-(4-трифторметоксифенил)винил]бензальдегид. Цианодифенилстирол (543 мг, 1,88 ммоль) растворяют в сухом CH2Cl2 (10 мл) и охлаждают до -78°C на бане со смесью сухой лед/ацетон. К полученному раствору по каплям добавляют гидрид диизобутилалюминия в гексанах (3,7 мл, 3,7 ммоль). Реакционную смесь перемешивают в течение 4 часов, в процессе чего она нагревается до комнатной температуры. Целевой альдегид образуется исключительно посредством ГХ/МС. К реакционной смеси добавляют воду и метанол, что вызывает выделение пузырьков газа и образование геля. Полученную гетерогенную смесь разбавляют CH2Cl2 и фильтруют через фриттовый разделитель фаз (Biotage). Органический слой собирают и упаривают, получая твердое вещество желтого цвета (450 мг, 81%), которое очищают ГХ-МС. Полученный продукт используют в следующей реакции без дополнительной очистки.
Стадия 3. 4-[(Е)-2-(4-трифторметоксифенил)винил]бензальдегид O-((2S,3R,4R,5S,6S)-3,5-диметокси-6-метил-4-пропокситетрагидропиран-2-ил)оксим. Альдегид, полученный на стадии 1 (0,1 г, 0,3 ммоль), и соединение E-32 (0,3 ммоль) растворяют в абсолютированном EtOH (10 мл), полученный раствор нагревают до 40°C и выдерживают при указанной температуре с перемешиванием в течение ночи. После этого в охлажденный раствор добавляют воду (5 мл), что вызывает образование белого осадка. Раствор распределяют между H2O (5 мл) и EtOAc (3×5 мл) и объединенные органические слои сушат над MgSO4, фильтруют и упаривают, получая твердый продукт темно-желтого цвета. Очистка колоночной хроматографией с нормальной фазой (элюирование с градиентом: EtOAc-гексаны) приводит к получению целевого продукта (72 мг, 40%) в виде твердого вещества светло-желтого цвета: т.пл. 124-132°C; 1H ЯМР (300 МГц, CDCl3) δ 8,13 (с, 1Н), 7,63 (д, J=9,0 Гц, 2H), 7,54 (м, 4H), 7,21 (д, J=9,0 Гц, 2H), 7,11 (д, J=9,0 Гц, 2H), 5,63 (с, 1Н), 3,71 (м 1Н), 3,70-3,50 (м, 4H), 3,59 (с, 3H), 3,55 (с, 3H), 3,20 (т, J=9,0 Гц, 1Н), 1,68 (м, 2H), 1,31 (д, J=6,0 Гц, 3H), 0,98 (т, J=7,6 Гц, 3H); Масс-спектроскопия с ионизацией электрораспылением: m/z 524 ([M+H]+).
Представленные далее соединения получают с использованием условий, описанных в примере 8.
4-[(E)-2-(4-трифторметилфенил)винил]бензальдегид O-((2S,3R,4R,5S,6S)-4-этокси-3,5-диметокси-6-метилтетрагидропиран-2-ил)оксим (соединение 2)
Выход оксима: 60%, твердое вещество желтовато-коричневого цвета: т.пл. 150-153°C; 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,41 (с, 1Н), 7,84 (д, J=8,1 ГЦ, 2H), 7,75-7,67 (м, 6H), 7,46 (с, 2H), 5,49 (д, J=2,0 ГЦ, 1Н), 3,73-3,66 (ушир.с, 2H), 3,56-3,47 (м, 3H), 3,45 (с, 3H), 3,43 (с, 3H), 3,04 (т, J=10,0 Гц, 1Н), 1,17 (м, 6H); Масс-спектроскопия с ионизацией электрораспылением: m/z 494 ([M+H]+).
4-{(E)-2-[4-(1,1,2,2-тетрафтор-2-гептафторпропилоксиэтил)фенил]винил}бензальдегид O-((2S,3R,4R,5S,6S)-4-этокси-3,5-диметокси-6-метилтетрагидропиран-2-ил)оксим (соединение 3)
Выход оксима: 85%; масло желтого цвета: 1H ЯМР (400 МГц, ДМСО-d6) δ 8,40 (с, 1Н), 7,68 (м, 4H), 7,50 (м, 3H), 7,40 (д, J=4,0 Гц, 1Н), 7,15 (д, J=8,0 Гц, 1Н), 5,48 (с, 1Н), 3,74 (м, 1Н), 3,67 (м, 1Н), 3,55-3,46 (м, 4H), 3,45 (с, 3H), 3,43 (с, 3H), 3,04 (т, J=9,2 Гц, 1Н), 1,17 (м, 6H); Масс-спектроскопия с ионизацией электрораспылением: m/z 707 ([M-H]-).
4-[(Е)-2-(4-Ацетилфенил)винил]бензальдегид O-((2S,3R,4R,5S,6S)-4-этокси-3,5-диметокси-6-метилтетрагидропиран-2-ил)оксим (соединение 4)
Выход оксима 56%; твердое вещество желтовато-коричневого цвета: т.пл. 164-167°C; 1H ЯМР (400 МГц, ДМСО-d6) δ 8,41 (с, 1Н), 7,97 (д, J=8,0 Гц, 2H), 7,77 (д, J=8,0 Гц, 2H), 7,72 (д, J=8,0 Гц, 2H), 7,68 (д, J=8,3 Гц, 2H), 7,45 (с, 2H), 5,48 (с, 1Н), 3,86 (с, 3H), 3,74 (ушир.с, 1Н), 3,73-3,66 (м, 1Н), 3,54-3,46 (м, 3H), 3,45 (с, 3H), 3,43 (с, 3H), 3,04 (т, J=8,0 Гц, 1Н), 1,17 (м, 6H); Масс-спектроскопия с ионизацией электрораспылением: m/z 485 ([M+H2O]+).
4-[(Е)-2-(4-трифторметоксифенил)винил]бензальдегид O-((2S,3R,4R,5S,6S)-4-этокси-3,5-диметокси-6-метилтетрагидропиран-2-ил)оксим (соединение 5)
Выход оксима 24%; твердое вещество светло-желтого цвета: т.пл. 91-101°C; 1H ЯМР (300 МГц, CDCl3) δ 8,13 (с, 1Н), 7,63 (д, J=9,0 Гц, 2H), 7,55-7,51 (м, 3H), 7,23-7,17 (м, 3H), 7,11 (д, J=9,0 Гц, 2H), 5,64 (д, J=3,0 Гц, 1Н), 3,79-3,60 (м, 5H), 3,59 (с, 3H), 3,55 (с, 3H), 3,20 (т, J=9,0 Гц, 1Н), 1,32-1,24 (м, 6H); Масс-спектроскопия с ионизацией электрораспылением: m/z 532 ([M+Na]+).
4-[(Е)-2-(3-Трифторметилфенил)винил]бензальдегид O-((2S,3R,4R,5S,6S)-4-этокси-3,5-диметокси-6-метилтетрагидропиран-2-ил)оксим (соединение 6)
Выход оксима 62%; масло коричневого цвета: 1H ЯМР (400 МГц, ДМСО-d6) δ 8,40 (с, 1Н), 7,99 (с, 1Н), 7,94 (ушир.с, 1Н), 7,72-7,63 (м, 6H), 7,47 (с, 2H), 5,48 (с, 1Н), 3,74 (м, 1Н), 3,73-3,68 (м, 1Н), 3,54-3,47 (м, 3H), 3,45 (с, 3H), 3,43 (с, 3H), 3,04 (т, J=8,0 Гц, 1Н), 1,17 (м, 6H); Масс-спектроскопия с ионизацией электрораспылением: m/z 494 ([M+H]+).
4-[(Е)-2-(4-Пентафторэтилоксифенил)винил]бензальдегид O-((2S,3R,4R,5S,6S)-4-этокси-3,5-диметокси-6-метилтетрагидропиран-2-ил)оксим (соединение 7)
Выход оксима 7 мг (6%) в виде стеклообразного вещества бледно-желтого цвета: 1H ЯМР (300 МГц, CDCl3) δ 8,13 (с, 1Н), 7,63 (д, J=8,1 Гц, 2H), 7,56-7,51 (м, 5H), 7,24 (д, J=4,5 Гц, 2H), 7,11 (д, J=8,1 Гц, 2H), 5,63 (д, J=1,8 Гц, 1Н), 3,79-3,60 (м, 5H), 3,59 (с, 3H), 3,55 (с, 3H), 1,32-1,25 (м, 6H); Масс-спектроскопия с ионизацией электрораспылением ESIMS m/z 582 ([M+H]+).
4-[(Е)-2-(4-трифторметилоксифенил)винил]бензальдегид O-((2S,3R,4R,5S,6S)-3,4,5-триметокси-6-метилтетрагидропиран-2-ил)оксим (соединение 8)
Выход оксима 37 мг (30%) в виде твердого белого вещества: т.пл. 120-128°C; 1H ЯМР (400 МГц, CDCl3) δ 8,40 (с, 1Н), 7,75 (д, J=8,0 Гц, 2H), 7,68-7,65 (м, 4H), 7,42-7,30 (м, 4H), 5,50 (с, 1Н), 3,80-3,79 (м, 1Н), 3,56-3,52 (м, 1Н), 3,43 (с, 3H), 3,42 (с, 3H), 3,40-3,37 (м, 1Н), 3,38 (с, 3H), 3,05 (т, J=8,0 Гц, 1Н), 1,17 (д, J=4,0 Гц, 3H); Масс-спектроскопия с ионизацией электрораспы