Дипептиды в качестве кормовых добавок
Иллюстрации
Показать всеИзобретение относится к кормовым добавкам, содержащим дипептиды или их соли, при этом один аминокислотный остаток дипептида представляет собой DL-метионильный остаток, а другой аминокислотный остаток дипептида представляет собой аминокислоту в L-конфигурации, выбранную из группы, включающей лизин, треонин, триптофан, гистидин, валин, лейцин, изолейцин, фенилаланин, аргинин, цистеин и цистин. Также описаны кормовые смеси, содержащие такие добавки, и способ получения указанных дипептидов. 7 н. и 24 з.п. ф-лы, 17 ил., 10 табл., 25 пр.
Реферат
Настоящее изобретение относится к новым связанным с метионином искусственным и природным дипептидам незаменимых, лимитирующих аминокислот, таких, например, как лизин, треонин и триптофан, серусодержащих аминокислот - цистеина и цистина, а также к их синтезу и применению в качестве кормовых добавок для кормления пользовательных животных, таких как куры, свиньи и жвачные, но прежде всего также для кормления рыб и ракообразных, разводимых в аквакультурах.
Уровень техники
Незаменимые аминокислоты (сокращенно "ЕАА", от англ. "essential ammo acids"), к которым относятся метионин, лизин, треонин, триптофан, гистидин, валин, лейцин, изолейцин, фенилаланин и аргинин, а также обе серусодержащие аминокислоты - цистеин и цистин - являются важными компонентами кормов и играют важную роль при промышленном выращивании пользовательных животных, таких, например, как куры, свиньи и жвачные. При этом решающее значение имеет прежде всего оптимальное распределение незаменимых аминокислот и достаточное снабжение ими организма животных. Поскольку в корме на основе природных источников белка, таких, например, как соя, кукуруза и пшеница, определенные незаменимые аминокислоты часто содержатся в недостаточном количестве, целенаправленное дополнение такого корма синтетическими незаменимыми аминокислотами, такими, например, как DL-метионин, L-лизин, L-треонин или L-триптофан, позволяет, во-первых, ускорить рост животных, соответственно повысить лактацию у высокопродуктивных молочных коров, а во-вторых, повысить также эффективность усвоения корма. В этом состоит значительное экономическое преимущество. Рынки кормовых добавок имеют большое промышленное и хозяйственное значение. Помимо этого спрос на кормовые добавки постоянно повышается и на развивающихся рынках, что не в последнюю очередь объясняется возрастающей ролью в мире таких стран, как, например, Китай и Индия.
L-Метионин ((S)-2-амино-4-метилтиомасляная кислота) является для животных многих видов первой лимитирующей аминокислотой среди всех незаменимых аминокислот и поэтому играет одну из важнейших ролей в рационе питания животных и в качестве кормовой добавки (Rosenberg и др., J. Agr. Food Chem., 5, 1957, сс.694-700). Однако при классическом химическом синтезе метионин образуется в виде рацемата, представляющего собой смесь из D- и L-метионинов в соотношении 50:50. Такой рацемический DL-метионин, однако, можно использовать непосредственно в качестве кормовой добавки, поскольку у животных некоторых видов в условиях in vivo существует механизм превращения неприродного D-энантиомера метионина в его природный L-энантиомер. При этом сначала происходит дезаминирование D-метионина под действием неспецифической D-оксидазы в α-кетометионин, который затем под действием L-трансаминазы превращается в L-метионин (Baker D.H., "Amino acids in farm animal nutrition", под ред. D'Mello J.P.F., Wallingford (UK), CAB International, 1994, cc.37-61). Таким путем в организме повышается доступное количество L-метионина, который затем может использоваться в организме животного для его роста. Ферментативное превращение D-метионина в L-метионин было обнаружено у кур, свиней и коров, но прежде всего и у рыб, морских креветок и пресноводных креветок. Так, например, по результатам исследований Sveier и др. (Aquacult. Nutr., 7(3), 2001, cc.169-181) и Kim и др. (Aquaculture, 101(1-2), 1992, сс.95-103) было установлено, что превращение D-метионина в L-метионин возможно у плотоядных атлантических лососей и радужных форелей. То же самое удалось обнаружить Robinson и др. (J. Nutr., 108(12), 1978, сс.1932-1936) и Schwarz и др. (Aquaculture, 161, 1998, сс.121-129) у всеядных видов рыб, таких, например, как сомообразные и карповые. Помимо этого Forster и Dominy (J. World Aquacult. Soc., 37(4), 2006, сс.474-480) в экспериментах с кормлением всеядных морских креветок вида Litopenaeus vannamei установили, что DL-метионин обладает такой же эффективностью, что и L-метионин. В 2007 г. во всем мире было произведено свыше 700000 тонн кристаллического DL-метионина, соответственно рацемического жидкого гидроксианалога метионина (ГАМ, рац-2-гидрокси-4-(метилтио)масляная кислота (ГММ)) и твердого ГАМ в виде его кальциевой соли и успешно использовалось непосредственно в качестве кормовой добавки при разведении животных с однокамерным желудком, таких, например, как сельскохозяйственная птица и свиньи.
В отличие от метионина лизин, треонин и триптофан можно использовать в качестве кормовых добавок только в виде L-энантиомеров каждого из них, поскольку D-энантиомеры каждой из трех этих незаменимых и лимитирующих аминокислот не могут превращаться организмом в физиологических условиях в соответствующие L-энантиомеры. Так, в частности, мировой сбыт одного только L-лизина, представляющего собой первую лимитирующую аминокислоту у свиней, составил в 2007 г. более одного миллиона тонн. Мировой же сбыт двух других лимитирующих незаменимых аминокислот - L-треонина и L-триптофана - составил в 2007 г. лишь более 100000 т, соответственно чуть меньше 3000 т.
DL-Метионин, ГАМ, а также L-лизин, L-треонин и L-триптофан обычно непосредственно используют в качестве добавки к кормам для животных с однокамерным желудком, таких, например, как сельскохозяйственная птица и свиньи. В отличие от этого добавление таких незаменимых аминокислот, как метионин, лизин, треонин или же ГАМ, к кормам для жвачных оказывается неэффективным, поскольку основное его количество разлагается в рубце жвачных под действием микробов. В результате такого разложения незаменимых аминокислот лишь незначительная часть от всего их добавленного к корму количества попадает в тонкий кишечник животного, где обычно происходит их всасывание в кровь. Среди незаменимых аминокислот в первую очередь метионин, потребляемый жвачными, играет решающую роль, поскольку только при оптимальном снабжении их организма этой аминокислотой обеспечивается высокая лактация. Для возможности высокоэффективного обеспечения организма жвачных метионином его требуется применять в форме, защищенной от разложения в рубце. В этом отношении существует несколько возможностей по приданию D,L-метионину, соответственно рац-ГАМ подобных свойств. Одна из таких возможностей по приданию метионину высокой стойкости к разложению в рубце состоит в нанесении на метионин соответствующего защитного слоя, соответственно в его распределении в пригодной для применения в этих целях защитной матрице. Благодаря этому метионин может практически без потерь проходить через рубец. В дальнейшем защитный слой удаляется, например, в сычуге в результате кислотного гидролиза, а высвобождающийся при этом метионин может затем всасываться в тонком кишечнике жвачного. Для применения в подобных целях пригодны имеющиеся в продаже продукты, например продукт Mepron® фирмы Evonik Degussa и продукт Smartamine™ фирмы Adisseo. Получение метионина, соответственно нанесение на него покрытия в большинстве случаев является технически сложным и трудоемким процессом и поэтому связано с высокими затратами. Помимо этого нанесенное на поверхность готовых гранул покрытие может легко повреждаться от механической нагрузки и истирания при переработке кормов, что может привести в конечном итоге к снижению эффективности защиты или даже к ее полной утрате. Поэтому защищенные метиониновые гранулы невозможно перерабатывать в более крупные комбикормовые гранулы, поскольку при такой переработке также произошло бы разрушение защитного слоя под действием механических нагрузок. Этот фактор существенно ограничивает применение подобных продуктов. Еще одна возможность по повышению стойкости метионина к разложению в рубце состоит в химическом образовании производных метионина, соответственно ГАМ. При этом функциональные группы молекулы защищают приемлемыми защитными группами. Так, например, карбоксильную функциональную группу можно в этих целях этерифицировать спиртами. Таким путем удается уменьшить разложение в рубце под действием микроорганизмов. В качестве примера имеющегося в продаже продукта с химической защитой можно назвать продукт Metasmart™, представляющий собой рацемический изопропиловый эфир гидроксианалога метионина (HMBi). Согласно WO 00/28835 биологическая доступность HMBi для жвачных составляет по меньшей мере 50%. Недостаток химического образования производных метионина, соответственно ГАМ часто состоит в их худшей биодоступности и сравнительно низком содержании собственно действующего вещества.
Наряду с проблемой разложения добавляемых к корму незаменимых аминокислот, таких как метионин, лизин или треонин, в рубце жвачных с различными проблемами можно также столкнуться при добавлении незаменимых аминокислот к корму для рыб и ракообразных. В результате стремительного экономического развития рыбоводства и разведения ракообразных в высокоиндустриальных аквакультурах в последние годы постоянно возрастает значение той роли, которую именно в этой области играет возможность оптимального, экономичного и эффективного дополнения рациона питания животных незаменимыми и лимитирующими аминокислотами (Food and Agriculture Organization of the United Nation (FAO) Fisheries Department, "State of World Aquaculture 2006", 2006, Рим; International Food Policy Research Institute (IFPRI), "Fish 2020: Supply and Demand in Changing Markets", 2003, Вашингтон, округ Колумбия). При этом, однако, в отличие от сельскохозяйственной птицы и свиней при применении кристаллических незаменимых аминокислот в качестве добавки к кормам для определенных видов рыб и ракообразных можно столкнуться с различными проблемами. Так, в частности, в публикации Rumsey и Ketola (J. Fish. Res. Bd. Can., 32, 1975, сс.422-426) говорится, что применение соевой муки в сочетании с индивидуально добавленными кристаллическими аминокислотами не приводило к усилению роста радужных форелей. По результатам исследований, проведенных Murai и др. (Bull. Japan. Soc. Sci. Fish., 50(11), 1984, с.1957), удалось установить, что ежедневное кормление карповых кормами с высокой долей добавленных к ним кристаллических аминокислот приводило к выведению более 40% свободных аминокислот из организма через жабры и почки. В связи с быстрым всасыванием добавленных аминокислот вскоре после поедания корма происходит очень быстрое повышение концентрации аминокислот в плазме крови рыб ("быстрая реакция"). Однако другие аминокислоты из природных источников белка, таких, например, как соевая мука, к этому моменту еще не находятся в плазме крови, что может привести к асинхронности в одновременной усвояемости всех важных аминокислот. Вследствие этого часть высококонцентрированных аминокислот быстро выводится из организма, соответственно быстро метаболизируется в нем и используется, например, в качестве исключительно источника энергии. В результате этого у карповых при применении кристаллических аминокислот в качестве кормовых добавок происходит лишь незначительное усиление роста, соответственно не происходит никакого усиления роста (Аое и др., Bull. Jap. Soc. Sci. Fish., 36, 1970, сс.407-413). В случае же ракообразных дополнение их корма кристаллическими незаменимыми аминокислотами может привести к возникновению еще и других проблем. В связи с медленным поеданием корма определенными ракообразными, такими, например, как креветки вида Litopenaeus Vannamei, по причине длительного пребывания корма в воде добавленные к нему водорастворимые аминокислоты удаляются из него в результате их растворения (вымывания), что приводит к эвтрофикации водоема, а не к усилению роста животных (Alam и др., Aquaculture, 248, 2005, сс.13-16). Тем самым незаменимые аминокислоты для эффективного снабжения ими организма рыб и ракообразных, разводимых в аквакультурных хозяйствах, требуют для определенных видов животных и определенных условий применения их выпуска в специальной форме, например в соответствующим образом химически или физически защищенной форме. Преследуемая при этом цель состоит, во-первых, в том, чтобы продукт оставался достаточно стойким в водной среде в процессе кормления животных и не удалялся из корма в результате растворения. Во-вторых, в конечном итоге должна обеспечиваться возможность оптимального и высокоэффективного усвоения аминокислотного продукта, потребленного животным, его организмом.
Ранее уже предпринимались многочисленные усилия по разработке приемлемых добавок к кормам для рыб и ракообразных, особенно кормовых добавок на основе незаменимых аминокислот - метионина и лизина. Так, например, в WO 89/06497 описано применение ди- и трипептидов в качестве добавки к кормам для рыб и ракообразных. Такие кормовые добавки должны способствовать росту животных. При этом, однако, использовали преимущественно ди- и трипептиды из заменимых, а также нелимитирующих аминокислот, таких, например, как глицин, аланин и серии, содержащихся во многих растительных источниках белков в более чем достаточных количествах.
В качестве метионинсодержащих дипептидов в указанной публикации описаны только DL-аланил-DL-метионин и DL-метионил-DL-глицин. Однако по этой причине эффективное содержание действующего вещества в дипептиде составляет лишь 50% (моль/моль), что с экономической точки зрения следует классифицировать как серьезный недостаток. В WO 02/088667 описаны энантиоселективный синтез и применение олигомеров из ГАМ и аминокислот, таких, например, как метионин, в качестве добавок к кормам, в том числе, в частности, и добавок к кормам для рыб и ракообразных. Применение таких кормовых добавок должно обеспечивать возможность ускоренного роста животных. Описанные в указанной публикации олигомеры образуют путем протекающей при ферментативном катализе реакции, получаемые в результате которой индивидуальные олигомеры обладают исключительно широким молекулярно-массовым распределением (полидисперсностью). По указанным причинам подобный способ неизбирателен, дорог и сложен в осуществлении и связан с дорогостоящей и трудоемкой очисткой получаемых им продуктов. У Dabrowski и др. в US 2003/0099689 описано применение синтетических пептидов в качестве кормовых добавок для стимулирования роста водных животных. При этом на массовую долю пептидов может приходиться от 6 до 50% от всей массы кормовой смеси. Такие синтетические пептиды состоят преимущественно из незаменимых аминокислот. Однако энантиоселективный синтез подобных синтетических олиго- и полипептидов исключительно сложен и дорог, а возможность его реализации в промышленном масштабе связана со значительными трудностями. Помимо этого эффективность полипептидов отдельной аминокислоты является спорной, поскольку они часто лишь очень медленно превращаются или вовсе не превращаются в физиологических условиях в свободные аминокислоты. Так, например, у Baker и др. (J. Nutr., 112, 1982, сс.1130-1132) говорится, что поли-L-метионин по причине его полной нерастворимости в воде не обладает никакой биологической ценностью в отношении кур, поскольку его всасывание в их организм невозможно.
Наряду с применением новых химических производных незаменимых аминокислот, таких, например, как метионинсодержащие пептиды и олигомеры, исследовались также различные возможности по физической защите незаменимых аминокислот, такие, например, как нанесение покрытия на незаменимую аминокислоту, соответственно ее включение в защитную матрицу.
Так, например, Alam и др. (Aquacult. Nutr., 10, 2004, сс.309-316, и Aquacultwe, 248, 2005, сс.13-19) установили, что снабженные покрытием метионин и лизин в отличие от таковых без покрытия оказывают исключительно положительное влияние на рост молодых креветок курума (Marsupenaeus japonicus). Хотя применение специального покрытия и позволило предотвратить вымывание метионина и лизина из кормовых гранул, тем не менее подобному подходу присущи некоторые серьезные недостатки. Получение аминокислот, соответственно нанесение на них покрытия в большинстве случаев является технически сложным и трудоемким процессом и поэтому связано с высокими затратами. Помимо этого покрытие, нанесенное на окончательно снабженную им аминокислоту, может легко повреждаться от механической нагрузки и истирания при переработке кормов, что может привести к снижению эффективности физической защиты аминокислоты или даже к полной утрате такой физической защиты. К этому же следует добавить, что покрытие или применение матрицы снижает содержание аминокислоты и поэтому часто является неэкономичным.
Задача изобретения
В основу настоящего изобретения была положена задача в первую очередь предложить кормовое средство, соответственно кормовую добавку для применения в рационе питания животных на основе нового метионинсодержащего заменителя, в котором метионин ковалентно связан с незаменимой и лимитирующей аминокислотой, такой, например, как L-лизин, L-треонин и L-триптофан, и который можно было бы использовать в качестве кормовой добавки для кормления пользовательных животных, таких как куры, свиньи и жвачные, но прежде всего также для кормления рыб и ракообразных, разводимых в аквакультурах.
С учетом описанных выше недостатков, присущих уровню техники, задача изобретения заключалась прежде всего в разработке химически защищенного продукта на основе комбинации из ковалентно связанных между собой DL-метионина и незаменимой аминокислоты, такой, например, как L-лизин, L-треонин или L-триптофан, для применения в рационе питания различных пользовательных животных, таких как куры, свиньи и жвачные, а также в рационе питания многих видов всеядных, растительноядных и плотоядных рыб и ракообразных, обитающих в морской или пресной воде. Подобный продукт наряду с функцией источника метионина должен также выполнять функцию источника всех других незаменимых аминокислот. Такой продукт должен в первую очередь обладать механизмом замедленного высвобождения, т.е. медленным и непрерывным высвобождением свободного метионина и незаменимой аминокислоты в физиологических условиях. Помимо этого такой продукт в химически защищенной форме, состоящий из метионина и незаменимой аминокислоты, должен обладать стойкостью к разложению в рубце и быть тем самым пригодным для применения в рационе питания всех жвачных. Для применения в качестве добавки к кормам для рыб и ракообразных такой продукт, представленный в указанной выше форме, должен характеризоваться низкой растворимостью (вымываемостью) в воде во избежание его удаления из всей кормовой гранулы, соответственно всего кормового экструдата.
Еще одна задача изобретения заключалась в том, чтобы предложить заменитель кристаллических незаменимых аминокислот в качестве кормового средства, соответственно кормовой добавки, который помимо исключительно высокой биологической ценности и биологической доступности был бы простым в обращении с ним и обладал бы высокой сохраняемостью, а также стойкостью в обычных условиях производства комбикормов, прежде всего при гранулировании и экструзии.
Таким путем, например, для кур, свиней, жвачных, рыб и ракообразных наряду с кристаллическими незаменимыми аминокислотами должно обеспечиваться наличие дополнительных эффективных источников незаменимых аминокислот, у каковых источников полностью бы отсутствовали недостатки известных продуктов или такие недостатки присутствовали бы лишь в меньшем объеме.
Помимо этого задача изобретения состояла в разработке различных новых, гибких способов синтеза дипептидов, содержащих только один метиониновый остаток, прежде всего синтеза L-EAA-DL-метионина (I) и DL-метионил-L-EAA (II). Один из таких способов синтеза должен допускать возможность использовать в качестве исходного материала типичные исходные, промежуточные и побочные продукты промышленного процесса получения DL-метионина.
Описание изобретения
Указанная задача решается с помощью кормовых добавок, содержащих дипептиды или их соли, при этом один аминокислотный остаток дипептида представляет собой DL-метионильный остаток, а другой аминокислотный остаток дипептида представляет собой аминокислоту в L-конфигурации, выбранную из группы, включающей лизин, треонин, триптофан, гистидин, валин, лейцин, изолейцин, фенилаланин, аргинин, цистеин и цистин.
В предпочтительном варианте кормовая добавка содержит дипептиды общей формулы DL-метионил-L-ЕАА (соответствует смеси из D-метионил-L-ЕАА и L-метионил-L-ЕАА) и/или L-EAA-DL-метионин (соответствует смеси из L-EAA-D-метионина и L-EAA-L-метионина), где L-EAA представляет собой аминокислоту в L-конфигурации, выбранную из группы, включающей лизин, треонин, триптофан, гистидин, валин, лейцин, изолейцин, фенилаланин, аргинин, цистеин и цистин.
Объектом изобретения является далее кормовая смесь, содержащая указанную выше кормовую добавку.
Кормовая добавка, содержащая L-EAA-DL-метионин и/или DL-метионил-L-ЕАА и их соли, пригодна для применения в качестве кормовой добавки в кормовых смесях для кормления сельскохозяйственной птицы, свиней и жвачных, но прежде всего также для кормления рыб и ракообразных, разводимых в аквакультурах.
В предпочтительном варианте кормовая смесь содержит L-EAA-DL-метионин и DL-метионил-L-ЕАА в количестве от 0,01 до 5 мас.%, предпочтительно от 0,05 до 0,5 мас.%.
Применение L-EAA-DL-метионина и DL-метионил-L-ЕАА зарекомендовало себя при этом в качестве наиболее предпочтительного, поскольку эти дипептиды благодаря своей низкой растворимости обладают исключительно высокой стойкостью к вымыванию.
Помимо этого такое соединение проявляет хорошую стойкость к гранулированию и экструзии при производстве кормов. Дипептиды L-EAA-DL-метионин и DL-метионил-L-ЕАА стабильны в смесях с обычными компонентами и кормовыми средствами, такими, например, как зерновые (в частности, кукуруза, пшеница, тритикале, ячмень, просо и другие), белковый корм растительного или животного происхождения (в частности, соевые бобы и рапс, a также продукты их дальнейшей переработки, бобовые (например, горох, фасоль, люпин и т.д.), рыбная мука и другие), а также в комбинации с добавленными незаменимыми аминокислотами, протеинами, пептидами, углеводами, витаминами, минеральными веществами, жирами и маслами.
Еще одно преимущество состоит в том, что благодаря высокому относительному содержанию действующих веществ - L-EAA-DL-метионина и DL-метионил-L-ЕАА - на кг вещества по сравнению с DL-метионином и L-EAA на моль L-EAA-DL-метионина, соответственно DL-метионил-L-ЕАА экономится моль воды.
В одном из предпочтительных вариантов предлагаемого в изобретении применения кормовая смесь содержит протеины и углеводы, предпочтительно на основе рыбной, соевой или кукурузной муки, и может быть дополнена незаменимыми аминокислотами, протеинами, пептидами, витаминами, минеральными веществами, углеводами, жирами и маслами.
В особенно предпочтительном варианте DL-метионил-L-ЕАА и L-EAA-DL-метионин присутствуют в кормовой смеси индивидуально в виде D-метионил-L-ЕАА, L-метионил-L-ЕАА, L-EAA-D-метионина или L-EAA-L-метионина, в виде смеси между собой, соответственно также в виде смеси с D-метионил-D-ЕАА, L-метионил-D-EAA, D-EAA-D-метионином или D-EAA-L-метионином, предпочтительно в каждом случае дополнительно в смеси с DL-метионином, на долю которого в предпочтительном варианте приходится от 0,01 до 90 мас.%, более предпочтительно от 0,1 до 50 мас.%, особенно предпочтительно от 1 до 30 мас.%, и предпочтительно в каждом случае дополнительно в смеси с L-EAA, такой, например, как L-лизин, на долю которой в предпочтительном варианте приходится от 0,01 до 90 мас.%, более предпочтительно от 0,1 до 50 мас.%, особенно предпочтительно от 1 до 30 мас.%.
В еще одном предпочтительном варианте предлагаемого в изобретении применения животными, разводимыми и выращиваемыми в аквакультурных хозяйствах, являются пресноводные и морские рыбы и ракообразные, выбранные из группы, включающей карповых, форелей, лососевых, сомовых, окуневых, камбаловых, осетровых, тунцовых, угревых, лещей, тресковых, морских креветок, криль и пресноводных креветок, особенно предпочтительно из группы, включающей белого толстолобика (Hypophthalmichthys molitrix), белого амура (Ctenopharyngodon idelld), сазана (Cyprinus carpio), пестрого толстолобика (Aristichthys nobilis), золотого карася (Carassius carassius), катлю (Catia Catid), лабео роха (Labeo rohita), тихоокеанского и атлантического лососей (Salmon salar и Oncorhynchus kisutch), радужную форель (Oncorhynchus mykiss), канального сомика (Ictalurus punctatus), африканского сома (Glorias gariepinus), пангасиуса (Pangasius bocourti и Pangasius hypothalamus), нильскую тиляпию (Oreochromis niloticus), ханоса (Chanos chanos), кобию (Rachycentron canadum), белую тихоокеанскую креветку (Litopenaeus vannarnei), черную тигровую креветку (Penaeus monodon) и гигантскую пресноводную креветку (Macrobrachium rosenbergii).
Согласно изобретению L-EAA-DL-метионин (L-EAA-DL-Met) (I) и DL-метионил-L-EAA (DL-Met-L-EAA) (II) или их соли с щелочными и щелочноземельными металлами, такие, например, как труднорастворимая кальциевая или цинковая соль, применяют в виде D-метионил-L-ЕАА, L-метионил-L-EAA, L-EAA-D-метионина или L-EAA-L-метионина либо в виде соответствующих смесей диастереомеров индивидуально или в смеси с DL-метионином, индивидуально или в смеси с L-EAA в качестве добавки в кормовых смесях, предпочтительно в качестве добавки к кормам для сельскохозяйственной птицы, свиней и жвачных, особенно предпочтительно для рыб и ракообразных:
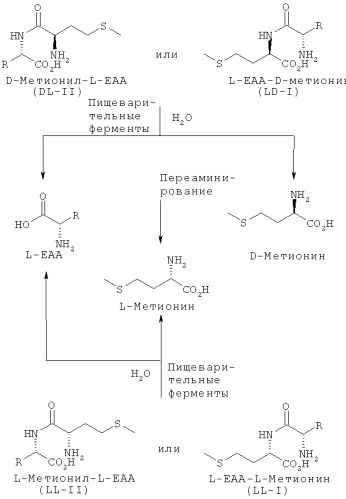
L-EAA-DL-метионин (I) существует в виде обоих диастереомеров L-EAA-D-Met (LD-I) и L-EAA-L-Met (LL-I). Равным образом и дипептид DL-метионил-L-EAA (II) существует в виде двух разных стереоизомеров D-Met-L-EAA (DL-II) и L-Met-L-EAA (LL-II). При этом только оба диастереомера L-EAA-L-Met (LL-I) и L-Met-L-EAA (LL-II) являются природными, тогда как оба других диастереомера L-EAA-D-Met (LD-I) и D-Met-L-EAA (DL-II) являются неприродными (см. схему 1).
Схема 1
Остаток R в ЕАА имеет при этом следующие значения:
в формуле Ia, соотв. IIa R обозначает 1-метилэтил- (валин)
в формуле Ib, соотв. IIb R обозначает 2-метилпропил- (лейцин)
в формуле Ic, соотв. IIc R обозначает (1S)-1-метилпропил- (изолейцин)
в формуле Id, соотв. IId R обозначает (1R)-1-гидроксиэтил- (треонин)
в формуле Ie, соотв. IIe R обозначает 4-аминобутил- (лизин)
в формуле If, соотв. IIf R обозначает 3-[(аминоиминометил)- (аргинин)
амино]пропил-
в формуле Ig, соотв. IIg R обозначает бензил- (фенилаланин)
в формуле Ih, соотв. IIh R обозначает (1H-имидазол-4-ил)метил- (гистидин)
в формуле Ij, соотв. IIj R обозначает (1H-индол-3-ил)метил- (триптофан)
При этом стереоизомеры L-EAA-D-метионин (LD-I), L-EAA-L-метионин (LL-I), D-метионил-L-ЕАА (DL-II) и L-метионил-L-ЕАА (LL-II) можно использовать индивидуально или в виде смесей между собой в качестве кормовой добавки, предпочтительно в качестве добавки к кормам для сельскохозяйственной птицы, свиней, жвачных, рыб, ракообразных, а также домашних животных.
Наряду с разработкой нового способа синтеза L-EAA-DL-метионина (I) и DL-метионил-L-ЕАА (II) одним из основных объектов настоящего изобретения является также применение соединений формул I и II в виде смеси диастереомеров, представляющей собой смесь из D-метионил-L-ЕАА (DL-II) и L-метионил-L-ЕАА (LL-II), соответственно смесь из L-EAA-D-метионина (LD-I) и L-EAA-L-метионина (LL-I), или в виде индивидуального диастереомера, представляющего собой D-метионил-L-ЕАА (DL-II), L-метионил-L-ЕАА (LL-II), L-EAA-D-метионин (LD-I), соответственно L-EAA-L-метионин (LL-I), в качестве ростостимулирующего кормового средства для сельскохозяйственной птицы, свиней и жвачных, а также для всеядных, плотоядных и растительноядных рыб и ракообразных в аквакультурных хозяйствах. Помимо этого применение L-EAA-DL-метионина (I), соответственно DL-метионил-L-EAA (II) в качестве кормовой добавки позволяет повысить лактацию у высокопродуктивных молочных коров.
Так, в частности, согласно изобретению было установлено, что L-EAA-DL-метионин (I), соответственно DL-метионил-L-EAA (II) в виде смеси диастереомеров, представляющей собой смесь из L-EAA-D-метионина (LD-I) и L-EAA-L-метионина (LL-I) в соотношении 50:50, соответственно смесь из D-метионил-L-EAA (DL-II) и L-метионил-L-EAA (LL-II) в соотношении 50:50, либо в виде соответствующего индивидуального диастереомера может в физиологических условиях ферментативно расщепляться в организме кур, свиней, коров, рыб, таких, например, как карпы и форели, а также ракообразных, таких, например, как Litopenaeus Vannamei (белая тихоокеанская креветка) и Macrobrachium Rosenbergii (гигантская пресноводная креветка), на свободный D-, соответственно L-метионин и соответственно на L-EAA (см. схему 2).
Для этого, например, из кур, всеядных карпов, плотоядных форелей и всеядных белых тихоокеанских креветок (Litopenaeus Vannamei) выделяли соответствующие пищеварительные ферменты, которые в оптимизированных опытах in vitro подвергали в условиях, сравнимых с физиологическими, взаимодействию с DL-метионил-L-EAA (II) в виде смеси диастереомеров, представляющей собой смесь из D-метионил-L-EAA (DL-II) и L-метионил-L-ЕАА (LL-II) в соотношении 50:50, соответственно с L-EAA-DL-метионином (I), представляющим собой смесь из L-EAA-D-метионина (LD-I) и L-EAA-L-метионина (LL-I) в соотношении 50:50, либо с каждым из соответствующих индивидуальных диастереомеров, представляющим собой D-метионил-L-EAA (DL-II), L-метионил-L-EAA (LL-II), L-EAA-D-метионин (LD-I) или L-EAA-L-метионин (LL-I). Согласно изобретению особенность расщепления L-EAA-DL-метионина (I), соответственно DL-метионил-L-EAA (II) заключается в том, что наряду с двумя природными диастереомерами - L-EAA-L-метионином (LL-I) и L-метионил-L-ЕАА (LL-II) - в физиологических условиях могут расщепляться также два неприродных диастереомера - L-EAA-D-метионин (LD-I) и D-метионил-L-EAA (DL-II) (см. фиг.1-17). Сказанное относится и к применению смеси D-метионил-L-ЕАА (DL-II) и L-метионил-L-ЕАА (LL-II), смеси D-метионил-L-EAA (DL-II) и L-EAA-D-метионина (LD-I) (см. фиг.12), соответственно смеси L-метионил-L-EAA (LL-II) и L-EAA-D-метионина (LD-I) (см. фиг.12), и к применению общей смеси всех диастереомеров, и к применению каждого из индивидуальных диастереомеров (см. фиг.1-11 и 13-17).
Схема 2
Природные дипептиды L-EAA-L-Met (LL-I) и L-Met-L-EAA (LL-II) расщепляли действием пищеварительных ферментов, выделенных из плотоядных радужных форелей, всеядных зеркальных карпов, всеядных белых тихоокеанских креветок и кур (см. таблицу 1).
| Таблица 1 | ||||
| Вид Дипептид | Форель (плотоядная) | Зеркальный карп (всеядный) | Белая тихоокеанская креветка (всеядная) | Курица (всеядная) |
| L-Met-L-Val (LL-IIa) | x | x | x | |
| L-Met-L-Leu (LL-IIb) | x | x | x | |
| L-Met-L-Ile (LL-IIc) | x | x | x | |
| L-Met-L-Thr (LL-IId) | x | x | x | |
| L-Met-L-Lys (LL-IIe) | x | x | x | |
| L-Met-L-Arg (LL-IIf) | x | x | x | |
| L-Met-L-Phe (LL-IIg) | x | x | x | |
| L-Met-L-His (LL-IIh) | x | x | x | |
| L-Met-L-Trp (LL-IIj) | x | x | x | |
| L-Val-L-Met (LL-Ia) | x | x | x | |
| L-Leu-L-Met (LL-Ib) | x | x | x | |
| L-Ile-L-Met (LL-Ic) | x | x | x | |
| L-Thr-L-Met (LL-Id) | x | x | x | x |
| L-Lys-L-Met (LL-Ie) | x | x | x | x |
| L-Arg-L-Met (LL-If) | x | x | x | |
| L-Phe-L-Met (LL-Ig) | x | x | x | |
| L-His-L-Met (LL-Ih) | x | x | x | |
| L-Trp-L-Met (LL-Ij) | x | x | x |
Для этого из пищеварительных трактов рыб и морских креветок выделяли ферменты. Затем полученными растворами ферментов расщепляли дипептиды L-EAA-L-Met (LL-I) и L-Met-L-EAA (LL-II). Для лучшей сопоставимости перевариваемости дипептидов ферментами, выделенными из различных видов животных, использовали такие же условия, что и в опытах по перевариванию in vitro (37°C, pH 9).
Все природные дипептиды расщеплялись под действием пищеварительных ферментов, выделенных из плотоядной радужной форели (см. фиг.3 и 4), всеядного зеркального карпа (см. фиг.1 и 2), всеядной белой тихоокеанской креветки (см. фиг.5 и 6) и курицы (см. фиг.16). Процессы расщепления L-Met-L-EAA (LL-II) обычно протекают несколько быстрее, чем процессы расщепления аналогичных дипептидов L-EAA-L-Met (LL-I).
С целью максимально наглядно продемонстрировать ферментативное расщепление неприродных дипептидов - L-EAA-D-Met (LD-I) и D-Met-L-EAA (DL-II) - под действием пищеварительных ферментов, выделенных из рыб различных видов, исследования проводили в соответствии с приведенной ниже экспериментальной матрицей (см. таблицу 2).
| Таблица 2 | ||||||||||||
| Дипептид Вид | D-Met-L-Trp (DL-IIj) | D-Met-L-Thr (DL-IId) | D-Met-L-Lys (DL-IIe) | D-Met-L-Leu (DL-IIb) | D-Met-L-Ile (DL-IIc) | D-Met-L-Phe (DL-IIg) | L-Trp-D-Met (DL-Ij) | L-Thr-D-Met (DL-Id) | L-Lys-D-Met (DL-Ie) | L-Leu-D-Met (DL-Ib) | L-Ile-D-Met (DL-Ic) | L-Phe-D-Met (DL-Ig) |
| Форель (плотоядная) | x | x | x | x | x | x | x | x | ||||
| Зеркальный карп (всеядный) | x | x | x | x | x | x | x | x | ||||
| Белый амур (растительноядный) | x | x | x | x | x | x | x | x | ||||
| Белая тихоокеанская креветка (всеядная) | x | x | x | x | x | x | x | x | ||||
| Тиляпия (всеядная) | x | x | x | x | ||||||||
| Курица (всеядная) | x | x | x | x | x | x |
Для этого из пищеварительных трактов рыб и морских креветок выделяли ферменты. Затем полученными растворами ферментов расщепляли химически синтезированные дипептиды L-EAA-D-Met (LD-I) и D-Met-L-EAA (DL-II). Для лучшей сопоставимости перевариваемости дипептидов ферментами, выделенными из различных видов животных, использовали такие же условия, что и в опытах по перевариванию in vitro (37°C, pH 9).
Все неприродные дипептиды L-EAA-D-Met (LD-I) и D-Met-L-EAA (DL-II) расщепляются под действием пищеварительных ферментов, выделенных из всеядного зеркального карпа (см. фиг.7), растительноядного белого амура (см. фиг.8), плотоядной радужной форели (см. фиг.11), всеядной белой тихоокеанской креветки (см. фиг.10) и курицы (см. фиг.17). Процессы расщепления D-Met-L-EAA (DL-II) протекают несколько медленнее, чем процессы расщепления аналогичных дипептидов L-EAA-D-Met (LD-I). Под действием же пищеварительных ферментов, выделенных из тиляпии (см. фиг.9), расщепление D-Met-L-EAA (DL-II) происходило быстрее, чем расщепление дипептидов L-EAA-D-Met (LD-I). Наиболее быстро перевариваются дипептиды D-Met-L-Lys (DL-IIe) и L-Lys-D-Met (LD-Ie). Преобладающая часть лизинсодержащих дипептидов в условиях реакции in vitro расщеплялась под действием всех использовавшихся пищеварительных ферментов уже по истечении 5 ч.
Полученные результаты свидетельствуют о том, что каждый использовавшийся неприродный дипептид (см. фиг.7-11 и 17) может расщепляться под действием пищеварительных ферментов рыб различных видов, морских креветок и кур. При этом применение ферментов, выделенных из плотоядных радужных форелей, всеядных зеркальных карпов, тиляпий, белых тихоокеанских креветок, растительноядных белых амуров, а также кур позволило экспериментально подтвердить, что неприродные дипептиды L-EAA-D-Met (LD-I) и D-Met-L-EAA (DL-II) могут расщепляться in vitro животными всех видов несмотря на явные различия в их пищеварительных системах. Добавление дипептидов L-EAA-D-Met (LD-I) и/или D-Met-L-EAA (DL-II) к корму позволяет, таким образом, целенаправленно дозировать присутствующие в нем в недостатке незаменимые аминокислоты (DL-Met и L-EAA).
На примере дипептидов на основе аминокислот - L-триптофана и DL-метионина - исследовали расщепление смесей природных и неприродных дипептидов. Смесь диастереомеров, состоящая из обоих неприродных дипептидов L-Trp-D-Met (LD-Ij) и D-Met-L-Trp (DL-IIj), расщеплялась полностью, равно как и смесь из природного дипептида L-Met-L-Trp (LL-IIj) и неприродного дипептида L-Trp-D-Met (LD-Ij). Эффект "замедленного высвобождения" выражен у смеси LD-Ij/DL-IIj гораздо более явно, чем у смеси LD-Ij'/LL-IIj, т.е. аминокислоты триптофан и метионин высвобождаются при ферментативном переваривании дипептидов медленнее друг по отношению к другу и в течение более продолжительного периода времени.
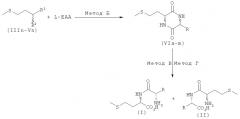
Положенная в основу изобретения задача решается также с помощью дипептида или его соли общей формулы DL-метионил-DL-EAA или DL-EAA-DL-метионин, где ЕАА обозначает аминокислоту, предпочтительно в L-конфигурации, выбранную из группы, включающей лизин, треонин, триптофан, гистидин, валин, лейцин, изолейцин, фенилаланин, аргинин, цистеин и цистин. При этом равным образом предпочтителен метионильный остаток в D-, соответственно L-конфигурации. К подобным дипептидам относятся Met-Lys, Met-Thr, Met-Trp, Met-His, Met-Val, Met-Leu, Met-Ile, Met-Phe, Met-Arg, Met-Cys и Met-цистин, в каждом случае в конфигурациях DD, LD, DL и LL, а также Lys- Met, Thr-Met, Trp-Met, His-Met, Val-Met, Leu-Met, He-Met, Phe-Met, Arg-Met, Cys-Met и цистин-Met, в каждом случае в конфигурациях DD, LD, DL и LL.
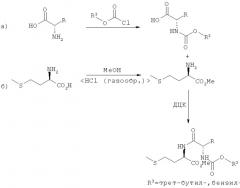
Положенная в основу изобретения задача решается далее с помощью способа получения дипептида, содержащего только один метионильный остаток, формулы DD/LL/DL/LD-I или DD/LL/DL/LD-II: