Способ лечения спинальных арахноидитов и арахноидальных кист
Иллюстрации
Показать всеИзобретение относится к области медицины, в частности к нейрохирургии. Проводят декомпрессию спинномозгового канала, вскрывают твердую мозговую оболочку (ТМО), осуществляют диссекцию субарахноидальных спаек и стенок кист до восстановления проходимости субарахноидальных пространств с последующим ушиванием ТМО. При этом в случае ограниченных спинальных кистах или одиночных спайках доступ осуществляют непосредственно над местом компрессии. При протяженных арахноидальных кистах доступ осуществляют в центральной части кисты, при этом разрез кожи и мягких тканей производят в проекции заинтересованного сегмента спинного мозга. После диссекции видимых субарахноидальных спаек в дорсальное и/или вентральное пространство дурального мешка вводят ультратонкий гибкий эндоскоп с рабочей поверхностью 2,8 мм, разделяют спайки и стенки кист при помощи его манипуляторов, восстанавливают проходимость ликворных пространств и осуществляют широкую ревизию субарахноидального пространства в краниальном и каудальном направлениях. Способ позволяет снизить травматичность лечения спинальных арахноидитов и арахноидальных кист и уменьшить послеоперационные осложнения, что достигается за счет щадящей технологии разъединения рубцов и спаек.7 ил., 1 пр.
Реферат
Изобретение относится к области медицины, в частности к нейрохирургии, и может быть использовано для хирургического лечения адгезивных спинальных арахноидитов и арахноидальных кист.
Спинальный арахноидит чаще локализуется в грудном и поясничном отделах и в области конского хвоста. Выделяют четыре клинические формы спинального арахноидита: 1) корешково-чувствительную; 2) двигательно-спинномозговую; 3) корешково-спинномозговую или смешанную; 4) корешково-заднестолбовую [Полищук Н.Е., Корж Н.А., Фищенко В.Я. Повреждения позвоночника и спинного мозга (механизмы, клиника, диагностика, лечение). - Киев: Книга плюс, 2001. - 388 с.].
При спинальных арахноидитах возможны острый, подострый и хронический варианты течения. Острый спинальный арахноидит наиболее характерен для пациентов с тяжелыми системными инфекциями, например сепсисом и бактериальным менингитом, и протекает тяжело, сопровождаясь гипертермией, лихорадочным состоянием, явлениями ответа острой фазы, в наиболее сложных ситуациях осложняясь гемореологическими нарушениями, полиорганной недостаточностью и т.д. Неврологическая симптоматика развивается быстро, иногда в течение нескольких дней и даже часов, и носит характер острого поперечного миелита с грубой проводниковой симптоматикой. Подострый спинальный арахноидит также протекает на фоне инфекций, однако более латентно, развиваясь в течение месяцев, на фоне нормальной или субфебрильной температуры. В неврологическом статусе на первое место чаще выступают корешковые синдромы, а проводниковая симптоматика присоединяется позже. При хроническом спинальном арахноидите четкий инфекционный агент определить часто не удается, а само заболевание прогрессирует очень медленно; на первый план выступают постепенно нарастающие явления спастического и афферентного пареза, а также тазовые расстройства [Di leva A, Barolat G, Tschabitscher M, et al. Lumbar arachnoiditis and thecaloscopy: brief review and proposed treatment algorithm., Cent Eur Neurosurg., 2010 Nov;71(4):207-12].
Что касается арахноидальных спинальных кист, то они клинически могут напоминать экстрамедуллярную опухоль, что до широкого внедрения нейровизуализации иногда приводило к диагностическим ошибкам. Арахноидальная киста проявляется медленно прогрессирующими проводниковыми расстройствами, нарушениями ликвороциркуляции, несколько реже - корешковой симптоматикой, обычно соответствующей локализации одной из спаек, составляющих стенку кисты. [Warnke JP, Mourgela S. Endoscopic treatment of lumbar arachnoiditis. Minim Invasive Neurosurg., 2007 Feb; 50(l):l-6].
Консервативное лечение спинальных арахноидитов и арахноидальных кист применяют в виде антибиотиков, уротропина, йодистых препаратов, аутогемотерапии, тканевой терапии, введения воздуха в субарахноидальное пространство. Хирургическое лечение занимает первое место, особенно при ограниченных кистозных арахноидитах. Основной целью операций при арахноидите является удаление или разъединение оболочечных сращений, рубцов, кист, давящих на мозговую ткань либо вызывающих нарушения циркуляции цереброспинальной жидкости. Операции при спинальном арахноидите показаны при наличии компрессии спинного мозга, а также при нарастающих двигательных, чувствительных нарушениях и корешковых болях, связанных с ограниченным слипчивым процессом или с образованием кист. Хирургические вмешательства при арахноидите также показаны и при неэффективности консервативной терапии в хронической или резидуальной стадии воспалительного процесса.
На сегодняшний день известен способ хирургического лечения спинальных арахноидитов и арахноидальных кист путем проведения ламинэктомии, при этом вскрывают твердую мозговую оболочку, разъединяют субарахноидальные спайки до восстановления проходимости субарахноидальных пространств (СП), опорожняют кисты с обязательным тщательным ушиванием твердой оболочки. (Нейротравматология. Справочник. Под ред. Коновалова А.Н., Лихтмана Л.Б., Потапова А.А., М., Феникс, 1994, с. 5-7). Однако данная методика является инвазивной и травматичной. Кроме того в послеоперационном периоде часто возникают осложнения в виде вспышки дремлющей инфекции, что затем может привести к миелиту и образованию повторных сращений рубцов и спаек.
Технический результат предлагаемого нами способа заключается в минимальной инвазивности и травматичности лечения спинальных арахноидитов и арахноидальных кист и снижении послеоперационных осложнений за счет максимально щадящей техники разъединения рубцов и спаек.
Технический результат достигается тем, что для лечения спинальных кистозных арахноидитов осуществляют декомпрессию спинномозгового канала, вскрытие твердой мозговой оболочки, диссекцию субарахноидальных спаек и стенок кист до восстановления проходимости субарахноидальных пространств с последующим ушиванием твердой мозговой оболочки, причем после диссекции видимых субарахноидальных спаек в дорсальное и/или вентральное пространство дурального мешка вводят ультратонкий гибкий эндоскоп с рабочим каналом диаметром 1,2 мм и диаметром рабочей поверхности 2,8 мм, разделяют спайки и стенки кист при помощи его манипуляторов, восстанавливают проходимость ликворных пространств и осуществляют широкую ревизию субарахноидального пространства в краниальном и каудальном направлениях.
Способ осуществляется следующим образом.
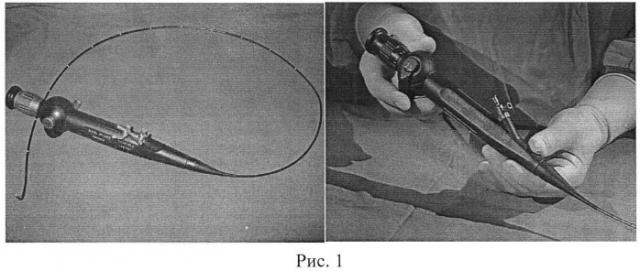
Для лечения спинальных арахноидитов и арахноидальных кист нами впервые в отечественной нейрохирургии был применен метод текалоскопии. Текалоскопия (thecaloscopy) - хирургическая минимально инвазивная операция, основанная на введении гибкого эндоскопа в дуральный мешок. Для этого используют гибкий эндоскоп (фиброскоп) производства Karl Storz (Германия). На рисунке 1 показан общий вид эндоскопа. Длина двух возможных комплектаций эндоскопа составляет 40 см и 70 см соответственно. Последнего варианта достаточно для проведения полноценной ревизии всего субарахноидального пространства от корешков конского хвоста до краниовертебрального перехода у взрослого пациента. Фиброскоп совместим со стандартной эндоскопической стойкой.
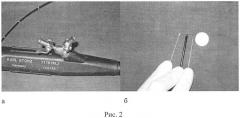
Для управления на основании фиброскопа предусмотрен манипулятор, дающий возможность изгиба его дистальной части до 270 градусов в двух направлениях. Эта функция позволяет осуществлять полноценную визуализацию и ревизию вентральных и дорсальных субарахноидальных пространств. Диаметр рабочей поверхности составляет 2,8 мм, при этом она имеет источник света, видеокамеру для трансляции изображения и 1 рабочий канал диаметром 1,2 мм (рис. 2а, б). Этот канал используется для ирригации во время оперативного вмешательства, а также для введения под контролем зрения манипуляторов, позволяющих разделять спайки и брать биопсию.
Вмешательство проводят в положении пациента лежа на животе. Поскольку текалоскопия является минимально инвазивным вмешательством, возможно ее выполнение как под эндотрахеальным наркозом, так и в условиях местной инфильтрационной анестезии пункционным доступом. В случае операции на верхне-шейном отделе позвоночника голову больного жестко фиксируют скобой Mayfleld. Эндоскопическую стойку располагают напротив оперирующего хирурга. Используют также интраоперационную рентгеноскопию.
Согласно принципам минимально инвазивной хирургии, доступ должен быть настолько мал, насколько это возможно, однако полностью соответствовать задачам вмешательства. В соответствии с этим возможны различные тактики операционного доступа.
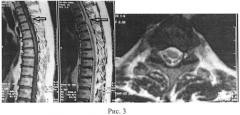
При ограниченных спинальных кистах или одиночных спайках доступ осуществляют непосредственно над местом компрессии, что позволяет осуществить микрохирургическое иссечение спаек. На рисунке 3 показан отграниченный спинальный адгезивный арахноидит на уровне Th3. На рисунке 4 показан микрохирургический адгезиолиз перед проведением текалоскопической стадии операции.
При протяженных арахноидальных кистах доступ осуществляют в центральной части кисты. Это позволяет одинаково удобно осуществлять манипуляции эндоскопом как в краниальном, так и в каудальном направлениях. На рисунке 5 показана протяженная арахноидальная посттравматическая киста на уровне Th9-Th11.
При использовании открытого доступа, в соответствии с выбранной тактикой, под контролем интраоперационной рентгенографии производят разрез кожи и мягких тканей в проекции необходимого сегмента спинного мозга. Скелетируют остистые отростки и дужки позвонков на заинтересованном уровне. Далее производят экономную костную резекцию, которая в типичном случае ограничивается дужкой одного позвонка (что соответствует длине кожного разреза 5-7 см). Длина разреза твердой мозговой оболочки чаще не превышает 2 см. Принципиальное значение имеет эффективный гемостаз (в том числе с применением современных гемостатических материалов), поскольку даже минимальное кровотечение затрудняет эндоскопическую визуализацию.
После микрохирургической диссекции видимых спаек и стенок кист осуществляют основной этап хирургического вмешательства - текалоскопию. Фиброскоп вводят в дорсальное субарахноидальное пространство и/или в вентральное путем изгиба дистального конца инструмента манипулятором (рис.6). При необходимости положение эндоскопа контролируют при помощи электронно-оптического преобразователя. Манипуляции по разделению спаек и фенестрации кист осуществляют манипуляторами. Все манипуляции при текалоскопии осуществляют плавно, без применения силы, во избежание выраженной тракции спинного мозга и нарастания неврологической симптоматики. Кровотечения, источником которых могут служить сосуды арахноидальной оболочки, часто патологически измененные, останавливают путем продолжительной ирригации физиологическим раствором. В нашей практике не встречалось значительных по объему и продолжительности кровотечений. Также для коагуляции сосудов применяют полупроводниковый диодный лазер.
В некоторых случаях герметичного шва оболочки недостаточно и необходима пластика твердой мозговой оболочки (ТМО), в том числе с применением коллагеновых трансплантатов.
Было прооперировано 29 пациентов, из которых 17 - по поводу адгезивного спинального арахноидита (8 - отграниченные формы, 9 - диффузные формы), 12 - спинальных арахноидальных кист (7 - посттравматические, 5 - идиопатические). Оперативное вмешательство по поводу кистозных и спаечных процессов включало в себя диссекцию видимых спаек и стенок кист, затем введение в дорсальное и/или вентральное пространство дурального мешка ультратонкого гибкого эндоскопа с рабочим каналом диаметром 1,2 мм и диаметром рабочей поверхности 2,8 мм, и текалоскопическое разделение спаек, фенестрацию стенок кист и эксплорацию субарахноидального пространства каудальнее и краниальнее места оперативного доступа. Средний период наблюдения пациентов составил 11,4 месяцев. Регресс неврологической симптоматики был отмечен при контрольных обследованиях у 87% пациентов, оперированных по поводу кистозно-спаечных процессов; среднее улучшение составило 1,4 балла по модифицированной шкале Frankel и 1,8 баллов по шкале Ashworth (рис.7).
На рис.7 указаны результаты контрольного обследования пациентов (средний катамнез 11,4 мес): а - модифицированная шкала Frankel (улучшение моторной функции в среднем на 1,4 балла)*; 6 - шкала Ashworth (снижение спастичности в конечностях в среднем на 1,8 баллов)**.
* Модифицированная шкала Frankel: A (полное поражение) - двигательные функции и чувствительность ниже уровня поражения отсутствуют; B (только чувствительность) - частично сохранена чувствительность ниже уровня поражения, произвольные движения отсутствуют; C - (минимальные двигательные функции) - сохранность двигательных функций со значительным снижением силы до 2 баллов; D (двигательные функции сохранны) - сохранность двигательных функций ниже уровня поражения с силой более 3 баллов; пациент может передвигаться с помощью или без таковой; E (нормальное функционирование) - нормальные двигательные функции и чувствительность.
** Модифицированная шкала Ashworth: 0 - нет повышения тонуса; 1 - легкое повышение тонуса, ощущаемое при сгибании или разгибании сегмента конечности в виде незначительного сопротивления в конце движения; 1* -легкое повышение тонуса, ощущаемое при сгибании или разгибании сегмента конечности во второй половине фазы движения; 2 - умеренное повышение тонуса, выявляющееся в течение всего движения, но не затрудняющее выполнение пассивных движений; 3 - значительное повышение тонуса, затрудняющее выполнение пассивных движений; 4 - пораженный сегмент конечности фиксирован в положении сгибания или разгибания (сгибательная или разгибательная контрактура).
Преходящие нарушения глубокой чувствительности отмечались у 9% пациентов и регрессировали на фоне консервативной терапии. При повторных МРТ рецидив спаечного процесса был выявлен у 1 пациентки (3,1%). Послеоперационные осложнения включали в себя 1 раневую ликворею и 1 случай транзиторной межреберной невралгии. Серьезных интраоперационных осложнений (кровотечение, перфорация твердой мозговой оболочки) зафиксировано не было. Средний срок госпитализации составил 7,6 дней. Таким образом, текалоскопия является эффективной и безопасной минимально инвазивной манипуляцией, которая может широко применяться при хирургическом лечении адгезивных спинальных арахноидитов и арахноидальных кист. При меньшем сроке госпитализации и объеме хирургической агрессии метод обеспечивает быстрое восстановление пациентов. Дальнейшее исследование позволит нам расширить показания к текалоскопии и оценить отсроченные результаты хирургического лечения.
Пример осуществления способа
Пациентка С., 29 лет. Инвалид I группы. При поступлении в нейрохирургическое отделение ФГБУ НЦН РАМН предъявляет жалобы на затруднение движений, чувство спастики в ногах, снижение чувствительности в конечностях, эпизодическое недержание мочи и кала. Ходьба на короткие расстояния с поддержкой. В возрасте 17 лет при криминальном нападении получила сочетанные травмы: закрытая черепно-мозговая травма, ушиб головного мозга. Позвоночно-спинномозговая травма на уровне шейно-грудного перехода. Множественные ножевые ранения шеи, брюшной, грудной полостей, пневматоракс слева, разрыв селезенки. Сразу после полученных ранений полностью отсутствовали движения в руках и ногах, чувствительность, самостоятельное мочеиспускание и дефекация. На фоне многолетней реабилитации отмечен значительный прогресс, пациентка начала ходить на значительные расстояния, частично восстановились функции тазовых органов. Примерно за 1,5 года до поступления отметила медленное ухудшение неврологической симптоматики, затруднение движений в конечностях и усиление онемения. Консервативная терапия и реабилитация оказались неэффективны, в связи с чем консультирована нейрохирургом и предложено оперативное лечение.
Диагноз: Посттравматический кистозно-слипчивый арахноидит на уровне C7-Th1. Миелопатия на уровне C7-Th1.
В неврологическом статусе - спастический тетрапарез до 3 баллов в нижних конечностях, 4 баллов - в верхних конечностях, снижение поверхностной чувствительности с уровня Th2, грубые нарушения глубокой чувствительности в ногах, нарушения функции тазовых органов по типу нейрогенного мочевого пузыря. При МРТ выявляется очаг миелопатии на уровне C7-Th1, кистозно-спаечный процесс на данном уровне, нарушения ликвородинамики (в режиме МР-миелографии).
Пациентке произведено оперативное вмешательство - адгезиолиз на уровне Th1, текалоскопическое разделение спаек. При этом была выявлена грубая спайка, фиксировавшая спинной мозг на уровне C7-Th1, которая была иссечена. После диссекции видимых субарахноидальных спаек в дорсальное и вентральное пространства дурального мешка был введен ультратонкий гибкий эндоскоп с рабочим каналом диаметром 1,2 мм и диаметром рабочей поверхности 2,8 мм. При текалоскопии каудальнее места оперативного доступа (уровень Th4-Th5) обнаружены грубые вентральные и дорсальные спайки, также фиксировавшие спинной мозг и служившие стенками арахноидальных кист. С помощью манипуляторов эндоскопически были разделены и иссечены выявленные спайки и стенки кист. После чего отмечено восстановление пульсации спинного мозга и нормализация пассажа ликвора.
Пациентка активизирована на следующий день после проведенного вмешательства. Отмечен регресс неврологической симптоматики в виде снижения спастичности (на 1 балл по шкале Ashworth), отсутствие тазовых нарушений, улучшение поверхностной и глубокой чувствительности. Рана зажила первичным натяжением, выписана на 6 сутки после операции. При контрольном обследовании через 6 месяцев улучшение в неврологическом статусе оказалось стабильным, данных за рецидив спаечного процесса нет. Пациентка самостоятельно ходит, продолжила обучение в высшем учебном заведении.
Таким образом, ухудшение симптоматики через 11 лет после травмы у пациентки было, вероятно, обусловлено декомпенсацией спинального кровообращения на фоне прогрессирующего спаечного процесса в месте травматического повреждения с компрессией спинного мозга и нарушением ликвородинамики. Возможным механизмом развития отсроченного спаечного процесса у таких больных некоторые авторы по аналогии с отсроченным периодом тяжелой черепно-мозговой травмы считают аутоиммунные реакции. Текалоскопия позволила эффективно осуществить фенестрацию спаек и декомпрессию спинного мозга, в том числе каудальнее места оперативного доступа, где спайки не были четко верифицированы при дооперационном МРТ. Метод позволил добиться стабильного регресса неврологической симптоматики, значительно улучшить качество жизни пациентки и способствовал ранней медико-социальной реабилитации.
Метод текалоскопии применен нами впервые в отечественной нейрохирургии. Исходя из представленных данных лечения спинальных кистозных арахноидитов текалоскопия является эффективной и безопасной минимально инвазивной манипуляцией, которая может широко применяться в хирургическом лечении данной патологии. Предварительные результаты нашей работы показывают, что метод обладает преимуществом перед открытым микрохирургическим вмешательством, обеспечивая лучший клинический результат при меньшем сроке госпитализации и объеме хирургической агрессии, а также более быстрое восстановление пациентов. Кроме того, текалоскопия позволяет осуществлять биопсии экстрамедуллярных объемных образований, видеоассистенцию при синдроме фиксированного спинного мозга. Дальнейшее исследование позволит нам расширить показания к текалоскопии и оценить отсроченные результаты хирургического лечения.
Способ лечения спинальных кистозных арахноидитов, включающий проведение декомпрессии спинномозгового канала, вскрытие твердой мозговой оболочки, диссекции субарахноидальных спаек и стенок кист до восстановления проходимости субарахноидальных пространств с последующим ушиванием твердой мозговой оболочки, отличающийся тем, что при ограниченных спинальных кистах или одиночных спайках доступ осуществляют непосредственно над местом компрессии, при протяженных арахноидальных кистах доступ осуществляют в центральной части кисты, при этом разрез кожи и мягких тканей производят в проекции заинтересованного сегмента спинного мозга, после диссекции видимых субарахноидальных спаек в дорсальное и/или вентральное пространство дурального мешка вводят ультратонкий гибкий эндоскоп с рабочей поверхностью 2,8 мм, разделяют спайки и стенки кист при помощи его манипуляторов, восстанавливают проходимость ликворных пространств и осуществляют широкую ревизию субарахноидального пространства в краниальном и каудальном направлениях.