Способ получения диарилкарбоната
Иллюстрации
Показать всеИзобретение относится к способу получения диарилкарбоната, включающему следующие стадии: а) получение фосгена при взаимодействии хлора с монооксидом углерода, б) взаимодействие полученного на стадии а) фосгена с не менее чем одним монофенолом в присутствии содержащего щелочь водного основания, протекающее с образованием диарилкарбоната и содержащего хлорид щелочного металла отработанного водного раствора, в) отделение и переработка образовавшегося на стадии б) диарилкарбоната, г) отделение остатков растворителя от оставшегося на стадии в) раствора, содержащего хлорид щелочного металла, до того как раствор, содержащий хлорид щелочного металла, направляют на осмотическую мембранную дистилляцию на стадии д), д) концентрирование по крайней мере части оставшегося на стадии г) раствора, содержащего хлорид щелочного металла, с помощью осмотической мембранной дистилляции, причем в качестве акцептора воды применяют раствор гидроксида щелочного металла, е) электрохимическое окисление по крайней мере части содержащего хлорид щелочного металла раствора со стадии д) с образованием хлора, раствора гидроксида щелочного металла и при необходимости водорода. В способе с высоким выходом получают продукцию с высокой степенью чистоты. 17 з.п. ф-лы, 1 ил., 6 пр.
Реферат
Изобретение относится к технологии получения ароматических карбонатов, в частности к способу получения диарилкарбоната.
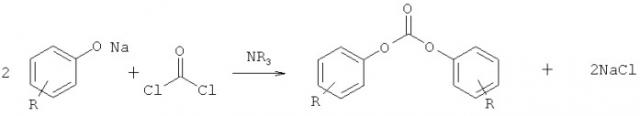
Получение диарилкарбонатов (дифенилкарбоната) проводят, как правило, по непрерывной схеме, с получением фосгена и с последующей реакцией монофенолов и фосгена в инертном растворителе в присутствии щелочи и азотного катализатора на границе раздела фаз.
Получение диарилкарбонатов, например, при взаимодействии на границе раздела фаз, в принципе описано в литературе, см., например. Chemistry and Physics of Polycarbonates, Polymer Reviews, H. Schnell, Том 9, John Wiley and Sons, Inc. (1964), с.50/51.
В патенте США №4016190 представлен способ получения диарилкарбонатов, который реализуют при температурах выше 65°С. В соответствии с этим способом значение рН вначале поддерживают низким (рН 8-9), а затем высоким (рН 10-11).
Оптимизация способа путем интенсификации перемешивания и поддержания значений температуры и рН в узких пределах, а также и выделение продукта представлены в заявках на европейский патент №1219589А1, №1216981А2, №1216982А2 и №784048А1.
Однако для этих известных способов требуются дорогостоящие операции по очистке, связанные с высоким содержанием в отработанных водных растворах этих процессов фенолов, которые могут создавать угрозу окружающей среде; в связи с этим появляется серьезная проблема по нейтрализации отработанных водных растворов на очистных сооружениях. В соответствии с этим в международной заявке на патент №03/070639 А1 описано удаление органических примесей в сточных водах с помощью экстракции метиленхлоридом.
Обычно содержащий хлорид натрия раствор сбрасывают после освобождения от растворителей и органических остатков.
В соответствии с заявкой на европейский патент №1200359 В1 (заявка на международный патент №2000078682 А1) и патентом США №6340736 содержащие хлорид натрия отработанные водные растворы могут быть очищены с помощью озонолиза и после этого использованы для электролиза хлорида натрия. Недостаток этого способа состоит в том, что озонолиз представляет собой очень затратную операцию.
В соответствии с заявкой на европейский патент №541114 А2 содержащий хлорид натрия поток отработанной воды упаривают до полного удаления воды и оставшуюся соль с органическими примесями подвергают термической обработке, в результате которой органические составляющие разлагаются. При этом особое предпочтение отдается использованию инфракрасного излучения. Недостаток данного способа состоит в том, что воду необходимо выпаривать полностью, поэтому способ оказывается экономически несостоятельным.
В соответствии с заявкой на международный патент №03/7063 9А1 отработанные водные растворы из производства дифенилкарбоната очищают с помощью экстракции и после этого подают ее на электролиз хлорида натрия. Однако с помощью описанного способа при электролизе хлорида натрия можно использовать не более 26% хлорида натрия из отработанных водных растворов производства дифенилкарбоната, так как при подаче более значительных количеств содержащих хлорид натрия отработанных водных растворов поступающая в их составе на электролиз вместе с хлоридом натрия вода нарушила бы водный баланс при электролизе хлорида натрия.
Содержащие хлорид натрия растворы, которые образуются при производстве дифенилкарбоната, имеют в типичном случае содержание хлорида натрия от 13 до 17 масс.%. В соответствии с этим ни при каких условиях весь присутствующий в растворах хлорид натрия не может быть возвращен на электролиз хлорида натрия для получения хлора и раствора гидроксида натрия. При концентрации хлорида натрия 17 масс.% при проведении стандартного электролиза хлорида натрия с приобретаемыми коммерческим путем ионообменными мембранами, которые работают с переносом 3,5 молей воды на моль натрия, удается использовать только около 23% хлорида натрия из таких содержащих хлорид натрия растворов. При повышении концентрации до насыщенного состояния раствора хлорида натрия, равного примерно 25 масс.%, количество утилизируемого в рецикле хлорида натрия составит 38% от всего содержащегося в растворе хлорида натрия. Полный рецикл раствора, содержащего хлорид натрия, до настоящего времени не известен.
В то же время известны способы концентрирования отработанных водных растворов, содержащих хлориды щелочных металлов, основанные на отводе из них воды.
В соответствии с международной заявкой на патент №01/38419 раствор, содержащий хлорид натрия, можно выпаривать термическим способом и тогда можно подавать в электролизер высококонцентрированный раствор хлорида натрия. Однако выпаривание представляет собой энергоемкий и затратный процесс.
Можно также использовать, например, обратный осмос или в особо предпочтительном случае мембранную дистилляцию или мембранные контакторы (см. MELIN; RAUTENBACH, Membran-verfahren; SPRINGER, Берлин, 2003). Недостатком при этом становится большой расход энергии для преодоления высокого осмотического давления, из-за чего и такие способы оказываются неэкономичными.
Недостаток представленных выше интегрированных способов состоит в том, что в сочетании с получением диарилкарбоната на электролиз могут подаваться только растворы хлорида натрия с определенной предельной концентрацией (от 10 до 20 масс.%), вследствие чего последующую утилизацию хлорида натрия можно проводить только в ограниченном объеме или же приходится прибегать к энергозатратному и дорогостоящему концентрированию.
Исходя из представленного выше уровня техники, задача изобретения состояла в разработке способа получения диарилкарбонатов, в соответствии с которым с высоким выходом получается продукция высокой чистоты и снижается давление на окружающую среду или, соответственно, снимается проблема нейтрализации отработанных водных растворов на очистных сооружениях за счет максимального рецикла образующихся в производстве растворов, представляющих собой отработанные водные растворы из производства диарилкарбонатов.
Кроме того, при рецикле превращение хлорида натрия в хлор и раствор гидроксида натрия с возможным получением водорода в результате электролиза должно протекать по ресурсосберегающей технологии с минимальным расходом энергии.
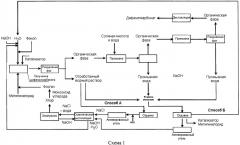
Поставленная задача решается способом утилизации содержащих хлорид натрия отработанных растворов, образующихся при разделении фаз, при котором для электролиза проводится предварительное концентрирование раствора хлорида натрия из производства диарилкарбоната с помощью осмотической мембранной дистилляции.
Было обнаружено, что при получении диарилкарбонатов по непрерывной схеме в результате реакции монофенолов с фосгеном на границе раздела фаз в инертном растворителе в присутствии щелочи и азотсодержащего катализатора образующиеся в качестве отходов водные растворы, содержащие хлорид натрия, могут быть без трудоемкой очистки направлены на концентрирование с помощью мембранной дистилляции после установки в них значения рН, равного восьми или менее восьми, и после простой обработки активированным углем, и после этого они могут поступать на электрохимическое окисление содержащегося в них хлорида натрия с получением хлора, раствора гидроксида натрия и в соответствующих случаях водорода, при этом хлор, по крайней мере частично, может быть возвращен на получение фосгена.
В соответствии с изложенным объектом изобретения является способ получения диарилкарбоната и утилизация образующихся при разделении фаз отработанных водных растворов. В частности, особенность способа состоит в концентрировании с помощью осмотической мембранной дистилляции содержащих хлорид натрия отработанных водных растворов, образующихся при разделении фаз в производстве дифенилкарбоната, для переработки их на следующей стадии электролиза хлорида щелочного металла. При этом одновременно можно разбавлять образующийся при электролизе раствор гидроксида натрия и непосредственно использовать его в качестве исходного продукта в процессе получения дифенилкарбоната.
Соответствующий изобретению способ получения диарилкарбоната включает следующие стадии:
а) получение фосгена при взаимодействии хлора с монооксидом углерода,
б) взаимодействие полученного на стадии а) фосгена с не менее чем одним монофенолом в присутствии содержащего щелочь водного основания, в частности основания, в состав которого входит натрий, в случае необходимости в присутствии азотсодержащего катализатора и в случае необходимости в присутствии органического растворителя, протекающее с образованием диарилкарбоната и содержащего хлорид щелочного металла, в частности содержащего хлорид натрия, отработанного водного раствора,
в) отделение и переработка образовавшегося на стадии б) диарилкарбоната,
г) в случае необходимости отделение остатков растворителя и остатков катализатора, если он использовался, от образовавшегося на стадии в) содержащего хлорид натрия раствора, в частности, с помощью экстракции или же продувки раствора водяным паром и/или с помощью обработки адсорбентами, в частности активированным углем,
д) осмотическая мембранная дистилляция по крайней мере части полученного на стадии в) или на стадии г) раствора, содержащего хлорид щелочного металла,
е) электрохимическое окисление по крайней мере части содержащего хлорид щелочного металла раствора со стадии д) с образованием хлора, раствора гидроксида щелочного металла и в соответствующем случае водорода.
В особо предпочтительном варианте реализации способ отличается тем, что на стадии в) или на стадии г) перед обработкой адсорбентами в растворе устанавливают значение рН, равное восьми или менее восьми, в предпочтительном случае от шести до восьми.
В еще одном предпочтительном варианте реализации способ отличается тем, что по крайней мере часть полученного на стадии е) хлора возвращается на стадию получения фосгена а).
В еще одном предпочтительном варианте реализации по крайней мере часть полученного на стадии е) раствора гидроксида щелочного металла используется в качестве акцептора воды в процессе осмотической мембранной дистилляции в соответствии со стадией д).
В еще одном особо предпочтительном варианте реализации по крайней мере часть полученного разбавленного раствора гидроксида щелочного металла возвращается в процесс получения диарилкарбоната в соответствии со стадией б).
Полученный после разделения фаз в соответствии со стадией в) содержащий хлорид щелочного металла раствор (водные отходы реакции) может быть использован в процессе осмотической мембранной дистилляции как таковой или же он может быть объединен с полученными при промывке водными фазами со стадии переработки (объединенные водные отходы процесса), в предпочтительном случае он используется как таковой после отделения остатков растворителя и в случае необходимости от остатков катализатора в соответствии со стадией г).
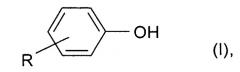
Монофенолами, которые более всего подходят для использования в новом способе, являются фенолы формулы (I)
где
R означает атом водорода, галогена или же разветвленный или неразветвленный алкильный остаток с числом атомов углерода от одного до девяти или алкоксикарбонильный остаток.
Предпочтительными соединениями являются фенол, такие алкилфенолы, как крезолы, п-трет-бутилфенол, п-кумилфенол, п-н-октилфенол, п-изооктилфенол, п-н-нонилфенол и п-изононилфенол, такие галогензамещенные фенолы, как п-хлорфенол, 2,4-дихлорфенол, п-бромфенол и 2,4,6-трибромфенол, или же метиловый эфир салициловой кислоты. Особое предпочтение отдается фенолу.
Используемая для образования фенолята на стадии б) щелочь может представлять собой, например, растворы гидроксидов щелочных металлов из ряда: гидроксид натрия, калия, лития; предпочтение отдается гидроксиду натрия, который в соответствии с новым способом в предпочтительном случае используют в виде раствора с концентрацией от 10 до 55 масс.%. В особо предпочтительном случае раствор гидроксида щелочного металла используют в количестве от 1,0 до 1,1 мольных эквивалентов из расчета на фенол.
Реакцию на стадии б) можно ускорять с помощью таких азотсодержащих катализаторов, как третичные амины, N-алкилпиперидины или ониевые соли.
Применяемый аминный катализатор может иметь открытую цепь или он может быть циклическим, предпочтение отдается трибутиламину, триэтиламину и N-этил-пиперидину. Предпочтительно, когда в соответствующем изобретению способе катализатор используют в виде раствора с концентрацией от 1 до 55 масс.%.
Предпочтительно, когда концентрация катализатора составляет от 0,0001 моля до 0,1 моля из расчета на монофенол.
Понятие ониевых солей относится в данном случае к таким соединениям, как NR4X, где R может означать алкильный и/или арильный остаток, и/или атом водорода и Х означает анион.
Фосген можно использовать на стадии б) в жидком виде, в виде газа или в виде раствора в инертном растворителе.
В предпочтительном случае при реализации нового способа на стадии б) могут быть использованы инертные растворители, например дихлорметан, толуол, различные дихлорэтаны и хлорпропановые соединения, хлорбензол и хлортолуол. В предпочтительном случае используют дихлорметан.
В предпочтительном случае реакцию на стадии б) проводят по непрерывной схеме и в особо предпочтительном случае ее проводят в пробочном режиме без значительного продольного перемешивания. В соответствии с этим процесс может протекать, например, в трубных реакторах. Перемешивание двух фаз (водной и органической фазы) можно обеспечивать за счет встроенных в трубки диафрагм, статических смесителей и/или, например, насосов. Соответствующую стадии б) реакцию можно проводить в один или в два этапа, в особо предпочтительном случае ее проводят в два этапа.
Если на стадии б) реализация способа основана на двух этапах, то в предпочтительном случае на первом этапе соответствующего изобретению способа взаимодействие начинается со смешивания исходных продуктов - фосгена, инертного растворителя, который в предпочтительном случае изначально служил растворителем для фосгена, и монофенола, который в предпочтительном случае до этого был уже растворен в растворе гидроксида щелочного металла. Время пребывания для первого этапа в типичном случае лежит в пределах от 2 секунд до 300 секунд, в особо предпочтительном случае от 4 секунд до 200 секунд. Целесообразно, когда значение рН на первом этапе устанавливают за счет соотношения раствора гидроксида щелочного металла, монофенола и фосгена так, чтобы значение рН лежало в пределах от 11,0 до 12,0, в предпочтительном случае от 11,2 до 11,8, в особо предпочтительном случае от 11,4 до 11,6. Температуру реакции на первом этапе поддерживают с помощью охлаждения в предпочтительном случае ниже 40°С, в особо предпочтительном случае ниже 35°С.
После этого на втором этапе соответствующего изобретению способа завершают реакцию с образованием диарилкарбоната. Время пребывания в предпочтительном случае реализации способа составляет от 1 минуты до 2 часов, в особо предпочтительном случае от 2 минут до 1 часа, в самом предпочтительном случае от 3 минут до 30 минут. На втором этапе предпочтительного способа реализации постоянно контролируется значение рН (в предпочтительном случае при проведении процесса по непрерывной схеме осуществляется текущий контроль известными способами) и поддерживается соответствующее значение рН добавлением раствора гидроксида щелочного металла. В частности, количество подаваемого раствора щелочного металла регулируют так, чтобы значение рН в реакционной смеси на втором этапе процесса лежало в пределах от 7,5 до 10,5, в предпочтительном случае от 8 до 9,5, в особо предпочтительном случае от 8,2 до 9,3. Температуру реакции на втором этапе поддерживают с помощью охлаждения в предпочтительном случае ниже 50°С, в особо предпочтительном случае ниже 40°С и в самом предпочтительном случае ниже 35°С.
Однако приведенные в данной заявке общие или предпочтительные области значений параметров или, соответственно, характеристик могут сочетаться между собой или между соответствующими пределами и предпочтительными пределами в любых вариантах.
В предпочтительном варианте реализации способа на стадии б) используют фосген в отношениях от 1:2 до 1:2,2 по отношению к монофенолу. Растворитель прибавляют так, чтобы после реакции диарилкарбонат получался в виде раствора с концентрацией от 5 до 60%, в предпочтительном случае от 20 до 45%.
Предпочтительно, когда на стадии в) после реакции на стадии б) органическую фазу, содержащую диарилкарбонат, промывают водной жидкостью и после каждой операции по промывке тщательно отделяют ее от водной фазы. В качестве промывочной жидкости используют водные жидкости для отделения катализатора, например такую разбавленную минеральную кислоту, как соляная кислота или фосфорная кислота, в предпочтительном случае используют соляную кислоту, а для следующей далее очистки используют полностью обессоленную воду. Раствор диарилкарбоната после промывки и отделения промывочной жидкости оказывается обычно мутным. Концентрация соляной кислоты или фосфорной кислоты в промывочной жидкости может составлять, например, от 0,5 до 1,0 масс.%. Например, а также в предпочтительном случае органическую фазу промывают два раза.
В качестве устройства для разделения фаз при отделении промывочной жидкости от органической фазы могут быть использованы в общем случае известные специалисту отстойники, сепараторы фаз, центрифуги или коагуляторы или также комбинации из этих устройств.
При реализации соответствующего изобретению способа, несмотря на необходимость отделения растворителя, можно получать диарилкарбонат высокой чистоты, составляющей более 99,85%.
В предпочтительном варианте после проведения синтеза диарилкарбоната проводят выделение диарилкарбоната в виде его раствора в использовавшемся для синтеза органическом растворителе, например в метиленхлориде.
Для получения диарилкарбоната высокой чистоты растворитель после этого упаривают. Отгонка растворителя может осуществляться на нескольких стадиях выпаривания. Так, например, это осуществляется в одной или в нескольких соединенных последовательно дистилляционных колоннах, и в результате этого происходит отделение растворителя от диарилкарбоната.
Стадию очистки в) можно проводить в один или в несколько этапов. Эти этапы могут быть реализованы, например, в рамках непрерывной схемы так, чтобы температура в кубе при дистилляции составляла от 150°С до 310°С, в предпочтительном случае от 160°С до 230°С. Используемое для проведения дистилляции давление составляет при этом, в частности, от 1 до 1000 мбар, в предпочтительном случае от 5 до 100 мбар.
Очищенные таким способом диарилкарбонаты отличаются особенно высокой чистотой (по данным газовой хроматографии более 99,95%) и исключительно хорошими свойствами при переэтерефикации, благодаря чему на их основе можно после этого получать поликарбонат прекрасного качества.
Применение диарилкарбонатов для получения ароматических олиго- и поликарбонатов способом переэтерификации в расплаве известно по литературным источникам, оно описано, например, в Encyclopedia of Polymer Science, Том 10 (1969), Chemistry and Physics of Polycarbonates, Polymer Reviews, H. Schnell, Том 9, John Wiley and Sons, Inc. (1964), или в патенте США №5340905.
Остающийся на стадии в) водный раствор в предпочтительном случае освобождают от таких легколетучих органических загрязнений, как, например, остатки использовавшегося при проведении синтеза органического растворителя и в случае необходимости от остатков катализатора, для этого используют, например, дистилляцию или продувку водяным паром. После этого остаются водные отходы, содержащие растворенный хлорид натрия (от 10 до 20 масс.%) и растворенные карбонаты натрия (от 0,3 до 1,5 масс.%). При этом карбонаты образуются, например, в результате гидролиза фосгена в качестве побочной реакции при получении диарилкарбоната. Отработанные водные растворы, кроме этого, содержат органические соединения, например фенолы (например, незамещенный фенол, алкилфенолы).
В особо предпочтительном варианте реализации проводят обработку предварительно очищенных отработанных водных растворов адсорбентами, в предпочтительном случае активированным углем.
В соответствии с предпочтительным вариантом реализации способа значение рН на стадии процесса в) или г) понижают добавлением соляной кислоты или хлористого водорода.
Предпочтительный вариант реализации способа состоит в том, что из содержащих хлорид щелочного металла отработанных водных растворов удаляют воду способами, основанными на концентрировании.
Концентрирование растворов с хлоридом натрия с помощью осмотической дистилляции представляет собой энергосберегающий способ, в частности, в том случае, когда получаемый при электролизе хлорида натрия раствор гидроксида натрия используют в качестве акцептора воды. Преимущество этого способа состоит, в частности, в том, что при производстве дифенилкарбоната используют разбавленный раствор гидроксида натрия, и в соответствии с этим появляется дополнительная возможность снижения расхода воды для разбавления раствора гидроксида натрия.
Особо предпочтительным при этом является способ, отличающийся тем, что содержащий хлорид щелочного металла раствор со стадии г) перед электролизом е) концентрируют с помощью осмотической дистилляции с раствором гидроксида натрия в качестве акцептора воды (стадия д).
При комбинировании соответствующих изобретению способов использования электролизных ячеек и способов концентрирования можно теоретически возвращать из отработанных водных растворов до 100% хлорида натрия.
Осмотическая дистилляция протекает в результате молекулярной и в соответствующих случаях кнудсеновской диффузии водяного пара через мембрану. Вследствие этого скорость диффузии зависит от разницы в давления водяного пара по обе стороны мембраны, а также от ее пористости, толщины и изогнутости.
Для достижения эффективного концентрирования надо в качестве акцептора воды использовать концентрированный раствор гидроксида щелочного металла, в предпочтительном случае гидроксида натрия или калия, в особо предпочтительном случае гидроксида натрия.
В соответствующем изобретению способе в качестве материала мембраны надо использовать химически стойкий материал, например полипропилен. Используемые мембраны в предпочтительном случае должны представлять собой капиллярные мембраны с длиной капилляров от 30 до 6000 мкм и с диаметром от 0,01 до 0,7 мкм.
Лучше всего на роль мембран подходят липофильные мембраны, например, Accurel РР 50/200, Accurel РР 50/280, Accurel РР 150/330, Accurel РР Q3/2 или Accurel S 6/2 фирмы Membrana.
В предпочтительном случае способ реализуют так, чтобы осмотическая дистилляция проходила при температуре от 10 до 100°С, в более предпочтительном случае от 20 до 50°С. При этом температура используемого раствора гидроксида натрия может быть выше, чем температура содержащих хлорид натрия отработанных водных растворов.
Осмотическую дистилляцию проводят при абсолютном давлении от 1 до 1,4 бара, в предпочтительном случае при давлении от 1,1 до 1,2 бара.
Перепад давлений между раствором хлорида щелочного металла и раствором гидроксида щелочного металла в наиболее предпочтительном варианте реализации способа должен составлять от 20 до 150 бар, в предпочтительном случае от 30 до 100 бар.
Далее приводится более детальное описание процесса электролиза хлорида щелочного металла. Следующее далее описание, относящееся к электролизу хлорида натрия, следует рассматривать всего лишь как пример, поскольку, как уже указывалось выше, принципиально в способе может быть использован хлорид любого щелочного металла (в частности хлориды лития, натрия, калия), тогда как использование хлорида натрия и, соответственно, гидроксида натрия на предшествующих стадиях представляет собой предпочтительный вариант реализации способа.
Обычно для электролиза содержащих хлорид натрия растворов используют, например, мембранные способы электролиза (это представлено в книге Peter Schmittinger, CHLORINE, издательство Wiley-VCH, 2000). Для этого используют разделенную на две части электролизную ячейку, состоящую из анодного пространства с анодом и катодного пространства с катодом. Анодное и катодное пространства разделены мембраной. В анодное пространство заливают содержащий хлорид натрия раствор с концентрацией хлорида натрия обычно более 300 г/л. На аноде происходит окисление хлоридных ионов до хлора, который выводят из ячейки вместе с содержащим хлорид натрия раствором, концентрация которого понизилась (примерно до 200 г/л). Под действием электрического поля ионы натрия проходят через ионообменную мембрану в катодное пространство. При этом перемещении каждый моль натрия в зависимости от мембраны переносит от 3,5 до 4,5 молей воды. Это приводит к тому, что в анолите содержание воды уменьшается. В отличие от анолита на катодной стороне идет электролиз воды до гидроксидных ионов и водорода, то есть вода расходуется. Поступающей с ионами натрия в катодное пространство воды достаточно для того, чтобы поддерживать концентрацию в растворе гидроксида натрия на выходе в пределах от 31 до 32 масс.% при концентрации на входе 30% и плотности тока 4 кА/м2. В катодном пространстве идет электрохимическое восстановление воды, которое приводит к образованию гидроксидных ионов и водорода.
В альтернативном варианте в качестве катода можно использовать газодиффузионный электрод, на котором происходит взаимодействие кислорода с электронами с образованием гидроксидных ионов, и тогда водород не образуется. С поступающими в катодное пространство через ионообменную мембрану ионами натрия гидроксидные ионы образуют гидроксид натрия. В катодное пространство обычно подают раствор гидроксида натрия с концентрацией 30 масс.%. Выводят же раствор гидроксида натрия с концентрацией от 31 до 32 масс.%. При этом преследуется цель получения как можно более высокой концентрации раствора гидроксида натрия, поскольку обычно раствор гидроксида натрия хранят и перемещают в виде 50%-ной щелочи. Однако в настоящее время приобретаемые коммерческим путем мембраны неустойчивы к действию щелочи с концентрацией, превышающей 32 масс.%, из-за чего раствор гидроксида натрия приходится концентрировать путем термического упаривания.
При электролизе хлорида натрия с таким содержащим хлорид натрия раствором в анолит поступает дополнительная вода, но через мембрану в католит переходит только вода. Когда количество воды, поступающей с содержащим хлорид натрия раствором, превышает то ее количество, которое может поступить в католит, концентрация хлорида натрия в анолите падает, и электролиз уже нельзя проводить по непрерывной схеме. При очень низких концентрациях хлорида натрия может идти побочная реакция образования кислорода.
Экономически оправдано использование максимального количества содержащих хлорид натрия растворов и тогда может оказаться целесообразным увеличение транспорта воды через мембрану. Этот эффект можно получить за счет выбора подходящих мембран, как это представлено в патенте США №4025405. Эффект увеличенного транспорта воды приводит к тому, что используемое обычно добавление воды для поддержания концентрации щелочи может оказаться излишним.
В соответствии с патентом США №3773634 электролиз, сопровождающийся переносом большого количества воды через мембрану, можно проводить в тех случаях, когда концентрация щелочи составляет от 31 до 43 масс.% и концентрация хлорида натрия составляет от 120 до 250 г/л.
В соответствии со способом, которому отдается предпочтение, отделение на стадии г) содержащих хлорид натрия жидких отходов реакции проводят после разделения фаз и удаления с помощью экстракции и продувки водяным паром растворителя и катализатора, если он использовался, а также с помощью обработки активированным углем после установления определенного значения рН.
В соответствии с этим содержащие хлорид натрия водные отходы могут быть непосредственно направлены на осмотическую дистилляцию д).
В отличие от уровня техники (заявка на международный патент №03/70639), в соответствии с которым для электролиза хлорида натрия можно использовать только 26% хлорида натрия, содержащегося в отработанных водных растворах производства дифенилкарбоната, в рамках соответствующего изобретению способа можно возвратить в процесс более 26% хлорида натрия из отработанных водных растворов.
Новый способ можно также проводить с электролизом хлорида щелочного металла, при котором на катоде не выделяется водород; в этом варианте катод заменяют на газодиффузионный электрод, на котором кислород восстанавливается до гидроксильных ионов.
Если, например, на смежном участке не используется водород для химических реакций, то можно отказаться от получения водорода как обязательного побочного продукта. Преимущество такого способа состоит в том, что при этом происходит экономия энергии при электролизе, обусловленная более низким напряжением при электролизе с использованием газодиффузионного электрода.
Поступающий из производства дифенилкарбоната содержащий хлорид натрия раствор содержит обычно до 18 масс.% хлорида натрия, если он представляет собой отработанные водные растворы реакции. Однако когда отработанные водные растворы реакции объединяют с промывными водами, концентрация хлорида натрия составляет, например, около 13 масс.%. Если электролиз поставляет хлор и раствор гидроксида натрия только для производства дифенилкарбоната, то в электролизе может быть использована лишь небольшая часть содержащих хлорид натрия отработанных водных растворов. В соответствии с этим при обычных ионообменных мембранах и при стандартных параметрах проведения процесса в ходе электролиза хлорида натрия можно использовать не более 26% хлорида натрия из содержащих хлорид натрия отработанных водных растворов производства дифенилкарбоната с концентрацией 17 масс.%. Стандартные параметры проведения процесса электролиза хлорида натрия включают концентрацию рассола по ходу процесса от 200 до 240 г/л и концентрацию гидроксида натрия от 31 до 32 масс.%. В соответствии с этим полный рецикл образующегося хлорида натрия был до настоящего времени невозможен. Повышение концентрации путем термического выпаривания воды в настоящее время неэкономично, поскольку хлорид натрия представляет собой очень дешевый продукт.
В рамках соответствующего изобретению способа можно направить на рецикл значительно больше чем 26% хлорида натрия из образующихся отработанных водных растворов при концентрации 17 масс.%, когда электролиз хлорида натрия поставляет хлор и раствор гидроксида натрия исключительно для производства дифенилкарбоната. Обычно электролиз хлорида натрия функционирует для нескольких смежных химических потребителей хлора, и при этом не все потребители могут направлять на рецикл содержащий хлорид натрия раствор. Количество хлорида натрия в отработанных водных растворах, которые могут быть снова использованы, возрастает в том случае, когда электролиз хлорида натрия поставляет раствор гидроксида натрия и хлор не только для производства диарилкарбонатов.
Еще один предпочтительный вариант нового способа состоит в том, что концентрацию в отработанных водных растворах производства диарилкарбонатов можно повысить в результате прибавления твердого хлорида щелочного металла и направить их на электролиз хлорида щелочного металла. Благодаря этому можно снова использовать более 50% хлорида щелочного металла из отработанных водных растворов производства дифенилкарбоната.
Однако это возможно лишь при условии, что хлор и раствор гидроксида щелочного металла используются не только в производстве диарилкарбоната.
В особо предпочтительном случае для электролиза е) используют содержащие хлорид щелочного металла водные растворы, у которых значение рН составляет менее 7. Установку значения рН проводят в предпочтительном случае с помощью соляной кислоты, но можно для этого использовать и газообразный хлористый водород.
В соответствии с еще одним предпочтительным способом электролиз хлорида натрия проводят так, чтобы раствор хлорида натрия, который выходит из ячейки, имел концентрацию хлорида натрия менее 200 г/л. В соответствии с этим концентрация выходящего из ячейки раствора гидроксида щелочного металла может составлять менее 30 масс.%.
Перенос воды через ионообменную мембрану зависит не только от рабочих параметров, но и от типа используемой мембраны. В рамках соответствующего изобретению способа предпочтение отдается использованию таких ионообменных мембран, которые при соответствующих изобретению условиях, относящихся к концентрации хлорида натрия и щелочи, обеспечивают перенос воды через мембрану в количестве более 4,5 молей воды на моль натрия.
При этом плотность тока определяют из расчета на поверхность мембраны, в частности она составляет от 2 до 6 кА/м2. В особо предпочтительном случае используют аноды с увеличенной поверхностью. Понятие анодов с увеличенной поверхностью относится к таким анодам, у которых физическая поверхность значительно превышает проецируемую поверхность. Анодами с увеличенной поверхностью являются, например, пористые электроды или электроды фетрового типа. Благодаря этому для анодных процессов представляется очень большая поверхность электродов и значительно снижается локальная плотность тока. Поверхность анода в предпочтительном случае выбирают так, чтобы локальная плотность тока из расчета на физическую поверхность электрода не превышала 3 кА/м2. Чем больше поверхность и чем ниже локальная плотность тока, тем более низкой может быть выбранная концентрация хлорида натрия в рассоле и тем большее количество хлорида натрия в отработанных водах может быть утилизировано.
В предпочтительном случае значение рН в содержащих хлорид натрия отработанных водных растворах перед электролизом е) не должно превышать 7, в особо предпочтительном случае оно составляет от 0,5 до 6.
Электролиз хлорида щелочного металла следует проводить так, чтобы концентрация хлорида щелочного металла в выходящем из ячейки растворе хлорида щелочного металла составляла от 100 до 280 г/л для хлорида натрия и/или чтобы концентрация выходящей из ячейки щелочи составляла от 13 до 33 масс.%.
Особое предпочтение отдается концентрациям, которые представляют возможность для работы ячеек при низком напряжении. Для этого в предпочтительном случае концентрация выходящего из ячейки раствора хлорида щелочного металла составляет от 110 до 220 г/л хлорида щелочного металла и/или концентрация выходящей из ячейки щелочи составляет от 20 до 30 масс.%.
Используемые при электролизе ионообменные мембраны должны в предпочтительном случае обеспечивать перенос воды на моль натрия в количестве более 4,0 молей воды на моль натрия, в особо предпочтительном случае от 4,5 до 6,5 молей воды на моль натрия.
В предпочтительном случае способ реализуют так, чтобы температура при электролизе е) была в пределах от 70 до 100°С, в более предпочтительном случае от 80 до 95°С.
Электролиз проводят при абсолютном давлении от 1 до 1,4 бара, в предпочтительном случае от 1,1 до 1,2 бара.
В частности, соотношение давлений между анодным и катодным пространствами выбирают так, чтобы давление в катодном пространстве было выше давления в анодном пространстве. Различие в давлениях между катодным и анодным пространствами в особо предпочтительном варианте реализации способа должно составлять от 20 до 150 мбар, в предпочтительном случае от 30 до 100 мбар.
При пониженных концентрациях хлорида щелочного металла могут быть также использованы специальные покрытия для анодов. В частности, покрытие для анода может содержать наряду с оксидом рутения и другие компоненты из благородных металлов седьмой и восьмой побочных групп Периодической системы элементов. Так, например, анодное покрытие может быть дотировано соеди