Вакцина против pcsk9
Иллюстрации
Показать всеИзобретение относится к области иммунологии и биотехнологии. Представлен иммуноген для индуцирования иммунного ответа против белка PCSK9, содержащий антигенный пептид PCSK9, выбранный из группы, состоящей из раскрытых в описании SEQ ID NO: 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 314, 318 и 319, содержащих аминокислотную последовательность TRFHRQ, и SEQ ID NO: 182, 183, 184, 185, 186, 187, 188, 317, 401, 402 и 403, содержащих аминокислотную последовательность SIPWNLE, где указанный антигенный пептид PCSK9 конъюгирован с иммуногенным носителем, выбранным из CRM197 или Qbeta вирусоподобной частицы (VLP). Описана композиция для индуцирования иммунного ответа против белка PCSK9, содержащая по меньшей мере два иммуногена в иммунологически эффективных количествах, где первый иммуноген представляет собой указанный иммуноген. Раскрыта композиция для индуцирования иммунного ответа против белка PCSK9, содержащая по меньшей мере два иммуногена в иммунологически эффективных количествах, где первый иммуноген выбран из группы иммуногенов, содержащих аминокислотную последовательность SIPWNLE, и где второй иммуноген выбран из группы иммуногенов, содержащих аминокислотную последовательность TRFHRQ; и где композиция может содержать дополнительно по меньшей мере один адъювант. Также представлена фармацевтическая композиция для предупреждения, лечения или облегчения PCSK9-связанных расстройств, содержащая: в терапевтически эффективном количестве указанный иммуноген, или одну из указанных композиций и фармацевтически приемлемый эксципиент. Изобретение позволяет получить эффективную вакцину против расстройств, связанных с взаимодействием белка PCSK9 с его рецептором LDLR. 7 н. и 17 з.п. ф-лы, 19 ил., 6 табл., 9 пр.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к обеспечению новых иммуногенов, содержащих антигенный пептид PCSK9, предпочтительно связанный с иммуногенным носителем для предупреждения, лечения и облегчения PCSK9-связанных расстройств. Изобретение также относится к способам изготовления этих лекарственных средств, их иммуногенным композициям и фармацевтическим композициям и их применению в медицине.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Пропротеин-конвертаза субтилизин/кексин 9 типа (называемая в дальнейшем "PCSK9"), также известная как нервная апоптоз-регулируемая конвертаза 1 ("NARC-i"), представляет собой протеиназа K-подобную субтилазу, идентифицированную в качестве как 9-го члена семейство PCSK млекопитающих; см. Seidah et al., 2003, PNAS 100:928-933. Ген PCSK9 расположен на человеческой хромосоме 1р33-р34.3. PCSK9 экспрессируется в клетках, способных к пролиферации и дифференцировке, включающих, например, гепатоциты, мезенхимальные клетки почек, интестинальные клетки подвздошной кишки и эпителий толстой кишки, а также эмбриональные нейроны мозгового пузыря.
Первоначальный синтез PCSK9 представлен в форме неактивного предшественника фермента, или зимогена, с молекулярной массой примерно 72 кДа, который подвергается аутокаталитическому, внутримолекулярному процессингу в эндоплазматическом ретикулуме ("ЭР") для активации его функциональных свойств. Последовательность гена для человеческого PCSK9, которая имеет длину примерно 22 т.п.н. с 12 экзонами, кодирующими 692-аминокислотный белок, можно найти, например, под депозитарным №NP_777596.2. Последовательности нуклеиновых кислот PCSK9 человека, мыши и крысы были депонированы; см., например, GenBank номера доступа: АХ 127530 (также АХ207686), АХ207688 и АХ207690, соответственно.
Человеческий PCSK9 представляет собой секретируемый белок, экспрессирующийся главным образом в почках, печени и кишечнике. Он имеет три домена: ингибиторный продомен (аминокислоты 1-152; включающие сигнальную последовательность по аминокислотам 1-30), каталитический домен (аминокислоты 153-448) и С-концевой домен длиной 210 остатков (аминокислоты 449-692), который богат цистеиновыми остатками. PCSK9 синтезируется в виде зимогена, который подвергается аутокаталитическому расщеплению между продоменом и каталитическим доменом в эндоплазматическом ретикулуме. Продомен остается связанным со зрелым белком после расщепления и комплекс секретируется. Цистеии-богатый домен может играть роль, аналогичную Р-(процессинг) доменам других Фурин/Кексин/Субтилизин-подобных сериновых протеаз, которые, по-видимому, необходимы для сворачивания и регуляции активированных протеаз. Мутации в PCSK9 ассоциированы с аномальными уровнями холестерина липопротеинов низкой плотности (LDL-c) в плазме крови (Horton et al., 2006 Trends. Biochem. Sci, 32(2):71-77).
PCSK9, которому приписывается роль в дифференцировке гепатоцитов и нервных клеток (Seidah et al., выше), высоко экспрессируется в эмбриональной печени и в значительной степени вовлечен в гомеостаз холестерина.
Весьма желательна идентификация соединений и/или агентов, эффективных в лечении сердечно-сосудистых заболеваний. Снижение уровней холестерина LDL, как уже было продемонстрировано в клинических испытаниях, непосредственно связано с частотой коронарных приступов; Law et al., 2003 BMJ 326: 1423-1427. Более того, недавно было показано, что умеренное пожизненное снижение уровней холестерина LDL в плазме по существу коррелировало со значительным снижением частоты коронарных приступов; Cohen et al., выше. Это было обнаружено даже в популяциях с высокой распространенностью факторов риска сердечно-сосудистых заболеваний, не связанных с липидами; выше.
Соответственно, огромное значение имеет идентификация терапевтического агента, обеспечивающего контроль уровней холестерина LDL.
Соответственно, огромное значение имеет изготовление лекарственного средства, которое ингибирует или противодействует активности PCSK9 и соответствующей роли, которую PCSK9 играет при различных терапевтических состояниях.
Экспрессия или повышающая регуляция PCSK9 ассоциирована с повышенными уровнями холестерина LDL в плазме, а ингибирование или отсутствие экспрессии PCSK9 ассоциировано с низкими уровнями холестерина LDL в плазме. Примечательно, что более низкие уровни холестерина LDL, ассоциированные с вариациями в последовательности PCSK9, обеспечивало защиту против заболевания коронарной артерии; Cohen, 2006 N. Engl. J. Med. 354: 1264-1272.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к иммуногену, содержащему антигенный пептид PCSK9 и возможно иммуногенный носитель.
Изобретение также относится к способам получения такого антигенного пептида PCSK9, возможно связанного с иммуногенным носителем.
Изобретение также относится к иммуногенным композициям, содержащим такой антигенный пептид PCSK9, возможно связанный с иммуногенным носителем, возможно содержащим один или несколько адъювантов, предпочтительно один или два адъюванта.
Другой аспект изобретения относится к фармацевтическим композициям, содержащим антигенный пептид PCSK9 согласно изобретению, или его иммуногенную композицию, а также к медицинским применениям таких композиций.
В частности, изобретение относится к антигенному пептиду PCSK9 по изобретению или его иммуногенной или фармацевтической композиции для применения в качестве лекарственного средства, предпочтительно для лечения, облегчения или профилактики PCSK9-связанных расстройств.
В частности, изобретение относится к антигенному пептиду PCSK9 по изобретению или его иммуногенной или фармацевтической композиции для применения в качестве лекарственного средства, предпочтительно для лечения, облегчения или профилактики заболеваний, ассоциированных с повышенным уровнем холестерина.
Антигенные пептиды PCSK9 по изобретению особенно подходят для лечения пациентов-людей, имеющих повышенный уровень холестерина LDL или состояние, ассоциированное с повышенным уровнем холестерина LDL, например, липидное расстройство (например, гиперлипидемию, гиперлипидемию I типа, II типа, III типа, IV типа или V типа, вторичную гипертриглицеридемию, гиперхолестеринемию, семейную гиперхолестеринемию, ксантоматоз, дефицит холестеринацетилтрансферазы) или подверженных риску их развития. Антигенный пептид PCSK9 по изобретению также подходит для лечения пациентов-людей, имеющих атеросклеротические состояния (например, атеросклероз), заболевание коронарной артерии, сердечно-сосудистое заболевание, и пациентов, подверженных риску развития этих расстройств, например, в связи с присутствием одного или более факторов риска (например, гипертензии, курения, диабета, ожирения или гипергомоцистеинемии).
В еще одном аспекте в настоящем изобретении предложено применение антигенного пептида PCSK9 по изобретению или его иммуногенной композиции или фармацевтической композиции в изготовлении лекарственного средства для лечения болезни Альцгеймера.
В одном из воплощений антигенный пептид PCSK9 или его иммуногенную композицию или фармацевтическую композицию вводят вместе с другим агентом.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ:
Фиг.1: Структура PDB человеческого PCSK9, связанного с доменом EGF-А LDL-R (3BPS), демонстрирующая 5 пептидных последовательностей в PCSK9 (пептид 1-5), выбранных за их причастность к взаимодействию между этими двумя белками.
Фиг.2: Мышей иммунизировали пептидами от VR_9.1 до VR_9.9, конъюгированными с VLP, используя квасцы с CpG в качестве адъюванта, и антительные ответы на полноразмерный рекомбинантный человеческий PCSK9 измеряли путем титрования сывороток в ELISA-анализе. Результаты представлены в виде реципрокных титров для каждой из 6 мышей на группу, с реципрокным титром, измеренным как разведение сыворотки, дающее оптическую плотность считывания 0,5.
Фиг.3: Антительные ответы на полноразмерный рекомбинантный мышиный белок PCSK9, как представлено на Фиг.2.
Фиг.4: Уровни холестерина в плазме измеряли в сыворотках вакцинированных мышей (в тех же образцах, которые использовали для анализов антител на Фиг.2 и 3)
Фиг.5: Образцы плазмы, используемые на Фиг.2-4, тестировали при различных разведениях на их способность ингибировать взаимодействие между рекомбинантным PCSK9 и внеклеточным доменом рецептора LDL, как измерено анализом FRET.
Фиг.6: Разведения образцов плазмы из вакцинаций пептидами VR_9 5 и VR_9.6 в анализе FRET, демонстрирующие дозозависимое ингибирование взаимодействия между PCSK9 и рецептором LDL.
Фиг.7: Комплекс PCSK9 (ленты) и EGF-A (заполненное пространство) из PDB:3BPS. Потенциальные участки PCSK9, которые могут взаимодействовать с доменами LDLR, отличными от EGF-A, показаны эллипсом.
Фиг.8: Представлен комплекс PCSK9 (ленты) и EGF-A (заполненное пространство) с аминокислотами, соответствующими пептидам VR_13/14 (А) и VR_15/16(B) и VR_9.5(C).
Фиг.9 и 10: Ответы антител в плазме у мышей, вакцинированных пептидами VR_9.5 и с VR_9.10 no VR_9.16. Антитела к мышиному PCSK9 измеряли с помощью ELISA-анализа серийных разведении плазмы с использованием полноразмерного мышиного белка PCSK9. Индивидуальные кривые титрования показаны для 8 мышей на группу, где ELISA ответы плазмы мышей, иммунизированных неконъюгированным VLP, показаны в качестве контроля.
Фиг.11: Сывороточные антительные ответы на полноразмерный человеческий белок PCSK9, индуцированные у мышей BALB/c и C57BL/6, вакцинированных либо пептидом VR_9.5, либо VR_9.10, конъюгированным с VLP (с использованием квасцов +/-CpG в качестве адъюванта), либо CRM197 (с использованием TiterMax в качестве адъюванта). Антитела к человеческому PCSK9 измеряли путем титрования сывороток в ELISA-анализе. Результаты представлены в виде log реципрокных титров, определенных при оптической плотности 1,0 для каждой из 8 мышей в группе.
Фиг.12: Сывороточные антительные ответы на полноразмерный мышиный белок PCSK9, индуцированные у мышей BALB/c и C57BL/6, вакцинированных, как описано для Фиг.11. Результаты представлены в виде log реципрокных титров, определенных при оптической плотности 0,5 для каждой из 8 мышей в группе.
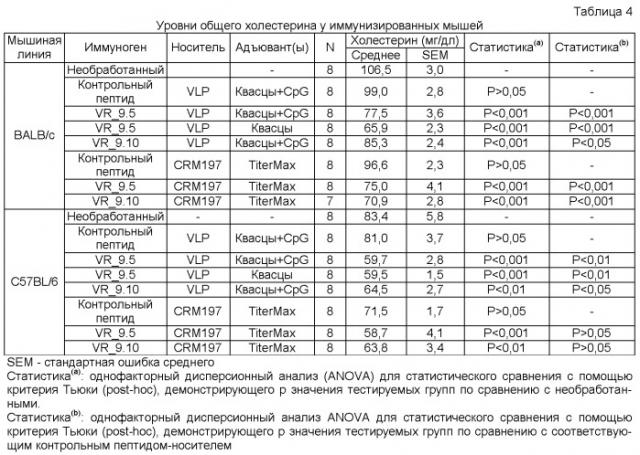
Фиг.13: Общие уровни холестерина, измеренные в образцах сыворотки у вакцинированных мышей BALB/c (те же образцы использовали для анализов антител на Фиг.11 и 12).
Фиг.14: Общие уровни холестерина, измеренные в образцах сыворотки у вакцинированных мышей C57BL/6 (те же образцы использовали для анализов антител на Фиг.11 и 12).
Фиг.15: Антительные ответы на полноразмерный человеческий PCSK9, индуцированные у мышей BALB/c, иммунизированных пептидами VR_9.5 или с VR 9.17 по VR,9.35, конъюгированными с VLP, с использованием квасцов плюс CpG в качестве адъюванта. Антитела к человеческому PCSK9 измеряли путем титрования сывороток в ELISA-анализе. Результаты представлены в виде log реципрокных титров, определенных при оптической плотности 1,0 для каждой из 8 мышей а группе.
Фиг.16: Антительные ответы на полноразмерный мышиный PCSK9, индуцированные у мышей BALB/c, иммунизированных, как описано для Фиг, 15, Антитела к мышиному PCSK9 измеряли путем титрования сывороток в ELISA-анализе. Результаты представлены в виде log реципрокных титров, определенных при оптической плотности 0,5 для каждой из 8 мышей в группе.
Фиг.17: Общие уровни холестерина, измеренные в образцах сыворотки от вакцинированных мышей BALB/c (те же образцы использовали для анализов антител на Фиг.15 и 16.
Фиг.18: Комплекс PCSK9 (ленты) и EGF-A (заполненное пространство) с участками PCSK9, содержащими аминокислотные последовательности, связанные с мутациями приобретения (gain-) или потери функции (loss-of-function) и/или поверхностными белками, экспонирующими эпитопы, указанные эллипсами.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Антигенный пептид PCSK9 по изобретению
Настоящее изобретение относится к иммуногену, содержащему антигенный пептид PCSK9, возможно связанный с иммуногенным носителем.
В одном из воплощений антигенный пептид PCSK9 представляет собой участок PCSK9, содержащий от 4 до 20 аминокислот и, при введении субъекту, способный снижать уровень LDL-холестерина в крови указанного субъекта. Предпочтительно, указанный субъект представляет собой млекопитающее, предпочтительно человека. Предпочтительно, указанный антигенный пептид PCSK9 способен снижать уровень LDL-холестерина по меньшей мере на 2%, 5%, 10%, 20%, 30% или 50%.
В одном из воплощений антигенный пептид PCSK9 представляет собой участок PCSK9, который участвует во взаимодействии PCSK9 с рецептором LDL.
В одном из воплощений антигенный пептид PCSK9 представляет собой участок PCSK9, который участвует во взаимодействии PCSK9 с рецептором LDL, содержащий от 4 до 20 аминокислот и, при введении субъекту, способный снижать уровень LDL-холестерина в крови указанного субъекта. Предпочтительно, указанный субъект представляет собой млекопитающее, предпочтительно человека. Предпочтительно, указанный антигенный пептид PCSK9 способен снижать уровень LDL-холестерина по меньшей мере на 2%, 5%, 10%, 20%, 30% или 50%.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93,, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122,123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 189, 190, 191, 192, 193, 194, 195, 196, 197, 198, 199, 200, 201, 202, 203, 204, 205, 206, 207, 208, 209, 210, 211, 212, 213, 214, 215, 216, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 283, 284, 285, 286, 287, 288, 289, 290, 291, 292, 293, 294, 295, 296, 297, 298, 299, 300, 301, 302, 303, 304, 305, 306, 307, 308, 309, 310, 311, 312, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 350, 351, 352, 353, 354, 355, 356, 357, 358, 359, 360, 361, 362, 363, 364, 365, 366, 367, 368, 369, 370, 371, 372, 373, 374, 375, 376, 377, 378, 379, 380, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 420, 421, 422, 423, 424, 425, 426, 427, 428, 429, 430, 431, 432, 433, 434, 435, 436, 437, 438, 439, 440, 441, 442, 443, 444, 445, 446, 447, 448, 449, 450, 451, 452, 453, 454, 455, 456, 457, 458, 459, 460, 461, 462, 463, 464, 465, 466, 467, 468, 469, 470, 471, 472, 473, 474, 475, 476, 477, 478, 479, 480, 481, 482, 483, 484, 485, 486, 487, 488, 489, 490, 491, 492, 493, 494, 495, 496, 497, 498, 499, 500, 501, 502, 503, 504, 505, 506, 507, 508, 509, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 549, 550, 551, 552, 553, 554, 555, 556, 557, 558, 559, 560, 561, 562, 563, 564, 565, 566, 567, 568, 569, 570, 571, 572, 573, 574, 575, 576, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587 и 588.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:1-312, 330-398, 421, 423, 424, 426 и 428-588.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 189, 190, 191, 192, 193, 194, 195, 196, 197, 198, 199, 200, 201, 202, 203, 204, 205, 206, 207, 208, 209, 210, 211, 212, 213, 214, 215, 216, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 283, 284, 285, 286, 287, 288, 289, 290, 291, 292, 293, 294, 295, 296, 297, 298, 299, 300, 301, 302, 303, 304, 305, 306, 307, 308, 309, 310, 311, 312, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 350, 351, 352, 353, 354, 355, 356, 357, 358, 359, 360, 361, 362, 363, 364, 365, 366, 367, 368, 369, 370, 371, 372, 373, 374, 375, 376, 377, 378, 379, 380, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397 и 398.
В одном из воплощений антигенный пептид PCSK9 представляет собой участок PCSK9, который может участвовать во взаимодействии с доменом EGF-A рецептора LDL. Примеры таких участков представлены на Фиг.1.
В одном из воплощений антигенный пептид PCSK9 представляет собой участок PCSK9, который может участвовать во взаимодействии с доменом EGF-A рецептора LDL, содержащий от 4 до 20 аминокислот и, при введении субъекту, способный снижать уровень LDL-холестерина в крови указанного субъекта. Предпочтительно, указанный субъект представляет собой млекопитающее, предпочтительно человека. Предпочтительно, указанный антигенный пептид PCSK9 способен снижать уровень LDL-холестерина по меньшей мере на 2%, 5%, 10%, 20%, 30% или 50%.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 13, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:1.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22. 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44 и 45.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 15, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:4S.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100 и 101.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 14, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:102.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144 145 и 146.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 13, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:147.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166,167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180 и 181.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 13, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:182.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:182, 183, 184, 185, 186, 187, 188, 189, 190, 191, 192, 193, 194, 195, 196, 197, 198, 199, 200, 201, 202, 203, 204, 205, 206,207,208, 209, 210, 211, 212, 213, 214, 215, 216, 217, 218, 219, 220, 221, 222, 223, 224, 225 и 226.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 13, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:330.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 350, 351, 352, 353, 354, 355, 356, 357, 358 и 359.
В предпочтительном воплощении антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:19, 56, 63, 109, 153, 165, 184, 186, 187, 188, 332 и 424.
В предпочтительном воплощении антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:19, 56, 63, 109, 153 и 184.
В предпочтительном воплощении антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:56, 184, 186, 187, 188 и 332.
В наиболее предпочтительном воплощении антигенный пептид PCSK9 представляет собой пептид, имеющий последовательность SEQ ID NO:56.
В более предпочтительном воплощении антигенный пептид PCSK9 представляет собой пептид, имеющий последовательность SEQ ID NO:184 или 187.
В наиболее предпочтительном воплощении антигенный пептид PCSK9 представляет собой пептид, имеющий последовательность SEQ ID NO:184.
В наиболее предпочтительном воплощении антигенный пептид PCSK9 представляет собой пептид, имеющий последовательность SEQ ID NO:332.
В одном из воплощений антигенный пептид PCSK9 выбран из участка PCSK9, который может участвовать во взаимодействии с иным, чем домен EGF-A, участком рецептора LDL. Примеры таких участков представлены на Фиг.7 и 8.
В одном из воплощений антигенный пептид PCSK9 представляет собой участок PCSK9, который может участвовать во взаимодействии с иным, чем домен EGF-A, участком рецептора LDL, содержащий от 4 до 20 аминокислот и, при введении субъекту, способный снижать уровень LDL-холестерина в крови указанного субъекта. Предпочтительно, указанный субъект представляет собой млекопитающее, предпочтительно человека. Предпочтительно, указанный антигенный пептид PCSK9 способен снижать уровень LDL-холестерина по меньшей мере на 2%, 5%, 10%, 20%, 30% или 50%.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 12, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:227.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO: 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261 и 262.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 13, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:263.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 283, 284, 285, 286, 287, 288, 289, 290, 291, 292, 293, 294, 295, 296, 297, 298, 299, 300, 301, 302, 303, 304, 305, 306 и 307.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 13, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:360.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:360, 361, 362, 363, 364, 365, 366, 367, 368, 369, 370, 371, 372, 373, 374, 375, 376, 377, 378, 379, 380, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397 и 398.
В одном из воплощений антигенный пептид PCSK9 выбран из участка продомена PCSK9 (SEQ ID NO:329).
В одном из воплощений антигенный пептид PCSK9 представляет собой участок продомена PCSK9, содержащий от 4 до 20 аминокислот и, при введении субъекту, способный снижать уровень LDL-холестерина в крови указанного субъекта. Предпочтительно, указанный субъект представляет собой млекопитающее, предпочтительно человека. Предпочтительно, указанный антигенный пептид PCSK9 способен снижать уровень LDL-холестерина по меньшей мере на 2%, 5%, 10%, 20%, 30% или 50%.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:308, 309, 310, 311 и 312.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 12, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:309.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:309, 429, 430, 431, 432, 433, 434, 435, 436, 437, 438, 439, 440, 441, 442, 443, 444, 445, 446, 447, 448, 449, 450, 451, 452, 453, 454, 455, 456, 457, 458, 459, 460, 461, 462 и 463.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 12, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:508.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:508, 509, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542 и 543.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 13, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:310.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:310, 464, 465, 466, 467, 468, 469, 470, 471, 472, 473, 474, 475, 476, 477, 478, 479, 480, 481, 482, 483, 484, 485, 486, 487, 488, 489, 490, 491, 492, 493, 494, 495, 496, 497, 498, 499, 500, 501, 502, 503, 504, 505, 506 и 507.
В одном из воплощений антигенный пептид PCSK9 представляет собой пептид, содержащий от 5 до 13, предпочтительно от 6 до 8 последовательных аминокислот фрагмента PCSK9 из SEQ ID NO:544.
В одном из воплощений антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:544, 545, 546, 547, 548, 549, 550, 551, 552, 553, 554, 555, 556, 557, 558, 559, 560, 561, 562, 563, 564, 565, 566, 567, 568, 569, 570, 571, 572, 573, 574, 575, 576, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587 и 588.
В предпочтительном воплощении антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:312, 421, 422, 423, 426, 427, 428, 445, 482, 525 и 563.
В более предпочтительном воплощении антигенный пептид PCSK9 выбран из группы, состоящей из SEQ ID NO:445, 482, 525 и 563.
В наиболее предпочтительном воплощении антигенный пептид PCSK9 представляет собой пептид, имеющий последовательность SEQ ID NO:445.
Такие антигенные пептиды PCSK9 могут быть использованы отдельно или в комбинации, предпочтительно при конъюгировании с иммуногенным носителем, для индукции аутоантител против PCSK9 у субъекта с целью лечения, предупреждения или облегчения PCSK9-связанных расстройств.
Специалисту в данной области техники очевидно, какие методы могут быть использованы для подтверждения того, подпадает ли конкретная конструкция под объем настоящего изобретения. Такие методы включают, но не ограничиваются этим, методы, описанные в разделе Примеров настоящей заявки, а также следующее.
Способность антигенного пептида PCSK9 по изобретению индуцировать аутоантитела против PCSK9 можно измерять у мышей, используя тест, описанный в примере 3 настоящей заявки. Способность аутоантител, индуцированных антигенным пептидом PCSK9 по изобретению, уменьшать уровень циркулирующего в плазме холестерина можно измерять у мышей, используя тест, описанный в примере 3. Способность аутоантител, индуцированных антигенным пептидом PCSK9 по изобретению, ингибировать взаимодействие между PCSK9 и рецепторами LDL можно измерять непосредственно, используя тест, описанный в примере 3 (анализ FRET (резонансный перенос энергии флуоресценции)), или опосредованно путем измерения повышающей регуляции рецепторов LDL клеточной поверхности, которая является следствием блокирования PCSK9-опосредованной понижающей регуляции (а также описанной в релевантной литературе либо с использованием клеточных линий in vitro, либо путем измерения уровней рецепторов LDL в биопсиях печени животных, экспрессирующих антитела (например, посредством Вестерн-блоттинга)).
Термин "биологическая активность антигенного пептида PCSK9", при использовании в данной заявке, относится к способности антигенных пептидов PCSK9 по изобретению индуцировать аутоантитела против PCSK9 у пациента.
Предпочтительно, указанный антигенный пептид PCSK9 при введении субъекту, способен снижать уровень LDL-холестерина в крови указанного субъекта. Предпочтительно, указанный субъект представляет собой млекопитающее, предпочтительно человека. Предпочтительно, указанный антигенный пептид PCSK9 способен снижать уровень LDL-холестерина по меньшей мере на 2%, 5%, 10%, 20%, 30% или 50%.
В одном из воплощений антигенные пептиды PCSK9 по настоящему изобретениию имеют такой размер, что они имитируют участок, выбранный из полного домена PCSK9, в котором обнаружен нативный эпитоп. В конкретном воплощении антигенные пептиды PCSK9 по изобретению имеют длину менее 100 аминокислот, предпочтительно менее 75 аминокислот, более предпочтительно менее 50 аминокислот, еще более предпочтительно менее 40 аминокислот.Антигенные пептиды PCSK9 по изобретению имеют длину обычно 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 аминокислот, предпочтительно от 4 до 20 аминокислот, например, от 6 до 12, от 6 до 8 или от 9 до 12 аминокислот.
Конкретные примеры антигенных пептидов PCSK9 по изобретению предложены в перечне последовательностей и включают пептиды длиной от 5 до 17 аминокислот.
Антигенные пептиды по изобретению включают аминокислотную последовательность, происходящую из участка PCSK9 млекопитающего, предпочтительно PCSK9 человека (SEQ ID NO:399) или PCSK9 мыши (SEQ ID NO:400), более предпочтительно PCSK9 человека, такой происходящий участок PCSK9 либо соответствует аминокислотной последовательности встречающегося в природе PCSK9, либо соответствуют варианту PCSK9, т.е. аминокислотной последовательности встречающегося в природе PCSK9, в которой небольшое число аминокислот было замещено, добавлено или делетировано, но которая сохраняет по существу такие же иммунологические свойства. Кроме того, такой происходящий участок PCSK9 может быть дополнительно модифицирован с помощью аминокислот, особенно на N- и С-концах. для обеспечения конформационного ограничения антигенного пептида PCSK9 и/или для обеспечения связывания антигенного пептида PCSK9 с иммуногенным носителем после проведения соответствующей химии.
Антигенные пептиды PCSK9, описанные в данной заявке, охватывают функционально активные варианты пептидов, происходящие из аминокислотной последовательности PCSK9, в которой аминокислоты были делегированы, вставлены или заменены без существенного уменьшения их иммунологических свойств, т.е. такие функционально активные варианты пептидов сохраняют значительную биологическую активность антигенного пептида PCSK9. Как правило, такие функционально активные варианты пептидов имеют аминокислотную последовательность, гомологичную, предпочтительно высоко гомологичную, аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO:1-312, 330-398 и 420-588.
В одном из воплощений такие функционально активные варианты пептидов демонстрируют по меньшей мере 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95%-ную идентичность с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO:1-312, 330-398 и 420-588.
Сходство последовательностей полипептидов, которую также называют идентичностью последовательностей, обычно измеряют с использованием программного обеспечения для анализа последовательностей. Программное обеспечение для анализа белка выравнивает сходные последовательности с использованием критериев сходства, относящихся к различным заменам, делециям и другим модификациям, включая консервативные аминокислотные замены. Например, GCG содержит такие программы, как "Gap" и "Bestfit", которые можно использовать с параметрами по умолчанию для определения гомологии последовательностей или идентичности последовательностей между близкородственными полипептидами, такими как гомологичные полипептиды из организмов различных видов, или между белком дикого типа и его мутеином. См., например, GCG версию 6.1. Полипептидные последовательности также можно сравнивать с использованием FASTA. применяя параметры по умолчанию или рекомендованные параметры, программа GCG версии 6.1. FASTA (например, FASTA2 и FASTA3) обеспечивает выравнивания и процентную идентичность последовательностей областей с наилучшим перекрыванием между запросными и поисковыми последовательностями (Pearson, Methods Enzymol. 183:63-98 (1990); Pearson, Methods Mol. Biol. 132:185-219 (2000)). Альтернативный алгоритм при сравнении последовательности по изобретению с базой данных, содержащей большое количество последовательностей из различных организмов, представляет собой компьютерную программу BLAST, особенно blastp или tbiastn с использованием параметров по умолчанию. См., например, Altschul et al., J. Mol. Biol. 215:403-410 (1990); Altschu! et al., Nucleic Acids Res. 25:3389-402 (1997).
Функционально активные варианты содержат встречающиеся в природе функционально активные варианты, такие как аллельные варианты и видовые варианты и не встречающиеся в природе функционально активные варианты, которые могут быть получены, например, методами мутагенеза или прямым синтезом.
Функционально активный вариант отличается от любого из пептидов, представленных в SEQ ID NO:1-312, 330-398 и 420-588, примерно на, например, 1, 2, 3, 4 или 5 аминокислотных остатков и все же сохраняет биологическую активность антигенного PCSK9. Если это сравнение требует выравнивания, то последовательности выравнивают с максимальной гомологией. Сайт вариации может быть представлен в любом месте пептида, пока биологическая активность по существу сходна с пептидом, представленным в SEQ ID NO:1-312, 330-398 и 420-588.
Руководство относительно того, как сделать фенотипически молчащие аминокислотные замены, представлено в Bowie et al., Science, 247: 1306-1310 (1990), которое учит, что существуют две основные стратегии исследования устойчивости аминокислотной последовательности к изменению.
Первая стратегия использует устойчивость к аминокислотным заменам в ходе естественного отбора в процессе эволюции. При сравнении аминокислотных последовательностей в различных видах можно идентифицировать аминокислотные положения, которые были консервативными между видами. Эти консервативные аминокислоты, по-видимому, важны для функции белка. В огличие от этого, аминокислотные положения, в которых замены были допущены естественным отбором, указывают на положения, которые не являются критичными для функции белка. Таким образом, положения, допускающие аминокислотную замену, можно модифицировать, сохраняя при этом специфическую иммуногенную активность модифицированного пептида.
Вторая стратегия использует генную инженерию для введения аминокислотных изменений по конкретным положениям клонированного гена для идентификации участков, критичных для функции белка. Например, можно использовать сайт-направленный мутагенез или аланин-сканирующий мутагенез (Cunningham et al., Science, 244: 1081-1085 (1989). Полученные варианты пептидов затем можно тестировать в отношении специфической биологической активности антигенного PCSK9.
Согласно Bowie и др., эти две стратегии обнаружили, что белки являются неожиданно устойчивыми к аминокислотным заменам. Авторы также указывают, какие аминокислотные изменения, по-видимому, являются допустимыми в некоторых аминокислотных положениях в белке. Например, наиболее замаскированные или внутренние (в третичной структуре белка) аминокислотные остатки требуют неполярных боковых цепей, тогда как некоторые признаки поверхностных или наружных боковых цепей обычно являются консервативными.
Спосбы введения мутации в аминокислоты белка хорошо известны специалистам в данной области См., например, Ausubel (ed.), Current Protocols in Molecular Biology, John Wiley and Sons, Inc. (1994); Т.Maniatis, E.F.Fritsch and J.Sambrook, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor laboratory, Cold Spring Harbor, N.Y. (1989)).
Мутации также можно вводить с использованием имеющихся в продаже наборов, таких как "QuikChangeTM Site-Directed Mutagenesis Kit" (Stratagene), или непосредственно пептидным синтезом. Получение функционально активного варианта для антигенного пептида PCSK9 путем замены аминокислоты, которая по существу не влияет на функцию указанного антигенного пептида PCSK9, может быть выполнено специалистом в данной области техники.
Тип аминокислотной замены, который можно сделать в одном из пептидов согласно изобретению, представляет собой консервативную аминокислотную замену. "Консервативная аминокислотная замена" представляет собой замену, в которой аминокислотный остаток заменен другим аминокислотным остатком, имеющим группу боковой цепи R) со сходными химическими свойствами (например, зарядом или гидрофобностью). В общем, консервативная аминокислотная замена по существу не изменяет функциональные свойства белка. В тех случаях, когда две или более аминокислотных последовательностей отличаются друг от друга консервативными заменами, процент идентичности последовательностей или степень сходства можно корректировать в сторону увеличения для корректировки консервативной природы замены. Способы осуществления такой корректировки хорошо известны специалистам в данной области техники. См., например, Pearson, Methods Mol. Biol. 243:307-31 (1994).
Примеры групп аминокислот, которые имеют боковые цепи со сходными химическими свойствами, включают 1) алифатические боковые цепи: глицин, эланин, валин, лейцин и изолейцин; 2) элифатические гидроксильные боковые цепи: серин и треонин; 3) амид-содержащие боковые цепи: аспарагин и глутамин; 4) ароматические боковые цепи: фенилаланин, тирозин и триптофан; 5) основные боковые цепи: лизин, аргинин и гистидин; 6) кислотные боковые цепи: аспарагиновая кислота и глутаминовая кислота; и 7) серосодержащие боковые цепи: цистеин и метионин. Предпочтительные группы для консервативных аминокислотных замен представляют собой: валин-лейцин-изолейцин, фенилаланин-тирозин, лизин-аргинин, аланин-валин, глутамат-аспартат и аспарагин-глутамин.
Альтернативно, консервативная замена представляет собой любое изменение, имеющее положительное значение в РАМ250 матрице логарифмического правдоподобия (log-likelihood matrix), описанной в Gonnet et al., Science 256:1443-45 (1992). "Умеренно консервативная" замена представляет собой любое изменение, имеющее неотрицательное значение в РАМ250 матрице логарифмического правдоподобия.
Функционально активный вариант пептида также может быть выделен с использованием метода гибридизации. Кратко, ДНК, имеющую высокую гомологию со всей или с частью последовательности нуклеиновой кислоты, кодирующей интресующий пептид, например SEQ ID NO:1-312, 330-398 и 420-588, используют для получения функционально активного пептида. Поэтому антигенный пептид PCSK9 по изобретению также включает пептиды, которые функционально эквивалентны одному или более чем одному из пептидов SEQ ID NO:1-312, 330-398 и 420-588 и которые кодируются молекулой нуклеиновой кислоты, которая гибридизуется с нуклеиновой кислотой, кодирующей любую из SEQ ID NO:1-312, 330-398 и 420-588 или ее комплементом. Специалист в данной области может легко определить последова