Наносоединения платины и способы их применения
Иллюстрации
Показать всеИзобретение относится к биосовместимой конъюгированной полимерной наночастице, дикарбонил-липидному соединению, соединению в виде везикул, мицелл или липосом, содержащих множество наночастиц, включающих указанное дикарбонил-липидное соединение, способу лечения рака или метастаз, биосовместимому полимеру, а также к конъюгату. Биосовместимая конъюгированная полимерная наночастица включает основную цепь сополимера, причем по меньшей мере один мономер полимера содержит две боковые цепи, выбранные из группы, состоящей из карбоновой кислоты, амида и сложного эфира, и указанные боковые цепи отделены друг от друга 1-10 атомами углерода, атомами кислорода или атомами серы, или любыми их комбинациями. Далее вышеуказанная наночастица содержит множество боковых цепей, ковалентно связанных с указанной основной цепью, причем указанные боковые цепи выбраны из группы, состоящей из моносахаридов, дикарбоновых кислот, полиэтиленгликоля и их комбинаций; и множество соединений платины, диссоциируемо связанных с указанной основной цепью. Множество соединений платины связано с указанной основной цепью через по меньшей мере одну координационную связь между карбонильным кислородом карбонильной или амидной группы основной цепи и атомом платины соединения платины. Указанное соединение платины выбрано из соединений Pt(II), соединений Pt (IV) и любых их комбинаций. Также изобретение направлено на дикарбонил-липидные соединения, в которых соединение платины диссоциируемо связано с дикарбонильным соединением. Изобретение также направлено на способы лечения рака и метастаз. Способы включают отбор субъекта, нуждающегося в лечении рака или метастаз, и введение субъекту эффективного количества наночастиц, соединений или композиций изобретения. Технический результат - получение биосовместимых конъюгированных полимерных наночастиц для химиотерапевтического средства на основе платины. 7 н. и 33 з.п. ф-лы, 1 табл., 29 ил., 12 пр.
Реферат
По настоящей заявке испрашивается приоритет и преимущество согласно 35 U.S.С. 119(е) Американской предварительной заявки 61/149,725, поданной 4 февраля 2009 года и 61/240,007, поданной 4 сентября 2009 года, содержание которых во всей своей полноте вводится в настоящее описание посредством ссылки.
Настоящее изобретение осуществлено по гранту «Era of Hope Scholar Award» от Министерства обороны США с номером W81XWH-07-1-0482 и гранду «Postdoctoral Award» от Министерства обороны США с номером W81XWH-09-1-0728. Правительство США имеет определенные права на данное изобретение.
Область техники, к которой относится изобретение
Настоящее изобретение относится к биосовместимым конъюгированным полимерным наночастицам, включающим основную цепь сополимера, множество боковых цепей, ковалентно связанных с основной цепью, и множество соединений платины, диссоциируемо связанных с основной цепью.
Уровень техники
Рак является второй ведущей причиной смертности в США с прогнозируемыми 1444180 новыми случаями и 565650 смертельными исходами в 2008 году. Цитотоксические средства, которые применяются в стандартной химиотерапии, неизбирательно воздействуют на любые клетки, находящиеся в процессе деления, что вызывает дозолимитирующие токсические эффекты. Существует острая потребность в развитии новых стратегий, более избирательно воздействующих на опухоль.
Применение нановекторов содержит в себе потенциал для качественного изменения химиотерапии раковых заболеваний путем избирательного воздействия на опухоль. Ряд полимерных нановекторов находятся в настоящее время в разработке или на стадии клинических испытаний, и сильно изменяют фармакодинамический и фармакокинетический профиль активного агента. Однако большинство этих полимерных структур снижают эффективность конъюгированного активного агента, основанную на увеличении поглощения опухолью для повышения терапевтического индекса.
Цисплатин является одним из основных направлений в режимах химиотерапии для большинства видов рака (Kelland L. The resurgence of platinum-based cancer chemotherapy. Nat Rev Cancer. 2007 Aug; 7(8):573-84). Однако его применение ограничено из-за сильной нефротоксичности. К тому же нановекторный состав на основе цисплатина, являющегося терапией первой линии для многих видов рака, представляет собой проблему, требующую усилий.
Раскрытие изобретения
Представлено рациональное конструирование полимерной структуры для химиотерапевтического средства на основе платины, такого как цисплатин и оксалиплатин, которая вызывает самосборку в наночастицу. Наночастица поддерживает эффективность активного агента и по сравнению с цисплатином, или оксалиплатином, или карбоплатином оказывает повышенное противоопухолевое действие с пониженной системной и нефротоксичностью при внутривенном введении мышам, несущим опухоль. Данное повышение терапевтического индекса цисплатина или оксалиплатина, возможное благодаря нанотехнологии, может быть использовано для применения наноплатинатов в клиническом лечении многих видов рака.
Изобретение направлено на биосовместимую конъюгированную полимерную наночастицу, включающую основную цепь сополимера, множество боковых цепей, ковалентно связанных с указанной основной цепью, и множество соединений платины, диссоциируемо связанных с указанной основной цепью. В целом, соединение платины диссоциируемо связано с основной цепью посредством связи через боковую цепь. В некоторых вариантах соединение платины связано с боковой цепью, по меньшей мере, через одну координационную связь.
Другой аспект изобретения направлен на биосовместимые конъюгированные полимерные наночастицы, включающие основную цепь полималеиновой кислоты (РМА), такую как основная цепь поли(изобутилен-alt-малеиновой кислоты) (PIMA). Основная цепь включает от 25 до 50 мономеров. Также включенными являются множество боковых цепей PEG, ковалентно связанных с указанной основной цепью. Боковые цепи PEG имеют молекулярную массу от 200 до 3000 дальтон. Количество боковых цепей PEG составляет от 50% до 100% включительно количества мономерных звеньев основной цепи полимера. Также включенными являются множество боковых групп цисплатина или оксалиплатина, диссоциируемо связанных с основной цепью. Количество боковых групп цисплатина составляет от 25% до 75% включительно количества мономерных звеньев основной цепи полимера.
Еще другой аспект изобретения направлен на биосовместимые конъюгированные полимерные наночастицы, включающие основную цепь поли(изобутилен-alt-малеиновой кислоты). Основная цепь состоит примерно из 40 мономеров. Также включенными являются множество боковых цепей PEG, ковалентно связанных с основной цепью. Боковые цепи PEG имеют молекулярную массу примерно 2000 дальтон. Количество боковых цепей PEG больше чем 90% мономерных звеньев указанной основной цепи полимера. Также включенными являются множество боковых групп цисплатина или оксалиплатина, диссоциируемо связанных с основной цепью. Количество боковых групп цисплатина или оксалиплатина составляет от 25% до 75% включительно количества мономерных звеньев основной цепи полимера.
Еще другой аспект изобретения направлен на биосовместимые конъюгированные полимерные наночастицы, включающие основную цепь поли(изобутилен-alt-малеиновой кислоты). Основная цепь включает от 25 до 50 мономеров. Также включенными являются множество боковых цепей глюкозамина, ковалентно связанных с указанной основной цепью. Количество боковых цепей глюкозамина составляет от 50% до 100% включительно мономерных звеньев указанной основной цепи полимера. Также включенными являются множество боковых групп цисплатина или оксалиплатина, диссоциируемо связанных с основной цепью. Количество боковых групп цисплатина или оксалиплатина составляет от 25% до 75% включительно количество мономерных звеньев основной цепи полимера.
Другой аспект изобретения направлен на биосовместимые конъюгированные полимерные наночастицы, включающие основную цепь поли(изобутилен-alt-малеиновой кислоты). Основная цепь содержит от 25 до 50 мономеров. Также включенными являются множество боковых цепей глюкозамина, ковалентно связанных с указанной основной цепью. Количество боковых цепей глюкозамина больше чем 75% мономерных звеньев указанной основной цепи полимера. Также включенными являются множество боковых групп цисплатина или оксалиплатина, диссоциируемо связанных с основной цепью. Количество боковых групп цисплатина или оксалиплатина составляет от 25% до 75% включительно количества мономерных звеньев основной цепи полимера.
Еще другой аспект изобретения направлен на наночастицы, конъюгированные с комплексом карбоновая кислота-платина II (Pt(II)), включающие комплекс карбоновая кислота-(Pt(II)) и множество липид-полимерных цепей. Карбоновая часть указанного комплекса карбоновая кислота-цисплатин/оксалиплатин является ковалентно связанной с указанными липид-полимерными цепями.
Другой аспект изобретения направлен на везикулярное, мицеллярное или липосомное соединение, включающее множество наночастиц формулы, как описано здесь.
Еще другой аспект изобретения направлен на фармацевтические композиции, включающие любые наночастицы или соединения, описанные здесь, и фармацевтически приемлемый носитель.
Еще другой аспект изобретения направлен на способ лечения рака или метастаз. Способ включает выбор субъекта, нуждающегося в лечении рака или метастаз, и введение субъекту эффективного количества любых наночастиц, соединений или композиций, описанных здесь.
Перечень фигур
Фигура 1 представляет схему синтеза РМА-Цисплатин. Нагрузка разного количества цисплатина на полимер влияет на размер наночастиц, как измерено методом DLS или ТЕМ. Показан график исследования цитотоксичности носителя полиизобутилен-малеиновой кислоты (PIMA) 2 и конъюгата (Р1МА-ЦИСПЛАТИН) (6).
Фигура 2 показывает схему дериватизации РМА с помощью EDA. Дериватизированный полимер использовали для синтеза комплекса цисплатина. График показывает действие разных обработок на жизнеспособность клеток LLC через 48 часов инкубирования.
Фигура 3 показывает схему синтеза PMA-GA-Цисплатин. Образование комплекса с цисплатином проводили в течение 48 часов. Это вызвало образование наночастиц с размером в диапазоне примерно 100 нм, как видно из измерений DLS.
Фигура 4. График слева показывает количество активного цисплатина, который высвобождается из наночастицы PMA-GA-Цисплатин при инкубировании с лизатом LLC. График справа «концентрация-эффект» показывает действие разных обработок на жизнеспособность клеток карциномы легкого Льюис при инкубировании с активными агентами в течение 48 часов. Жизнеспособность клеток измеряли с помощью MTS анализа.
Фигуры 5А-5Е являются линейными графиками (Фиг.5А и 5В) и гистограммами (Фиг.5С-5Е), показывающими эффективность и профиль токсичности свободного цисплатина и наночастицы цисплатина в модели карциномы легкого Льюис. Опухоли индуцировали путем инъекции клеток LLC мышам c57/BL6. Показано действие обработок на объем опухоли (Фиг.15А) и массу тела (Фиг.5В) в течение периода обработки. Животным трижды вводили дозу (показано стрелками на оси X). Данные представлены как среднее±станд.откл., n=4-8. Также показано действие обработки на массу почек (Фиг.5С) и селезенки (Фиг.5D) как маркер нефротоксичности и гематологической токсичности (n=4-6). Изображения в верхней части каждого графика показывают иллюстративные органы от каждой обрабатываемой группы. Фиг.5Е показывает биораспределение Pt в почках и опухоли, измеренное с использованием ICP-спектроскопии через 24 ч после ведения свободного цисплатина или наночастиц цисплатина (доза цисплатина 8 мг/кг).
Фигура 6 представляет собой схему, показывающую синтез PMA-GA-Цисплатин (8).
Фигура 7. Действие PMA-GA-Цисплатин на карциному легкого Льюис. Клетки инкубировали в течение 48 часов с лекарственными средствами или носителями и затем тестировали на жизнеспособность с использованием MTS анализа.
Фигура 8. Действие разных обработок на рост опухоли и массу тела in vivo. Опухоли индуцировали путем инъекции LLC клеток мышам c57/BL6.
Фигура 9 представляет собой график количества платины, нагруженной в полимер, которое было рассчитано с использованием метода UV-VIS спектроскопии.
Фигура 10. Схема, показывающая синтез липидного комплекса малеиновая кислота-цисплатин, который может образовывать мицеллы в воде.
Фигуры 11А и 11В являются схемами, показывающими конструирование наночастицы цисплатина на основе SAR. Фиг.11А показывает механизм, лежащий в основе внутриклеточной активации цисплатина посредством гидратирования. Уходящие группы цисплатина и аналогов (показано синими линиями) заменены ОН до ДНК-связывания. Фиг.11В показывает химический синтез PIMA-цисплатин и комплекса PIMA-глюкозамин (PIMA-GA)-цисплатин. Трансформация полималеинового ангидрида (n=40) (I) в полималеиновую кислоту [PIMA] (2) делает возможным комплексообразование [NH2]2Pt[OH]2 через дикарбоксилато связь (6). Дериватизация одного фрагмента PIMA глюкозамином (4) и образование комплекса с [NH2]2Pt[OH]2 может привести к образованию двух изомеров (8) и (10), в зависимости от рН, характеризующихся уникальными ЯМР спектрами Pt (Фиг.11В).
Фигуры 12А и 12В представляют характеристику наночастиц цисплатина. Повышение количества Pt на основной цепи PIMA (n=40) увеличивает размер образующейся наночастицы. При оптимальном соотношении Pt к полимеру авторы изобретения получили наночастицы меньше чем 150 нм, размер отсечен ниже, что делает возможным преимущественный хоминг в опухоли. На Фиг.12А показано, что при дериватизации всех мономерных звеньев PIMA глюкозамином и последовательном комплексообразовании с Pt образуются наночастицы меньше чем 150 нм. На Фиг.12В показано общее количество платины, нагруженное на мг полимера при данном соотношении.
Фиг.13А-13Е представляют собой линейные графики, показывающие in vitro характеристику наночастиц цисплатина. На Фиг.13А и 13В показана зависимость «концентрация-эффект» разных обработок на жизнеспособность клеток, как измерено с использованием MTS анализа. Ось Х показывает эквивалентные концентрации цисплатина. При использовании полимерных контролей доза используемого полимера была эквивалентна дозе, которую использовали для доставки этой конкретной дозы цисплатина в комплексную форму. PIMA также был дериватизирован этилендиамином для образования PIMA-EDA, что обеспечивает среду для образования комплекса с платиной, аналогичную PIMA-GA. В отличие от PIMA-GA, PIMA-EDA проявляет внутреннюю токсичность. PIMA-GA-Цисплатин [кислый] относится к изомеру, образованному в кислой среде комплексообразования, в то время как PIMA-GA-Цисплатин [щелочной] относится к изомеру, образованному в щелочной среде. На Фиг.13С-13Е показано действие наночастиц PIMA-GA-Цисплатин на жизнеспособность LLC клеток, когда основная цепь PIMA (40 мономерных звеньев) является дериватизированной до разной степени. PIMA-GA-Цисплатин содержит 30 из 40 мономерных звеньев, дериватизированных глюкозамином, в то время как все мономерные звенья PIMA-GA-40 и PIMA-GA-200 являются дериватизированными. [а] и [b] относятся к изомерам, образованным в кислой и щелочной средах, когда полимеры образуют комплекс с цисплатином. В Таблице 1 представлены соответствующие значения IC50.
Фигуры 14A-14J представляют FACS изображения (Фиг.14А-14Н) и гистограммы (Фиг.14I и 14J), на которых показано, что обработка PIMA-GA-Цисплатин индуцирует гибель клеток. Иллюстративные FACS изображения клеток 4Т1 (Фиг.14A-14D) и LLC (Фиг.14Е-14Н) показывают процент в каждом квадранте после обработок свободным цисплатином или наночастицами цисплатина. Карбоплатин использовали в качестве контроля для сравнения (Фиг.14D и 14Н). Клетки инкубировали с лекарственными средствами в течение 24 ч, после чего метили Annexin-V FITC и окрашивали пропидиум иодидом.
Фигура 15 представляет собой схему, показывающую мечение полимера PIMA-GA с помощью FITC для отслеживания клеточного поглощения наночастиц.
Фигура 16 представляет собой линейный график, показывающий действие рН и среды комплексообразования Pt на кинетику высвобождения. Наночастицы инкубировали при рН 5.5 или рН 8.5 в диализном мешке и количественно определяли высвобождение в динамике по времени. Использующиеся наночастицы [PIMAGA-Цисплатин (O->Pt)] были генерированы путем образования комплекса полимера и цисплатина в условиях кислого рН [6.4], за исключением PIMA-GA-Цисплатин (Pt->N), когда образование комплекса проходило в условиях щелочного рН с образованием стабильного изомера [PIMA-GA-Цисплатин (N->Pt)]. Данные представлены как среднее±станд. откл. от n=3.
Фигуры 17A-17D представляют собой линейные графики (Фиг.17А и 17 В) и гистограммы (Фиг.17С и 17D), на которых показано, что наночастицы PIMA-GA-цисплатин проявляют сходное противоопухолевое действие с пониженной системной токсичностью по сравнению со свободным цисплатином в модели рака молочной железы 4Т1. Линейные графики показывают действие обработок на объем опухоли (Фиг.17А) и массу тела (Фиг.17В) в течение периода обработки. Животным трижды вводили дозу (показано стрелками на оси X). Данные представлены как среднее±станд. откл., n=4-8. Гистограммы показывают действие обработки на массу селезенки (Фиг.18С) и почек (Фиг.17D) как маркер нефротоксичности и гематологической токсичности (n=4-6)*Р<0.05 в сравнении с группой, обработанной носителем [ANOVA с последующим апостериорным сравнением по критерию Ньюмана Кеулса]. Карбоплатин [3 мг/кг] использовали в качестве контроля.
Фигуры 18А и 18В представляют собой гистограмму (Фиг.18А) и линейный график (Фиг.18В), на которых показано ингибирование наночастицами PIMA-GA-цисплатин роста опухоли в модели K-rasLSL/PtenfI/fI рака яичников. Как видно на Фиг.18А, количественная оценка биолюминесценции показала значительно уменьшенный сигнал от люциферазы опухоли мышей, обработанных наночастицей цисплатина по сравнению с носителем (р<0.05, однофакторный дисперсионный анализ ANOVA). На Фиг.18В показана токсичность лекарственного средства, оцененная путем измерения общей массы тела. Ежедневные записи массы тела показали значительную потерю массы тела в группе, обработанной свободным цисплатином по сравнению с обеими группами, обработанными наночастицей цисплатина (1.25 мг/кг и 3 мг/кг) (Р<0.05, двухфакторный дисперсионный анализ ANOVA).
Фигуры 19А и 19 В представляют собой гистограммы, на которых показано распределение Pt после введения цисплатина, наночастиц цисплатина [PIMA-GA-Цисплатина (O->Pt)] или карбоплатина в раке молочной железы или раке яичников. Обработки проводили, как описано на Фиг.17 и 18. Уровень Pt в разных тканях, взятых после вскрытия, количественно оценивали методом масс-спектрометрии с индуктивно связанной плазмой (ICP).
Фигуры 20А и 20В представляют собой схемы, на которых показан SAR-инспирированный конструирование наночастицы оксалиплатина. На Фигуре 20А показан механизм, лежащий в основе внутриклеточной активации оксалиплатина посредством гидратирования. На Фигуре 20В показан химический синтез комплекса PIMA- оксалиплатин и PIMA-глюкозамин (PIMA-GA)-оксалиплатин. Оксалиплатин-ОН может образовывать комплекс с PIMA посредством дикарбоксилато связей. Дериватизация одного фрагмента PIMA глюкозамином и образование комплекса с оксалиплатином могут привести к образованию двух изомеров в зависимости от рН.
Фигуры 21А и 21В представляют собой линейные графики, на которых показана зависимость «концентрация-эффект» разных обработок на жизнеспособность клеток, как измерено с помощью MTS анализа. Для этого исследования использовали клеточную линию рака молочной железы, клеточные линии рака легкого Льюис (Фиг.21А) и 4Т1 (Фиг.21В). Ось Х показывает эквивалентные концентрации платины. При использовании полимерных контролей доза полимера была эквивалентна дозе, которую использовали для доставки данной конкретной дозы оксалиплатина в комплексную форму. PIMA-GA-ox относится к изомеру [PIMA-GA-Оксалиплатин (O->Pt)], образованному в кислой среде комплексообразования. Кривая PIMA-GA-оксалиплатин сдвинута влево, что указывает на более высокую эффективность наночастиц в отношении противоопухолевой активности по сравнению со свободным оксалиплатином.
Фигуры 22А-22Е представляют собой линейные графики (Фиг.26А и 26В) и гистограммы (Фиг.22С-22Е), на которых показано, что наночастицы PIMA-GA-оксалиплатин проявляют аналогичный противоопухолевый эффект с уменьшенной системной токсичностью по сравнению со свободным оксалиплатином в модели рака молочной железы 4Т1. Линейные графики показывают действие обработок на объем опухоли (Фиг.22А) и массу тела (Фиг.22 В) в течение периода обработки. Животным вводили дозу три раза. Данные представлены как среднее±станд. откл., n=4-8. Гистограммы показывают действие обработки на массу опухоли (Фиг.22С), почек (Фиг.22D) и селезенки (Фиг.22Е) как маркер нефротоксичности и гематологической токсичности (n=4-6).
Фигура 23 является линейным графиком, на котором показана завсимость «концентрация-эффект» разных комплексов оксалиплатина на жизнеспособность клеток, как измерено с помощью MTS анализа.
Фигура 24 является линейным графиком, на котором показано действие цисплатина, карбоплатина и PIMA-GA-200(A) на жизнеспособность клеток.
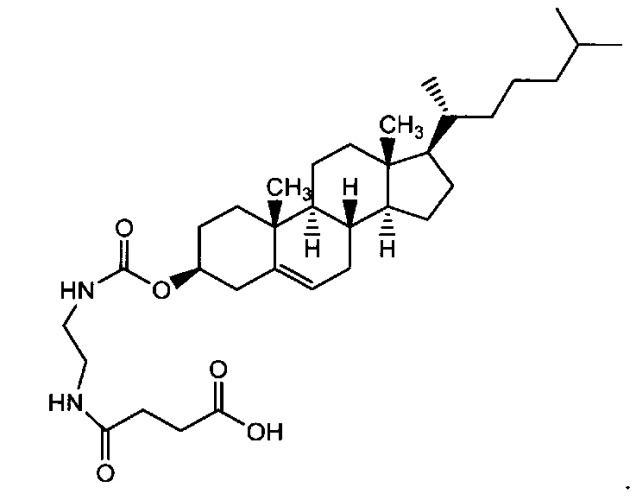
Фигура 25А является схемой, на которой показан синтез конъюгата холестерин-янтарная кислота и образование комплекса Pt с конъюгатом.
Фигура 25В показывает динамическое рассеяние лазерного излучения липонаночастиц. Размер липонаночастиц составляет меньше чем 150 нм.
Фигура 26 является линейным графиком, показывающим кинетику высвобождения Pt из липонаночастицы с течением времени и влияние рН. Скорость высвобождения выше в условиях кислого рН, соответствующего кислому рН внутри опухоли, что способствует селективному высвобождению активного платината в опухоли.
Фигуры 27А-27С представляют собой линейные графики, на которых показано действие липонаночастицы цисплатина на жизнеспособность клеток 4Т1 рака молочной железы. Выживаемость клеток измеряли при помощи MTS анализа. Обработка липонаночастицами привела к быстрой гибели клеток в течение 12 часов по сравнению с цисплатином или карбоплатином (Фиг.27А). Было обнаружено, что во все три момента времени липонаночастица цисплатина была более эффективной, чем цисплатин. Карбоплатин является наименее эффективным из всех тестированных платинатов (Фиг.27А-27С).
Фигуры 28А и 28В представляют собой линейные графики, на которых показано действие липонаночастицы цисплатина на жизнеспособность устойчивой к цисплатину линии клеток (СР20) гепатоцеллюлярного рака и линии клеток рака легкого Льюис (LLC). Цисплатин действует на СР20 только при самой высокой концентрации, тогда как клетки являются восприимчивыми к липонаночастице цисплатина (Фиг.28А). Карбоплатин не оказывает действия в этом диапазоне концентраций (Фиг.28А и 28В). Липонаночастица цисплатина показала противораковый эффект выше, чем свободный цисплатин на LLC (Фиг.28В).
Фигуры 29А-29Е представляют собой линейные графики (Фиг.29А и 29В) и гистограммы (Фиг.29С-29Е), на которых показана эффективность липонаночастицы цисплатина в синергической модели опухоли 4Е1 in vivo. Линейные графики показывают действие разных обработок на рост опухоли (Фиг.29А и 29С) и массу тела (как маркер системной токсичности, Фиг.29В). Гистограммы показывают массу почки (Фиг.29D) и селезенки (Фиг.29Е) как маркеры нефротоксичности и гематологической токсичности. Как видно из фигур, липонаночастица цисплатина индуцировала большую противоопухолевую активность при пониженной системной и нефротоксичности.
Осуществление изобретения
Изобретение направлено на биосовместимые конъюгированные полимерные наночастицы, включающие основную цепь сополимера, множество боковых цепей, ковалентно связанных с указанной основной цепью, и множество соединений платины, диссоциируемо связанных с указанной основной цепью. В целом, соединения платины связаны с основной цепью посредством связи с боковыми цепями.
В одном варианте сополимер включает мономеры малеиновой кислоты.
В предпочтительном варианте сополимер представляет собой поли(изобутилен-alt-малеиновую кислоту) (PIMA или РМА).
В некоторых вариантах сополимер содержит от 2 до 100 мономерных звеньев. В некоторых вариантах сополимер содержит от 25 до 50 мономерных звеньев.
В некоторых вариантах боковые цепи являются выбранными из группы, состоящей из полимеров, моносахаридов, карбоновых кислот, дикарбоновых кислот, амидов и их комбинаций.
В предпочтительных вариантах боковые цепи представляет собой полиэтиленгликоль (PEG). Боковые цепи PEG могут быть представлены формулой -C(O)-NH-PEG.
В некоторых вариантах боковые цепи PEG имеют молекулярную массу от 100 до 5000 дальтон. В некоторых вариантах боковые цепи PEG имеют молекулярную массу от 1000 до 3000 дальтон. В предпочтительном варианте боковые цепи PEG имеют молекулярную массу примерно 2000 дальтон.
В некоторых вариантах боковыми цепями являются моносахариды. В предпочтительном варианте моносахаридами является глюкозамин. Моносахаридные боковые цепи могут быть представлены как -С(0)-сахарид.
В изобретении могут применяться любые соединения платины. Предпочтительно, чтобы соединением платины являлось соединение платины (II) или платины (IV). В некоторых вариантах соединение платины (II) является выбранным из группы, состоящей из цисплатина, оксалиплатина, карбоплатина, параплатина, сартраплатина и их комбинаций. В предпочтительном варианте боковой группой соединения платины (II) является цисплатин или оксалиплатин.
В некоторых вариантах соединение платины (II) является выбранными из
группы, включающей Pt(NH3)2, Pt(NH3)(2-метилпиридин), и , где р равно 0-3. В предпочтительном варианте соединением платины (II) является Pt(NH3)2.
В некоторых вариантах соединением платины (II) является , где р равно 0-3.
В некоторых вариантах соединение платины (II) включает, по меньшей мере, два атома азота, при этом указанные атомы азота напрямую связаны с платиной. В другом варианте два атома азота связаны друг с другом через факультативно замещенный линкер, например ациклический или циклический линкер. Циклический линкер означает связующий фрагмент, который содержит, по меньшей мере, одну кольцевую структуру. Циклическими линкерами могут являться арил, гетероарил, циклил или гетероциклил.
В некоторых вариантах, по меньшей мере, один атом азота, который связан с платиной, является кольцевым атомом гетероарила или гетероциклила. В предпочтительном варианте гетероарил представляет собой факультативно замещенный пиридин, например 2-метилпиридин.
В некоторых вариантах множество боковых цепей соответствует количеству от 50% до 100% включительно количества мономерных звеньев указанной полимерной основной цепи. Это означает, что от 50% до 100% мономерных звеньев имеют, по меньшей мере, одну боковую цепь, связанную с мономерным звеном. Общее количество боковых цепей может быть больше, чем общее количество мономерных звеньев. Например, две боковых цепи могут быть присоединены к мономеру малеиновой кислоты.
В некоторых вариантах множество боковых цепей соответствует количеству больше чем 90% количества мономерных звеньев указанной основной цепи полимера.
В некоторых вариантах множество соединений платины соответствует количеству от 10% до 100% включительно количества мономерных звеньев указанной основной цепи полимера. В целом, существует взаимно однозначное соответствие между соединениями платины и мономерными субъединицами. Таким образом, процент относится к отношению количества мономерных звеньев, которые связаны с соединением платины, к общему количеству мономерных звеньев, присутствующих в основной цепи полимера.
В некоторых вариантах множество соединений платины соответствует количеству от 25% до 75% включительно количества мономерных звеньев указанной основной цепи полимера.
В целом, от 10 до 500 мкг соединения платины может быть нагружено на 1 мг полимера. Предпочтительно, чтобы от 50 до 250 мкг, более предпочтительно от 150 до 200 мкг соединения платины было нагружено на 1 мг полимера. В некоторых вариантах авторы изобретения получили нагрузку 175±5 мкг/мг полимера.
В некоторых вариантах боковые цепи содержат дикарбоновые кислоты. В некоторых вариантах дикарбоновые кислоты имеют формулу HOOC-R-COOH, где R представляет собой а C1-С6 алкил, С3-С6 алкенил или С2-С6 алкинил. В предпочтительном варианте дикарбоновой кислотой является малеиновая кислота.
В некоторых вариантах сополимер содержит, по меньшей мере, один мономер, имеющий формулу -CH(CO2H)-R-CH(C(O)R')-, где R представляет собой связь, C1-С6 алкилен, где алкилен может включать одну или более двойных или тройных связей; и R' является замещенным атомом азота. Предпочтительно, чтобы R представлял собой связь.
В некоторых вариантах от 50% до 100% включительно мономерных субъединиц в основной цепи полимера представляют собой -CH(CO2H)-R-CH(C(O)R')-, где R представляет собой связь, C1-С6 алкилен, где алкилен может включать одну или более двойных или тройных связей; и R' является факультативно замещенным атомом азота.
В некоторых вариантах, по меньшей мере, 90% или более мономерных субъединиц в основной цепи полимера представляют собой -CH(CO2H)-R-CH(C(O)R')-, где R является связью, C1-С6 алкиленом, при этом алкилен может включать одну или более двойных или тройных связей; и R' является замещенным атомом азота.
В некоторых вариантах сополимер включает, по меньшей мере, один мономер, имеющий формулу -CH(CO2H)-R-CH(C(O)R')CH2C(Me2)- или -CH(C(O)R')-R-СН(CO2H)- СН2С(Ме2)-, где R является связью, C1-С6 алкиленом, при этом алкилен может включать одну или более двойных или тройных связей; и R' является замещенным атомом азота. Предпочтительно, чтобы R представлял собой связь.
В некоторых вариантах сополимер содержит от 50% до 100% включительно мономеров, имеющих формулу -CH(CO2H)-R-CH(C(O)R')CH2C(Me2)- или -CH(C(O)R')-R-CH(CO2H)-CH2C(Me2)-, где R является связью, C1-С6 алкиленом, при этом алкилен может включать одну или более двойных или тройных связей; и R' является замещенным атомом азота.
В некоторых вариантах сополимер содержит, по меньшей мере, 90% мономеров, имеющих формулу -CH(CO2H)-R-CH(C(O)R')CH2C(Me2)- или -CH(C(O)R')-R-СН(CO2H)-СН2С(Ме2)-, где R является связью, C1-С6 алкиленом, при этом алкилен может содержать одну или более двойных или тройных связей; и R' является замещенным атомом азота.
В одном варианте R' представляет собой или NH(CH2CH2O)mCH, где m равно 1-150.
В некоторых вариантах, по меньшей мере, один мономер полимера содержит две боковые цепи, выбранные из группы, состоящей из карбоновой кислоты, амида и сложного эфира. Указанные боковые цепи отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные амидные и эфирные боковые цепи были отделены друг от друга двумя атомами углерода. Предпочтительно, чтобы, по меньшей мере, одна из боковых цепей не являлись карбоновой кислотой.
В некоторых вариантах, по меньшей мере, один мономер полимера содержит две боковые цепи карбоновой кислоты. Указанные боковые цепи карбоновой кислоты отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи карбоновой кислоты были отделены друг от друга двумя атомами углерода. Указанные атомы углерода могут быть связаны друг с другом посредством простой или двойной связи.
В некоторых вариантах, по меньшей мере, один мономер полимера содержит боковые цепи карбоновой кислоты и амида. Указанные боковые цепи карбоновой кислоты и амида отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи карбоновой кислоты и амида были отделены друг от друга двумя атомами углерода. Указанные атомы углерода могут быть связаны друг с другом посредством простой или двойной связи.
В некоторых вариантах, по меньшей мере, один мономер полимера содержит боковые цепи карбоновой кислоты и сложного эфира. Указанные боковые цепи карбоновой кислоты и сложного эфира отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи карбоновой кислоты и сложного эфира были отделены друг от друга двумя атомами углерода. Указанные атомы углерода могут быть связаны друг с другом посредством простой или двойной связи.
В некоторых вариантах, по меньшей мере, один мономер полимера содержит боковые цепи амида и сложного эфира. Указанные боковые цепи амида и сложного эфира отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи амида и сложного эфира были отделены друг от друга двумя атомами углерода. Указанные атомы углерода могут быть связаны друг с другом посредством простой или двойной связи.
В некоторых вариантах, по меньшей мере, один мономер полимера содержит две боковые цепи амида. Указанные боковые цепи амида отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи амида и сложного эфира были отделены друг от друга двумя атомами углерода.
В некоторых вариантах, по меньшей мере, один мономер полимера содержит две боковые цепи сложного эфира. Указанные боковые цепи сложного эфира отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи амида и эфира были отделены друг от друга двумя атомами углерода.
В некоторых вариантах полимер включает две боковых цепи, выбранные из группы, состоящей из карбоновой кислоты, амида и сложного эфира. Указанные боковые цепи отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи амида и сложного эфира были отделены друг от друга двумя атомами углерода. Предпочтительно, чтобы, по меньшей мере, одна из боковых цепей не являлась карбоновой кислотой.
В некоторых вариантах полимер содержит, по меньшей мере, две боковые цепи карбоновой кислоты. Указанные боковые цепи карбоновой кислоты отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи карбоновой кислоты были отделены друг от друга двумя атомами углерода.
В некоторых вариантах полимер содержит боковые цепи карбоновой кислоты и амида. Указанные боковые цепи карбоновой кислоты и боковые цепи амида отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи карбоновой кислоты и амида были отделены друг от друга двумя атомами углерода.
В некоторых вариантах полимер содержит боковые цепи карбоновой кислоты и сложного эфира. Указанные боковые цепи карбоновой кислоты и сложного эфира отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи карбоновой кислоты и сложного эфира были отделены друг от друга двумя атомами углерода.
В некоторых вариантах полимер содержит боковые цепи амида и сложного эфира. Указанные боковые цепи амида и сложного эфира отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи амида и сложного эфира были отделены друг от друга двумя атомами углерода. Указанные атомы углерода могут быть связаны друг с другом посредством простой или двойной связи.
В некоторых вариантах полимер содержит две боковые цепи амида. Указанные боковые цепи амида отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи амида и сложного эфира были отделены друг от друга двумя атомами углерода.
В некоторых вариантах полимер содержит две боковые цепи сложного эфира. Указанные боковые цепи сложного эфира отделены друг от друга 1, 2, 3, 4, 5, 6, 7, 8, 9 или десятью атомами углерода, кислорода, азота, серы или их комбинацией. Предпочтительно, чтобы указанные боковые цепи амида и сложного эфира были отделены друг от друга двумя атомами углерода.
Размер наночастиц изобретения может изменяться в диапазоне 25-250 нм, предпочтительно 50-200 нм, более предпочтительно 80-160 нм и наиболее всего предпочтительно 90-110 нм. Без привязки к какой-либо теории, преимущественный хоминг наночастиц размером в диапазоне 80-160 нм в опухоли происходит в результате увеличенной проницаемости и задержания. Смотри, например, Moghimi, et al., Pharmacol Rev. 2001 Jun; 53(2):283-318.
В некоторых вариантах соединение платины диссоциируемо связано с указанной основной цепью посредством, по меньшей мере, одной координационной связи. Без привязки к какой-либо теории, координационная связь является более доступной и, таким образом, более легко высвобождает соединение платины.
В некоторых вариантах связывание соединения платины с основной цепью биополимера, кроме того, включает карбоксилато связь. В некоторых вариантах соединение платины связано с основной цепью посредством координационной связи и карбоксилато связи.
Должно быть понятно, что, несмотря на описание связи с основной цепью, опытному в данной области специалисту будет очевидно, что соединение платины, в целом, связано с одной или более боковыми цепями, которые само по себе связаны с основной цепью. Таким образом, любое описание связывания соединения платины с основной цепью включает случаи, когда соединение платины связано с боковой цепью, которая, кроме того, связана с основной цепью.
В некоторых вариантах координационная связь находится между атомом платины соединения платины и кислородом боковой цепи. Предпочти