Способ получения нитевидных кристаллов активного материала положительного электрода литий-воздушного аккумулятора
Иллюстрации
Показать всеИзобретение относится к активному материалу положительного электрода литий-воздушного аккумулятора в виде нитевидных кристаллов состава KxMnO2 (x=0,1-0,15) длиной от 0,1 мкм до 2 мм и диаметром от 20 до 30 нм для обратимого восстановления кислорода на положительном электроде. А также относится к способу его получения, включающему растворение в воде перманганата калия и персульфата калия и перемешивание смеси при pH среды от 2 до 4 в течение 2-12 часов, при температуре 95°C с последующей фильтрацией, промывкой продукта и высушиванием при 60°C. Использование указанного материала позволяет достигать высокой удельной электрохимической емкости. 2 н.п. ф-лы, 5 ил., 1 табл., 2 пр.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к неорганической химии и может быть использовано, в частности, для получения электрокатализатора в виде нитевидных кристаллов состава KxMnO2 (x=0,1-0,15) со структурой α-MnO2, обладающего высокой электрохимической активностью по отношению к обратимому восстановлению кислорода на положительном электроде литий-воздушного аккумулятора.
Уровень техники
Литий-кислородные аккумуляторы, потенциалообразующим процессом в которых является окисление лития кислородом воздуха, относятся к новому типу химических источников тока (ХИТ). Удельная емкость таких элементов питания превышает аналогичный показатель для литий-ионных аккумуляторов в 5-10 раз. Для обеспечения обратимости реакции окисления в состав материала катода включают соответствующий катализатор. В работе (Debart A, Bruce Р G, Armstrong G et al. An O2 cathode for rechargeable lithium batteries: The effect of a catalyst. // Journal of Power Sources 2007 174 1177-1182) было показано, что в качестве таких катализаторов могут быть применимы оксиды переходных металлов, причем наибольшая эффективность достигается при использовании туннельных структур диоксида марганца (в особенности α-фазы, образующей туннели 2×2). Самую высокую разрядную емкость и стабильность при циклировании удалось получить при использовании анизотропных нанокристаллов диоксида марганца (Debart A, Paterson A J, Bruce Р G et al. α-MnO2 Nanowires: A Catalyst for the O2 Rechargeable Lithium Batteries. // Angewandte Chemie 2008 47 4521-4524).
Нитевидные кристаллы с туннельной структурой в системе Mn-O - хорошо изученные и доступные объекты с низкой стоимостью, малой токсичностью и экологической безопасностью. Способность марганца находиться в своих соединениях в смешанных степенях окисления и образовывать сложные каркасные структуры, состоящие из сочлененных определенным образом октаэдров MnO6 с различным типом катионов, размещающихся в пустотах каркаса, предопределяют большое разнообразие «классических» марганецсодержащих оксидных материалов: катализаторов, топливных ячеек и др.
В работе (Yang R, Wang Z, Dai L et al. Synthesis and characterization of single-crystalline nanorods of α-MnO2 and γ-MnOOH. // Materials Chemistry and Physics 2005 93 149-153) синтез одномерных кристаллов диоксида марганца проводился путем восстановления перманганата калия графитом в 12 М водном растворе H2SO4 при 0°C и постоянном перемешивании. Были получены кристаллы диаметром 10 нм и длиной 100-200 нм. Данная методика получения отличается от настоящего изобретения как по химической природе продукта (составу), так методике получения.
Наиболее близкими к предложенному по технической сущности и количеству совпадающих признаков являются работы по синтезу нитевидных нанокристаллов α-MnO2 для применения в литий-кислородных аккумуляторах, полученных методом гидротермальной обработки растворов. Оксид марганца синтезировали при реакции восстановления KMnO4 (Gao Y, Wang Z, Wan J et al. A facile route to synthesize uniform single-crystalline α-MnO2 nanowires. // Journal of Crystal Growth 2005 2 79 415-419), либо сопропорционирования между Mn2+ и MnO4 - (Huang X, Attia A, Yang Y et al. Controllable synthesis of α- and β-MnO2: cationic effect on hydrothermal crystallization. // Nanotechnology 2008 19 225606) (при pH=6-7). Длительность гидротермальной обработки составляла от 24 до 48 часов при температуре от 140 до 180°C. Недостатком этой методики в отличие от настоящего изобретения является невозможность получения материала с количественным выходом, а также большая продолжительность синтеза при достаточно высоких температурах и наличие специального оборудования и соблюдение повышенных мер по технике безопасности для осуществления синтеза.
Совокупность существенных признаков изобретения
Настоящее изобретение позволяет решить задачу получения активного материала в виде одномерных кристаллов с количественным выходом, не прибегая к сложным синтетическим подходам. Это позволяет добиться высокой электрохимической емкости положительного электрода литий-воздушного аккумулятора при невысокой стоимости составных материалов. К настоящему изобретению относится способ получения нитевидных кристаллов состава KxMnO2 (x=0,1-0,15) длиной от 0,1 мкм до 2 мм и диаметром от 20 до 30 нм, включающий растворение в воде перманганата калия и персульфата калия с последующим перемешиванием при pH среды от 2 до 4 в течение 2-12 часов при температуре 95°C, фильтрацией, промывкой продукта и высушиванием при 60°C.
Технический результат
При низких трудо- и энергозатратах и простом техническом исполнении получены нитевидные кристаллы состава KxMnO2 (x=0,1-0,15), которые имеют структуру α-MnO2, длину - от 0,1 мкм до 2 мм и диаметр от 20 до 30 нм, что делает их перспективными для использования, в качестве электрохимически активного материала положительного электрода за счет возможности изменения степени окисления марганца в составе кристаллического каркаса и высокой подвижности лития в кристаллических туннелях, что позволяет достигать высокой удельной электрохимической емкости.
Детальные описания способа получения
Нитевидные кристаллы KxMnO2 (x=0,1-0,15) были получены путем растворения при перемешивании в воде перманганата калия и персульфата. Синтез проводится в течение суток при температуре 95°C и постоянном перемешивании при pH от 2 до 4.
В результате синтеза после фильтрации, промывки продукта и сушки при температуре 60°C образовывались наноразмерные нити и сложные микроструктуры «сборки», состоящие из таких нитевидных кристаллов (Рис.1) длиной от 0,1 мкм до 2 мм и диаметром от 20 до 30 нм.
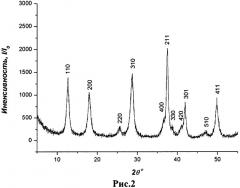
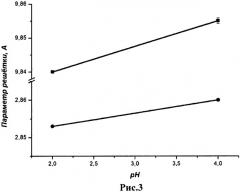
Данные рентгенофазового анализа (Рис.2) показывают, что образцы представляют собой тетрагональную модификацию α-MnO2 (пр. группа I4/m) с параметрами решетки, приведенными на Рис.3.
Количество калия в структуре определялось методом масс-спектрометрии. Полученные данные представлены в Таблице 1. Диаметр нитевидных кристаллов зависит от количества калия в структуре, с увеличением х их диаметр возрастает в связи с ростом параметров кристаллической решетки.
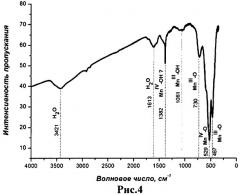
Согласно данным ИК-спектроскопии образцы содержат хемосорбированную или гидратную воду, т.к. присутствуют линии в районе 3000-3600 см-1, соответствующие деформационным колебаниям воды. Колебания при 300-700 см-1 соответствуют решеточным колебаниям Mn-O (Julien С, Massot М. Spectroscopic studies of the local structure in positive electrodes for lithium batteries. // Physical Chemistry Chemical Physics, 2002, 4, 4226-4235). Некоторое смещение положений и слабое изменение интенсивностей колебаний решеточных Mn-O происходят вследствие изменения локальной структуры, которое может быть связано с образованием вакансий в позициях марганца при диспропорционировании Mn(III) в кислой среде. Колебания ~1100 см-1 соответствуют колебаниям решеточных -OH групп (Рис.4).
Электрохимическая активность ультадисперсных нитевидных кристаллов KxMnO2 исследована с помощью модельных литий-кислородных ячеек. Ячейки состояли из металлического лития, герметично запаянного с помощью пластины твердого электролита типа литий-замещенного NASICON (Na Super Ionic CONductor) и композитного положительного электрода, состоящего из углеродной матрицы и синтезированного катализатора. Материал положительного электрода содержит от 5 до 75% активного материала, 10-90% активированного угля и не более 5% фторопласта в качестве пластификатора. Ячейки протестированы током 20-100 мА/г катодного материала в диапазоне напряжений 2-4 В. Потенциал разомкнутой цепи литий-воздушной ячейки составил примерно 3.1 В. При поляризации постоянным током происходило смещение потенциала до 2.5-2.7 В (процесс разрядки ячейки) и 3.6-4.2 В (процесс зарядки); удельная электрохимическая емкость, рассчитанная на массу катодного материала, составила более 3 А·ч на 1 грамм материала катода (Рис.5).
Изобретение иллюстрируется следующими рисунками, таблицами и примерами.
Рис.1. Микрофотографии нитевидных кристаллов, полученных при разных pH.
Рис.2. Дифрактограмма образца KxMnO2 со структурой α-MnO2.
Рис.3. Зависимость параметров решетки нитевидных кристаллов от pH.
Рис.4. ИК-спектр полученного образца KxMnO2 при рН=4.
Рис.5. Разрядный и зарядный циклы литий-воздушной батареи с катодом на основе активированного угля и нитевидных кристаллов.
Пример 1.
50 мл дистиллированной воды растворили KMnO4 (37 масс.%) и K2S2O8 (63 масс.%). Синтез идет в течение 2-12 часов при температуре 95°C и постоянном перемешивании. После охлаждения до комнатной температуры осадок был отфильтрован, промыт дистиллированной водой и высушен при 60°C в течение суток. pH раствора от 4 до 1.5 регулировался добавлением концентрированной H2SO4. Свойства полученного материала представлены в Таблице 1 и на Рис.1-5.
Пример 2.
0.2 М растворы KMnO4 и K2S2O8 сливались и перемешивались в течение 2-12 часов при температуре 95°C. После охлаждения до комнатной температуры образовавшийся осадок был отфильтрован, промыт дистиллированной водой и высушен при 60°C в течение суток. pH раствора от 2 до 4 регулировался добавлением концентрированной H2SO4. Свойства полученного материала представлены в Таблице 1 и на Рис.1-5.
| Таблица 1 | ||
| Степень окисления марганца и состав по калию для полученных образцов | ||
| pH | x(KxMnO2) | Степень окисления Mn |
| 4 | 0,134 | 3,866 |
| 2 | 0,123 | 3,877 |
Материал, предложенный в настоящем изобретении, представляет большой интерес для использования в качестве активной компоненты положительного электрода литий-воздушного аккумулятора. Интерес определяется высокими электрохимическими свойствами с емкостью более 2000 мАч/г и стабильностью при циклировании с деградацией не более 10% после 10 циклов.
1. Активный материал положительного электрода литий-воздушного аккумулятора в виде нитевидных кристаллов состава KxMnO2 (x=0,1-0,15) длиной от 0,1 мкм до 2 мм и диаметром от 20 до 30 нм для обратимого восстановления кислорода на положительном электроде.
2. Способ получения электрокатализатора по п.1, включающий растворение в воде перманганата калия и персульфата калия и перемешивание смеси при pH среды от 2 до 4 в течение 2-12 часов, при температуре 95°C с последующей фильтрацией, промывкой продукта и высушиванием при 60°C.