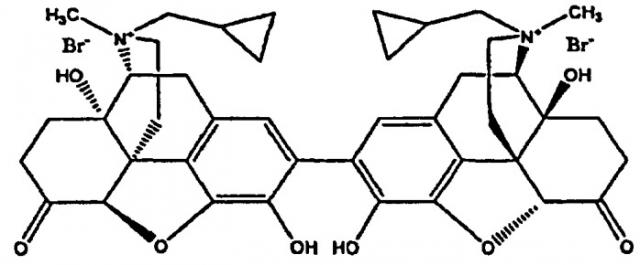
Составы для парентеральной доставки соединений и их применение
Иллюстрации
Показать всеВ настоящем изобретении предложены составы, обеспечивающие эффективную доставку композиций на основе метилналтрексона. Фармацевтическая композиция по изобретению содержит эффективное количество метилналтрексона, кальцийэтилендиаминтетрауксусную кислоту (ЭДТА) или кальциево-динатриевую соль ЭДТА и гидрохлорида глицин в водном растворе. Указанный раствор имеет рН от примерно 3 до примерно 4. Также описан способ получения состава метилналтрексона. Предложенные составы подходят для предотвращения, лечения, замедления, ослабления или снижения степени тяжести побочных эффектов, возникающих в результате применения болеутоляющих опиоидов. Композиция характеризуется высокой стабильностью при длительном хранении в жестких условиях. 2 н. и 28 з.п. ф-лы, 4 ил., 20 табл., 14 пр.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка на изобретение испрашивает приоритет на основании предварительной заявки на патент США, серийный номер 60/835574, поданной 4 августа 2006 года, полное описание которой включено в настоящую заявку посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
[0002] Опиоиды широко применяются при лечении пациентов с прогрессирующими раковыми заболеваниями и другими заболеваниями в терминальной стадии с целью облегчения страданий. Опиоиды являются наркотическими медицинскими препаратами, которые активируют опиоидные рецепторы, локализованные в центральной нервной системе, что приводит к облегчению боли. Однако опиоиды также взаимодействуют с рецепторами, расположенными вне центральной нервной системы, что приводит к возникновению побочных эффектов, в том числе запоров, тошноты, рвоты, задержке мочи и сильному зуду. Наиболее существенному воздействию подвергается желудочно-кишечный тракт (ЖКТ), где опиоиды вызывают затруднение опорожнения желудка и подавляют пропульсивную активность кишечника, тем самым уменьшая скорость продвижения содержимого через кишечник, что может вызвать запор. Эффективность опиоидов при уменьшении боли часто ограничена из-за возникающих побочных эффектов, которые могут приводить к ухудшению состояния здоровья пациента и часто вынуждают пациентов прекратить применение опиоидных анальгетиков.
[0003] Результаты проведенных исследований позволяют предположить, что помимо побочных эффектов, вызванных приемом болеутоляющих опиоидов, на активность желудочно-кишечного тракта (ЖКТ) могут также оказывать воздействие эндогенные опиоидные соединения, которые также могут участвовать в нормальном регулировании перистальтики кишечника и переноса жидкостей через слизистые оболочки как у животных, так и у человека (Koch, Т. R, et al., Digestive Diseases and Sciences 1991, 36, 712-728; Schuller, A.G.P., et al., Society of Neuroscience Abstracts 1998. 24, 524, Reisine, Т., и Pasternak, G., Goodman & Gilman's The Pharmacological Basis of Therapeutics Ninth Edition 1996, 521-555 и Bagnol, D., et al., Regul. Pept. 1993, 47, 259-273). Таким образом, отклонения от нормального физиологического содержания эндогенных соединений и/или рецепторной активности могут приводить к дисфункции кишечника.
[0004] Например, пациенты, перенесшие хирургические операции, особенно операции на брюшной полости, часто страдают от дисфункции кишечника, например, послеоперационной кишечной непроходимости, которая может быть вызвана колебаниями естественных уровней опиоидов. Аналогичным образом, женщины после родов зачастую страдают от послеродовой кишечной непроходимости, которая, как полагают, вызвана аналогичными колебаниями естественного уровня опиоидов в результате родового стресса. Дисфункция кишечника, связанная с послеоперационной или послеродовой кишечной непроходимостью, обычно может продолжаться в течение 3-5 дней, достигая недели и более в некоторых серьезных случаях. Введение опиоидных анальгетиков пациенту после хирургической операции, являющееся в настоящее время почти всеобщей практикой, может усилить дисфункцию кишечника, замедляя тем самым восстановление нормального функционирования кишечника, продлевая время пребывания в больнице и увеличивая стоимость медицинского обслуживания.
[0005] Были проведены исследования опиоидных антагонистов, таких как налоксон, налтрексон и налмефен, в качестве средств, уменьшающих нежелательное воздействие опиоидов на периферическую нервную систему. Однако эти вещества воздействуют не только на периферические опиоидные рецепторы, но также и на участки центральной нервной системы, так что иногда они аннулируют положительные анальгетические эффекты опиоидов или вызывают синдром отмены опиоидов. Предпочтительные подходы к контролированию побочных эффектов, вызванных опиоидами, включают применение соединений, являющихся антагонистами периферически действующих опиоидов, которые не сразу преодолевают гематоэнцефалический барьер. Например, было показано, что метилналтрексон, являющийся периферически действующим µ-опиоидным антагонистом, и родственные соединения можно применять с целью сдерживания у пациентов побочных эффектов, вызываемых опиоидами (например, запора, зуда, тошноты и/или рвоты). См., например, патенты США 5972954, 5102887, 4861781 и 4719215; и Yuan, С.-S. et al. Drug и Alcohol Dependence 1998, 52. 161.
[0006] Были описаны составы на основе метилналтрексона в качестве периферически действующего антагониста µ-опиоидного рецептора (см., например, патенты США 6608075, 6274591 и 6559158). Однако было обнаружено, что метилналтрексон в некоторых средах и при некоторых условиях образует продукты разложения. См., например, US 2004266806A1. Таким образом, требуется получение лекарственных форм, обеспечивающих эффективную доставку метилналтрексона без значительного разложения метилналтрексона при охлаждении и/или при комнатной температуре.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0007] В настоящем изобретении предложены некоторые составы на основе метилналтрексона. Согласно некоторым вариантам реализации в изобретении предложены составы, имеющие улучшенные характеристики стабильности при длительных сроках хранения активного соединения при охлаждении, а также при комнатной температуре. Предложенные составы можно применять для парентерального введения метилналтрексона. Изобретение включает способы получения и применения указанных составов, а также продукты и наборы, содержащие предложенные составы.
[0008] Согласно некоторым вариантам реализации изобретения предложена фармацевтическая композиция, содержащая эффективное количество по меньшей мере одного активного соединения, выбранного из по меньшей мере метилналтрексона или его фармацевтически приемлемой соли, и кальциевую соль хелатирующего агента в водном растворе.
[0009] Согласно другим вариантам реализации изобретения предложены жидкие составы, содержащие метилналтрексон или его фармацевтически приемлемую соль, кальциевую соль, хелатирующий агент, изотонический агент и водный растворитель. Согласно некоторым вариантам реализации изобретения кальциевая соль и хелатирующий агент представляют собой одно соединение в виде кальциевой соли хелатирующего агента. Согласно некоторым вариантам реализации изобретения, кальциевую соль хелатирующего агента выбирают из кальциевой соли этилендиаминтетрауксусной кислоты (EDTA), кальциевой соли диэтилентриаминпентауксусной кислоты (DTPA), кальциевой соли гидроксиэтилендиаминтриуксусной кислоты (HEDTA), кальциевой соли этиленгликоль-бис-(2-аминоэтил)-N,N,N',N'-тетрауксусной кислоты (EGTA), кальциевой соли нитрилотриуксусной кислоты (NTA), цитрата кальция и производных их кальциевых солей. Согласно некоторым вариантам реализации изобретения кальциевая соль хелатирующего агента представляет собой кальциевую соль EDTA.
[0010] Согласно некоторым вариантам реализации изобретения составы также дополнительно содержат стабилизатор. Согласно некоторым вариантам реализации изобретения стабилизатор выбирают из глицина, бензойной кислоты, лимонной, гликолевой, молочной, яблочной и малеиновой кислоты. Согласно некоторым вариантам реализации изобретения стабилизатор представляет собой глицин.
[0011] Согласно некоторым вариантам реализации изобретения, состав содержит метилналтрексон или его фармацевтически приемлемую соль, кальциевый хелатирующий агент, стабилизатор, изотонический агент и водный растворитель. Согласно некоторым вариантам реализации изобретения, состав содержит метилналтрексон или его фармацевтически приемлемую соль, кальциевую соль EDTA, глицин и хлорид натрия в водном растворе.
[0012] В целом, предложенные составы можно применять для предотвращения, лечения или уменьшения степени тяжести побочных эффектов, возникающих в результате применения опиоидов, в том числе для ингибирования желудочно-кишечной дисфункции (например, запора, гипоперистальтики кишечника, закупорки, гипоперистальтики желудка, сужения сфинктера ЖКТ, увеличения тонуса сфинктера, ингибирования желудочно-кишечной перистальтики, ингибирования перистальтики кишечника, ингибирования опорожнения желудка, замедления опорожнения желудка, неполного опорожнения, тошноты, рвоты, вспучивания, вздутия живота), покраснения кожных покровов, потоотделения, дисфории, зуда, задержки мочи и т.д. Предложенные составы можно применять для введения пациентам, проходящим краткий курс лечения опиоидами (например, пациентам, восстанавливающимся после хирургической операции (на брюшной полости, ортопедической, операции после травмы и т.д.), пациентам, восстанавливающимся после травм, и пациентам, восстанавливающимся после рождения ребенка). Составы также можно применять для введения пациентам, постоянно принимающим опиоиды (например, неизлечимо больным пациентам, принимающим опиоидную терапию (например, пациентам с диагнозом СПИД, пациентам с раковыми заболеваниями или пациентам с сердечно-сосудистыми заболеваниями); пациентам, постоянно принимающим опиоидную терапию с целью обезболивания (например, от боли в спине); пациентам, принимающим опиоидную терапию с целью облегчения синдрома отмены опиоидов).
[0013] Дополнительные применения предложенных составов включают предотвращение, лечение или уменьшение степени тяжести симптомов, связанных с расстройствами или состояниями, возникающими в результате нормальной или аберрантной активности эндогенных опиоидов. Указанные расстройства или состояния включают, среди прочего, кишечную непроходимость (например, послеродовую кишечную непроходимость, кишечную непроходимость при параличе), желудочно-кишечную дисфункцию, которая развивается после операции на брюшной полости (например, колэктомии, в том числе, без ограничения, правосторонней гемиколэктомии, левосторонней гемиколэктомии, поперечной гемиколэктомии, подготовке в колэктомии и низкой передней резекции), такую как послеоперационная кишечная непроходимость и идиопатический запор. Предложенные составы также можно применять при лечении состояний, включающих, например, раковые заболевания, связанные с ангиогенезом, воспалительные заболевания (например, синдром раздраженного кишечника), иммуносупрессию, сердечно-сосудистые заболевания (например, брадикардию, гипотонию), хронические воспаления и/или хронические боли, серповидноклеточную анемию, повреждения сосудов и ретинопатию, пониженную секрецию желчи, пониженную секреторную активность поджелудочной железы, спазм желчевыводящих путей и повышенный гастроэзофагеальный рефлюкс.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0014] Фиг.1А и фиг.1В: Влияние CaEDTA и NaEDTA на образование 2',2-бис-метилналтрексона в присутствии железа при 40°С (фиг.1А) и комнатной температуре, 25° (фиг.1В). Как кальциевая соль ЭДТА, так и натриевая соль ЭДТА являются эффективными ингибиторами образования продукта разложения в виде 2',2'-бис-метилналтрексона.
[0015] Фиг.2А, 2В, 2С и 2D: Влияние CaEDTA на образование 7-дигидроксиметилналтрексона в растворах. Оценивали влияние CaEDTA и NaEDTA на образование 7-дигидроксиметилналтрексона в присутствии железа при 40°С (фиг.2А) и комнатной температуре, 25°С (фиг.2В). Эффективным ингибитором образования продукта разложения в виде 7-дигидроксиметилналтрексона является кальциевая соль ЭДТА, а не натриевая соль ЭДТА. Оценивали влияние CaEDTA на образование 7-дигидроксиметилналтрексона в растворе после хранения в течение месяца при комнатной температуре (фиг.2С) и при 40°С (фиг.2D). Присутствие CaEDTA уменьшало образование 7-дигидроксиметилналтрексона при обеих температурах. Через один месяц при комнатной температуре содержание продукта разложения уменьшалось от 0.34% до 0.11%; и при 40°С /относительной влажности (OВ) 75% указанное содержание уменьшалось от 0.64% до 0.14%. Присутствие NaEDTA в пробах может даже приводить к увеличению содержания образующегося 7-дигидроксиметилналтрексона.
[0016] Фиг.3А и фиг.3В: Влияние CaEDTA в растворе метилналтрексона на образование продукта разложения метилналтрексона, имеющего RRT (относительное время удерживания), равное 0.79 ("продукт разложения 0.79"). Оценивали влияние CaEDTA и NaEDTA на образование продукта разложения 0.79 при комнатной температуре, 25°С (фиг.3А), и при 40°С (фиг.3В). Кальциевая соль ЭДТА не являлась эффективной в отношении ингибирования образования продукта разложения 0.79 и могла приводить к увеличению содержания образующегося продукта разложения.
[0017] На фиг.4 представлены идентифицированные продукты разложения метилналтрексона, соответствующие относительные времена удерживания (RRT) и соответствующие катализаторы и/или ингибиторы их образования, которые были идентифицированы.
ПОДРОБНОЕ ОПИСАНИЕ НЕКОТОРЫХ ВАРИАНТОВ РЕАЛИЗАЦИИ ИЗОБРЕТЕНИЯ
[0018] В изобретении предложены фармацевтические составы, имеющие улучшенные характеристики стабильности при некоторых условиях. Композиции, наборы и продукты, содержащие предложенные составы, характеризуются длительными сроками хранения и также могут храниться при благоприятных условиях при комнатной температуре. Таким образом, композиции, наборы и продукты, содержащие предлагаемые составы, обеспечивают улучшенную доставку терапевтических препаратов пациентам, на которых применение метилналтрексона оказывает лечебное воздействие.
[0019] Например, предлагаемые составы подходят для лечения, предотвращения, замедления или уменьшения степени тяжести или частоты возникновения побочных эффектов, связанных с введением опиоидов, в том числе желудочно-кишечной дисфункции (например, запора, гипоперистальтики кишечника, закупорки, желудочной гипоперистальтики, сужения сфинктера ЖКТ, увеличения тонуса сфинктера, ингибирования желудочно-кишечной перистальтики, ингибирования перистальтики кишечника, ингибирования опорожнения желудка, замедления опорожнения желудка, неполного опорожнения, тошноты, рвоты, вспучивания, вздутия живота), дисфории, зуда, задержки мочи, подавления дыхания, спазма папиллярной мышцы, сердечно-сосудистых эффектов, ригидности грудных стенок и подавления кашля, депрессии стрессовой реакции и иммуносупрессии, связанной с применением наркотического обезболивания и т.д. Дополнительные эффекты от введения опиоидов могут включать, например, аберрантную миграцию или пролиферацию эндотелиальных клеток (например, васкулярных эндотелиальных клеток), увеличение ангиогенеза, и приводить к повышению смертности за счет продуцирования условно-патогенных возбудителей инфекции (например, Pseudomonas aeruginosa). Составы можно применять для введения пациентам, проходящим краткосрочный курс лечения опиоидами (например, пациентам, страдающим от послеоперационной желудочно-кишечной дисфункции и принимающим опиоиды в течение непродолжительного периода времени). Составы также можно применять для введения пациентам, постоянно принимающим опиоиды (например, неизлечимо больным пациентам, подвергающимся опиоидной терапиии, таким как больные СПИДом, пациенты с раковыми заболеваниями, пациенты с сердечно-сосудистыми заболеваниями; пациенты, постоянно принимающие опиоиды с целью обезболивания; пациенты, принимающие опиоиды с целью облегчения синдрома отмены опиоидов).
[0020] Кроме того, применение предлагаемых составов включает, например, предотвращение, замедление, лечение или уменьшение степени тяжести симптомов, связанных с расстройствами или состояниями, возникающими в результате нормальной или аберрантной активности эндогенных опиоидов. Указанные расстройства или состояния включают, помимо прочего, кишечную непроходимость (например, послеродовую кишечную непроходимость, кишечную непроходимость при параличе), желудочно-кишечную дисфункцию, которая развивается после операции на брюшной полости (например, колэктомии, в том числе, без ограничения, правосторонней гемиколэктомии, левосторонней гемиколэктомии, поперечной гемиколэктомии, подготовке к колэктомии и низкой передней резекции), такую как послеоперационная кишечная непроходимость и идиопатический запор. Предлагаемые составы также можно применять при лечении состояний, включающих раковые заболевания, связанные с ангиогенезом, иммуносупрессию, серповидноклеточную анемию, сосудистые повреждения и ретинопатию, и при лечении заболеваний, вызванных воспалением (например, синдрома раздраженного кишечника), иммуносупрессии и хронического воспаления.
Определения
[0021]Термин "концентрат" относится к фармацевтической композиции, содержащей предложенный состав, в которой концентрация активного вещества (веществ) выше, чем концентрация в обычной стандартной лекарственной форме, подходящей для непосредственного введения пациенту. Концентрат можно непосредственно применять для введения пациенту, но, как правило, при приготовлении для введения пациенту его дополнительно разбавляют до концентрации обычной стандартной лекарственной формы. Весь объем концентрата или его аликвоту можно применять при приготовлении стандартной лекарственной формы (форм) для лечения, например, согласно способам, предложенным в настоящем изобретении. Согласно некоторым вариантам реализации изобретения концентрат является примерно в 2 раза, примерно в 5 раз, примерно в 10 раз, примерно в 25 раз, примерно в 50 раз, примерно в 100 раз или примерно в 200 раз более концентрированным, чем стандартная лекарственная форма. Согласно некоторым вариантам реализации изобретения концентрат является примерно в 50 раз, примерно в 100 раз или примерно в 200 раз более концентрированным, чем стандартная лекарственная форма.
[0022] Применяемый в настоящем описании термин "эффективное количество" соединения или фармацевтически приемлемого состава представляет собой количество, обеспечивающее требуемый терапевтический и/или профилактический эффект. Согласно некоторым вариантам реализации изобретения, "эффективное количество" представляет собой по меньшей мере минимальное количество соединения, или состава, содержащего соединение, которое является достаточным для лечения одного или нескольких симптомов заболевания или состояния, связанного с модулированием периферийных µ-опиоидных рецепторов, например, побочных эффектов, вызванных опиоидной обезболивающей терапией (например, желудочно-кишечной дисфункции (например, нарушения перистальтики кишечника, запора и т.д.), тошноты, рвоты и т.д.). Согласно некоторым вариантам реализации изобретения "эффективное количество" соединения или состава, содержащего указанное соединение, является достаточным для лечения симптомов, связанных с заболеванием, вызванным аберрантной эндогенной активностью периферийных опиоидов или µ-рецепторов опиоидов (например, идиопатического запора, кишечной непроходимости и т.д.).
[0023] Термин "состав" относится к композиции для введения пациенту, которая содержит по меньшей мере одно фармацевтически активное соединение (например, по меньшей мере метилналтрексон) в комбинации с одним или несколькими наполнителями или другими фармацевтическими добавками. В общем случае, конкретные наполнители и/или другие фармацевтические добавки, как правило, выбирают с целью достижения требуемой стабильности, высвобождения, распределения и/или активности активного соединения (соединений) при применении.
[0024] Термин "субъект", применяемый в настоящем описании, означает млекопитающее, которому вводят состав или композицию, содержащую указанный состав, и включает людей и животных, таких как домашние животные (например, лошади, собаки, кошки и т.д.).
[0025] Термин "терапевтически активное соединение" или "активное соединение" относится к веществу, в том числе биологически активному веществу, которое можно применять с целью терапии (например, терапии человека или в ветеринарии), в том числе для профилактического и/или терапевтического лечения. Терапевтически активные соединения могут представлять собой органические молекулы, которые являются лекарственными соединениями, пептидами, белками, карбогидратами, моносахаридами, олигосахаридами, полисахаридами, нуклеопротеином, мукопротеином, липопротеином, синтетическим полипептидом или белком, молекулами небольшого размера, связанными с белком; гликопротеином, стероидом, нуклеиновой кислотой, ДНК, РНК, нуклеотидом, нуклеозидом, олигонуклеотидами, антисмысловым олигонуклеотидами, липидом, гормоном и витамином. Альтернативным образом или дополнительно терапевтически активные соединения могут представлять собой любое вещество, применяемое в качестве лекарственного препарата для лечения, предотвращения, замедления, уменьшения или облегчения заболевания, состояния или расстройства. Терапевтически активные соединения, которые можно применять в составах, предложенных в настоящем изобретении, включают опиоидные антагонисты, опиоидные болеутоляющие соединения и т.п. Дополнительное подробное описание соединений, применяемых в качестве терапевтически активных соединений, приведено ниже. Терапевтически активное соединение включает соединение, которое усиливает действие или эффективность второго соединения, например, путем усиления активности или уменьшения нежелательных эффектов второго соединения. Термины "лечить" или "лечение", применяемые в настоящем описании, относятся к частичному или полному облегчению, подавлению, задержке наступления, уменьшению частоты случаев, улучшению и/или облегчению расстройства или состояния или одного или нескольких симптомов расстройства, заболевания или состояния.
[0026] Применяемое в настоящем описании выражение "стандартная доза" относится к физически отдельной дозе состава, подходящего для лечения субъекта. Однако следует иметь в виду, что суммарное ежедневное применение состава, предлагаемого в настоящем изобретении, определяется лечащим врачом в рамках тщательного медицинского обследования. Величина индивидуальной эффективной дозы для любого конкретного субъекта или организма зависит от множества факторов, в том числе конкретного заболевания, подвергаемого лечению, и степени тяжести заболевания; активности применяемого конкретного активного соединения; применяемой конкретной композиции; возраста, массы тела, общего состояния здоровья, пола и режима питания субъекта; времени введения и скорости выведения применяемого конкретного активного соединения; продолжительности лечения; лекарственных препаратов и/или дополнительных курсов лечения, применяемых в сочетании или одновременно с конкретным применяемым соединением (соединениями) и других подобных факторов, хорошо известных в области медицины.
[0027] Выражение "лекарственная форма" относится к средствам, обеспечивающим возможность хранения и/или введения состава субъекту. Например, состав можно хранить во флаконе или шприце. Состав также можно хранить в контейнере, который защищает состав от света (например, УФ-излучения). Альтернативным образом, контейнер или флакон, который сам не обязательно защищает состав от света, можно хранить во втором контейнере для хранения (например, поместив в коробку, пакет и т.д.), который защищает состав от света.
[0028] В настоящем изобретении предложены составы и лекарственные формы для парентерального введения метилналтрексона, в том числе его фармацевтически приемлемых солей. Применяемый в настоящем описании термин "метилналтрексон" включает N-метилналтрексон и его соли. Метилналтрексон описан, например, в патентах США 4176186; 4719215; 4861781; 5102887; 5972954; 6274591; заявках на патент, опубликованных в США под номерами 20020028825 и 20030022909; и публикациях WO 99/22737 и WO 98/25613, содержание которых включено в настоящее описание посредством ссылок.
[0029] В общем случае, фармацевтически приемлемые соли включают без ограничения хлорид, бромид, иодид, нитрат, сульфат, бисульфат, фосфат, кислую соль фосфорной кислоты, соли изоникотиновой кислоты, ацетат, лактат, салицилат, цитрат, тартрат, пантотенат, битартрат, карбонат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкаронат, сахарат, формиат, карбоксилат, бензоат, глутамат, сульфонат, метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат, селенати памоат(т.е. 1,1'-метилен-бис-(2-гидрокси-3-нафтоат). Согласно некоторым вариантам реализации изобретения соли применяемые в составах согласно настоящему изобретению, представляют собой ранее описанные соли метилналтрексона, например метилналтрексона бромид и т.д. Однако изобретение не ограничивается этими конкретными солями. Другие соли и их смеси можно адаптировать для применения в лекарственном составе согласно изобретению с тем, чтобы достичь подходящей совокупности параметров, характеризующей доставку соединения в организме, предлагаемую в настоящем изобретении (например, хлориды, сульфаты, бисульфаты, тартраты, нитраты, цитраты, битартраты, фосфаты, соли яблочной кислоты, соли малеиновой кислоты, бромиды, иодиды, соли фумаровой кислоты, сульфонаты, карбоксилаты или сукцинаты и т.д.). Альтернативным образом или дополнительно периферически действующий антагонист опиоидного рецептора (например, метилналтрексон) можно при необходимости применять в виде основания, его химических и хиральных производных и других солей.
[0030] К бромидной соли метилналтрексона также относятся, например, N-метилналтрексона бромид, N-метилналтрексона гидробромид, метилналтрексона бромид, метилналтрексона гидробромид, налтрексона метобромид, N-метилналтрексон, MNTX, SC-37359, MRZ-2663-BR и N-циклопропилметилнорокси-морфина метобромид. Метилналтрексон можно приобрести в порошковой форме в компании Mallinckrodt Pharmaceuticals, St. Louis, Mo., где его выпускают в виде белого кристаллического порошка, хорошо растворимого в воде. Температура плавления метилналтрексона составляет 254-256°С. Согласно некоторым вариантам реализации изобретения составы содержатся во флаконе. Согласно некоторым вариантам реализации изобретения, состав содержится во флаконе, содержащем стандартную дозу метилналтрексона. Согласно указанным вариантам реализации состав может содержать примерно от 0.5 мг до примерно 200 мг бромида метилналтрексона. Согласно некоторым вариантам реализации изобретения, стандартная доза может содержать от примерно 1 мг до примерно 80 мг, от примерно 5 мг до примерно 40 мг, или от примерно 8 мг до 12 мг, от примерно 18 мг до примерно 24 мг.
[0031] Метилналтрексон имеет хиральные центры и, следовательно, может встречаться в виде стереохимических изомеров при размещении заместителей у этих хиральных центров. Указанные стереохимические изомеры относятся к соединениям, подходящим для применения в настоящих составах. Соединения, применяемые в композициях и способах согласно настоящему изобретению, могут представлять собой индивидуальные стереоизомеры, а также смеси стереоизомеров. Согласно некоторым аспектам в способах, предлагаемых в настоящем изобретении, применяют соединения, которые по существу представляют собой чистые стереоизомеры. Предполагается, что композиции, предлагаемые в настоящем изобретении, также включают все таутомеры.
[0032] Применяемые в настоящем документе термины "R" и "S" обычно используют в номенклатуре органической химии для обозначения определенной конфигурации хирального центра. Термин "R" относится к "правовращающим изомерам" и применяется для обозначения конфигурации хирального центра, в котором, если смотреть вдоль связи по направлению к группе с самым низким старшинством, группы располагаются по старшинству по часовой стрелке (от самого высокого старшинства к самому низкому). Термин "S" или "левовращающий изомер" применяют для обозначения конфигурации хирального центра, в котором, если смотреть вдоль связи по направлению к группе с самым низким старшинством, группы располагаются по старшинству против часовой стрелки (от самого высокого старшинства к самому низкому). Старшинство групп основано на их атомном номере (самый тяжелый изотоп является первым). Неполный перечень групп с различным старшинством и обсуждение стереохимии приведены в книге: The Vocabulary of Organic Chemistry, Orchin, et a!., John Wiley and Sons Inc., page 126 (1980), содержание которой полностью включено в настоящее описание посредством ссылки.
[0033] Согласно некоторым вариантам реализации изобретения отдельные R-N изомеры метилналтрексона можно применять в составах и способах. Применяемое в настоящем документе обозначение "R-N-изомер" метилналтрексона относится к указанным соединениям с (R) конфигурацией относительно атома азота. Отдельные изомерные соединения включают без ограничения R-N изомерные метилналтрексоновые соединения, описанные в заявке на патент США с серийным номером 11/441395, поданной 25 мая 2006 года, опубликованной под номером WO 2006/127899, содержание которой включено в настоящий документ посредством ссылки. Согласно некоторым вариантам реализации изобретения, активное соединение представляет собой R-N изомер метилналтрексона или его соль. R-N изомер метилналтрексона, как было показано в USSN 11/441395, представляет собой опиоидный антагонист.
[0034] Согласно некоторым вариантам реализации изобретения отдельные S-N изомеры метилналтрексона можно применять в составах и способах. Применяемое в настоящем документе обозначение "S-N-изомер" метилналтрексона относится к указанным соединениям с (S) конфигурацией относительно атома азота. Отдельные изомерные соединения включают без ограничения S-N изомер соединений метилналтрексона, описанный в заявке на патент США, с серийным номером 11/441452, поданной 25 мая 2006 года, опубликованной под номером WO 2006/127898, содержание которой включено в настоящее описание посредством ссылки. Согласно некоторым вариантам реализации изобретения активное соединение представляет собой S-N изомер метилналтрексона или его соли. S-N изомер метилналтрексона, как было показано в USSN 11/441452, представляет собой опиоидный антагонист.
[0035] Согласно некоторым вариантам реализации изобретения составы на основе метилналтрексона, предложенные в настоящем изобретении, представляют собой смесь стереоизомеров, характеризующуюся действием опиоидного антагониста. Например, метилналтрексон может представлять собой смесь R-N и S-N метилналтрексона, так что сама смесь имеет эффект антагониста и может применяться в способах, описанных в настоящем изобретении для опиоидных антагонистов. В некоторых вариантах реализации изобретения применяют R-N метилналтрексон, который по существу не содержит S-N метилналтрексон.
[0036] Согласно некоторым вариантам реализации изобретения по меньшей мере примерно 99.6%, 99.7%, 99.8%, 99.85%, 99.9%, или 99.95% метилналтрексона находится в (R) конфигурации относительно атома азота. Способы определения количества (R)-N-изомера, присутствующего в пробе по сравнению с количеством (S)-N-изомера, присутствующего в той же самой пробе, подробно описаны в публикации W02006/127899, которая включена в настоящий документ посредством ссылки. Согласно другим вариантам реализации изобретения метилналтрексон содержит 0.15%, 0.10% или меньше (S)-N-изомера.
[0037] Точное количество метилналтрексона (или комбинации метилналтрексона и любого другого конкретного активного вещества), которое необходимо для достижения фармацевтически эффективного количества, варьируется в зависимости от конкретного субъекта, биологического вида субъекта, его возраста и общего состояния здоровья, степени тяжести побочных эффектов или заболевания, конкретного соединения (соединений), способа введения и т.п. Суммарная ежедневная доза метилналтрексона (например, бромида метилналтрексона), как правило, находится в диапазоне 10-200 мг, предпочтительно 20-100 мг, для взрослого человека массой 70 кг. Стандартный лекарственный состав согласно изобретению обычно содержит 1-250 мг активного соединения (например, бромида метилналтрексона) на дозу, 5-100 мг активного соединения на дозу, 10-50 мг активного соединения на дозу или примерно 8 мг или примерно 12 мг или примерно 24 мг активного соединения на дозу. Согласно некоторым вариантам реализации изобретения эффективное количество метилналтрексона для введения взрослому человеку массой 70 кг может содержать от примерно 10 мг до примерно 50 мг соединения (например, бромида метилналтрексона) на стандартную дозу, при введении один или несколько раз в день. Следует принимать во внимание, что диапазоны доз, приведенные выше, только дают представление о введении активного соединения взрослому человеку. Количество, которое следует ввести, например, ребенку или младенцу, может быть определено практикующим врачом или специалистом в данной области техники и может быть ниже или таким же, как при введении взрослому.
Составы
[0038] В настоящем изобретении предложены составы, обеспечивающие сохранность метилналтрексона без существенного образования продуктов разложения при хранении, в том числе хранении при комнатной температуре. Таким образом, предложенные составы способны обеспечивать улучшенные характеристики стабильности метилналтрексона при хранении. Например, согласно некоторым вариантам реализации изобретения состав содержит метилналтрексон, кальциевую соль хелатирующего агента, изотонический агент и носитель. Согласно некоторым вариантам реализации изобретения состав содержит метилналтрексон, кальциевую соль хелатирующего агента, изотонический агент, стабилизатор и носитель. Согласно некоторым вариантам реализации изобретения рН состава находится в интервале между примерно 2 и примерно 5.
[0039] В настоящем изобретении предложены составы и способы доставки метилналтрексона, обеспечивающие улучшенные характеристики при хранении и лучшую сохранность фармацевтических композиций на основе метилналтрексона. В частности, в настоящем изобретении предложены составы, которые являются стабильными и подоходят для парентерального введения композиций на основе метилналтрексона. Предложенные составы для парентерального введения могут включать стерильный раствор для инъекции, стерильную суспензию для инъекции, стерильные эмульсии и дисперсии.
[0040] Например, согласно некоторым вариантам реализации изобретения, составы содержат метилналтрексон и кальциевую соль хелатирующего агента в изотоническом растворе. Согласно некоторым вариантам реализации изобретения составы содержат метилналтрексон, кальциевую соль хелатирующего агента и стабилизатор в изотоническом растворе.
[0041] Как правило, предлагаемые составы содержат одно или несколько активных соединений вместе с одним или несколькими наполнителями, такими как, например, один или несколько хелатирующих агентов, ион кальция, изотонические вещества, носители, буферные вещества, вспомогательные растворители, разбавители, консерванты и/или поверхностно-активные вещества или их комбинации. Специалисту в данной области техники известно, что один и тот же ингредиент может иногда выполнять более одной функции или может выполнять различные функции в различных составах и/или частях составов в зависимости от количества ингредиента и/или присутствия других ингредиентов и/или активного соединения (соединений). Активное соединение может содержать от примерно 0.5 мг до примерно 200 мг бромида метилналтрексона. Согласно некоторым вариантам реализации изобретения активное соединение может содержать от примерно 1 мг до примерно 80 мг, от примерно 5 мг до примерно 40 мг, или примерно 8, или примерно 12 мг, примерно 16 мг, примерно 18 мг, или примерно 24 мг бромида метилналтрексона.
[0042] Согласно некоторым вариантам реализации изобретения состав содержит хелатирующий агент. Согласно некоторым вариантам реализации изобретения хелатирующий агент может присутствовать в составе в количестве от примерно 0.01 мг/мл до примерно 2 мг/мл или от примерно 0.1 мг/мл до примерно 1 мг/мл, или от примерно 0.2 мг/мл до примерно 0.8 мг/мл состава. Согласно некоторым вариантам реализации изобретения хелатирующий агент может присутствовать в составе в количестве от примерно 0.2 мг/мл, примерно 0.3 мг/мл, примерно 0.4 мг/мл, примерно 0.5 мг/мл, или примерно 0.6 мг/мл.
[0043] Авторами настоящего изобретения было обнаружено, что применение хелатирующего агента является эффективным для ингибирования образования по меньшей мере одного продукта разложения. Таким образом, добавление по меньшей мере одного хелатирующего агента является чрезвычайно полезным в составах, которые содержат метил налтрексон, и обеспечивает защиту от образования продуктов разложения, катализируемого металлами, и/или от выпадения осадка. Подходящие хелатирующие агенты включают любые фармацевти