Способ трансдермального переноса активных субстанций с использованием ниосом на основе пэг-12 диметикона
Иллюстрации
Показать всеИзобретение относится к медицине и косметологии и может быть использовано для эффективной трансдермальной доставки широкого спектра активных субстанций (АС). Заявлен способ трансдермальной доставки АС в составе ниосом, полученных из ПЭГ-12 диметикона, характеризующийся тем, что АС включаются в ниосомы при концентрации 10% путем гомогенизации на АПВ гомогенизаторе геля, содержащего 10% ниосом. Изобретение обеспечивает повышение трансдермального эффекта внутритканевой доставки АС в составе ниосом. 3 табл., 2 ил.
Реферат
Изобретение относится к медицине и косметологии и может быть использовано для доставки активных субстанций в ткани организма через кожные покровы без их механического повреждения и разрушения целостности липидного слоя эпидермиса.
Включение активных субстанций в ниосомы на основе ПЭГ-12 диметикона с обработкой на АПВ гомогенизаторе обеспечивает эффективную пролонгированную дозированную трансдермальную доставку активных субстанций в клетки тканей, не нарушая их целостности.
Ниосомы состоят из оболочки нерастворимого в воде двойного слоя неионогенного эмульгатора ПЭГ-12 диметикон, по структуре подобного строению элементарных биологических мембран и заключенного внутри капсулы и или ее стенки в зависимости от липофильности активной субстанции. Диметикон кополиолы, образующие ниосомы, представляют собой гипоаллергенные соединения кислорода, водорода, кремния и углерода. Наличие ковалентной связи Si-O_в гидрофобной части молекулы полидиметилсилоксановой основы эмульгатора, которая обладает большой эластичностью и реакционной способностью, позволяет направленно доставлять в ткани широкий спектр активных субстанций: антибиотиков, витаминов, растительных и животных экстрактов, низкомолекулярных пептидов при помощи реакционноспособных участков и целенаправленно их выпускать из везикулы.
Известен метод доставки БАВ с помощью силоксановых эмульгаторов (патент США - US Patent 5364633. Silicone vesicles and entrapment, 15/11/1994), сущность которого заключается во включении растворимого в воде БАВ в везикулы, сформированные из силоксанового поверхностно-активного вещества, предварительном растворении БАВ и вовлечении его в везикулу при добавлении силоксанового поверхностно-активного вещества, легкого перемешивания смеси, дальнейшего удаления избытка воды и БАВ.
Недостатком метода является слабая воспроизводимость везикул, сопровождающаяся образованием мицелл (неполноценных везикул с незначительным внутренним объемом), и, как следствие, недостаточное включение активных веществ в везикулы. Это сопровождается увеличением расхода силоксанового эмульгатора, что может привести к возможному раздражению кожного покрова и удорожанию целевого продукта.
В качестве ближайшего аналога может служить техническое решение, раскрываемое в патенте РФ 2383328, где для переноса активных веществ через кожу используются трансдермальные переносчики - ниосомы, представляющие комплексы амфифильных молекул ПЭГ 12 диметикона, окружающих активные компоненты. Прокладывая себе дорогу через эпидермальный барьер, переносчики тянут за собой БАВ. В качестве БАВ в геле используются экстракт стволовых клеток плаценты свиньи, гиалуроновая кислота, масло авокадо, концентрат Actiflow лаборатории SILAB (Франция), содержащий полисахариды и витамин PP. Содержание ниосом на основе ПЭГ 12 диметикона в составе геля составляет 10-30 масс.%.
Недостатком прототипа является невысокий процент включения активных субстанций из-за их высокой молекулярной массы, большой разброс величин ниосом - от 10 до 10000 нм, что делает невозможным преодоление кожного барьера для крупных молекул, затрудняет стандартизацию конечного продукта, приводит к снижению терапевтической эффективности и дополнительным затратам.
Целью изобретения является повышение трансдермального эффекта внутритканевой доставки активных субстанций в составе ниосом. Поставленная цель достигается применением АПВ гомогенизатора, позволяющего получить низкомолекулярные компоненты.
По отношению к прототипу, заявляемое изобретение отличает то, что полученные из ПЭГ-12 диметикона ниосомы имеют высокий трансдермальный эффект за счет использования АПВ гомогенизатора (APV Lab Series Homogenizers). Это увеличивает процент включения активных субстанций (АС) и стандартизирует размер ниосом, что в итоге позволяет повысить эффективность трансдермальной внутритканевой доставки.
Сущность изобретения
Ниосомы, полученные из ПЭГ-12 диметикона с включенными во внутренний объем активными субстанциями с помощью АПВ гомогенизатора, представляют собой полноценные мультиламеллярные структуры стандартного размера от 20 до 100 нм (рис.1), включающие высокий процент иммобилизованных АС, стабильные при хранении.
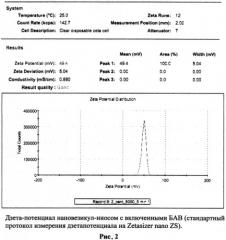
Стабильность кремнийорганических частиц против агломерации в значительной степени зависит от электростатической устойчивости, обусловленной значением дзета-потенциала больше, чем +30 mV или ниже -30 mV. Величины дзета-потенциалов образцов ниосом, определенные на Zetasizer nano ZS, составили диапазон от 49,4 mV до 54,6 mV (рис.2). Предложенный метод обладает хорошей воспроизводимостью и высоким процентом включения активных субстанций в ниосомы на основе ПЭГ-12 диметикона.
Осуществление изобретения
В качестве АС для инкапсулирования в ниосомы на основе ПЭГ-12 диметикона возможно использовать различные фармакологические субстанции, экстракты растительного и животного происхождения. В качестве примеров показана возможность достижения технического результата при инкапсулировании в различных композициях дигидрокверцетина, экстракта коры дуба, клеток плаценты животного происхождения, аскорбиновой кислоты, токоферола ацетата.
Для осуществления способа предлагается использовать гель, содержащий ниосомы для лечения и профилактики пародонтоза. Многонаправленность действия геля позволяет не только убирать внешние проявления пародонтоза, но и бороться с причинами, вызвавшими это заболевание. Ниосомы, полученные из ПЭГ-12 диметикона с включенными во внутренний объем дигидрокверцетином, экстрактом коры дуба и экстрактом клеток плаценты животного происхождения с помощью АПВ гомогенизатора, представляют собой полноценные мультиламеллярные структуры стандартного размера от 20 до 100 нм. Использование кремнийорганических наноконтейнеров - ниосом, позволяет доставить активные субстанции в глубокие слои пародонта, а не работать локально на поверхности поврежденной слизистой полости рта.
Объективно оценить состояние пародонта у больных ОХГКГ до лечения позволило изучение показателей индексов: ПМА, ПИ, CPITN, ИГ. Среднее значение показателя индекса ПИ (0.96±0.12) характеризовало наличие воспалительного процесса в десне. Показатель ПМА (18.52±2.04) отражал преимущественную локализацию воспалительного процесса в десневых сосочках и маргинальной части десны. Индекс CPITN (0.98±0.17) свидетельствовал о нуждаемости в лечебных мероприятиях, в выполнении правил гигиены по уходу за полостью рта и местной медикаментозной терапии. Среднее значение ИГ (1.84±0.39) характеризовало общее гигиеническое состояние полости рта пациентов как удовлетворительное.
| Таблица 1 | |||||
| Значения пародонтальных индексов до и после применения стоматологических средств | |||||
| Подгруппа 1 | Стоматологические средства | Пародонтальные индексы | |||
| ПМА % | ПИ | CPITN | ИГ (баллы) | ||
| до лечения | |||||
| 18,52±2,04 | 0,96±0,12 | 0,98±0,17 | 1,84±0,19 | ||
| непосредственно после лечения | |||||
| 0,05% р-р хлоргексидина | 4,87±0,26* | 0,37±0,05* | 0,23±0,06* | 1,24±0,06* | |
| 2 | 5% настойка эвкалипта | 11,73±1,21* | 0,55±0,16* | 0,26±0,45* | 1,31±0,18* |
| 3 | ниосомальный гель с АС, изготовленный при механическом встряхивании | 2,48±0,42* | 0,14±0,03* | 0,15±0,02* | 1,16±0,05* |
| 4 | ниосомальный гель с АС, изготовленный при АПВ гомогенизации | 0,46±0,07* | 0,04±0,01* | 0,06±0,01* | 1,04±0,03* |
| *Р≤0,05 по сравнению с данными до лечения. |
Индексная оценка пародонта непосредственно после лечения больных исследуемыми препаратами показала, что достоверным преимуществом обладал ниосомальный гель с АС, изготовленный при АПВ гомогенизации, применение которого не только быстро устраняло признаки воспаления, но и улучшало гигиеническое состояние пародонта.
Наиболее высокая терапевтическая активность наблюдалась у геля с 10% содержанием ниосом, имеющего в своем составе дигидрокверцетин 1% и экстракт коры дуба 0,5%.
Примерами переноса гидрофильных и липофильных АС с помощью ниосом на основе ПЭГ-12 диметикона, служат 5% раствор аскорбиновой кислоты и 5% масляный раствор токоферола ацетата. Эти компоненты могут применяться в качестве антиоксидантов для профилактики повреждающего действия на организм и лечения осложнений при комбинированном лечении онкологических больных.
1.1. Фаза А приготавливается при комнатной температуре путем механического перемешивания компонентов в смесителе.
Изготовление фазы Б производится путем добавления 2% ПЭГ-12 диметикона к 5% раствору аскорбиновой кислоты в отдельной емкости. Процесс проводят при комнатной температуре и интенсивном механическом встряхивании на шейкере, в течение 5 минут. Фазу Б, содержащую 5% ниосом, вносят в фазу А при перемешивании. Для стабилизации концентрации водородных ионов (pH) до 6,6-7,0 и формирования структуры геля вносят фазу Г. Образовавшийся в результате гель обрабатывают на АПВ гомогенизаторе APV Lab Series Homogenizers - 1000 (Фаза Д).
1.2. Выполняется аналогично примеру 1, только ниосом вносится в количестве 10%.
1.3. Выполняется аналогично примеру 1, только ниосом вносится в количестве 15%.
Фазы приготовления и рецептура геля с аскорбиновой кислотой представлены в таблице 2.
| № п/п | Таблица 2 | |
| Фазы приготовления и рецептура геля с аскорбиновой кислотой | ||
| Наименование ингредиента | Содержание в % (по массе) | |
| Фаза А | ||
| 1 | Дистиллированная вода | до 100 |
| 2 | Консервант | 0,05 |
| 3 | Гелеобразователь | 2,5 |
| 4 | Отдушка | 0,15 |
| 5 | Гиалуроновая кислота | 0,1 |
| Фаза Б | ||
| 6 | Ниосомы, содержащие аскорбиновую кислоту | 5,10,15 |
| Фаза Г | ||
| 7 | Триэтаноламин | 2,0 |
| Фаза Д | ||
| 8 | Обработка геля на АПВ гомогенизаторе |
2. Способ трансдермального переноса липофильных активных субстанций по п.1, отличающийся тем, что они предварительно смешиваются в отдельной емкости с ПЭГ-12 диметиконом.
На примере липофильной доставляемой активной субстанции в качестве образца мы использовали 5% масляный раствор токоферола ацетата.
2.1. Фаза А приготавливается при комнатной температуре путем механического перемешивания компонентов в смесителе.
Изготовление фазы В отличается предварительным смешиванием 2% ПЭГ-12 диметикона с 5% масляным раствором токоферола ацетата в отдельной емкости и только затем добавлением дистиллированной воды. Процесс проводят при комнатной температуре и интенсивном механическом встряхивании на шейкере в течение 5 минут. Фазу В, содержащую 5% эмульсию ниосом, вносятся в фазу А при перемешивании. Для стабилизации концентрации водородных ионов (pH) до 6,6-7,0 и формирования структуры геля вносят фазу Г. Образовавшийся в результате гель эмульгируют на АПВ гомогенизаторе APV Lab Series Homogenizers - 1000 (Фаза Д).
2.2. Выполняется аналогично примеру 1, только эмульсия ниосом на основе ПЭГ-12 диметикона вносится в количестве 10%.
2.3. Выполняется аналогично примеру 1, только ниосом на основе ПЭГ-12 диметикона вносится в количестве 15%.
Фазы приготовления и рецептура геля с масляным раствором токоферола ацетата представлены в таблице 3.
| Таблица 3 | |
| Фазы приготовления и рецептура геля с токоферолом ацетата | |
| № п/п | Фазы приготовления и рецептура геля с токоферолом ацетата |
| Наименование ингредиента | Содержание в % (по массе) | |
| Фаза А | ||
| 1 | Дистиллированная вода | до 100 |
| 2 | Консервант | 0,05 |
| 3 | Гелеобразователь | 2,5 |
| 4 | Отдушка | 0,15 |
| 5 | Гиалуроновая кислота | 0,1 |
| Фаза В | ||
| 7 | Ниосомы, содержащие липидную фракцию (5% масляного раствора токоферола ацетата) | 5,10,15 |
| Фаза Г | ||
| 8 | Триэтаноламин | 2,0 |
| ФазаД | ||
| 9 | Обработка геля на АПВ гомогенизаторе |
В ходе проведенных исследований по формированию гелей с содержанием ниосом 5, 10 и 15% экспериментальным путем установлено, что наибольшей стабильностью обладают композиции с 10% содержанием ниосом на основе ПЭГ-12 диметикона (Государственная фармакопея СССР, XI издание, Выпуск 2).
Наиболее высокий процент включения водорастворимых соединений: 60-82% и жирорастворимых соединений в ниосомы: 78-91%, определялся титрометрически (Государственная фармакопея СССР, XI издание. Выпуск 2) и наблюдался при концентрации активных соединений 10% после воздействия АПВ гомогенизатора.
Способ трансдермальной доставки активных субстанций (АС) в составе ниосом, полученных из ПЭГ-12 диметикона, характеризующийся тем, что АС включаются в ниосомы при концентрации 10% путем гомогенизации на АПВ гомогенизаторе геля, содержащего 10% ниосом