Электрохимический способ получения порошка гексаборида кальция
Иллюстрации
Показать всеИзобретение относится к электрохимическому способу получения порошка гексаборида кальция, включающему электролиз солевого расплава, содержащего кальций- и борсодержащие компоненты. Способ характеризуется тем, что используют солевой расплав, содержащий хлорид кальция с добавками оксида кальция и борного ангидрида при суммарной концентрации добавок 6÷7 мас.%, в процессе электролиза поддерживают массовое соотношение борного ангидрида к оксиду кальция 3,72±0,01 мас.%, электролиз ведут в интервале температур 800÷850°C, с начальным импульсом плотности катодного тока 0,50 А/см2 в течение 1,5 сек, а далее при постоянной величине тока 4,5 А и плотности тока 0,10 А/см2 в течение 1,5÷3 часов. Предлагаемый способ позволяет получать целевой продукт прямым электрохимическим осаждением гексаборида кальция на катоде, имеет повышенный выход по току при упрощенной технологии получения целевого продукта. 2 пр., 2 ил.
Реферат
Изобретение относится к получению порошковых боридов, в частности к получению порошкового гексаборида кальция (СаВ6) с размером частиц 3÷45 мкм, который может быть использован в сильноточной электронике для изготовления катодов - термоэмиттеров высокой мощности, а также в качестве матрицы композиционного анодного материала в химических источниках тока.
Известен способ получения порошкообразного гексаборида кальция, в котором порошковую смесь бора и карбоната кальция с размером частиц 50÷60 мкм подают в струю аргоно-азотно-водородной плазмы с температурой 5600÷6000°C, где в течение очень короткого времени происходит термосинтез борида кальция SU 1810298, опубл. 23.04.1993 [1]. Синтезированный продукт собирают в охлаждаемом конденсаторе, средний размер полученных частиц 95÷110 нм. Согласно данному способу синтез борида происходит в газовой фазе. Способ имеет высокую производительность, однако требует высоких температур, сложного оборудования, а также порошкового элементарного бора, стоимость которого составляет сегодня от 8 до 12 тыс. руб/кг в зависимости от его чистоты. Исходя из этого, затраты на производство единицы массы целевого продукта будут очень высокими.
Известен способ получения порошкообразного гексаборида кальция термическим восстановлением карбоната кальция (CaCO3) элементарным бором при температуре 1400÷1500°C с последующим механическим размолом полученного спеченного продукта и водной отмывкой порошка борида (Высокотемпературные бориды. Серебрякова Т.И., Неронов В.А., Пешев П.Д. - М: Металлургия. Челябинское отделение. 1991) [2]. Способ требует высоких температур и механического размола спеченного продукта, где продукт загрязняется примесями с дробящих тел и стенок мельницы.
На снижение температуры синтеза, повышение выхода целевого продукта, на использование менее дорогих реактивов направлен электрохимический способ получения порошкообразного гексаборида кальция (CN 102242371, опубл. 16.11.2011) [3], который может быть принят в качестве прототипа к заявленному способу. Данный способ осуществляют в два этапа. На первом этапе порошки кальций- и борсодержащего сырья в заданном атомном соотношении кальция к бору 1:6 тщательно смешивают, смесь загружают в воду, полученную взвесь нагревают с перемешиванием при температуре 80÷100°C в течение 2 часов. В течение этого времени происходит гидротермальный синтез бората кальция примерного валового состава CaC6O10 с выпадением его в осадок. Осадок отделяют от воды фильтрованием, подсушивают до сыпучего состояния и прессуют в таблетки диаметром ≈5 и толщиной ≈3 мм. Полученные таблетки спекают в муфельной печи при температуре 650°C в течение 3 часов, их остаточная пористость находится в пределах 20÷30%. Подготовленные таким образом таблетки пористого бората кальция помещают в проволочную корзину, подвешенную на молибденовом стержне-токоподводе.
На втором этапе в электрохимическом реакторе наплавляют эвтектическую смесь солей CaCl2-NaCl, опускают в этот расплав корзину с таблетками бората кальция на токоподводе (катод), сверху на небольшую глубину погружают анод из спеченного диоксида олова (SnO2) и включают постоянный ток электролиза. Состав расплавленного электролита позволяет вести процесс электролиза в области температур 520÷700°C. Растворимость бората кальция в расплаве CaCl2-NaCl при указанных температурах ничтожно мала, поэтому ионы В3+ в расплаве практически отсутствуют, что препятствует осуществлению электрохимического способа получения гексабората кальция, как целевого продукта по следующим причинам. Поскольку твердый борат кальция (в таблетках) не проводит электрический ток, т.е. является изолятором, он не может быть восстановлен электрохимически на катоде, поэтому его восстанавливают химически, то есть кальцием, выделяющимся на металлической проволоке корзины - катода в ходе электролиза. Таким образом, электролиз в данном случае нужен лишь для постоянного воспроизводства восстановителя - кальция, растворенного в солевом расплаве.
Механизм восстановления неэлектропроводных оксидов при электролизе расплавов на основе хлорида кальция (кембриджский процесс) известен (Н.И. Шуров, Ю.П. Зайков, А.П. Храмов, В.А. Ковров, А.В. Суздальцев. Физическая химия и электрохимия расплавленных и твердых электролитов: Доклады XVI Российской конференции, Екатеринбург, Изд. Уральского Федерального Университета. 2013. С.399-402) [4]. Недостатком подобных процессов вторичного восстановления оксидов является их очень малая скорость и низкий выход целевого продукта по количеству затраченного электричества, редко превышающий 25÷30%. Это обусловлено тем, что активный восстановитель - кальций, растворенный в солевом расплаве, бесполезно расходуется на окисление кислородом на межфазной границе воздух - солевой расплав и на другие побочные реакции, например, с графитовым контейнером для солевого расплава.
По этим причинам способ по прототипу не может иметь высокую производительность, максимальный выход целевого продукта по количеству затраченного электричества не должен превышать 30%.
Нужно отметить кроме того, что согласно способу по CN 102242371 получают ультрадисперсный (субмикронный) порошок CaB6 для применения в химических источников тока. Ультрадисперсный порошок CaB6 весьма неудобен в работе из-за его потерь в виде пыли при технологических операциях взвешивания, фасовки, прессовки и т.д. Субмикронные порошки многократно труднее очистить от примесей, чем порошки с микронными размерами кристаллов. Аэрозоли таких порошков вредны для человеческого организма.
Задача настоящего изобретения заключается в повышении производительности процесса получения чистого микроразмерного порошка гексаборида кальция при снижении финансовых затрат и энергетических ресурсов на его получение, а также в расширении сферы применения порошка.
Для решения поставленной задачи предложен электрохимический способ получения порошка гексаборида кальция, включающий электролиз солевого расплава, содержащего кальций- и борсодержащие компоненты, при этом используют солевой расплав, содержащий хлорид кальция с добавками оксида кальция и борного ангидрида при суммарной концентрации добавок 6÷7 мас.%, в процессе электролиза поддерживают массовое соотношение борного ангидрида к оксиду кальция 3,72±0,01, электролиз ведут в интервале температур 800÷850°C с начальным импульсом плотности катодного тока 0,50 А/см2 в течение 1,5 сек, а далее при постоянной величине тока 4,5 А и плотности тока 0,10 А/см2 в течение 1,5÷3 часов.
В отличие от прототипа в заявленном способе в начале процесса в электролизную ванну загружается не эвтектическая смесь солей CaCl2-NaCl, как в прототипе, а индивидуальная обезвоженная соль хлорид кальция CaCl2. Это обусловлено тем, что в индивидуальном хлориде кальция растворимость добавки B2O3 в присутствии другой добавки CaO многократно увеличивается, достигая их суммарной концентрации 6% при 800°C и 7% при 850°C.
Применение температур электролиза в пределах 800÷850°C вызвано необходимостью достаточно быстрого растворения в расплавленном электролите указанных реактивов с одновременной диссоциацией на ионы. При этом нижний предел температуры ограничен температурой плавления хлорида кальция (772°C), а перегрев расплава над температурой плавления соли должен быть не менее 20° для успешного ведения электролиза. Верхний предел температуры обусловлен тем, что при более высокой, чем 850°C температуре быстро возрастает летучесть расплава с потерей CaCl2 в виде паров, а также ценного борсодержащего компонента в виде пара BOCl. Подача на катод импульса повышенной плотности тока (0,50 А/см2) в течение 1,5÷2 сек в начале процесса нужна для мгновенного формирования большого количества наноразмерных зародышей СаВ6 - центров роста будущих кристаллов. В совокупности с последующим режимом электролиза в виде постоянной величины тока 4,5 А и плотности тока 0,10 А/см2 в течение 1,5÷3 часов в интервале температур 800÷850°C этот технологический прием позволяет получить порошок гексаборида кальция с размером частиц от 3 до 45 мкм.
Таким образом, электролиз в заявленном способе применяют не для воспроизводства восстановителя - кальция, растворенного в солевом расплаве, как это следует из описания процесса в прототипе, а по его основному назначению, то есть для прямого электрохимического осаждения гексаборида кальция на катоде. При этом выход продукта по затраченному количеству электричества составляет около 80%. Поскольку способ позволяет получить гексаборид кальция прямым электрохимическим осаждением на катоде, химическое восстановление бората кальция, описанное в прототипе, становится не нужным. Это позволяет получать порошок гексабората кальция в один этап, без подготовки кальций- и борсодержащего сырья, включающего изготовление прессованных и обожженных таблеток бората кальция, как это делают в прототипе. Размер кристаллов порошка, полученного заявленным способом больше, чем у полученного в прототипе, однако это не является недостатком способа. В применении к изготовлению катодов для сильноточной электроники предпочтителен микроразмерный порошок гексаборида кальция.
Технический результат заявляемого изобретения заключается в прямом электрохимическом осаждении гексаборида кальция на катоде, повышении выхода по току при упрощении технологии получения целевого продукта.
Способ осуществляли следующим образом. В качестве кальций- и борсодержащих компонентов использовали:
- Хлорид кальция (CaCl2) технический, кальцинированный, гранулированный, ГОСТ 450 - 77 с изм. 1-3;
- Оксид кальция (CaO) марки «ч»;
- Борный ангидрид (B2O3) - плавленый, марки «ч», ТУ 6-09-17-249-88.
Наплавление ванны осуществляли следующим образом. Соль CaCl2 наплавляли в тигле при 850°C, сверху на расплав насыпали малыми порциями оксид кальция CaO, который растворяется в расплаве, затем порциями насыпали гранулы B2O3, которые по мере нагревания растворялись в расплаве CaCl2. После полного растворения B2O3 солевой расплав обычно становится прозрачным. В процессе наплавления и в ходе всего электролиза поддерживали соотношение борного ангидрида к оксиду кальция 3,72±0,01 мас.%.
При проведении электролиза в качестве электродов использовали круглые графитовые стержни. Рабочую часть анода и катода опускали в расплав, выше уровня расплава их защищали от окисления воздухом алундовыми трубками.
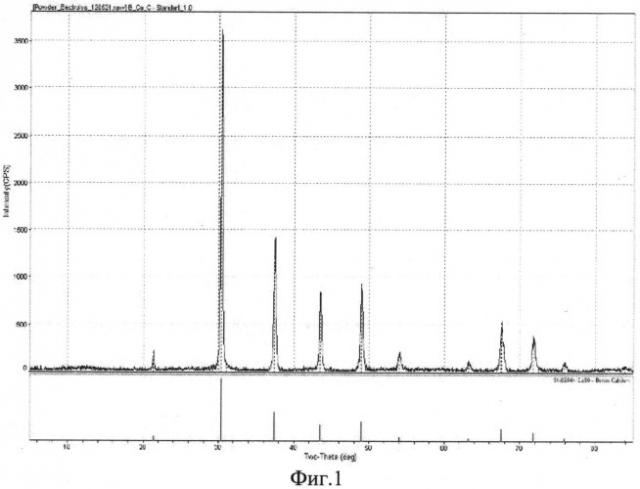
Фазовый состав порошков CaB6 определяли с помощью рентгеновского дифрактометра Rigaku D/Мах - 2000, гранулометрический состав исследовали на лазерном дифракционном анализаторе Malvern Mastersizer 2000.
Пример 1. В корундовом тигле при температуре 850°C было наплавлено 800 г расплава хлорида кальция, на который сверху был засыпан оксид кальция, а затем оксид бора из расчета их суммарной концентрации 5 мас.%, остальное - хлорид кальция. После 10 мин выдержки в расплав были опущены графитовые анод и катод. Вначале проводили очистной электролиз расплава в течение 30 мин для удаления растворенной воды. Далее электролиз по получению CaB6 вели при температуре 850°C с начальным импульсом плотности катодного тока ik=0,50 А/см2 в течение 1,5 сек, а затем при постоянной величине тока 4,5 А и плотности тока ik=0,10 А/см2 в течение 1,5 часов.
После окончания электролиза катод с осадком вынимали из расплава и после остывания до комнатной температуры помещали в стеклянный стакан с кипящей дистиллированной водой, в котором осадок отмывали от остатков соли. Далее осадок смывали в воронку на бумажный фильтр и дополнительно промывали разбавленной соляной кислотой, затем дистиллированной водой и спиртом. После этого промытый осадок вместе с фильтром сушили в сушильном шкафу при температуре 50°C. После снятия с фильтра получали мелкодисперсный порошок темно-коричного цвета массой 1,1 г. На фиг.1 приведена рентгеновская дифрактограмма полученного катодного осадка. Рентгенофазовый анализ показал, что порошок представляет собой чистый гексаборид кальция CaB6. Элементный химический анализ показал наличие примесей алюминия и железа, суммарное содержание которых составляет 2,5 мас.%. Поскольку кристаллическая решетка CaB6 не искажена (см. фиг.1), можно предполагать, что примеси железа и алюминия находились на поверхности кристаллов CaB6 вероятнее всего в форме гидроксидных пленок наноразмерной толщины; после дополнительной промывки порошка разбавленной соляной кислотой и водой был получен порошок CaB6 чистотой 99,8%. На фиг.2 показан гранулометрический состав полученного порошка CaB6. Гранулометрический анализ показал, что средний размер его кристаллов в поперечнике находится в диапазоне 3÷15 мкм. Теоретическая масса CaB6, вычисленная по закону Фарадея, должна быть 1,323 г, а в действительности получено 1,100 г. Таким образом, выход продукта по затраченному количеству электричества 6,75 А*час равен 83,1%. Производительность процесса 0,73 г/час.
Пример 2. Опыт проведен в том же технологическом регламенте, что в примере 1, но температура опыта составляла 800°C. Средний размер полученных кристаллов находится в диапазоне от 8 до 45 мкм при той же производительности процесса, что и в примере 1.
В описании к способу по CN 102242371 не приведены такие важнейшие базовые характеристики процесса как катодная плотность тока (А/см2), характеризующая интенсивность процесса, выход целевого продукта по току (в %), характеризующий энергоэффективность процесса, производительность процесса (г продукта/час электролиза) также не указана. По этой причине прямое сравнение результатов известного и заявленного способов невозможно. Однако косвенно на меньшую производительность процесса по прототипу указывает его большая длительность (от 10 до 20 часов) вместо 1,5÷3,0 часов у заявленного способа. Из опубликованных данных других авторов известно, что выход по току в подобных процессах не более 25÷28%. В заявленном способе он в три раза выше. Из этих данных следует вывод, что заявляемый способ имеет значительно меньшие удельные энергозатраты на производство единицы массы целевого продукта - гексаборида кальция. Кроме того, отсутствие технологических операций по приготовлению кальций- и борсодержащего сырья в виде таблеток бората кальция исключают дополнительные затраты энергии и трудозатраты.
Таким образом, заявленный электрохимический способ получения чистого порошка гексаборида кальция имеет более высокую производительность при снижении финансовых затрат и энергетических ресурсов, а полученный заявленным способом порошок имеет расширенную сферу применения.
Электрохимический способ получения порошка гексаборида кальция, включающий электролиз солевого расплава, содержащего кальций- и борсодержащие компоненты, отличающийся тем, что используют солевой расплав, содержащий хлорид кальция с добавками оксида кальция и борного ангидрида при суммарной концентрации добавок 6÷7 мас.%, в процессе электролиза поддерживают массовое соотношение борного ангидрида к оксиду кальция 3,72±0,01 мас.%, электролиз ведут в интервале температур 800÷850°C, с начальным импульсом плотности катодного тока 0,50 А/см2 в течение 1,5 сек, а далее при постоянной величине тока 4,5 А и плотности тока 0,10 А/см2 в течение 1,5÷3 часов.