Флуорохромный материал и способ его применения
Иллюстрации
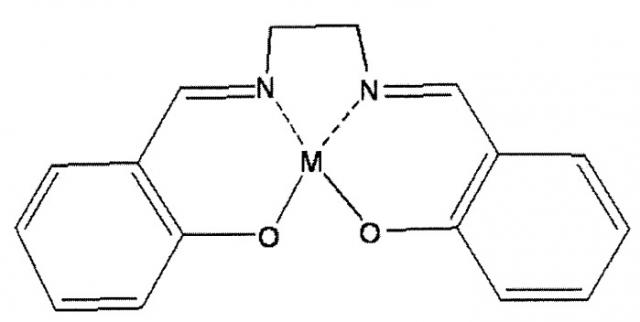
Показать всеИзобретение может быть использовано в медицине в качестве противоопухолевого лекарственного средства. Флуорохромный материал содержит комплекс металл-сален, представленный формулой
,
где М представляет собой железо, а пик люминисцентной длины волны около 380 нм. Способ введения флуорохромного материала индивидууму включает внешнее приложение магнитного поля индивидууму для направления материала к целевой области и затем применение внешнего света к целевой области, что позволяет материалу стать люминесцентным. Изобретение позволяет расширить применение комплекса железо-сален и использовать его как противоопухолевое лекарственное средство для индивидуумов. 2 н. и 3 з.п. ф-лы, 2 ил.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к флуорохромному материалу, полученному из комплекса металл-сален, и способу применения флуорохромного материала.
Уровень техники
Обычно, когда лекарственное средство вводится в живой организм, оно достигает пораженного участка и проявляет свои фармакологические эффекты на этом пораженном участке, тем самым проявляя свои терапевтические эффекты. С другой стороны, даже если лекарственное средство достигает ткани, иной, чем пораженный участок (другими словами, нормальной ткани), оно не будет терапевтическим.
Следовательно, является важным направить лекарственное средство на пораженный участок. Методика направления лекарственного средства к пораженному участку называется доставкой лекарственного средства, которая активно изучается и разрабатывается в последнее время. Эта доставка лекарственного средства имеет по меньшей мере два преимущества.
Одним преимуществом является то, что на пораженном участке ткани может быть получена достаточно высокая концентрация лекарственного средства. Фармакологические эффекты не будут наблюдаться до тех пор, пока концентрация лекарственного средства на пораженном участке не будет постоянным значением или большим. Терапевтические эффекты не могут быть ожидаемыми, если концентрация низкая.
Вторым преимуществом является то, что лекарственное средство направляется только к пораженному участку ткани, и, следовательно, побочные реакции в отношении нормальной ткани могут быть подавлены.
Такая доставка лекарственного средства является наиболее эффективной для лечения рака противоопухолевыми агентами. Большинство противоопухолевых агентов подавляет клеточный рост раковых клеток, которые активно делятся, так что противоопухолевые агенты будут также подавлять клеточный рост даже нормальной ткани, в которой клетки активно делятся, такой как костный мозг, корни волос или слизистая пищеварительного тракта.
Следовательно, раковые пациенты, которым вводят противоопухолевые агенты, страдают от побочных реакций, таких как анемия, потеря волос и рвота. Поскольку такие побочные реакции накладывают тяжелые отпечатки на пациентов, необходимо ограничить дозировку, тем самым вызывая проблему невозможности достичь фармакологических эффектов противоопухолевых агентов.
Обобщенным наименованием для противоопухолевых агентов, обладающих способностью совмещать алкильную группу (-CH2-CH2-) с, например, аминокислотным белком, являются алкилирующие противораковые лекарственные средства среди таких антинеопластических лекарственных средств. Они алкилируют ДНК и ингибируют репликацию ДНК, вызывая смерть клеток.
Это действие работает независимо от клеточных циклов, также работает на клетках в периоде G0, имеет сильное влияние на клетки, которые активно растут и имеют склонность к повреждению, например костный мозг, слизистая пищеварительного тракта, зародышевые клетки или корни волос.
Более того, антиметаболитные антинеопластические лекарственные средства представляют собой соединения, имеющие структуры, подобные структурам нуклеиновых кислот или метаболитов в процессе синтеза белка, поражают клетки путем, например, ингибирования синтеза нуклеиновых кислот и специфично действуют на клетки митотического периода.
Кроме того, противоопухолевые антибиотики представляют собой химические вещества, полученные микроорганизмами, имеют воздействия, такие как ингибирование синтеза ДНК и разрыв нити ДНК, и проявляют противоопухолевую активность.
Также микротрубочные ингибиторы обладают противораковыми эффектами, непосредственно воздействующими на микротрубочки, которые играют важную роль в сохранении нормальных функций клеток, например, путем образования веретена в ходе деления клетки, локализации клеточных органелл и переноса веществ. Микротрубочные ингибиторы воздействуют на клетки, которые активно делятся, и нервные клетки.
Более того, лекарственное средство на основе платины ингибирует синтез ДНК путем образования нитей ДНК, межцепных связей или связей ДНК-белок. Представителем лекарственного средства является цисплатин, но он вызывает тяжелое повреждение почек и требует восполнения большого количества жидкости.
Кроме того, полученные из гормонов антинеопластические лекарственные средства являются эффективными против гормонозависимых опухолей. Женские гормоны или антиандрогенные лекарственные средства вводятся в андрогензависимый рак простаты.
Также молекулярно-направленные лекарственные средства представляют собой лечение, направленное на молекулы, которые соответствуют молекулярным биологическим характеристикам, специфичным для соответствующих злокачественных опухолей.
Более того, ингибиторы топоизомеразы представляют собой ферменты для временного образования разрывов в ДНК и изменения числа переплетений нитей ДНК. Ингибитор топоизомеразы I представляет собой фермент, который образует разрывы в одной нити кольцевой ДНК, позволяя другой нити проходить, и затем закрывает разрывы; а ингибитор топоизомеразы II временно разрывает обе две нити кольцевой ДНК, позволяя другим двум нитям ДНК проходить между прежними двумя нитями и восстанавливать разорванные нити.
Кроме того, неспецифичные иммуностимуляторы ингибируют увеличение раковых клеток путем активации иммунной системы.
Большинство противоопухолевых агентов ингибирует клеточный рост раковых клеток, которые активно делятся, так что противоопухолевые агенты будут также ингибировать клеточный рост даже нормальной ткани, в которой клетки активно делятся, такой как костный мозг, корни волос или слизистая пищеварительного тракта. Следовательно, раковые пациенты, которым вводятся противоопухолевые агенты, страдают от побочных реакций, таких как анемия, потеря волос и рвота.
Поскольку такие побочные реакции накладывают тяжелые отпечатки на пациентов, необходимо ограничить дозировку, тем самым вызывая проблему невозможности в достаточной степени достичь фармакологических эффектов противоопухолевых агентов. Кроме того, в наихудшем сценарии существует возможность, что пациенты могут умереть от побочных реакций.
Таким образом, ожидается ингибирование побочных реакций и проведение лечения рака эффективно путем направления противоопухолевых агентов к раковым клеткам посредством доставки лекарственного средства и предоставления противоопухолевым агентам возможности интенсивно проявлять фармакологические эффекты на раковые клетки. Местные анестетики имеют такую же проблему.
Местные анестетики используются для лечения местного зуда и болей, например, слизистой или кожи, вызванных геморроидальным заболеванием, стоматитом, пародонтитом, кариесом, удалением зуба или операциями. Лидокаин (название продукта: ксилокаин) известен как представитель местного анестетика; однако лидокаин является быстродействующим, но имеет антиаритмический эффект.
Кроме того, если лидокаин, который является анестетиком, инъецируется в спинномозговую жидкость при спинальной анестезии, лидокаин будет распространяться по спинномозговой жидкости; и в наихудшем сценарии есть опасность, что лидокаин может достигнуть цервикальной области спинного мозга и тем самым вызвать остановку дыхательной функции и привести к критическим побочным реакциям.
Таким образом, ожидается ингибирование побочных реакций и проведение лечения рака эффективно путем направления противораковых агентов к раковым клеткам посредством доставки лекарственного средства и предоставления противораковым агентам возможности интенсивно проявлять фармакологические эффекты на раковые клетки.
Кроме того, также ожидается предотвращение распространения местного анестетика, и достижение продолжительных медицинских эффектов, и снижение побочных реакций путем доставки лекарственного средства.
Примером конкретного способа доставки лекарственного средства является применение носителя. Это означает загрузку имеющего склонность к концентрированию на пораженном участке носителя лекарственным средством и принуждение носителя нести лекарственное средство к пораженному участку.
Перспективным кандидатом в качестве носителя является магнитное вещество, и существует предложенный способ прикрепления носителя, который является магнитным веществом, к лекарственному средству, позволяющий носителю накапливаться в пораженном участке посредством магнитного поля (см., например, патентную литературу 1).
Однако при использовании магнитного вещества в качестве носителя было обнаружено, что трудно перорально вводить магнитный носитель, молекулы носителя обычно огромные, и существуют технические проблемы в части силы связывания и сродства между носителем и молекулами лекарственного средства; и трудно изначально достигнуть практического применения магнитного носителя.
Таким образом, авторы настоящего изобретения предложили местный анестетик, в котором боковые цепи, дающие положительную или отрицательную плотность спинового заряда, связаны с основным скелетом органического соединения, и который в целом пригоден до такой степени, что местный анестетик направляется посредством участия магнита, внешним магнитным полем; и если местный анестетик применяется к телу человека или животному, он остается в области, где магнитное поле применяется местно посредством магнитного поля вне тела, и медицинские эффекты, которые местный анестетик изначально имеет, проявляются в этой области. В указанной выше публикации в качестве примера такого лекарственного средства описывается комплекс железо-сален (см. патентную литературу 2).
Также раскрыто противораковое лекарственное средство, содержащее комплекс железо-сален (см., например, патентную литературу 3).
Список ссылок
Патентная литература
Патентная литература 1. Опубликованная японская заявка на патент (Kokai) № 2001-10978;
Патентная литература 2. W02008/001851;
Патентная литература 3. Опубликованная японская заявка на патент (Kokai) № 2009-173631.
Сущность изобретения
Объектом настоящего изобретения является расширение применения комплекса железо-сален.
Для того чтобы достигнуть описанного выше объекта, настоящее изобретение представляет собой новый флуорохромный материал, содержащий нижеприведенную химическую формулу (I).
(N,N'-Бис(салицилиден)этилендиамин металл)
химическая формула (I)
Однако М представляет собой Fe (железо), Cr (хром), Mn (марганец), Co (кобальт), Ni (никель), Mo (молибден), Ru (рубидий), Rh (родий), Pd (палладий), W (вольфрам), Re (рений), Os (осмий), Ir (иридий), Pt (платину), Nd (ниобий), Sm (самарий), Eu (европий) или Gd (гадолиний).
В частности, соединение, где М является железом, излучает микроволновую фосфоресценцию в диапазоне от 300 нм до 500 нм. Следовательно, как описано в опубликованной японской заявке на патент (Kokai) № 2009-173631, комплексное соединение металл-сален может быть получено флуоресцентным, и пораженный участок ткани может быть визуально подтвержден путем введения комплексного соединения металл-сален, представленного химической формулой (I), в качестве противоопухолевого лекарственного средства индивидууму, такому как человек или животное, магнитно направляя его к целевой раковой ткани и затем облучая пораженный участок ткани лазерным светом или флуоресценцией при проведении операции для удаления пораженного участка ткани.
Что касается среднего диаметра частиц комплексного соединения металл-сален, чрезмерно большой диаметр частиц, возможно, может вызывать закупорку кровеносных сосудов соединением. С другой стороны, если диаметр частиц маленький, соединение, возможно, может терять свое магнитное свойство. Следовательно, подходящий средний диаметр частиц соединения составляет от 2 до 60 мкм, предпочтительно от 5 до 20 мкм, более предпочтительно от 8 до 15 мкм, особенно предпочтительно от 9 до 12 мкм и оптимально 10 мкм.
Диаметр частиц устанавливается в описанном выше диапазоне в ходе процесса перекристаллизации. Например, на стадии 7 синтеза, описанного далее, указывается, что «конечное вещество было перекристаллизовано из раствора диэтилового эфира и парафина», и целевой диаметр частиц может быть получен путем увеличения температуры вплоть до 80 градусов Цельсия сразу перед перекристаллизацией и затем охлаждения до комнатной температуры в течение 12 часов.
Результатом исследования авторов настоящего изобретения явилось изменение свойства намагничивания комплексного соединения металл-сален в зависимости от диаметра частиц. Если диаметр частиц слишком маленький, меньше, чем необходимо, свойство намагничивания комплексного соединения металл-сален является недостаточным; и если такое комплексное соединение металл-сален вводится индивидууму, такому как человек или животное, существует возможность, что комплексное соединение металл-сален может быть не доставлено к целевой области внешним магнитным полем. С другой стороны, если диаметр частиц слишком большой, больше, чем необходимо, существует возможность, что магнитные частицы могут агрегировать в кровеносных сосудах.
Как описано в опубликованной японской заявке на патент (Kokai) № 2009-173631, комплекс металл-сален, представленный химической формулой (I), пригоден в качестве противоопухолевого лекарственного средства, имеющего такое магнитное свойство, что, если оно вводится индивидууму без использования магнитного носителя и внешнее магнитное поле (например, 0,3 Т) затем применяется к индивидууму, молекулы направляются к области, к которой применяется магнитное поле.
Новый флуорохромный материал, содержащий химическую формулу (I), упомянутую выше, может быть получен в соответствии с настоящим изобретением, как объяснено выше.
Краткое описание чертежей
Фиг.1 представляет собой характеристическую диаграмму, показывающую результаты люминесцентного теста комплекса металл-сален.
Фиг.2 представляет собой характеристическую диаграмму, показывающую результаты измерения диаметра частиц комплекса металл-сален.
Подробное описание вариантов
Получение комплекса металл-сален (железо-сален)
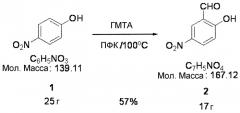
Стадия 1:
Смесь 4-нитрофенола (Соединение 1) (25 г, 0,18 моль), гексаметилентетрамина (25 г, 0,18 моль) и полифосфорной кислоты (200 мл) смешивали в течение одного часа при температуре 100 градусов Цельсия. Затем в эту смесь ввели 500 мл этилацетата и 1 л (литр) воды и перемешивали до полного растворения. Кроме того, когда добавили 400 мл этилацетата к этому раствору, раствор разделился на две фазы. Впоследствии водную фазу удалили из раствора, который разделился на две фазы; и оставшееся соединение дважды промыли основным растворителем и высушивали над безводным MgSO4. В результате синтезировали 17 г Соединения 2 (выход 57%).
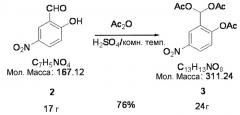
Стадия 2:
Соединение 2 (17 г, 0,10 моль), уксусный ангидрид (200 мл) и H2SO4 (минимально) перемешивали в течение одного часа при комнатной температуре. Конечный раствор смешивали в течение 0,5 часа в ледяной воде (2 л) до достижения гидролиза. Конечный раствор отфильтровывали и высушивали на воздухе, тем самым получая белый порошок. Порошок перекристаллизовывали с использованием растворителя, содержащего этилацетат. В результате получили 24 г Соединения 3 (выход 76%) в форме белых кристаллов.
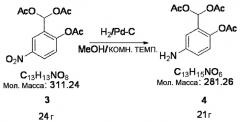
Стадия 3:
Смесь углерода (2,4 г) с нанесенным 10% палладием с Соединением 3 (24 г, 77 моль) и метанолом (500 мл) восстанавливали в течение ночи при 1,5 атм в водородной восстанавливающей среде. После завершения восстановления продукт фильтровали и получили 21 г Соединения 4 в виде коричневого масла.
Стадии 4, 5:
Соединение 4 (21 г, 75 ммоль) и ди(трет-бутил)дикарбонат (18 г, 82 ммоль) перемешивали в течение ночи в безводном дихлорметане (ДХМ) (200 мл) в атмосфере азота. Конечный раствор (Соединение 5) выпаривали в вакууме и затем растворяли в метаноле (100 мл). Затем добавили гидроксид натрия (15 г, 374 ммоль) и воду (50 мл) и раствор орошали в течение 5 часов. Затем раствор охлаждали, фильтровали, промывали водой и высушивали в вакууме, тем самым получая коричневое соединение. Конечный раствор дважды подвергали флэш-хроматографии с использованием силикагеля, тем самым получая 10 г Соединения 6 (выход 58%).
Стадия 6:
Соединение 6 (10 г, 42 ммоль) вводили в 400 мл безводного этанола, смесь орошали при нагревании и добавили несколько капель этилендиамина (1,3 г, 21 ммоль) в 20 мл безводного этанола при перемешивании в течение 0,5 часа. Смесь переместили в контейнер со льдом, где ее охлаждали и перемешивали в течение 15 минут. Затем ее промывали 200 мл этанола, фильтровали и высушивали в вакууме, тем самым получая 8,5 г (выход 82%) Соединения 7.
Стадия 7:
Соединение 7 (8,2 г, 16 ммоль) и триэтиламин (22 мл, 160 ммоль) вводили в обезвоженный метанол (50 мл) и раствор хлорида железа (III) (FeCl3) (2,7 г, 16 ммоль), добавленный к 10 мл метанола, перемешивали в течение одного часа в атмосфере азота при комнатной температуре, тем самым получая коричневое соединение. Коричневое соединение затем высушивали в вакууме.
Конечное соединение разбавляли 400 мл дихлорметана, промывали дважды основным раствором, высушивали в сульфате натрия (Na2SO4) и высушивали в вакууме. Конечное соединение перекристаллизовывали из раствора диэтилового эфира и парафина и при анализе с помощью высокоэффективной жидкостной хроматографии выявили 5,7 г (выход 62%) комплекса A (комплекс железо-сален) с чистотой 95% или выше.
Когда необходимо использовать металлический комплекс, отличный от комплекса железо-сален, хлорид металла, отличного от железа (MCl3: где М является металлом), может быть использован вместо хлорида железа (III) (FeCl3). Кстати, в японской заявке на патент № 2009-177112 заявителя настоящей заявки раскрывается, что комплекс марганец-сален, комплекс хром-сален и комплекс кобальт-сален, отличный от комплекса железо-сален, имеет такие магнитные свойства, что они могут быть направлены внешним магнитным полем. Затем, из опубликованной японской заявки на патент (Kokai) № 2009-173631 следует, что металлический комплекс железо-сален или подобный обладает противоопухолевым эффектом.
Тест на люминесценцию
Тест на люминесценцию посредством фотолюминесцентного измерения проводили в отношении комплекса железо-сален, представленного химической формулой (I).
Измерение проводили с использованием PHOTOLUMINOR-S для спектрального анализа высокого разрешения (производитель HORIBA, Ltd). Измерение проводили в состоянии, когда комплекс металл-сален был растворен в хлороформе.
Полученные результаты представлены на фиг.1. Ссылаясь на фиг.1 было подтверждено, что пик, характерный для комплекса железо-сален, представленного химической формулой (I), возникает около 380 нм. Кстати, пики подтверждались около 270 нм, 530 нм и 800 нм на фиг.1, но они представляют собой справочные пики для возбуждающего лазера (лазера, который испускает белый свет при колебании нескольких длин волн RGM в одно и то же время). Длина волны пика варьируется в зависимости от формы кристалла комплекса железо-сален.
Измерение диаметра частиц
Диаметр частиц комплекса железо-сален химической формулы (I) измеряли с использованием способа лазерной дифракции. Устройство, используемое для измерения, представляло собой приборы гранулометрического анализа Microtrac (MT-3000II, производитель NIKKISO CO., LTD.). Образец помещали в гексаметафосфат натрия; и конечный раствор диспергировали в течение 10 минут с использованием гомогенизатора, образец затем облучали лазерным светом и измеряли его дифракцию (рассеивание) для обнаружения сортировки. Условия измерения и результаты измерения следующие.
Условия измерения
Время измерения: 30 секунд
Проницаемость частиц: проницаемые
Форма частиц: несферическая
Показатель преломления частиц: 1,81
Растворитель: вода
Показатель преломления растворителя: 1,333
Результаты измерения
Результаты измерения показаны на фиг.2 и ниже.
Средний диаметр частиц: 11,79 мкм
Стандартное отклонение: 6,289
Результатом измерения явилось обнаружение того, что диаметр частиц комплекса железо-сален составил 11,8 мкм, что достаточно подходит для применения к индивидуумам.
Если комплекс металл-сален способен излучать флуоресцентный цвет, такой как вышеупомянутый, комплекс железо-сален вводится индивидууму, магнитное поле прикладывается извне к индивидууму для направления комплекса металл-сален к целевой области, и внешний свет затем применяется к целевой области, как объяснено выше, может быть подтверждена люминесценция комплекса металл-сален.
1. Флуорохромный материал, содержащий комплекс металл-сален, где комплекс металл-сален представлен следующей химической формулой (I):химическая формула (I) N,N′-Бис(салицилиден)этилендиамин металл,где М в химической формуле (I) представляет собой Fe, и пик люминесцентной длины волны составляет около 380 нм.
2. Флуорохромный материал по п.1, где после введения индивидууму комплекс металл-сален химической формулы (I) направляется к целевой области посредством магнитного поля вне индивидуума и проявляет фармакологические эффекты.
3. Флуорохромный материал по п.2, где комплекс металл-сален имеет такое магнитное свойство, что, если оно вводится индивидууму без использования магнитного носителя и внешнее магнитное поле накладывается на индивидуума, комплекс металл-сален будет направляться к области, к которой приложено магнитное поле.
4. Флуорохромный материал по любому из пп.1-3, где диаметр частиц соединения химической формулы (I) варьируется от 2 до 60 мкм.
5. Способ введения флуорохромного материала, содержащий комплекс металл-сален, представленный следующей химической формулой (I), индивидууму, включающий внешнее приложение магнитного поля индивидууму для направления флуорохромного материала к целевой области и затем применение внешнего света к целевой области, тем самым позволяя флуорохромному материалу в целевой области стать люминесцентным:химическая формула (I) N,N′-Бис(салицилиден)этилендиамин металл,где М представляет собой Fe.