Способ получения 4,5-дицианофталевой кислоты
Иллюстрации
Показать всеИзобретение относится к органической химии, конкретно к способу получения 4,5-дицианофталевой кислоты, которая может найти применение в качестве исходного соединения в синтезе 2,3,9,10,16,17,23,24-октакарбоксифталоцианинов, использующихся в терапии онкологических заболеваний. Согласно предлагаемому способу первая стадия включает взаимодействие 4,5-дикарбоксифталимида с водным раствором аммиака с раскрытием имидного цикла и получением аммонийной соли 4,5-дикарбоксифталамида. Вторая стадия включает дегидратацию полученной соли путем взаимодействия с дегидратирующими агентами в мольном соотношении 1:3 в диметилформамиде при -5-0°C с дальнейшей выдержкой при комнатной температуре с получением 4,5-дицианофталевой кислоты. В качестве дегидратирующего агента предпочтительно используют хлорокись фосфора или хлористый тионил. Способ позволяет получать целевой продукт с хорошим выходом. 1 з.п. ф-лы, 7 пр.
Реферат
Настоящее изобретение относится к органической химии, конкретно оно касается способа получения 4,5-дицианофталевой кислоты (ДЦФК).
ДЦФК представляет интерес в качестве исходного соединения для получения 2,3,9,10,16,17,23,24-октакарбоксифталоцианинов (оСРс), которые находят применение в виде их водорастворимых щелочных солей в качестве препаратов для фотодинамической, сонодинамической и каталитической терапии онкозаболеваний (Патент РФ 2193563, C07D 487/22, 2002.; ЖОХ. 2002. Т. 72. №2. С. 325; Рос. Хим. Журнал. 1998. Т. 42. №5. С. 140; J. Porphyrins Phthalocyanines. 1999. Vol. 3. P. 592; Патент РФ 2106146, А61К 31/40, 1998; РБЖ. 2009. №2. С. 3; РБЖ. 2010. №2. С. 82; Патент РФ 2375090, A61N 7/00, 2009).
Кроме того, ДЦФК представляет интерес в качестве исходного соединения для получения некоторых ее функциональных производных, например, диэфиров и N-замещенных имидов, которые могут быть использованы для синтеза соответствующих производных ОСРс, которые могут найти применение в технике и медицине. Так, некоторые октаалкиловые эфиры ОСРс проявляют жидкокристаллические свойства (Tetrahedron. 2008. Vol. 64. P. 4155-4161.; J. Materials Chemistry. 2007. Vol. 17. P. 3002-3007.), коньюгаты ОСРс с природными биологически активными молекулами, в частности с аминокислотами, являются потенциальными препаратами для терапии онкологических заболеваний.
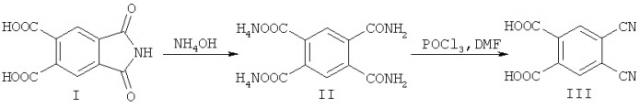
Задачей настоящего изобретения является разработка метода получения ДЦФК. Задача решается тем, что в качестве исходного соединения используют 4,5-дикарбоксифталимид(2,3-дигидро-1,3-диоксо-1Н-изоиндол-5,6-дикарбоновую кислоту, I), который превращают в аммонийную соль 4,5-дикарбоксифталамида (II) обработкой его водным раствором аммиака, с последующей дегидратацией диамида II до 4,5-дицианофталевой кислоты (III).
Процесс протекает по схеме:
На первой стадии 4,5-дикарбоксифталимид I перемешивают с 25% водным раствором аммиака в течение нескольких часов, в результате чего происходит раскрытие имидного цикла, затем аммиак отдувают на роторном испарителе, а аммонийную соль 4,5-дикарбоксифталамида II с количественным выходом высаживают из воды ацетоном.
На второй стадии диамид II дегидратируют взаимодействием с дегидратирующими агентами, предпочтительно с хлорокисью фосфора, либо с хлористым тионилом (мольное соотношение 1:3) в диметилформамиде при -5-0°C с дальнейшей выдержкой при комнатной температуре в течение часа с получением 4,5-дицианофталевой кислоты. Выход ДЦФК по двум стадиям составляет 70-78%.
Исходя из ДЦФК получены некоторые ее функциональные производные, а именно N-замещенные имиды и диэфир. Дигептиловый эфир был получен с выходом 71% взаимодействием ДЦФК с гептанолом в сухом хлористом метилене в присутствии дициклогексилкарбодиимида (DDC). Имиды - N-нонилимид и коньюгат с этиловым эфиром глицина - были синтезированы с выходом 67% и 48% взаимодействием ангидрида 4,5-дикарбоксифталонитрила с соответствующим амином в ледяной уксусной кислоте с добавлением каталитических количеств пиридина. Ангидрид 4,5-дикарбоксифталонитрила был получен нагреванием ДЦФК с ацетилхлоридом.
Предлагаемое изобретение иллюстрируется следующими примерами.
Пример 1. Получение исходного 4,5-дикарбоксифталимида (2,3-дигидро-1,3-диоксо-1H-изоиндол-5,6-дикарбоновой кислоты, I). Пиромеллитовую кислоту в количестве 20.0 г (78.7 ммоль) нагревают в 400 мл дистиллированной воды до полного растворения. Затем к охлажденному раствору при перемешивании прибавляют 4.7 мл (63.0 ммоль) 25% раствора аммиака. Перемешивание продолжают в течение 1-2 ч. После этого растворитель отгоняют на роторном испарителе, а полученную смесь аммонийных солей пиромеллитовой кислоты нагревают в круглодонной колбе, снабженной воздушным холодильником, в течение часа при температуре 260-270°C. Образовавшуюся смесь продуктов нагревают в дистиллированной воде до растворения большей части осадка. Нерастворимый в воде диимид пиромеллитовой кислоты (1.3 г, 8%) отделяют горячим фильтрованием, осадок на фильтре промывают небольшим количеством горячей воды. Из фильтрата при остывании выпадают кристаллы I, которые отфильтровывают и высушивают в вакуум-эксикаторе над хлористым кальцием. Получают 9.2 г (50%) I в виде крупных прозрачных кристаллов.
Найдено, %: С 50.89; Н 2.21; N 5.90. Вычислено, %: С 51.08; Н 2.14; N 5.96. ИК спектр (KBr), ν, см-1: 3458, 3217, 3065, 1782, 1732, 1705. Спектр ЯМР 1Н [ДМСО-d6], δ, м. д.: 7.98 (с, 2Н), 11.64 (с, 1Н).
Маточный раствор упаривают на роторном испарителе, выделяя возвратную пиромеллитовую кислоту (8.1 г, 41%).
Пример 2. Получение аммонийной соли 4,5-дикарбоксифталамида (II).
В круглодонную колбу помещают 100 мл 25% водного раствора аммиака. При интенсивном перемешивании добавляют 9.2 г (39.1 ммоль) мелкорастертого имида I, перемешивают 1 ч и оставляют на ночь. Затем аммиак отдувают на роторном испарителе, аммонийную соль 4,5-дикарбоксифталамида высаживают ацетоном, отфильтровывают и высушивают на фильтре, затем в вакуум-эксикаторе над хлористым кальцием. Получают 11.2 г (100%) II в виде белого порошка.
ИК спектр (KBr),ν, см-1: 3595, 1690, 1610, 1567, 1493, 1438, 1400, 1375, 1329.
Пример 3. Получение 4,5-дикарбоксифталонитрила (III). Растертую аммонийную соль 4,5-дикарбоксифталамида II в количестве 11.2 г (39.1 ммоль) добавляют к 45 мл диметилформамида, перемешивают до получения однородной суспензии. Затем раствор охлаждают до -5°С и добавляют 10.9 мл (117 ммоль) хлорокиси фосфора, поддерживая температуру в колбе в интервале -5-0°C. Затем реакционную массу перемешивают при комнатной температуре в течение 1 ч и выливают в смесь измельченного льда и этилацетата. Далее органический слой отделяют в делительной воронке, повторяют экстракцию водного слоя этилацетатом два раза. Объединенные органические фракции сушат над сульфатом магния. Остаток после отгонки растворителя перемешивают с толуолом в течение 1 часа, осадок отфильтровывают. Затем полученный осадок перемешивают со смесью хлороформ-ацетон, 1:1 в течение 15 минут, нерастворившийся осадок отфильтровывают, промывают на фильтре хлороформом. Фильтрат упаривают, получая 6.6 г (78%) III в виде белого порошка.
Найдено, %: С 55.90; Н 2.17; N 12.92. Вычислено, %: С 55.57; Н 1.87; N 12.96. ИК спектр (KBr), ν, см-1: 3115, 3053, 2243, 1741, 1717. Спектр ЯМР 1Н [ДМСО-d6], δ, м. д.: 8.45 (с, 2Н).
Пример 4. Получение дигептилового эфира 4,5-дицианофталевой кислоты (IV).
К суспензии 0.1 г (0.46 ммоль) ДЦФК в 2 мл хлористого метилена добавляют при -5-0°C и интенсивном перемешивании 0.2 г (0.97 ммоль) дициклогексилкарбодиимида и 0.14 мл (0.99 ммоль) 1-гептанола и продолжают перемешивание 1 час при этой температуре, затем оставляют на ночь при комнатной температуре. Выпавшую дициклогексилмочевину отделяют фильтрованием, растворитель отгоняют, остаток хроматографируют на силикагеле (элюент-хлороформ), выделяя 0.14 г (71%) IV с т.пл. 45-47°C.
Найдено, %: С 70.01; Н 7.85; N 6.82. Вычислено, %: С 69.88; Н 7.82; N 6.79. ИК спектр (KBr), ν, см-1: 3116, 3053, 2956, 2926, 2870, 2852, 2238. 1726, 1714. ГХ/МС: m/z 413.6 [M+H]+.
Пример 5. Получение ангидрида 4,5-дицианофталевой кислоты (V).
ДЦФК в количестве 0.5 г (2.3 ммоль) и 4 мл хлористого ацетила кипятят в течение 3 ч. Затем растворитель отгоняют, остаток обрабатывают толуолом. Образовавшийся осадок отфильтровывают, промывают небольшим количеством толуола и высушивают. Получают 0.44 г (96%) ангидрида ДЦФК.
ИК спектр (KBr), ν, см-1: 3118, 3056, 2244, 1864, 1756.
Пример 6. Получение N-нонилимида 4,5-дицианофталевой кислоты (VI).
Ангидрид ДЦФК в количестве 0.1 г (0.51 ммоль), 0.11 мл (0.61 ммоль) нониламина, 1 мл ледяной уксусной кислоты и 1 каплю пиридина кипятят в течение 1 часа. Затем растворитель отгоняют, остаток хроматографируют на силикагеле (элюент - хлористый метилен), выделяя 0.11 г (67%) VI с т.пл. 78-80°C.
Найдено, %: С 70.80; Н 6.63; N 12.94. Вычислено, %: С 70.57; Н 6.55; N 12.99. ИК спектр (KBr), ν, см-1: 3275, 3113, 3050, 2955, 2926, 2856, 2238, 1779, 1710. ГХ/МС: m/z 323.5 [М]+.
Пример 7. Получение коньюгата 4,5-дицианофталевой кислоты с этиловым эфиром глицина (VII).
Ангидрид ДЦФК в количестве 0.1 г (0.51 ммоль), 0.08 г (0.61 ммоль) гидрохлорида глицина, 1 мл ледяной уксусной кислоты и 0.1 мл пиридина кипятят в течение 2 часов. Затем растворитель отгоняют, остаток хроматографируют на силикагеле (элюент-хлористый метилен), выделяя 0.07 г (48%) VII с т.пл. 174-176°C.
Найдено, %: С 59.48; Н 3.25; N 14.76. Вычислено, %: С 59.37; Н 3.20; N 14.84. ИК спектр (KBr), ν, см-1: 3110, 3050, 2994, 2956, 2240, 1790, 1728. ГХ/МС: m/z 284.3 [М+Н]+.
Таким образом, разработан способ получения 4,5-дицианофталевой кислоты, показана возможность получения из нее различных функциональных производных, которые могут быть использованы для синтеза замещенных фталоцианинов, в частности производных ОСРс, например, проявляющих жидкокристаллические свойства либо являющихся потенциальными препаратами для терапии онкологических заболеваний.
1. Способ получения 4,5-дицианофталевой кислоты, включающий на первой стадии взаимодействие 4,5-дикарбоксифталимида с водным раствором аммиака с раскрытием имидного цикла и получением аммонийной соли 4,5-дикарбоксифталамида и на второй стадии дегидратацию полученной соли путем взаимодействия с дегидратирующими агентами в мольном соотношении 1:3 в диметилформамиде при -5-0°C и дальнейшей выдержке при комнатной температуре с получением 4,5-дицианофталевой кислоты.
2. Способ по п.1, отличающийся тем, что в качестве дегидратирующего агента используется хлорокись фосфора или хлористый тионил.