Лечение сахарного диабета с использованием инъекций инсулина с частотой менее одного раза в день
Иллюстрации
Показать всеИзобретение относится к способу лечения состояния или заболевания, при котором введение инсулина принесет пользу, включающему введение пациенту, нуждающемуся в этом, эффективных доз производного инсулина, представляющего собой инсулин NεB29-(Nα-(HOOC(CH2)14CO)-y-L-GIu) дез(В30), где указанное производное инсулина имеет пролонгированный профиль действия, и указанные дозы вводятся с интервалом от 24 часов до 336 часов. Изобретение обеспечивает лечение посредством введения указанного инсулина через увеличенные интервалы времени и упрощение схем лечения для удобства пациенту. 10 з.п. ф-лы, 4 пр., 5 табл., 3 ил.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к новой схеме введения инсулина, который i.а. является полезным для лечения сахарного диабета и гипергликемии, в частности для лечения инсулинзависимого сахарного диабета. Введение инсулина и инсулин включает применение аналогов, имеющих пролонгированный профиль действия по новой схеме приема.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Сахарный диабет часто требует введение инсулина для установления надлежащего контроля метаболизма (включающего главный образом гликемический контроль, а также на другие параметры метаболизма окажет благотворное действие лечение с помощью инсулина). Традиционная практика лечения инсулином представляет собой введение продукта инсулина один раз в день или чаще, дополнительно в сочетании с другими способами лечения, согласно описанию в доступных руководствах по лечению. Также в клинической практике применяют подкожные и внутривенные инъекции инсулина.
Одним широко применяемым способом лечения инсулином является введение долгодействующего продукта инсулина, также обозначаемого термином базальный инсулин, для полного или частичного удовлетворения потребности пациента в инсулине. Долгодействующий инсулин вводят один раз в день или чаще и применяют при диабете 1 типа и диабете 2 типа, а также при других болезненных состояниях, требующих инсулина (гиперкликемия любого происхождения).
В настоящее время лечение диабета 1 и 2 типов во все большей степени полагается на так называемое интенсивное лечение инсулином. При указанном режиме лечения пациента лечат множественными ежедневными инъекциями инсулина, включающими одну или две ежедневные инъекции долгодействующего инсулина для удовлетворения потребности в базальном инсулине, дополненные болюсными инъекциями быстродействующего инсулина для удовлетворения потребности в инсулине, вызываемой приемом пищи.
Принятые практики лечения диабета различных типов и гипергликемии изложены в публикациях:
- IDF Clinical Guidelines Task Force. Global Guideline for Type 2 Diabetes. Brussels: International Diabetes Federation, 2005, httD://www.idf.orq/webdata/docs/IDF%20GGT2D.Ddf.
- IDF Clinical Guidelines Task Force. Guideline for Management of PostMeal Glucose. Brussels: International Diabetes Federation, 2007, http://www.idf.org/webdata/docs/Guideline PMG final.pdf.
- D.M.Nathan, J.B.Buse, M.B.Davidson, E.Ferrannini, R.R.Holman, R.Sherwin, and B.Zinman. Management of hyperglycemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy: update regarding thiazolidinediones: a consensus statement from the American Diabetes Association and the European Association for the Study of Diabetes. Diabetes care 31 (1): 173-175, 2008,
Обзоры по основным аналогам инсулина и их свойствам и текущем клиническом применении можно i.а. найти в публикациях:
- Т.Heise and Т.R.Pieber. Towards peakless, reproducible and long-acting insulins. An assessment of the basal analogues based on isoglycaemic clamp studies. Diabetes Obes Metab 9 (5):648-659, 2007, и
- A.H.Barnett. A review of basal insulins. Diabet Med 20 (11):873-885, 2003.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
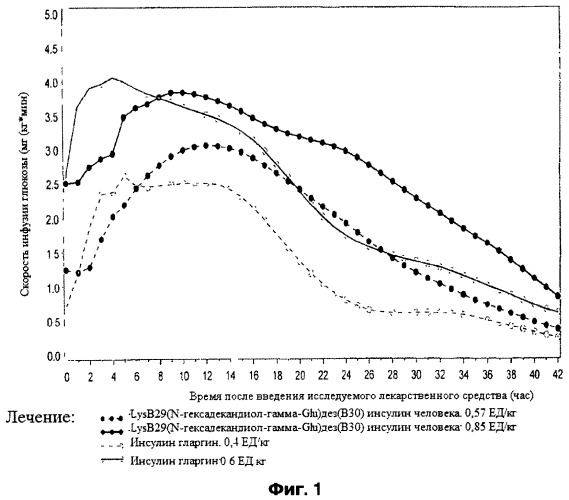
Фигура 1 иллюстрирует зависимость скорости выброса глюкозы от времени после введения исследуемого лекарственного средства.
Фигура 2 иллюстрирует зависимость уровня глюкозы в крови от времени после введения исследуемого лекарственного средства.
ОПИСАНИЕ ПРИМЕРОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение основано на неожиданном открытии, что можно лечить диабет и гипергликемию посредством введения инсулина через увеличенные интервалы времени. Например, доказано, что интервалы более 24 часов способствуют удовлетворительным режимам лечения диабета. Ряд преимуществ непосредственно вытекает из таких упрощенных схем лечения:
повышается удобство пациентов из-за необходимости вводить лекарственное средства реже раза в день;
дополнительно удобство повышается благодаря введению с частотой реже, чем два дня в неделю в течение части недели;
повышенное удобство потенциально улучшает соблюдение режима терапии пациентом, что в итоге улучшает отдаленный результат пациента.
Если устройство для введения используется для введения реже раза в день, стоимость лечения может уменьшиться в результате пониженного употребления игл или вспомогательных компонентов устройства.
В самых основных аспектах настоящее изобретение, таким образом, относится к способу лечения состояния или заболевания, при которых введение инсулина принесет пользу, включающий введение пациенту, нуждающемуся в этом, эффективных доз производного инсулина природного происхождения или аналога инсулина, где указанное производное инсулина имеет пролонгированный профиль действия и где указанные дозы вводят с интервалами более 24 часов.
Также настоящее изобретение относится к применению указанных производных инсулина в способах лечения, обсуждаемых в настоящем описании, и также настоящее изобретение относится к применению указанных производных инсулина при изготовлении фармацевтических композиций для лечения заболеваний и состояний, обсуждаемых в настоящем описании.
Заболевания и состояния, которые являются основными мишенями указанного способа, представляют собой сахарный диабет (1 и 2 типа) или другие состояния, для которых характерна гипергликемия, а также представляют интерес метаболические заболевания и состояния в общем, при которых метаболический эффект инсулина имеет клиническую значимость, такие как предиабет, нарушенная переносимость глюкозы, метаболический синдром, ожирение, кахексия, in vivo потеря/гибель бета-клеток, булимия и воспаление. Известно или считается, что все указанные типы состояний выиграют от стабильного метаболического состояния пациента, который имеет заболевание/состояние.
В любом случае, любая схема лечения, в которую включено введение инсулина, может быть модифицирована посредством осуществления настоящих сведений, что означает, что такие способы лечения включают введение имеющих пролонгированный профиль действия инсулинов, аналогов инсулина или их аналогов согласно сведениям, представленным в настоящем описании.
Схемы лечения согласно настоящему заболеванию
Настоящее изобретение наилучшим образом применяется для удобства пациента. Поэтому для каждого продукта инсулина, имеющего достаточно длительный профиль действия, будут применяться определенные интервалы введения для того, чтобы способствовать описанным режимам введения, где дозы вводят реже, чем раз в день. Таким образом, конечный способ применения зависит как от возможностей продукта, так и от предрасположенности и предпочтений пациента. Это объясняется тем фактом, что эффект любого инсулина зависит от потребности в инсулине определенного пациента и чувствительности к фармакодинамическому действию инсулина и, наконец, от предпочтений пациента в конкретной ситуации. Указанные условия могут меняться с течением времени как с течением долгих периодов (лет), так и день ото дня.
Тем не менее, настоящее изобретение обеспечивает ряд вариантов реализации общей схемы лечения.
Согласно одному варианту реализации способа согласно настоящему изобретению, дозы вводят с интервалами, по меньшей мере, в 36 часов. Согласно одному варианту реализации способа согласно настоящему изобретению, дозы вводят с интервалами, по меньшей мере, в 42 часа. Интервалы могут быть дольше, в зависимости i.а. от продолжительности пролонгированного действия использованного инсулина, аналога или производного. Поэтому, согласно некоторым вариантам реализации указанные дозы вводят с интервалами, по меньшей мере, в 48 часов, согласно другим вариантам реализации указанные дозы вводят с интервалом, по меньшей мере, в 72 часа, согласно другому варианту реализации указанные дозы вводят с интервалами, по меньшей мере, в 96 часов, согласно другому варианту реализации указанные дозы вводят с интервалами, по меньшей мере, в 120 часов.
Согласно другому варианту реализации, указанные дозы вводят с интервалами, по меньшей мере, в 144 часов, но также согласно настоящему изобретению можно применять большие интервалы, что означает, что указанные дозы можно вводить с интервалами, по меньшей мере, в 168 часов, а также такие большие интервалы, как, по меньшей мере, 336 часов, составляют вариант реализации настоящего изобретения.
Согласно одному варианту реализации указанные дозы вводят с максимальным интервалом в 312 часов.
Согласно другому варианту реализации указанные дозы вводят с максимальным интервалом в 288 часов.
Согласно другому варианту реализации указанные дозы вводят с максимальным интервалом в 264 часа.
Согласно другому варианту реализации указанные дозы вводят с максимальным интервалом в 240 часов.
Согласно другому варианту реализации указанные дозы вводят с максимальным интервалом в 216 часов.
Один вариант реализации предполагает, что указанные дозы вводят с максимальным интервалом в 192 часов, и согласно другому варианту реализации указанные дозы вводят с максимальным интервалом в 168 часов.
Согласно вариантам реализации настоящего изобретения дозы вводят через равные промежутки времени. Например, согласно одному из указанных вариантов реализации указанные дозы вводят через день. Согласно другому из указанных вариантов реализации указанные дозы вводят каждый третий день, и согласно другому из указанных вариантов реализации указанные дозы вводят каждый четвертый день. Согласно другим вариантам реализации изобретения, согласно которым указанные дозы вводят каждый пятый день, согласно которым указанные дозы вводят каждый шестой день, согласно которым указанные дозы вводят каждый седьмой день и согласно которым указанные дозы вводят каждый четырнадцатый день - тем не менее, настоящее изобретении также включает варианты реализации, где указанные дозы вводят каждый 8, 9, 10, 11, 12 или 13 день.
В качестве альтернативы введению через равные промежутки времени, согласно одному варианту реализации настоящего изобретения, дозы вводят по определенным дням недели. Это приносит преимущество для пациента, поскольку легче запомнить фиксированную недельную схему.
Поэтому согласно одному варианту реализации дозы вводят по определенным 3 дням недели. Согласно другому варианту реализации дозы вводят по определенным 2 дням недели.
Согласно одному варианту реализации никакие указанные определенные дни недели не располагаются рядом друг с другом. В случае схемы введения, включающей 3 дня недели, возможны следующие схемы введения: понедельник-среда-пятница, понедельник-среда-суббота, понедельник-четверг-суббота, вторник-четверг-суббота, вторник-четверг-воскресенье и четверг-пятница-воскресенье.
Согласно одному варианту реализации с использованием 2 определенных дней недели, дни недели согласно другому более конкретному варианту реализации изобретения разделены 2 или 3 другими днями недели - т.е. допускаются следующие схемы: понедельник-четверг; понедельник-пятница; вторник-пятница; четверг-суббота; среда-суббота; среда-воскресенье и четверг-воскресенье.
Способ по любому из пунктов формулы, где существенно ни один другой природный инсулин, аналог инсулина или производное природного инсулина или аналога инсулина не вводится указанному пациенту.
Инсулины с пролонгированным действием, полезные для настоящего изобретения
Интересующие производные с пролонгированными профилями действия описаны в публикации WO 2005/012347 (Novo Nordisk) и все считаются особенно полезными при применении настоящего изобретения на практике - в дальнейшем они обозначаются термином «производные 347».
Применение производного '347 в способе согласно настоящему изобретению
Способ согласно настоящему изобретению включает варианты реализации изобретения, в которых производное представляет собой '347 производное, т.е. производное природного инсулина или аналога инсулина содержит боковую цепь, присоединенную к α-аминогруппе N-терминального аминокислотного остатка В-цепи или к ε-аминогруппе остатка Lys, представленного в В-цепи родительского инсулина, при этом боковая цепь имеет общую формулу:
-W-X-Y-Z
где W представляет собой:
- α-аминокислотный остаток, содержащий карбоксильную группу в боковой цепи, который образует, с одной из его карбоксильных групп, амидную группу вместе с α-аминогруппой N-терминального аминокислотного остатка В-цепи или вместе с ε-аминогруппой остатка Lys, представленного в В-цепи родительского инсулина;
- цепь, состоящую из двух, трех или четырех α-аминокислотых остатков, соединенных вместе посредством амидных связей, которая - посредством амидных связей - связана с α-аминогруппой N-терминального аминокислотного остатка В-цепи в родительском инсулине, аминокислотные остатки W выбираются среди групп аминокислотных остатков, содержащих нейтральную боковую цепь и аминокислотных остатков, содержащих карбоксильную группу в боковой цепи таким образом, что W содержит, по меньшей мере, один аминокислотный остаток, который содержит карбоксильную группу в боковой цепи; или
- ковалентную связь между Х и α-аминогруппой N-терминального аминокислотного остатка В-цепи или ε-аминогруппой остатка Lys, представленного в В-цепи родительского инсулина;
Х представляет собой:
- -СО-;
- -СОСН(СООН)СО-
- -CON(СН2СООН)СН2СО-
- -CON(CH2COOH)CH2CON(CH2COOH)CH2CO-
- -CON(СН2СН2СООН)СН2СН2СО-
- -CON(СН2СН2СООН)СН2СН2CON(СН2СН2СООН)СН2СН2СО-
- -CONHCH(COOH)(CH2)4NHCO-;
- -CON(CH2CH2COOH)CH2CO- или
- -CON(CH2COOH)CH2CH2CO-.
который
а) если W представляет собой аминокислотый остаток или цепь аминокислотных остатков, образует посредством связи между подчеркнутым атомом углерода карбонильной группы образует амидную связь с аминогруппой W, или
б) если W представляет собой ковалентную связь, посредством связи между подчеркнутым атомом углерода карбонильной группы образует амидную связь с N-терминальной α-аминогруппой в В-цепи или с ε-аминогруппой остатка Lys, представленного в В-цепи родительского инсулина;
Y представляет собой:
- -(СН2)m- где m представляет собой целое число в пределах от 6 до 32;
- углеводородная цепь, содержащая 1, 2 или 3 -СН=СН- группы и некоторое количество -СН2-групп, достаточное для обеспечения общего количества атомов углерода В-цепи в пределах от 10 до 32;
- углеводородная цепь, имеющая формулу -(CH2)vC6H4(CH2)w- где v и w представляют собой целые числа или один из них равен нулю таким образом, что сумма v и W находится в пределах от 6 до 30; и
Z представляет собой:
- -СООН;
- -CO-Asp;
- -CO-Glu;
- -CO-Gly;
- -CO-Sar;
- -СН(СООН)2;
- -N(CH2COOH)2;
- -SO3Н; или
- -РО3Н;
и их любые комплексы с Zn2+ при условии, что если W представляет собой ковалентную связь, и Х представляет собой -СО-, то Z не представляет собой -СООН.
Согласно одному варианту реализации боковая цепь -W-X-Y-Z присоединяется к α-аминогруппе N-терминального аминокислотного остатка В-цепи родительского инсулина.
Согласно другому варианту реализации настоящего изобретения боковая цепь -W-X-Y-Z присоединяется к ε-аминогруппе остатка Lys, представленного в В-цепи родительского инсулина. Согласно еще одному аспекту изобретения боковая цепь -W-X-Y-Z присоединяется к ε-аминогруппе остатка Lys, расположенного в положении 28 В-цепи. Согласно дополнительному аспекту настоящего изобретения боковая цепь -W-X-Y-Z присоединяется к ε-аминогруппе остатка Lys, расположенного в положении 29 В-цепи. Согласно дополнительному аспекту настоящего изобретения боковая цепь -W-X-Y-Z присоединяется к ε-аминогруппе остатка Lys, расположенного в положении 30 В-цепи.
Компонент W боковой цепи -W-X-Y-Z может представлять собой ковалентную связь. В другом случае W может представлять собой остаток α-аминокислоты, содержащий карбоксильную группу в боковой цепи и 4-10 атомов углерода. В частности, W может представлять собой остаток α-аминокислоты, который может кодироваться генетическим кодом. Таким образом, W может, например, быть выбран из группы, состоящей из α-Asp, β-Asp, α-Glu и γ-Glu. Другими вариантами W могут быть, например, α-hGlu и δ-hGlu.
Согласно следующему варианту реализации W представляет собой цепь, состоящую из двух α-аминокислотных остатков, один из которых содержит от 4 до 10 атомов углерода и карбоксильной группы в боковой цепи, или цепь, содержащую от 2 до 11 атомов углерода, но не содержащую свободной карбоксильной группы, о-аминокислотный остаток со свободной карбоксильной группой может представлять собой нейтральный кодируемый α-аминокислотный остаток. Примерами W согласно настоящему варианту реализации являются: α-Asp-Gly; Gly-α-Asp; β-Asp-Gly; Gly-β-Asp; α-Glu-Gly; Gly-α-Glu; γ-Glu-Gly; Gly-γ-Glu; α-hGlu-Gly; Gly-α-hGlu; δ-hGlu-Gly и Gly-δ-hGlu.
Согласно следующему варианту реализации W представляет собой цепь, состоящую из двух α-аминокислотных остатков, независимо содержащих от 4 до 10 атомов углерода, и имеющих карбоксильные группы в боковой цепи. Один из указанных α-аминокислотных остатков или оба из них могут представлять собой кодируемые α-аминокислотные остатки. Примерами W согласно настоящему варианту реализации являются: α-Asp-α-Asp; α-Asp-α-Glu; α-Asp-α-hGlu; α-Asp-β-Asp; α-Asp-γ-Glu; α-Asp-δ-hGlu; β-Asp-α-Asp; β-Asp-α-Glu; β-Asp-α-hGlu; β-Asp-β-Asp; β-Asp-γ-Glu; β-Asp-δ-hGlu; α-Glu-α-Asp; α-Glu-α-Glu; α-Glu-α-hGlu; α-Glu-β-Asp; α-Glu-γ-Glu; α-Glu-δ-hGlu; γ-Glu-α-Asp; γ-Glu-α-Glu; γ-Glu-α-hGlu; γ-Glu-β-Asp; γ-Glu-γ-Glu; γ-Glu-δ-hGlu; α-hGlu-α-Asp; α-hGlu-α-Glu; α-hGlu-α-hGlu; α-hGlu-β-Asp; α-hGlu-γ-Glu; α-hGlu-δ-hGlu; δ-hGlu-α-Asp; δ-hGlu-α-Glu; δ-hGlu-α-hGlu; δ-hGlu-β-Asp; δ-hGlu-γ-Glu и δ-hGlu-δ-hGlu.
Согласно следующему варианту реализации W представляет собой цепь, состоящую из трех а-аминокислотных остатков, независимо содержащих от 4 до 10 атомов углерода, при этом аминокислотные остатки цепи выбирают из группы остатков, содержащих нейтральную боковую цепь, и остатков, содержащих карбоксильную группу в боковой цепи, таким образом, что цепь содержит, по меньшей мере, один остаток, который содержит карбоксильную группу в боковой цепи. Согласно одному варианту реализации аминокислотные остатки представляют собой кодируемые остатки.
Согласно следующему варианту реализации W представляет собой цепь, состоящую из четырех α-аминокислотных остатков, независимо содержащих от 4 до 10 атомов углерода, аминокислотные остатки цепи выбирают из группы остатков, содержащих нейтральную боковую цепь, и остатков, содержащих карбоксильную группу в боковой цепи, таким образом, что цепь содержит, по меньшей мере, один остаток, который содержит карбоксильную группу в боковой цепи. Согласно одному варианту реализации аминокислотные остатки представляют собой кодируемые остатки.
Согласно одному варианту реализации W может быть соединена с ε-аминогруппой остатка Lys в В-цепи через производное мочевины.
Компонент Х боковой цепи -W-X-Y-Z может представлять собой группу, имеющую формулу -СО- которая, через связь между подчеркнутым атомом углерода карбонильной группы, образует амидную связь с аминогруппой W или, если W представляет собой ковалентную связь, с N-терминальной α-аминогруппой В-цепи или с ε-аминогруппой остатка Lys, представленного в В-цепи родительского инсулина.
Согласно следующему варианту реализации компонент Х боковой цепи может представлять собой группу, имеющую формулу -СН(СООН)СО-, которая посредством связи между подчеркнутым атомом углерода карбонильной группы образует амидную связь с аминогруппой W или, если W представляет собой ковалентную связь, с N-терминальной α-аминогруппой В-цепи или с е-аминогруппой остатка Lys, представленного в В-цепи родительского инсулина.
Согласно следующему варианту реализации компонент Х боковой цепи может представлять собой группу, имеющую формулу -CON(СН2СООН)СН2СО-, которая посредством связи между подчеркнутым атомом углерода карбонильной группы образует амидную связь с аминогруппой W или, если W представляет собой ковалентную связь, с N-терминальной α-аминогруппой В-цепи или с ε-аминогруппой остатка Lys, представленного в В-цепи родительского инсулина.
Согласно следующему варианту реализации компонент Х боковой цепи может представлять собой группу, имеющую формулу -CON(СН2CH2COOH)CH2CO-, которая посредством связи между подчеркнутым атомом углерода карбонильной группы образует амидную связь с аминогруппой W или, если W представляет собой ковалентную связь, с N-терминальной α-аминогруппой В-цепи или с ε-аминогруппой остатка Lys, представленного в В-цепи родительского инсулина.
Согласно следующему варианту реализации компонент Х боковой цепи может представлять собой группу, имеющую формулу -CON(CH2COOH)CH2СН2СО-, которая посредством связи между подчеркнутым атомом углерода карбонильной группы образует амидную связь с аминогруппой W или, если W представляет собой ковалентную связь, с N-терминальной α-аминогруппой В-цепи или с ε-аминогруппой остатка Lys, представленного в В-цепи родительского инсулина.
Согласно следующему варианту реализации компонент Х боковой цепи может представлять собой группу, имеющую формулу -CON(CH2COOH)CH2CON(CH2COOH)CH2CO-, которая посредством связи между подчеркнутым атомом углерода карбонильной группы образует амидную связь с аминогруппой W или, если W представляет собой ковалентную связь, с N-терминальной α-аминогруппой В-цепи или с ε-аминогруппой остатка Lys, представленного в В-цепи родительского инсулина.
Согласно следующему варианту реализации компонент Х боковой цепи может представлять собой группу, имеющую формулу -CON(СН2СН2СООН)СН2СН2СО-, которая посредством связи между подчеркнутым атомом углерода карбонильной группы образует амидную связь с аминогруппой W или, если W представляет собой ковалентную связь, с N-терминальной α-аминогруппой В-цепи или с ε-аминогруппой остатка Lys, представленного в В-цепи родительского инсулина.
Согласно следующему варианту реализации компонент Х боковой цепи может представлять собой группу с формулой -CON(CH2CH2COOH)CH2CH2CON(CH2CH2COOH)CH2CH2CO- которая посредством связи между подчеркнутым атомом углерода в карбонильной группе и аминогруппой W образует амидную связь, или если W представляет собой ковалентную связь с N-терминальной α-аминогруппой в В-цепи или с ε-аминогруппой остатка Lys, представленного в В-цепи родительского инсулина.
Компонент Y боковой цепи -W-X-Y-Z может представлять собой группу с формулой -(СН2)m-, где m представляет собой целое число от 6 до 32, от 8 до 20, от 12 до 20 или от 12 до 16.
Согласно другому варианту реализации изобретения, Y представляет собой углеводородную цепь, содержащую 1, 2 или 3 -СН=СН- групп и некоторое количество групп -СН2-, достаточное для обеспечения общего количества атомов углерода В-цепи в пределах от 6 до 32, от 10 до 32, от 12 до 20 или от 12 до 16.
Согласно другому варианту реализации изобретения Y представляет собой углеводородную цепь с формулой -(CH2)vC6H4(CH2)w -, где v и w представляют собой целые числа или один из них равен нулю таким образом, что сумма v и W находится в пределах от 6 до 30, от 10 до 20 или от 12 до 16.
Согласно одному варианту реализации изобретения, компонент Z боковой цепи -W-X-Y-Z представляет собой -СООН, если W представляет собой ковалентную связь, и Х представляет собой -СО-, тогда Z не представляет собой -СООН.
Согласно другому варианту реализации Z представляет собой -CO-Asp.
Согласно другому варианту реализации Z представляет собой -CO-Glu.
Согласно другому варианту реализации Z представляет собой -CO-Gly.
Согласно другому варианту реализации Z представляет собой -CO-Sar.
Согласно другому варианту реализации Z представляет собой -СН(СООН)2.
Согласно другому варианту реализации Z представляет собой -N(СН2СООН)2.
Согласно другому варианту реализации Z представляет собой -SO3Н.
Согласно другому варианту реализации Z представляет собой -РО3Н.
Согласно другому варианту реализации W выбирается из группы, состоящей из α-Asp, β-Asp, α-Glu и γ-Glu; X представляет собой -СО- или -СН(СООН)СО; Y представляет собой -(СН2)m-, где m представляет собой целое число от 12 до 18, и Z представляет собой -СООН или -СН(СООН)2.
Группа инсулина, который в настоящем документе обозначается термином «родительский инсулин», производного '347 может представлять собой природный инсулин такой, как инсулин человека или свиньи. В другом случае родительский инсулин может представлять собой аналог инсулина.
В одной группе аналогов родительского инсулина остаток аминокислоты в положении А21 представляет собой Asn.
В одной группе аналогов родительского инсулина остаток аминокислоты в положении А21 представляет собой Gly. Конкретными примерами аналогов данной группы являются GlyA21 инсулин человека, GlyA21 дез(В30)инсулин человека и GlyA21ArgB31ArgB32 инсулин человека.
В другой группе аналогов родительского инсулина, аминокислотный остаток в положении В1 удален. Конкретным примером аналогов инсулина данной группы является дез(В1) инсулин человека.
В другой группе аналогов родительского инсулина, аминокислотный остаток в положении В30 удален. Конкретным примером аналогов инсулина данной группы является дез(В30) инсулин человека.
В другой группе аналогов родительского инсулина, аминокислотный остаток в положении В28 представляет собой Asp. Конкретным примером аналогов инсулина данной группы является AspB28 инсулин человека.
В другой группе аналогов родительского инсулина, аминокислотный остаток в положении В28 представляет собой Lys, и аминокислотный остаток в положении В29 представляет собой Pro. Конкретным примером аналогов инсулина данной группы является LysB28ProB29 инсулин человека.
В другой группе аналогов родительского инсулина, аминокислотный остаток в положении В30 представляет собой Lys, и аминокислотный остаток в положении В29 представляет собой любую кодируемую аминокислоту, кроме Cys, Met, Arg и Lys. Примером является аналог инсулина, в котором аминокислотный остаток в положении В29 представляет собой Thr, и аминокислотный остаток в положении В30 представляет собой Lys. Конкретным примером аналогов родительского инсулина данной группы является ThrB29LysB30 инсулин человека.
В другой группе аналогов родительского инсулина, аминокислотный остаток в положении В3 представляет собой Lys, и аминокислотный остаток в положении В29 представляет собой Glu. Конкретным примером аналогов инсулина данной группы является LysB3GluB29 инсулин человека.
Примерами '347 производных, полезных в настоящем изобретении, являются следующие соединения:
NεB29-(Nα-(HOOC(CH2)14CO)-γ-Glu)дез(В30) инсулин человека;
NεB29-(Nα-(HOOC(CH2)15CO)-γ-Glu)дез(В30) инсулин человека;
NεB29-(Nα-(HOOC(CH2)16CO)-γ-Glu)дез(В30) инсулин человека;
NεB29-(Nα-(HOOC(CH2)17CO)-γ-Glu)дез(В30) инсулин человека;
NεB29-(Nα-(HOOC(CH2)18CO)-γ-Glu)дез(В30) инсулин человека;
NεB29-(Nα-(HOOC(CH2)16CO)-γ-Glu-N(γ-Glu))дез(В30) инсулин человека;
NεB29-(Nα-(Asp-OC(CH2)16CO)-γ-Glu)дез(В30) инсулин человека;
NεB29-(Nα-(Glu-OC(CH2)14CO)-γ-Glu)дез(В30) инсулин человека;
NεB29-(Nα-(Glu-OC(CH2)14CO-)дез(В30) инсулин человека;
NεB29-(Nα-(Asp-OC(CH2)16CO-)дез(В30) инсулин человека;
NεB29-(Nα-(HOOC(CH2)16CO)-α-Glu-N-(β-Asp))дез(В30) инсулин человека;
NεB29-(Nα-(Glu-OC(CH2)13CO)-γ-Glu)дез(В30) инсулин человека;
NεB29-(Nα-(Sar-OC(CH2)13CO)-γ-Glu)дез(В30) инсулин человека;
NεB29-(Nα-(HOOC(CH2)13CO)-γ-Glu)дез(В30) инсулин человека;
NεB29-(Nα-(HOOC(CH2)13CO)-β-Asp)дез(В30) инсулин человека;
NεB29-(Nα-(HOOC(CH2)13CO)-α-Glu)дез(В30) инсулин человека;
NεB29-(Nα-(HOOC(CH2)16CO)-γ-D-Glu)дез(В30) инсулин человека;
NεB29-(Nα-(HOOC(CH2)14CO)-β-D-Asp)дез(В30) инсулин человека;
NεB29-(N-(HOOC(CH2)16CO-β-D-Asp)дез(В30) инсулин человека;
NεB29-(N-(HOOC(CH2)14CO-IDA)дез(В30) инсулин человека;
NεB29-[N-(HOOC(CH2)16CO)-N-(карбоксиэтил)-Glu]дез(В30) инсулин человека;
NεB29-[N-(HOOC(CH2)14CO)-N-(карбоксиэтил)-Glu]дез(В30) инсулин человека;
NεB29-[N-(HOOC(CH2)14CO)-N-(карбоксиэтил)-β-Ala]дез(В30) инсулин человека;
'347 производные могут обеспечиваться в виде существенно свободных от цинка соединений или в виде комплексов с цинком. Если обеспечиваются комплексы с цинком производного '347, два иона Zn2+, три иона Zn2+ или четыре иона Zn2+ могут быть связаны с каждым гексамером инсулина. Растворы комплексов производных инсулина с цинком содержат смеси таких видов.
Подробности, касающиеся подготовки, технологии приготовления лекарственного средства, фармакологии и других характеристик, имеющих значение для производных '347, изложены в публикации WO 2005/012347, которая включена в настоящее описание посредством ссылки.
Аналоги быстродействующего инсулина
Варианты реализации настоящего изобретения включают те варианты, в которых введение природного инсулина, аналога инсулина или его производных, имеющих пролонгированный профиль действия, сопровождается более частыми введениями быстродействующего природного инсулина, аналога инсулина или его производного и/или введением неинсулиного противодиабетического лекарственного средства.
Поэтому, один вариант реализации настоящего изобретения обеспечивает комбинированное лечение, при котором любой приемлемый инсулин, аналог или его производное, описанные выше (например, NεB29-(Nα-(HOOC(CH2)14CO)-γ-L-Glu)дез(В30) инсулин человека = LysВ29(Nε-гексадекандиол-γ-Glu)дез(В30) инсулин человека (Пример 4 в публикации WO 2005/012347)) и быстродействующий аналог инсулина применяются в сочетании, например, в комбинированном продукте, но также вводятся по отдельности. Таким образом, все определенные описания в настоящей заявке, которые сообщают подробности относительно инсулина, полезного в описываемом изобретении, относятся mutatis mutandis к комбинированному лечению, включающему те же соединения совместно с аналогами быстродействующего инсулина. Обычно быстродействующий инсулин выбирается из группы, состоящей из AspB28 инсулина человека; LysB29ProB29 инсулина человека и LysB3GluB29 инсулина человека. Комбинированный продукт не вызывал притупления реакции. Производное инсулина, описанное в публикации WO 2005/012347, может быть приготовлено в лекарственной форме совместно с аналогами быстродействующего инсулина, которые описаны в публикации WO 2007/074133, которая включена в настоящее описание посредством ссылки.
Согласно одному варианту реализации настоящее изобретение обеспечивает комбинированное лечение с помощью NεB29-(Nα-(НООС(CH2)14CО)-γ-L-Glu)дез(В30) инсулин человека и AspB28 инсулина человека совместно с фармацевтически приемлемыми носителями и вспомогательными веществами.
Производное инсулина согласно настоящему изобретению и аналог быстродействующего инсулина можно при необходимости смешивать в пропорции приблизительно 90/10%; приблизительно 80/20%, приблизительно 70/30%, приблизительно 60/40%, приблизительно 50/50%, приблизительно 40/60%, приблизительно 30/60%, приблизительно 20/80% или приблизительно 10/90%.
Другие сочетания
Согласно одному варианту реализации метода согласно настоящему изобретению, введение природного инсулина, аналога инсулина или его производного, имеющего пролонгированный профиль действия, дополнено введением неинсулинового противодиабетического лекарственного средства такого, как метформин.
Настоящее изобретение кратко сформулировано следующим образом:
Притязания:
1. Производное инсулина для лечения состояния или заболевания, при котором введение инсулина окажется полезным, включающего введение пациенту, нуждающемуся а таком лечении, эффективных доз производного инсулина, где указанное производное инсулина имеет пролонгированный профиль действия и где указанные дозы вводят с интервалами больше 24 часов.
2. Производное инсулина по п.1, где указанные дозы вводят с интервалом, по меньшей мере, в 36 часов.
3. Производное инсулина по п.2, где указанные дозы вводят с интервалом, по меньшей мере, в 48 часов.
4. Производное инсулина по п.3, где указанные дозы вводят с интервалом, по меньшей мере, в 72 часов.
5. Производное инсулина по п.4, где указанные дозы вводят с интервалом, по меньшей мере, в 96 часов.
6. Производное инсулина по п.5, где указанные дозы вводят с интервалом, по меньшей мере, в 120 часов.
7. Производное инсулина по п.6, где указанные дозы вводят с интервалом, по меньшей мере, в 144 часов.
8. Производное инсулина по п.7, где указанные дозы вводят с интервалом, по меньшей мере, в 168 часов.
9. Производное инсулина по любому из предыдущих пунктов, где указанные дозы вводят с максимальным интервалом в 336 часов.
10. Производное инсулина по любому из предыдущих пунктов, где указанные дозы вводят с максимальным интервалом в 312 часов.
11. Производное инсулина по любому из предыдущих пунктов, где указанные дозы вводят с максимальным интервалом в 288 часов.
12. Производное инсулина по любому из предыдущих пунктов, где указанные дозы вводят с максимальным интервалом в 264 часов.
13. Производное инсулина по любому из предыдущих пунктов, где указанные дозы вводят с максимальным интервалом в 240 часов.
14. Производное инсулина по любому из предыдущих пунктов, где указанные дозы вводят с максимальным интервалом в 216 часов.
15. Производное инсулина по любому из предыдущих пунктов, где указанные дозы вводят с максимальным интервалом в 192 часов.
16. Производное инсулина по любому из предыдущих пунктов, где указанные дозы вводят с максимальным интервалом в 168 часов.
17. Производное инсулина по любому из предыдущих пунктов, где указанные дозы вводят через равные промежутки времени.
18. Производное инсулина по п.17, где указанные дозы вводят через день.
19. Производное инсулина по п.17, где указанные дозы вводят через два дня.
20. Производное инсулина по п.17, где указанные дозы вводят каждый четвертый день.
21. Производное инсулина по п.17, где указанные дозы вводят через 4 дня.
22. Производное инсулина по п.17, где указанные дозы вводят через 5 дней.
23. Производное инсулина по п.17, где указанные дозы вводят через 6 дней.
24. Производное инсулина по п.17, где указанные дозы вводят через 13 дней.
25. Производное инсулина по любому из п.п.1-16, где указанные дозы вводят в определенные дни недели.
26. Производное инсулина по п.25, где указанные дозы вводят в определенные 3 дня недели.
27. Производное инсулина по п.25, где указанные дозы вводят в определенные 2 дня недели.
28. Производное инсулина по п.26 или 27, где указанные определенные дни недели не примыкают друг к другу.
29. Производное инсулина по п.27, где указанные определенные 2 дня разделены 2 и 3 другими днями недели.
30. Производное инсулина по любому из предыдущих пунктов, где введение производного инсулина, имеющего пролонгированный профиль действия, дополнено более частыми введениями быстродействующего природного инсулина или аналога инсулина и/или введением неинсулинового противодиабетического лекарственного средства.
31. Производное инсулина по любому из пп.1-29, где указанному пациенту не вводят существенно другой природный инсулин, аналог инсулина или производного природного инсулина или аналога инсулина.
32. Производное инсулина по п.31, где введение производного инсулина, имеющего пролонгированный профиль действия, дополнено введением неинсулинового противодиабетического лекарственного средства.
33. Производное инсулина по любому из предыдущих пунктов, где указанное производное природного инсулина или аналога инсулина содержит боковую цепь, присоединенную к α-аминогруппе N-терминального аминокислотного остатка В-цепи или к ε-аминогруппе остатка Lys, представленного в В-цепи родительского инсулина, при этом боковая цепь имеет общую формулу
-W-X-Y-Z,
где W представляет собой:
- α-аминокислотный остаток, содержащий карбоксильную группу в боковой цепи, который образует, с одной из euj карбоксильных групп, амидную группу вместе с α-аминогруппой N-терминального аминокислотного остатка В-цепи или вместе с ε-аминогруппой остатка Lys, представленного в В-цепи родительского инсулина;
- цепь, состоящую из двух, трех или четырех α-аминокислотных остатков, соединенных вместе посредством амидных связей, указанная цепь - посредством амидных связей - сое