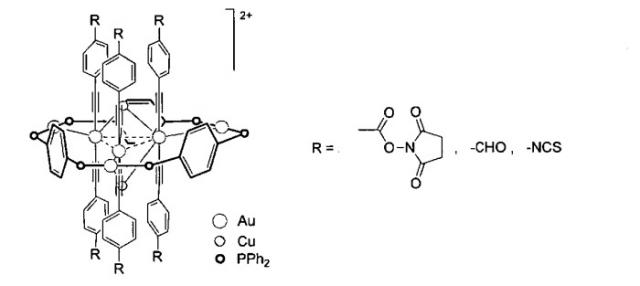
Алкинилфосфиновые золотомедные комплексы как люминисцентные метки для флуоресцентной микроскопии
Иллюстрации
Показать всеИзобретение относится к области химии металлорганических соединений, в частности к алкинилфосфиновым золотомедным комплексам, диссоциирующим в растворе с образованием ионов
.
Алкинилфосфиновые золотомедные комплексы способны образовывать ковалентные конъюгаты с белками, переходя при этом в водорастворимую форму, проявляют люминесцентные свойства и могут быть использованы в качестве меток для флуоресцентной микроскопии и в люминесцентном анализе. 5 ил., 4 табл., 3 пр.
Реферат
Изобретение относится к области химии металлорганических соединений, в частности к гетерометаллическим золотомедным комплексам, которые проявляют люминесцентные свойства и могут быть использованы в качестве меток для флуоресцентной микроскопии и в люминесцентном анализе. Изобретение может найти применение в аналитической химии, молекулярной биологии, биотехнологии, фармакологии и медицине для анализа in vitro.
В настоящее время известны комплексы переходных металлов (далее КПМ), которые проявляют люминесцентные свойства и используются в качестве меток в флуоресцентной микроскопии [1]. Такие комплексы обладают рядом преимуществ, по сравнению, например, с метками на основе органических люминофоров: их люминесценция характеризуется большими Стоксовыми сдвигами и большими временами жизни возбужденного состояния. Большой Стоксовый сдвиг упрощает разделение сигналов люминесценции и возбуждающего излучения и уменьшает самотушение в растворе. Большее время жизни возбужденного состояния люминесцентных КПМ позволяет, используя регистрацию времени затухания свечения образца (FLIM, fluorescence life time imaging), отсекать автофлюоресценцию биологических образцов, и тем самым повышать контрастность изображения и чувствительность детектирования.
Для практического применения наиболее интересны комплексы, способные к специфическому связыванию с определенными биомолекулами или клеточными структурами, и одним из типов меток на основе КПМ являются метки для ковалентного связывания белками [2].
К существенным недостаткам используемых в настоящий время меток на основе КПМ относится то, что люминесценция подавляющего большинства таких люминофоров подвержена тушению молекулярным кислородом и в присутствии воздуха квантовый выход люминесценции уменьшается на порядок по сравнению с дегазированным раствором.
Известны золотомедные алкинилфосфиновые комплексы, которые по решаемой технической задаче являются наиболее близкими к заявляемому изобретению и принятые в качестве прототипа [3]. Общее с заявленным изобретением является то, что комплексы-прототипы обладают интенсивной люминесценцией, микросекундными временами жизни и люминесценция комплексов незначительно снижается в присутствии кислорода.
Недостатком известных комплексов является относительно узкая область их применения за счет нерастворимости их в воде и физиологических средах, а также невозможности связывания их с белками.
Техническим результатом заявляемого изобретение является расширение области применения за счет возможности связывания с белками. Важным при этом в заявляемом изобретении является сохранение интенсивной люминесценции, в том числе и при наличии молекулярного кислорода.
Указанный технический результат достигается тем, что алкинилфосфиновые золотомедные комплексы, диссоциирующие в растворе с образованием ионов, способны образовывать ковалентные аддукты с аминогруппами, в частности с аминогруппами белков
что позволяет использовать их в качестве люминесцентных меток для флуоресцентной микроскопии.
Сущность заявляемого изобретения поясняется примерами конкретной реализации, которые иллюстрируются Фиг. 1-5.
На Фиг. 1 представлена схема синтеза комплекса [AuC2C6H4-4-COONC4H4O2].
На Фиг. 2 представлена схема синтеза комплекса [Au2(С2С6Н4-4-COONC4H4O2)2 PPh2C6H4PPh2].
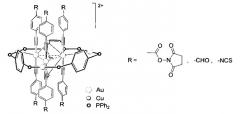
На Фиг. 3 представлена схема синтеза комплекса [Au6Cu2(С2С6Н4-4-COONC4H4O2)6(PPh2C6H4PPh2)3](PF6)2..
На Фиг. 4 и 5 представлены спектры люминесценции.
Заявляемое изобретение было апробировано в Санкт-Петербургском государственном университете в режиме реального времени, и результаты апробации приведены в виде конкретных примеров.
Пример 1.
Комплекс [Au6Cu2(C2C6H4-4-COONC4H4O2)6(PPh2C6H4PPh2)3](PF6)2.
Комплекс [AuC2C6H4-4-COONC4H4O2] (Фиг. 1). К суспензии 0.45 ммоль комплекса [Au(тетрагидротиофен)С1] в 2 мл ацетона добавляли раствор 0.56 ммоль 2,5-диоксопирролидин-1-ил-4-этинилбензоата в 2 мл ацетона и 10 капель триэтиламина, после чего реакционную смесь перемешивали в темноте до образования белого осадка. Осадок отделяли центрифугированием и промывали водно-этанольной смесью 1:1 по объему, этанолом и пентаном. Выход 97%.
Комплекс [Au2(C2C6H4-4-COONC4H4O2)2PPh2C6H4PPh2] (Фиг.2). В раствор 0.15 ммоль 1,4-бис(дифенилфосфино)бензола в 5 мл дихлорметана добавляли 0.32 ммоль [AuC2C6H4-4-COONC4H4O2] и перемешивали до полного растворения осадка, затем добавляли 2.5 мл толуола, после чего раствор пропускали через колонку с нейтральным алюмогелем и отгоняли растворитель. Выход 65%.
Комплекс [Au6Cu2(C2C6H4-4-COONC4H4O2)6(PPh2C6H4PPh2)3](PF6)2 (Фиг.3) (1)
К раствору 0.33 ммоль [Au2(C2C6H4-4-COONC4H4O2)2PPh2C6H4PPh2] в 3 мл дихлорметана добавили 0.22 ммоль [Cu(NCMe)4]PF6 и перемешивали реакционную смесь до образования желто-оранжевого раствора, после чего этот раствор пропустили через целиты, отогнали растворитель и перекристаллизовывали методом газофазной диффузии пентана в ацетон. Выход 81%. 31P ЯМР (D[6]-ацетон): 44.4 (с, 6Р), -144.8 (септ 2Р, PF6, JPF 712 Гц). 1Н ЯМР (D[6]-ацетон): 8.00 (дм, JHH=7.2 Гц, JPH 13 Гц, 24Н, Н-орто), 7.85 (м, 12Н, {P-C6H4-P}), 7.67 (т, JHH 7.4 Гц, 12Н, Н-пара), 7.51 (дд, JHH 7.4 Гц, 24Н, Н-мета), 7.56 (д, JHH 8.3 Гц, 12Н, C6H4), 7.05 (д, JHH 8.3 Гц, 12Н, C6H4), 2.95 (с, 24Н, CH2CH2). ESI-масс-спектр (m/z): 2060 (М2+).
Пример 2.
Комплекс синтезированный, как описано в примере 1, с использованием 1-этинил-4-изотиоционатобензола в качестве ацетиленового лиганда.
31Р ЯМР (D[6]-ацетон): 44.6 (с, 6Р), -144.8 (септ 2Р, PF6, JPF 712 Гц). 1Н ЯМР (D[6]-ацетон): 7.87 (дм, JHH=7 Гц, JPH=13 Гц, 24Н, орто-Н), 7.58 (м, 24Н, {P-C6H4-P}, пара-Н), 7.41 (м, 24Н, мета-Н), 6.67 (д, JHH=7.4 Гц, 12Н, С6Н4), 6.56 (с, JHH=7.4 Гц, 12Н, С6Н4).
Пример 3.
Комплекс синтезированный, как описано в примере 1, с использованием 4-этинилбензальдегида в качестве ацетиленового лиганда.
31Р ЯМР (D[6]-ацетон): 44.9 (с, 6Р), -144.8 (септ 2Р, PF6, JPF 712 Гц). 1Н ЯМР (D[6]-ацетон): 9.83 (с, 6Н, СНО), 8.02 (дм, JHH=7.2 Гц, JPH 14 Гц, 24Н, Н-орто), 7.88 (м, 12Н, {Р-С6Н4-Р}), 7.67 (т, JHH 7.4 Гц, 12Н, Н-пара), 7.49 (дд, JHH 7.4 Гц, 24Н, Н-мета), 7.35 (д, JHH 8.4 Гц, 12Н, C6H4), 7.02 (д, JHH 8.4 Гц, 12Н, С6Н4).
Для комплексов (1)-(3) были измерены фотофизические свойства, а именно: при комнатной температуре были измерены электронные спектры поглощения и спектры люминесценции, а также определены времена жизни возбужденного состояния и квантовые выходы люминесценции (таблица 1). Соединения (1)-(3) демонстрируют высокие квантовые выходы люминесценции и времена жизни люминесценции в диапазоне 2.4-3.3 мкс, аналогично свойствам прототипа.
| Таблица 1 | ||||||
| Фотофизические свойства комплексов | ||||||
| Соединение | Растворитель | λпогл, нм | λвозбуд, нм | λэмисс, нм | τ, микросек | Квантовый выход, % |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (1) | CH2Cl2 | 265, 300 пл, 317, 350 пл, 409 | 330, 350 пл, 408 | 570 | 3.3 | 50 |
| Ацетон | 353 пл, 408 | 331, 414 | 580 | 3.0 | ||
| Боратный буфер | 265, 348, 412 | 300, 330, 403 | 580 | 0.5 (36%), 3.4 (64%) | ||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| (2) | CH2Cl2 | 267, 316, 355 пл, 410 | 310, 345, 407 | 596 | 2.4 | 23 |
| (3) | CH2Cl2 | 266, 324, 338 пл, 360, 414 | 265, 335, 358 пл, 411 | 584 | 2.5 | 54 |
Было продемонстрировано, что комплексы (1)-(3) способны образовывать ковалентные конъюгаты с белками. Синтез конъюгатов осуществляли в 0.01 М Na-боратном буферном растворе, pH 8.4, в течение 1 часа. Удаление несвязавшейся метки осуществляли методом гель-хроматографии с использованием в качестве стационарной фазы геля Сефадекс-G75. В таблице 2 представлены результаты получения конъюгатов белков, а именно соевого ингибитора трипсина (СИТР), сывороточного альбумина человека (ЧСА), антител к ЧСА. При этом получающиеся конъюгаты являются растворимыми в воде и буферных растворах, в отличие от исходных меток.
| Таблица 2 | ||||
| Мольные соотношения белок/комплекс при образовании конъюгатов | ||||
| Белок | Мольное соотношение белок/комплекс, взятое для получения конъюгата | Мольное соотношение белок/комплекс в полученном конъюгате | ||
| (1) | (2) | (3) | ||
| СИТР | 1:3 | 1.0:1.3 | 1.0:2.1 | 1.0:1.7 |
| СИТР | 1:5 | 1.0:1.9 | 1.0:3.2 | 1.0:2.9 |
| ЧСА | 1:3 | 1.0:1.3 | 1.0:1.8 | 1.0:1.8 |
| ЧСА | 1:5 | 1.0:2.1 | 1.0:3.2 | 1.0:3.3 |
| Антитела к ЧСА | 1:5 | 1.0:2.6 | 1.0:3.3 | 1.0:3.0 |
| Антитела к ЧСА | 1:7 | 1.0:3.4 | 1.0:4.5 | 1.0:4.0 |
| Антитела к ЧСА | 1:10 | 1.0:4.8 | 1.0:6.7 | 1.0:6.0 |
При образовании ковалентных конъюгатов с белками спектры люминесценции меток практически не изменяются. Для примера на Фиг.4 представлены спектры люминесценции свободного комплекса (1) и его конъюгатов с белками. На Фиг.4: 1 - комплекс (1) в ацетоне, 2 - конъюгат 1-ЧСА в боратном буфере, 3 - конъюгат 1-антиЧСА в боратном буфере и 4 - конъюгат 1-СИТР в боратном буфере.
Как для меток-прототипов, люминесценция комплексов (1)-(3) не претерпевает существенного уменьшения в присутствии кислорода. Для примера на Фиг.5 представлены спектры люминесценции конъюгата (1) с ЧСА в дегазированном (кривая 1) и аэрированном (кривая 2) растворах.
Белки при образовании конъюгатов с комплексами также сохраняют свою структуру и биологическую активность, что было продемонстрировано на примере образования специфического комплекса «трипсин-ингибитор трипсина» и модельной реакции гидролиза трипсином специфического субстрата 4-нитроаналида N-бензоил-L-тирозина в присутствии нативного СИТР и СИТР меченного комплексами (1)-(3). Константы ингибирования были определены по методу Диксона и представлены в таблице 3.
| Таблица 3 | |
| Константы ингибирования при использовании СИТР и его конъюгатов с комплексами | |
| Форма ингибитора | Константа ингибирования (Ki), нМ |
| Нативный СИТР | 88 |
| Конъюгат СИТР комплексом (1) | 220 |
| Конъюгат СИТР комплексом (2) | 160 |
| Конъюгат СИТР комплексом (3) | 145 |
Константы Михаэлиса и удельные активности фермента реакции гидролиза представлены в таблице 4.
| Таблица 4 | ||
| Удельные активности и константы Михаэлиса для ферментативного гидролиза в присутствии СИТР и его конъюгатов с комплексами | ||
| Ферментативный гидролиз | Константа Михаэлиса (КМ), мМ | Удельная активность, мкмоль/(мин·мг) |
| Без ингибитора | 0.37 | 1.01 |
| В присутствии СИТР | 0.34 | 0.54 |
| В присутствии конъюгата | 0.36 | 0.62 |
| СИТР с комплексом (1) | ||
| В присутствии конъюгата | 0.35 | 0.58 |
| СИТР с комплексом (2) | ||
| В присутствии конъюгата | 0.34 | 0.56 |
| СИТР с комплексом (3) |
Полученные данные свидетельствуют о том, что ковалентное прикрепление меток (1)-(3) к белку не мешает его специфическому связыванию с аффинным партнером.
Технико-экономическая эффективность заявленного изобретения состоит, как показывают результаты приведенных примеров конкретной реализации, в существенном расширении области применения заявленных комплексов в качестве метки для флуоресцентной микроскопии за счет возможности связывания с белками. Важным при этом в заявляемом изобретении является сохранение интенсивности люминесценции при наличии молекулярного кислорода.
Заявленные комплексы проявляют люминесценцию с высоким квантовым выходом и микросекундными временами жизни. Люминесценция комплексов не подвергается существенному тушению кислородом воздуха, то есть заявленные комплексы демонстрируют люминесцентные характеристики не хуже прототипа. Существенное преимущество предлагаемых комплексов по сравнению с прототипом заключается в том, что они способны образовывать ковалентные конъюгаты с белками, переходя при этом в водорастворимую форму. При этом не наблюдается ни существенного изменения люминесценции комплекса, ни потери белком биологической активности, что позволяет использовать данные комплексы в качестве специфических меток в люминесцентном анализе и флуоресцентной микроскопии.
Список использованных источников информации
1. K.K.-W. Lo, A.W.-T. Choi, W.H.-T. Law. // Dalton Trans. 2012. V.41. P.6021-6047; Q. Zhao, C. Huang, F. Li. // Chem. Soc. ReV. 2011. V.40. P.2508-2524; V. Fernandez-Moreira, F.L. Thorp-Greenwood, M.P. Coogan. // Chem. Commun. 2010. V.46. P.186-202; K.L. Haas, K.J. Franz. // Chem. Rev. 2009. V.109. P.4921-4960; F.L. Thorp-Greenwood. // Organometallics 2012. V.31. P.5686-5692.
2. E. Ferri, D. Donghi, M. Panigati, G. Prencipe, L. D′Alfonso, I. Zanoni, C. Baldoli, S. Maiorana, G. D′Alfonso, E. Licandro. // Chem. Commun. 2010. V.46. P.6255-6257; K.W. Hubel, B.E. Henri // US 3280017 (A) 1966-10-18], иридия [D.-L. Ma, H.-J. Zhong, W.-C. Fu, D.S.-H. Chan, H.-Y. Kwan, W.-F. Fong, L.-H. Chung, C.-Y. Wong, C.-H. Leung. // PLoS ONE 2013. V.8. P.e55751], платины [D.R. McMillin, J.J. Moore. // Coordination Chemistry Reviews 2002. V.229. P.113-121; J.F. Hainfeld, F.R. Furuya, R.D. Powell // US 2005130207 (A1) 2005-06-16], а также комплексов лантаноидов [S. Mizukami, T. Yamamoto, A. Yoshimura, S. Watanabe, K. Kikuchi. // Angew. Chem. Int. Ed. 2011. V.50. P.8750-8752; K.N. Raymond, S. Petoud, S. Cohen, J. Xu // EP 1154991 (A1) 2001-11-21.
3. Koshevoy I.O. и др. Intensely luminescent alkynyl - Phosphine Gold(l)-Copper(l) complexes: Synthesis, characterization, photophysical, and computational studies // Inorg. Chem. 2009. T.48. №5. С.2094-2102 (прототип).
1. Алкинилфосфиновые золотомедные комплексы, диссоциирующие в растворе с образованием ионов в качестве люминесцентной метки для флуоресцентной микроскопии.