Средство для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек
Иллюстрации
Показать всеИзобретение относится к индустрии фармацевтических средств. Лекарственное средство содержит в качестве основы натриевую соль карбоксиметилцеллюлозы, а в качестве лечебных компонентов - комбинацию антисептика 0,01% раствор мирамистина и метронидазол. Согласно изобретению получено лекарственное средство, обладающее антисептическим, ранозаживляющим и сорбционным действием на местные гнойно-воспалительные процессы мягких тканей и слизистых оболочек, используемых в хирургии, дерматологии, акушерстве и гинекологии, оториноларингологии. 2 табл., 2 пр.
Реферат
Изобретение относится к области медицины, а именно к средствам, обладающим антимикробным, ранозаживляющим и сорбционным действием на местные гнойно-воспалительные процессы мягких тканей и слизистых оболочек, используемым в хирургии, дерматологии, акушерстве и гинекологии, оториноларингологии.
Актуальной проблемой современной хирургии является проблема лечения гнойных ран, что связано с распространенностью ран различной этиологии, гнойными осложнениями, высокой летальностью, большими материальными затратами на лечение. По данным некоторых авторов от всех хирургических заболеваний гнойные осложнения составляют 30-35%, а летальность от них достигает 25%.
Несмотря на разработку и внедрение новых методов лечения гнойных ран, использование лекарственных средств под повязкой является сегодня основным благодаря его доступности, простоте применения и экономической выгоде.
Среди лекарственных средств наружного применения широко используются мази и гели на основах, которые не травмируют поврежденную поверхность при нанесении на рану, обеспечивают дренаж ран, а лекарственные вещества, входящие в их состав, обеспечивают необходимое лечебное действие. Без сомнения современные препараты должны обладать разнонаправленным действием и сочетать в себе такие свойства, как широкая антимикробная активность, высокая дегидратирующая способность, стимуляция регенерации тканей.
Первостепенную роль в лечении гнойно-воспалительных процессов играют антибактериальные средства, среди которых в настоящее время значительно возрастает интерес к антисептикам и химиопрепаратам, широко известным и хорошо зарекомендовавшим себя в хирургической практике, в частности группа имидазола.
Для введения действующих веществ используют основы, обладающие не только хорошей консистенцией, атравматичностью при намазывании, но и выполняющие роль дренажа и абсорбции гнойного отделяемого из раны. В качестве таких основ широко используют сплавы полиэтиленоксидов, гели производных целлюлозы и др.
Прототипом изобретения послужил препарат, в состав которого входит натрия гипохлорит на геле полимера натриевой соли карбоксиметилцеллюлозы (NaКМЦ) (патент на изобретение №2235535 от 2004.09.10 «Средство для лечения местных гнойно-воспалительных процессов кожи и слизистых оболочек», патентообладатель Набокин И.И.).
Натрия гипохлорит, несмотря на его активность в отношении многих грамположительных и грамотрицательных бактерий, большинства патогенных грибов, вирусов и простейших, является соединением очень неустойчивым, эффективность которого быстро снижается в присутствии крови или ее компонентов. Кроме того, он имеет характерный запах хлора и обладает высокими коррозионными свойствами, что отрицательно сказывается на самочувствии обслуживающего персонала и пациентов.
Техническим результатом изобретения является создание лекарственного средства, обладающего антисептической, ранозаживляющей и сорбционной функциями.
Технический результат достигается тем, что средство для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек содержит в качестве основы натриевую соль карбоксиметилцеллюлозы, отличающееся тем, что в качестве лечебных компонентов содержит комбинацию антисептика 0,01% раствор мирамистина и метронидазол в следующих массовых долях:
| Раствор мирамистина 0,01% | 95,0-100,0 |
| (ФС 42-3498-98) | |
| Метронидазол | 1,0-2,0 |
| (ФС 42-2283-93) | |
| Натриевая соль карбоксиметилцеллюлозы | 4,0-6,0 |
| (ТУ 6-55-221-1453-96) |
Характеристика объектов
Мирамистин (бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид) - оригинальный, патентованный лекарственный препарат, антисептик, относится к группе катионных поверхностно активных веществ, а именно к четвертичным аммониевым соединениям. Обладает выраженным бактерицидным действием в отношении грамположительных и грамотрицательных, аэробных и анаэробных бактерий в виде монокультур и микробных ассоциаций, включая госпитальные штаммы с полирезистентностью к антибиотикам.
Метронидазол. Противопротозойный и противомикробный препарат, производное 5-нитроимидазола. Механизм действия заключается в биохимическом восстановлении 5-нитрогруппы метронидазола внутриклеточными транспортными протеинами анаэробных микроорганизмов и простейших. Восстановленная 5-нитрогруппа метронидазола взаимодействует с ДНК клетки микроорганизмов, ингибируя синтез их нуклеиновых кислот, что ведет к гибели бактерий. Активен в отношении Trichomonas vaginalis, Gardnerella vaginalis, Giardia intestinalis, Entamoeba histolytica, Lamblia spp., а также облигатных анаэробов Bacteroides spp. (в т.ч. Bacteroides fragilis, Bacteroides distasonis, Bacteroides ovatus, Bacteroides thetaiotaomicron, Bacteroides vulgatus), Fusobacterium spp., Veillonella spp., Prevotella (Prevotella bivia, Prevotella buccae, Prevotella disiens) и некоторых грамположительных микроорганизмов (Eubacter spp., Clostridium spp., Peptococcus spp., Peptostreptococcus spp., Mobiluncus spp.).
Натриевая соль карбоксиметилцеллюлозы (NaКМЦ) растворима в воде, в водных растворах щелочей, в органических растворителях и минеральных маслах - не растворяется. При этом натриевая соль карбоксиметилцеллюлозы образует вязкие прозрачные растворы, характеризуемые псевдопластичностью, а для некоторых сортов продукта - и тиксотропией (т.е. способностью самопроизвольно восстанавливать разрушенную механическим воздействием исходную структуру). В виде геля NaКМЦ взаимодействует с тканями и содержимым раны, равномерно распределяется по раневой поверхности, обеспечивает быструю и полную доставку лекарственных веществ к месту поражения, проявляет осмотическое действие при аппликации на рану, поглощая раневое отделяемое.
Способ осуществляется следующим образом.
Изготовление лекарственного средства включает две стадии.
Первая стадия: к соответствующей навеске натриевой соли карбоксиметилцеллюлозы добавляют рассчитанное количество 0,01% раствора мирамистина, перемешивают и оставляют на сутки при температуре (4±1)°С для набухания и получения однородной массы;
Вторая стадия: к предварительно измельченной навеске метронидазола по частям добавляют полученный гель натриевой соли карбоксиметилцеллюлозы с 0,01% раствором мирамистина и перемешивают до получения однородной массы.
Пример №1 по способу получения
К 4,0 массовым долям NaКМЦ добавляют 100,0 массовых долей 0,01% раствора мирамистина, перемешивают до получения однородной массы и оставляют на сутки при температуре (4±1)°С, затем к предварительно измельченной 1,0 массовой доле метронидазола по частям добавляют полученный гель натриевой соли карбоксиметилцеллюлозы с 0,01% раствором мирамистина и перемешивают до получения однородной массы.
Пример №2 по способу получения
К 6,0 массовым долям NаКМЦ добавляют 95,0 массовых долей 0,01% раствора мирамистина, перемешивают до получения однородной массы и оставляют на сутки при температуре (4±1)°С, затем к предварительно измельченной 2,0 массовой доле метронидазола по частям добавляют полученный гель натриевой соли карбоксиметилцеллюлозы с 0,01% раствором мирамистина и перемешивают до получения однородной массы.
Определение микробиологической активности средства для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек.
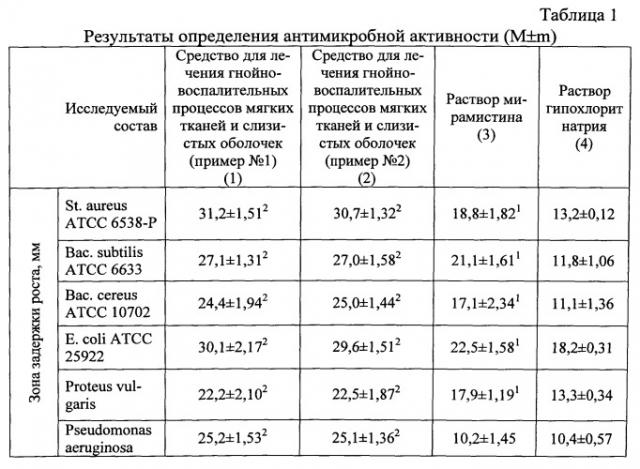
Антимикробное действие средства для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (пример №1 и пример №2) изучали методом диффузии в агар (ГФ XII, 2007) в отношении штаммов St. aureus ATCC 653 8-Р, Вас. subtilis ATCC 6633, Вас. cereus ATCC 10702, E.coli ATCC 25922, Proteus vulgaris и Pseudomonas aeruginosa ATCC 9027, Candida albicans ATCC 885-653. Результаты определения антимикробной активности представлены в табл.1.
Из данных, представленных в таблице 1, следует, что разработанное лекарственное средство обладает более высокой антимикробной активностью, которая обусловлена сочетанием антисептика и химиопрепарата, в отношении всех исследуемых тест-штаммов. Зона задержки роста при изучении спектра антимикробной активности разработанной мази (пример №1 и пример №2) наиболее выражена в отношении тест-штаммов St. aure-us ATCC 653 8-Р, E.coli ATCC 25922, что в 2,6 и 1,7 раза больше, чем зона задержки роста при исследовании прототипа (раствор гипохлорита натрия на NaКМЦ), различия между ними статистически достоверны.
Пример экспериментального применения
Изучение ранозаживляющей активности разработанного лекарственного средства проводили в эксперименте на самцах крыс породы «Вистар», массой 180-200 г, у которых моделировалась гнойная рана по методике П.И. Толстых (1976). Экспериментальные животные были разделены на три серии, по 36 животных в каждой:
В 1-й серии (модель) лечение не проводилось.
Во 2-й серии (контроль) проводили лечение протопипом (гипохлорит натрия на NaКМЦ).
В 3-й серии проводили лечение средством для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (пример №1).
В 4-й серии проводили лечение средством для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (пример №2).
Перевязки осуществлялись ежедневно. Течение раневого процесса у экспериментальных животных оценивали планиметрическим (метод Л.И. Поповой), микробиологическим, гистологическим методами, результаты исследований обработаны статистически (рассчитаны средние величины, критерий достоверности). Животные выводились из эксперимента путем передозировки эфирного наркоза на 1, 3, 5, 8, 10, 15 сутки.
После моделирования на 1-е сутки во всех сериях раны выглядели следующим образом: отмечалась гиперемия, отек окружающих тканей и краев ран, дно их было покрыто налетом фибрина с участками некроза, наблюдалось обильное гнойное отделяемое.
В процессе лечения купировался отек, происходило очищение поверхности раны от гнойно-некротических масс, появлялись грануляции и начиналась краевая эпителизация.
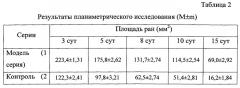
Данные планиметрического исследования свидетельствуют о более быстром уменьшении площади ран в 3-й и 4-й серии по сравнению с моделью и контролем (исходная площадь ран была 250 мм2), к 8-м суткам площади ран имели статистически значимые различия. Процесс заживления протекал быстрее в 3-й и 4-й серии по сравнению с контрольной и моделью. Результаты планиметрического исследования представлены в табл.2.
При сравнении серий 3 и 4 статистически значимых различий не выявлено.
Таким образом, полученные данные планиметрического исследования подтверждают высокую эффективность разработанного средства для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (пример №1 и №2). Оно способствует уменьшению площади ран на 99,2% на 15-е сутки, повышает скорость заживления в 1,5-3,2 раза по сравнению с контрольной серией.
Данные микробиологического исследования показали, что в 3-й и 4-й серии микробная обсемененность ран достоверно меньше, чем в контрольной серии начиная с 3-х суток и на протяжении всего срока наблюдения. В 3-й и 4-й серии на 5-е сутки микробная обсемененность ран в 5,4 раза меньше, чем в контрольной серии (15,2±2,2×105, 18,4±3,1×105 и 8,1±2,1×106 КОЕ/г, соответственно), на 10-е сутки - в 18,3 раза меньше, чем в контрольной серии (33,3±1,1×103, 40,1±2,4×103 и 6,1±1,5×105 КОЕ/г, соответственно). Таким образом, установлено, что средство для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (пример №1 и №2) в 5,4-18,3 раза сокращает микробную обсемененность ран по сравнению с прототипом (гипохлорит натрия на NaКМЦ).
Для полной оценки состояния раны в динамике был использован гистологический метод исследования раневых биоптатов, дающий возможность объективно оценить динамику течения раневого процесса.
На 1-е сутки после моделирования микроскопическая картина во всех сериях выглядит следующим образом. Вся поверхность раны покрыта массивным фибринозно-лейкоцитарный слоем. Большинство лейкоцитов - в состоянии распада. Соединительная ткань под лейкоцитарным струпом резко отечна, инфильтрирована сегментоядерными лейкоцитами и единичными макрофагами. Подлежащая соединительнотканная клетчатка разрыхлена, фибробласты ее полиморфны, имеют базофильную цитоплазму и набухшие, разрыхленные ядра. Кровеносные сосуды расширены. Встречаются очаги геморрагии диапедезного характера. Отечные явления распространяются на края кожи. Эпителий дистрофичен, вакуолизирован, край его уплощен.
На 3-и сутки в группе животных в контрольной серии поверхность раны покрыта струпом. Зачатки грануляционной ткани инфильтрированы полиморфно-ядерными лейкоцитами. На 10-е сутки происходило формирование эпителиального вала. Грануляционная ткань отграничена от интактной дермы и инфильтрирована полиморфно-ядерными лейкоцитами. На 15-е сутки раневой дефект был выполнен пучками незрелых коллагеновых волокон. Поверхность раневого дефекта покрыта эпидермисом, в котором отсутствовал роговой слой.
На 3-и сутки при лечении с использованием средства для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (пример №1 и №2) отмечается выраженная резкая граница грануляций и интактной кожи, слабая инфильтрация полиморфно ядерными лейкоцитами вновь образованных грануляций. На 10-е сутки уменьшение объема молодого коллагена вследствие ремоделирования рубца. Происходит восстановление кожи в области угла раневого дефекта. На 15-е сутки наблюдалось полное восстановление сетчатого слоя кожи за исключением производных: волосяных фолликулов и сальных желез.
В сериях, где лечение проводилось средством для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (пример №1 и №2), отмечается более быстрое очищение поверхности раны от лейкоцитарно-некротических масс (к 3-м суткам) и более активный рост грануляционной ткани. Начало роста эпителия по краям раны начинается с 3-х суток. К 7-10-м суткам значительная часть раны или вся ее поверхность эпителизированы.
Таким образом, применение разработанного средства для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек в I и II фазах раневого процесса повышает скорость заживления ран в 1,5-3,2 раза, способствует сокращению основных стадий течения раневого процесса в 1,3-2,3 раза, в 5,4-18,3 раза сокращает микробную обсемененность ран, ускоряет формирование и созревание грануляционной ткани, способствует ранней и быстрой эпителизации раневой поверхности, обладает высокой антимикробной активностью по сравнению с лечением прототипом изобретения (контрольная серия).
Средство для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек, содержащее в качестве основы натриевую соль карбоксиметилцеллюлозы и включающее в качестве лечебных компонентов комбинацию антисептика 0,01% раствор мирамистина и метронидазол в следующих массовых долях:
| Раствор мирамистина 0,01% | 95,0-100,0 |
| Метронидазол | 1,0-2,0 |
| Натриевая соль карбоксиметилцеллюлозы | 4,0-6,0 |