Способ получения средства, обладающего противовоспалительной, мочегонной и антиоксидантной активностью
Иллюстрации
Показать всеИзобретение относится к фармацевтической промышленности, а именно к способу получения средства, обладающего противовоспалительной, мочегонной и антиоксидантной активностью. Способ получения средства, обладающего противовоспалительной, мочегонной и антиоксидантной активностью, включающий измельчение побегов спиреи иволистной, представляющих собой смесь листьев, цветков и веточек, их трехкратную экстракцию методом дробной мацерации, перемешивание при настаивании, извлечения объединяют, отстаивают в течение суток, фильтруют, сгущают, сепарируют, сушат, при определенных условиях. Средство, полученное вышеописанным способом, проявляет выраженную противовоспалительную, мочегонную и антиоксидантную активность. 2 ил., 12 табл.
Реферат
Изобретение относится к фармацевтической промышленности и касается способа производства лекарственных препаратов из растительного сырья.
В последние годы отмечается неуклонный рост воспалительных заболеваний мочеполовой системы, желудочно-кишечного тракта, связанных с неблагоприятной экологической обстановкой, неправильным и нерациональным питанием. В России заболеваниями данной группы страдает каждый десятый житель [Электронный ресурс. URL: http://www.pharmvestnik.ru/publs/staryi-arxiv-gazetv/12455.html#.UlIe21DIYlQ]. В терапии воспалительных заболеваний широко используются синтетические лекарственные средства. Однако, при выраженном терапевтическом эффекте, они имеют побочные действия, противопоказания и ограничения к применению, не всегда предотвращают развитие рецидива заболевания после их отмены.
Преимуществом лекарственных растений и препаратов из них является их малая токсичность, возможность длительного применения без побочного действия, широкий спектр фармакологического действия.
Для лечения воспалительных заболеваний используется водный настой цветков ноготков лекарственных в соотношении (1:10) [Государственный реестр лекарственных средств по состоянию на 02.04.2012 [Электронный ресурс] URL: http://grls.rosminzdrav.ru]. Также применяют настои из цветков ромашки аптечной [Соколов, С.Я. Фитотерапия и фитофармакология / С.Я. Соколов. - М.: МИА, 2000. - 970 с.].
Использование водных извлечений в виде настоев и отваров имеют недостатки, заключающиеся в том, что сроки их годности после изготовления составляют 2 суток при температуре +4°C [Фармацевтическая технология. Технология лекарственных форм: учебник / И.И. Краснюк, Г.В. Михайлова, Т.В. Денисова, В.И. Скляренко; под ред. И.И. Краснюка, Г.В. Михайловой. - М.: ГОЭТАР - Медиа, 2011. - 657 с.]. При экстракции растительного сырья водой очищенной не происходит извлечение полного комплекса биологически активных веществ [Минина, С.А. Химия и технология фитопрепаратов: учебное пособие // С.А. Минина, И.Е. Каухова. - М.: ГОЭТАР - Медиа, 2009. - 560 с.]. От 50 до 90% действующих веществ остается в сырье.
В настоящее время хорошо себя зарекомендовали фитопрепараты на основе экстрактов сухих. В процессе получения экстрактов сухих обеспечивается максимальный выход биологически активных веществ (БАВ), возможна разработка дозированных лекарственных форм в виде гранул и таблеток.
Наиболее близким к заявляемому является способ получения средства, обладающего диуретической и противовоспалительной активностью [патент РФ 2342945, М. кл. A61K 36/73, A61P 13/00, A61P 29/00, опубл. 10.01.2009 г.]. Данный способ заключается в том, что в качестве источника сырья используют листья земляники садовой - Fragaria ananassa L. Воздушно-сухие листья измельчают до размера частиц 3 мм и экстрагируют 3 раза по 30 минут водой очищенной в соотношении сырье-экстрагент 1:10 в реакторе из нержавеющей стали с ложным дном вместимостью 100 л, снабженным якорной мешалкой, паровой рубашкой и гильзой для термометра. Водные извлечения объединяют. Очистку объединенных водных извлечений осуществляют фильтрацией через друк-фильтр и сепарированием. Упаривание объединенного водного извлечения проводят в циркуляционном вакуум-выпарном аппарате до 0,1 объема. Сушку проводят на распылительной сушилке. Выход готового продукта составляет 20% от массы растительного сырья.
К недостаткам известного способа относится то, что он не обеспечивает извлечение всего комплекса биологически активных веществ из растительного сырья, так как в данном способе извлекаются только водорастворимые соединения.
Техническим результатом предлагаемого способа является увеличение выхода целевого продукта, расширения сырьевой базы и спектра фармакологического действия.
Технический результат обеспечивается путем экстракции растительного сырья спиртом этиловым 40%, упаривания и сушки.
Новым в достижении технического результата является то, что в качестве растительного сырья используют побеги обмолоченные спиреи иволистной (Spiraea salicifolia L), представляющие собой смесь листьев, цветков и веточек не толще 3 мм.
Спирея иволистная представляет собой кустарник, высотой до 1,5 м, широко распространена на территории России. Надземные органы содержат кумарины, фенолкарбоновые кислоты (кофейная, феруловая), флавоноиды (гиперозид, дипентозид кверцетина). Их максимальное количество накапливается в побегах текущего года в период цветения. В народной медицине спирея иволистная применяется при заболеваниях желудочно-кишечного тракта и мочеполовой системы [Растительные ресурсы СССР: цветковые растения, их химический состав, использование. Семейства Hydrangeaceae-Haloragaceae. - СПб., 1991. - С.101].
Целью настоящего изобретения является повышение выхода биологически активных веществ и расширение спектра фармакологического действия, которые обеспечиваются экстракцией побегов спиреи иволистной - Spiraea salicifolia L. спиртом этиловым 40% трехкратной экстракцией, при соотношении сырье-экстрагент 1:14 в динамических условиях перемешивание сырья, температурой экстракции 55°C, тем, что после объединения извлечений проводят отстаивание.
Оптимальные параметры экстракции были установлены экспериментально (табл.1-5).
Новым является то, что в качестве экстрагента используется спирт этиловый 40%. Для установления оптимального экстрагента были получены извлечения с использованием воды очищенной и 10-90% спирта этилового. Содержание экстрактивных веществ в полученных извлечениях определяли по ГФ XI, флавоноидов спектрофотометрическим методом, основанном на реакции комплексообразования с алюминия хлоридом, расчет процентного содержания проводили в пересчете на рутин. Выход в извлечения фенолкарбоновых кислот контролировали спектрофотометрическим методом. Расчет процентного содержания суммы фенолкарбоновых кислот проводили в пересчете на кофейную кислоту по удельному показателю поглощения кофейной кислоты, равном 782 при длине волны 325 нм.
Вода очищенная извлекает меньше всего экстрактивных веществ, флавоноидов и фенолкарбоновых кислот. С увеличением концентрации спирта этилового идет увеличение выхода биологически активных веществ. Максимальное их количество извлекается с использованием 40% спирта этилового (табл.1). Дальнейшее увеличение концентрации спирта этилового в экстагенте приводит к снижению выхода экстрактивных веществ и суммы флавоноидов.
Новым является также и то, что для экстракции используют сырье с размером частиц 2 мм. Известно, что размер частиц сырья обусловливает полноту и скорость перехода в раствор экстрагируемых веществ. Оптимальная степень измельченности, при которой достигается наибольший выход экстрактивных веществ и флавоноидов при соотношении сырья и экстрагента 1:10 и комнатной температуре, составляет 2 мм (табл.2).
При экстракции сырья с измельчением менее 1 мм, возникают сложности с очисткой извлечения от мельчайших частиц сырья, поэтому в данном случае оптимальный размер частиц - 2 мм.
На выход экстрактивных и, соответственно, биологически активных веществ оказывает влияние соотношение сырье-экстрагент. Наибольшее количество экстрактивных и биологически активных веществ - флавоноидов и фенолкарбоновых кислот извлекается при соотношении сырья и экстрагента 1:14 (табл.3), что также является новым.
На повышение выхода экстрактивных веществ из лекарственного растительного сырья оказывает влияние температурный фактор и процесс перемешивания. Наибольшее количество экстрактивных веществ, флавоноидов и фенолкарбоновых кислот из побегов спиреи иволистной извлекается при температуре 55°C (табл.4). Использование более высоких температур в данном случае невыгодно с экономической точки зрения и обеспечивает стабильность химического состава целевого продукта.
Новым является - продолжительность ступеней экстракции: 1-я ступень - 120 мин, 2-я ступень - 90 мин, 3-я ступень - 60 мин (табл.5), обеспечивающая увеличение выхода целевого продукта.
Новым является то, что перед фильтрацией объединенных извлечений осуществляется их отстаивание при температуре +5°C в течение трех суток, что обеспечивает дополнительную очистку от сопутствующих и балластных веществ, которые выпадают в осадок. Это дает повышение содержания в целевом продукте основных биологически активных веществ - флавоноидов, фенолкарбоновых кислот, дубильных веществ.
Для расчета эффективности экстракции определяли выход экстрактивных веществ на каждой ступени экстракции, суммировали и рассчитывали выход по отношению к массе сухого сырья (табл.6).
Расчет процентного выхода экстрактивных веществ к массе сырья (Y,%) проводили по формуле:
, где
X - рассчитанная масса сухого остатка в общем объеме по трем ступеням, г, равная 3,3935;
m - масса абсолютно сухого сырья (9,279 г).
Эффективность экстракции S (%), по экстрактивным веществам рассчитывали по формуле:
, где
Y - выход экстрактивных веществ к абсолютно сухому сырью, %;
E - содержание экстрактивных веществ в сырье, %, равное 42,86%.
Эффективность экстракции сырья (по экстрактивным веществам) составляет 85,33%.
Авторами были проведены исследования по количественному содержанию суммы флавоноидов, фенолкарбоновых кислот, дубильных веществ, в целевых продуктах, полученных по известному способу и предлагаемому. Так, содержание по известному способу суммы флавоноидов составляет 5,12%, по предлагаемому - 6,83%; суммы фенолкарбоновых кислот по известному способу - 3,26%, по предлагаемому - 7,54%; дубильных веществ по известному способу - 11,28%, по заявляемому - 14,31% (табл.12).
Выход целевого продукта по известному способу - 20%, по предлагаемому - 28%.
Новым является то, что комплекс экстрагируемых биологически активных веществ по предлагаемому способу обладает не только противовоспалительным и мочегонным действием, а также антиоксидантной активностью (табл.7-11).
Сопоставительный анализ заявляемого решения и прототипа показывает, что заявляемый способ отличается от известного тем, что в качестве сырья используют побеги обмолоченные спиреи иволистной с размером частиц сырья - 2 мм. Экстракцию проводят спиртом этиловым 40% при соотношении сырье-экстрагент 1:14, при температуре экстракции 55°C со следующим временным контактом фаз: 1 контакт - 120 мин, 2 контакт - 90 мин, 3 контакт - 60 мин; отстаиванием извлечения при температуре +5°C перед фильтрацией, что соответствует критерию «новизна».
Новая совокупность существенных признаков обеспечивает увеличение целевого продукта на 40% и расширение сырьевой базы за счет широко произрастающей спиреи иволистной, что соответствует критерию «промышленная применимость».
При анализе известных способов было выявлено, что в них отсутствуют сведения о влиянии отличительных признаков заявляемого способа на достижение технического результата, следовательно, изобретение соответствует «изобретательскому уровню».
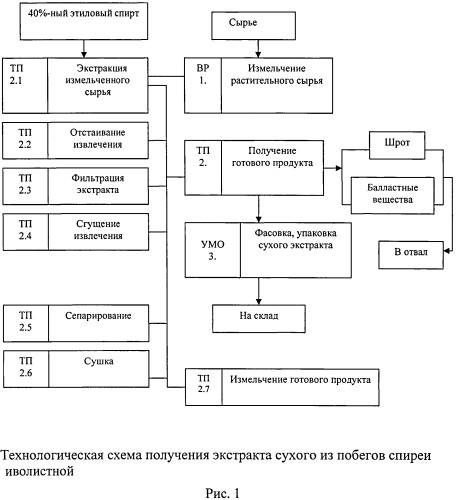
В результате экспериментально подобранных параметров процесса экстракции составлена схема технологического процесса получения экстракта сухого из побегов спиреи иволистной (рис.1).
Оптимальные условия экстракции были положены в основу технологического процесса. Пример конкретного выполнения способа.
Описание технологического процесса
100 г воздушно-сухих побегов спиреи иволистной с размером частиц сырья 2 мм помещают в экстрактор и заливают 1400 мл 40% спирта этилового. Экстракцию проводят на магнитной мешалке при температуре 55°C. Первый контакт фазы - 120 минут. Извлечение сливают в количестве 860 мл (плотность - 0,935 г/см3). Далее проводят еще две экстракции, заливая в экстрактор 40% этиловый спирт в объеме, равном объему слитого извлечения, и экстрагируют при втором контакте фаз 90 минут, при третьем контакте фаз - 60 мин. Получают 500 мл второго извлечения (плотность - 0,933 г/см) и 300 мл третьего извлечения (плотность 0,931 г/см).
Извлечения объединяют и отстаивают при температуре +5°C в течение 3 суток, фильтруют через друк-фильтр.
Фильтрат подают на упарку в ротационный испаритель. Упарку ведут при температуре реакционной массы 55°C и давлении 9,81 гПа до 1л первоначального объема. Водный остаток, содержащий биологически активные вещества, передают на операцию сепарирования. Получают очищенное извлечение в количестве 420 мл (плотность 1,039 г/см3) и осадок балластных веществ - 6,8 г (влажность - 62%), который не используется. Сушку проводят в распылительной сушилке.
Получают экстракт сухой в количестве 28 г, что составляет 28% от массы воздушно-сухого сырья.
Экстракт сухой представляет собой порошок от светло-коричневого до темно-коричневого цвета со слабым запахом и горьковатым слегка вяжущим вкусом.
Параметры стандартизации конечного продукта - экстракта сухого.
Качественное обнаружение биологически активных веществ:
- 0,1 г экстракта сухого растворяют в 20 мл 40% спирта этилового при нагревании на водяной бане в течение 10 мин, фильтруют через бумажный фильтр. К 2 мл фильтрата прибавляют 0,1 г порошка магния и 1 мл кислоты хлористоводородной концентрированной; перемешивают и нагревают на водяной бане 5 минут; постепенно появляется красное окрашивание (флавоноиды);
- 0,5 г экстракта сухого растворяют в 10 мл воды, перемешивают, нагревают на водяной бане в течение 10 минут и фильтруют. К 2 мл фильтрата прибавляют 2-3 капли раствора железоаммониевых квасцов; появляется черно-зеленое окрашивание (дубильные вещества).
Количественное определение суммы флавоноидов
Дифференциальный УФ-спектр спиртового раствора экстракта в присутствии алюминия хлорида имеет максимум поглощения в длинноволновой области при 412 нм и совпадает с максимумом поглощения рутина в комплексе с алюминием хлоридом (рис.2).
Около 0,1 г (точная навеска) экстракта сухого помещают в колбу со шлифом вместимостью 100 мл, прибавляют 30 мл 40% спирта этилового, колбу присоединяют к обратному холодильнику и нагревают на кипящей водяной бане в течение 15 мин. Затем колбу охлаждают до комнатной температуры. Содержимое колбы фильтруют через бумажный фильтр в мерную колбу вместимостью 50 мл и объем раствора доводят 40% спиртом этиловым до метки, перемешивают (раствор A).
В мерную колбу вместимостью 25 мл помещают 1 мл раствора A, прибавляют 1 мл 1% спиртового раствора алюминия хлорида и доводят раствор до метки 96% спиртом этиловым. Через 40 минут измеряют оптическую плотность раствора на спектрофотометре при длине волны 412 нм в кювете с толщиной слоя 10 мм.
В качестве раствора сравнения используют раствор, состоящий из 1 мл раствора A, 1 капли 10% раствора кислоты уксусной и доведенный 96% спиртом этиловым до метки в мерной колбе вместимостью 25 мл.
Параллельно измеряют оптическую плотность раствора РСО рутина, приготовленного аналогично испытуемому раствору.
Содержание суммы флавоноидов в пересчете на рутин и абсолютно сухой экстракт в процентах (X) вычисляют по формуле:
,
где D - оптическая плотность испытуемого раствора; D0 - оптическая плотность раствора РСО рутина; m - масса экстракта, г; m0 - масса РСО рутина, г; W - потеря в массе при высушивании экстракта в процентах.
Примечание. Приготовление раствора РСО рутина: около 0,05 г (точная навеска) РСО рутина, предварительно высушенного при температуре 130-135°C в течение 3 ч, растворяют в 85 мл 95% спирта этилового в мерной колбе вместимостью 100 мл при нагревании на водяной бане, охлаждают, количественно переносят в мерную колбу вместимостью 100 мл, доводят объем раствора тем же спиртом до метки и перемешивают.
Содержание суммы флавоноидов в экстракте сухом 6,83%.
Методика количественного определения суммы фенолкарбоновых кислот в сухом экстракте спиреи иволистной.
Для количественного определения фенолкарбоновых кислот применяли метод прямого спектрофотометрирования с использованием в качестве стандартного образца кофейную кислоту, т.к. максимум поглощения спиртового раствора экстракта сухого спиреи иволистной при 325 нм и совпадает с кофейной кислотой.
1 мл раствора А (полученного для количественного определения содержания суммы флавоноидов) помещают в мерную колбу вместимостью 50 мл и доводят объем раствора 95% спиртом этиловым до метки.
Оптическую плотность раствора определяют на спектрофотометре СФ-46 при длине волны 325 нм в кювете с длиной рабочего слоя 1 см. В качестве раствора сравнения используют 95% спирт этиловый.
Содержание суммы фенолкарбоновых кислот в пересчете на кофейную кислоту и воздушно-сухой экстракт в процентах (X) рассчитывают по формуле:
,
где D - оптическая плотность испытуемого раствора; m - масса сырья, г; W - потеря в массе при высушивании сырья, %; 782 - удельный показатель поглощения кофейной кислоты при 325 нм.
Содержание суммы фенолкарбоновых кислот в экстракте сухом 7,54%.
Количественное содержание дубильных веществ и влажность в экстракте сухом определяли по методикам ГФХ1 [Государственная Фармакопея СССР. - XI-е изд. - М.: Медицина. Т.1, 2 (1987, 1990)].
Содержание дубильных веществ составило 14,31%, влажность экстракта сухого 4,35%.
Противовоспалительная активность
Исследования выполнены на 60 крысах линии Wistar обоего пола массой 180-200 г, содержащихся на стандартном рационе питания при свободном доступе к воде и пище в условиях вивария. Исследования с животными проводились в соответствии с «Правилами Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и иных научных целей».
В эксперименте использовали методики исследования противовоспалительной активности на разных стадиях процесса воспаления: альтерации - по И.А. Ойвину [Ойвин, И.А. Методика изучения местных нарушений капиллярной проницаемости / И.А. Ойвин, СЛ. Шетель // Материалы по патогенезу воспаления и патологии белков крови. - Душанбе, 1961. - Т. 49, №5. - С.167-173], экссудации - по Ю.Е. Стрельникову [Стрельников, Ю.С. Сравнительная характеристика противовоспалительного действия некоторых пиримидиновых производных / Ю.С. Стрельников // Фармакология и токсикология. - 1960. - №6 - С.167-173], пролиферации - Ф.Н. Тринусу [Тринус, Ф.П. Нестероидные противовоспалительные средства / Ф.П. Тринус, Н.А. Мохорт, Б.М. Клебанов. - Киев, 1975. - 240 с.]. Экстракт сухой спиреи иволистной вводили крысам энтерально в виде водного раствора в дозе 100 мг/кг веса крысы, крысы контрольной группы получали воду очищенную в объеме 1 мл.
О воздействии экстракта сухого спиреи иволистной на альтерацию тканей и интенсивность процессов регенерации судили по динамике заживления кожно-мышечного дефекта у крыс, вызванного подкожным введением в область спины 0,5 мл 9% кислоты уксусной с одновременным введением раствора декстрана в дозе 300 мг/кг массы животного. Первое введение препаратов осуществляли за 1 час до введения уксусной кислоты, затем ежедневно 1 раз в сутки в течение 29 дней. На 9 и 29 сутки эксперимента оценивали площадь некротизированной ткани путем нанесения контура некроза на прозрачную пленку.
Оценку влияния спиреи иволистной экстракта сухого на экссудативную фазу воспаления проводили путем однократного введения в заднюю конечность животных 0,1 мл 3% формалина. Исследуемые препараты вводили за 1 час до инъекции, а затем через 5 и 18 часов. Оценку антиэкссудативной активности вычисляли, рассчитывая процент угнетения отека по отношению к контролю.
При изучении процесса образования фиброзно-грануляционной ткани стерильные ватные шарики массой 15 мг имплантировали крысам под кожу в области спины в асептических условиях. Изучаемые препараты вводили 1 раз в сутки в течение 7 дней. Затем образовавшиеся гранулемы взвешивали на аналитических весах сразу после извлечения и после высушивания (при 70°C в течение 24 часов до постоянной массы).
Результаты эксперимента статистически обрабатывали при доверительной вероятности 95%.
Как видно из таблицы 7, экстракт сухой спиреи иволистной в дозе 100 мг/кг оказывает противовоспалительное действие, о чем свидетельствуют уменьшение степени альтерации ткани и повышении интенсивности регенерации процессов в очаге воспаления. Площадь повреждения тканей на 9 и 29 день уменьшается на 14,9 и 19,9% соответственно.
Испытанная доза экстракта сухого спиреи иволистной оказывает антиэкссудативное действие, снижая отек лапки животных на 36,5% по сравнению с контрольной группой (табл.8).
Результаты изучения влияния исследуемых препаратов на стадию пролиферации представлены в таблице 9.
Процент стимуляции образования гранулемы под влиянием экстракта сухого спиреи иволистной составляет 30,9%. Стимуляция образования гранулемы экстрактом сухим возрастает по сравнению с контролем в 1,3 раза.
Мочегонная активность
Исследования проводили на 20 белых мышах массой 20 г по методу Е.Б. Берхина [1977]. Для исследования мочегонного действия использовали две группы животных по 10 мышей в каждой группе: опытной, контрольной. При изучении водного диуреза крыс содержали на постоянном пищевом рационе при свободном доступе к воде. До водной нагрузки животных выдерживали в течение двух часов без пищи и воды. Затем мышам вводили в желудок с помощью зонда водный раствор экстракта сухого в дозе 100 мг/кг. Объем вводимой жидкости с экстрактом составлял 2 мл одновременно с водной нагрузкой в количестве 0,3 мл на 10 г массы тела животного. Мочу собирали через каждый час в течение 4 часов. Контрольная группа мышей получала воду очищенную.
Сухой экстракт спиреи иволистной вызывал увеличение диуреза у животных на 87% в сравнении с контрольной группой (табл.10), что указывает на его мочегонную активность.
Антиоксидантная активность
Определение антиоксидантной активности экстракта сухого проводили in vitro на сыворотке донорской крови человека. К 2 мл сыворотки прибавляли 1 мл тестируемого экстракта, 0,1 мл 0,5 М раствора сульфата меди (II), в качестве индуктора ПОЛ, и инкубировали при t=37°C в течение 16 ч. В контрольном опыте вместо тест-препарата прибавляли 1 мл 0,05 М раствора этилендиаминтетрацетата (ЭДТА) как ингибитора ПОЛ. [Шаварда, А.Л. Антиоксидантная активность видов флоры Алтая / А.Л. Шаварда и [др.] // Растит, ресурсы. - 1998. - т.34. - вып.2. - С.1-8].
Определяли содержание ДК и МДА [Гончаренко, М.С. Метод оценки перекисного окисления липидов / М.С. Гончаренко, A.M. Латинова // Лабораторное дело. - 1985. - №1. - С.60-61].
Экстракт сухой снижал образование ДК в сравнении с контролем на 15%, МДА на 58% (табл.11), что свидетельствует об антиоксидантной активности предлагаемого средства.
Литература
1. Гончаренко, М.С. Метод оценки перекисного окисления липидов / М.С. Гончаренко, A.M. Латинова // Лабораторное дело. - 1985. - №1. - С.60-61.
2. Государственный реестр лекарственных средств по состоянию на 02.04.2012 [Электронный ресурс] URL: http://grls.rosminzdrav.ru
3. Государственная Фармакопея СССР. - XI-е изд. - М.: Медицина. Т.1, 2 (1987, 1990).
4. Минина, С.А. Химия и технология фитопрепаратов: учебное пособие // С.А. Минина, И.Е. Каухова. - М.: ГОЭТАР - Медиа, 2009. - 560 с.
5. Ойвин И.А. Методика изучения местных нарушений капиллярной проницаемости / И.А. Ойвин, СЛ. Шетель // Материалы по патогенезу воспаления и патологии белков крови. - Душанбе, 1961. - Т. 49, №5. - С.167-173. Растительные ресурсы СССР: цветковые растения, их химический состав, использование. Семейства Hydrangeaceae-Haloragaceae. - СПб., 1991. - С.101.
6. Соколов, С.Я. Фитотерапия и фитофармакология / С.Я. Соколов. - М.: МИА, 2000. - 970 с.
7. Стрельников, Ю.С. Сравнительная характеристика противовоспалительного действия некоторых пиримидиновых производных / Ю.С.Стрельников // Фармакология и токсикология. - 1960. - №6 - С.167-173.
8. Тринус, Ф.П. Нестероидные противовоспалительные средства / Ф.П. Тринус, Н.А. Мохорт, Б.М. Клебанов. - Киев, 1975. - 240 с.
9. Фармацевтическая технология. Технология лекарственных форм: учебник / И.И. Краснюк, Г.В. Михайлова, Т.В. Денисова, В.И. Скляренко; под ред. И.И. Краснюка, Г.В. Михайловой. - М.: ГОЭТАР - Медиа, 2011. - 657 с.
10. Шаварда, А.Л. Антиоксидантная активность видов флоры Алтая / А.Л. Шаварда и [др.] // Растит, ресурсы. - 1998. - т.34. - вып.2. - С.1-8.
| Таблица 1 | |||
| Выход суммы экстрактивных веществ, флавоноидов и фенолкарбоновых кислот в зависимости от типа и концентрации экстрагента | |||
| Экстрагент | Содержание, % | ||
| Экстрактивные вещества | Сумма флавоноидов | Сумма фенолкарбоновых кислот | |
| Вода очищенная | 31,49 | 0,55 | 1,30 |
| Спирт этиловый | |||
| 10% | 32,11 | 0,69 | 1,36 |
| 20% | 34,40 | 1,08 | 1,50 |
| 30% | 34,95 | 1,17 | 1,53 |
| 40% | 35,60 | 1,76 | 1,69 |
| 50% | 34,16 | 1,51 | 1,60 |
| 60% | 31,09 | 1,54 | 1,63 |
| 70% | 28,59 | 1,52 | 1,60 |
| 80% | 28,93 | 1,40 | 1,61 |
| 90% | 19,05 | 0,75 | 1,60 |
| Таблица 2 | |||
| Влияние соотношения сырье-экстрагент на выход экстрактивных веществ, флавоноидов и фенолкарбоновых кислот | |||
| Размер частиц сырья, мм | Содержание, % | ||
| Экстрактивные вещества | Сумма флавоноидов | Сумма фенолкарбоновых кислот | |
| 1 | 32,35 | 1,41 | 2,45 |
| 2 | 36,23 | 1,76 | 2,66 |
| 3 | 33,79 | 1,22 | 2,64 |
| 5 | 30,76 | 0,90 | 2,33 |
| Таблица 3 | |||
| Выход экстрактивных веществ, флавоноидов и фенолкарбоновых кислот в зависимости от соотношения сырья и экстрагента | |||
| Соотношение сырья и экстрагента | Содержание, % | ||
| Экстрактивные вещества | Сумма флавоноидов | Сумма фенолкарбоновых кислот | |
| 1:8 | 35,20 | 0,81 | 1,98 |
| 1:10 | 39,07 | 1,20 | 2,06 |
| 1:12 | 39,32 | 1,30 | 2,64 |
| 1:14 | 40,53 | 2,13 | 2,67 |
| 1:16 | 29,90 | 1,95 | 2,65 |
| Таблица 4 | |||
| Выход и экстрактивных веществ, флавоноидов, фенолкарбоновых кислот в зависимости от температуры экстракции | |||
| Температура экстракции, °C | Содержание, % | ||
| Экстрактивные вещества | Сумма флавоноидов | Сумма фенолкарбоновых кислот | |
| 30 | 40,51 | 2,14 | 2,68 |
| 40 | 40,76 | 2,18 | 2,78 |
| 45 | 40,82 | 2,20 | 2,81 |
| 50 | 40,94 | 2,74 | 2,90 |
| 55 | 41,16 | 2,31 | 3,39 |
| 60 | 41,18 | 2,32 | 3,38 |
| 65 | 41,17 | 2,30 | 3,37 |
| 70 | 41,19 | 2,31 | 3,38 |
| Таблица 5 | ||
| Выход экстрактивных веществ в зависимости от числа ступеней и времени экстракции | ||
| Ступень экстракции | Время, мин | Выход экстрактивных веществ, % |
| I | 60 | 41,16 |
| 90 | 43,82 | |
| 120 | 44,27 | |
| 150 | 44,26 | |
| II | 60 | 15,77 |
| 75 | 16,22 | |
| 90 | 17,88 | |
| 120 | 17,79 | |
| III | 30 | 10,83 |
| 60 | 10,81 | |
| 90 | 10,82 |
| Таблица 6 | ||||
| Результаты определения эффективности экстракции (из 10 г сырья) | ||||
| Содержание в сырье, % | Влажность сырья, % | Ступень экстракции | Содержание в г на ступени экстракции | Эффективность экстракции, % |
| Экстрактивные вещества | ||||
| 42,86 | 7,21 | 1 | 2,57398 | 85,33% |
| 2 | 0,64617 | |||
| 3 | 0,17332 | |||
| всего по трем ступеням | 3,39347 |
| Таблица 7 | ||||
| Влияние экстракта сухого спиреи иволистной на альтерацию и регенерацию при остром асептическом воспалении (M±m), n=6 | ||||
| Группа животных | 9 сутки | 29 сутки | ||
| Площадь некротизированной ткани, см2 | Степень уменьшения повреждения кожных покровов, % | Площадь некротизированной ткани, см2 | Степень уменьшения повреждения кожных покровов, % | |
| Контроль (H2O) | 5,50±0,20 | - | 3,26±0,10 | - |
| Спирея иволистная | 4,68±0,12 | -14,9 | 2,71±0,11 | -16,9 |
| Таблица 8 | ||
| Влияние экстракта сухого спиреи иволистной на экссудативную фазу воспаления (M±m), n=6 | ||
| Группа животных | Разность между объемами воспаленной и невоспаленной лапок, мл | Угнетения отека, % |
| Контроль (H2O) | 2,44±0,034 | 0 |
| Спирея иволистная | 1,55±0,10 | -36,5 |
| Таблица 9 | ||
| Влияние экстракта сухого спиреи иволистной на пролиферативную фазу воспаления (M±m), n=6 | ||
| Группа животных | Масса образовавшейся грануляционно-фиброзной ткани, мг | Стимуляция образования гранулемы, % |
| Контроль (Н2О) | 93,80 | 0 |
| Спирея иволистная | 122,78±2,51 | +30,9 |
| Таблица 10 | ||
| Мочегонная активность экстракта сухого спиреи иволистной (M±m), n=6 | ||
| Условие | Контроль (вода очищенная) | Экстракт спиреи иволистной |
| Количество мочи, мл | 1,5±0,1 | 2,8±0,05 |
| Увеличение диуреза в сравнении с контролем | +87% |
| Таблица 11 | ||
| Антиоксидантная активность экстракта сухого спиреи иволистной (M±m), n=6 | ||
| Условия опыта | Контроль | Сухой экстракт спиреи иволистной |
| Диеновый коньюгат (ДК), Оптические единицы | 3,98±0,1 | 3,39±0,1 |
| Степень снижения уровня ДК, % | -15% | |
| Малоновый диальдегид (МДА), мкМ/млмин | 2,15±0,1 | 1,71±0,05 |
| Степень снижения уровня МДА, % | -58% |
| Таблица 12 | |||
| Сравнительная характеристика заявленного способа с выбранным прототипом | |||
| № п/п | Параметр сравнения | Известный способ | Заявленный способ |
| 1 | Растительное сырье | Листья земляники лесной | Побеги спиреи иволистной |
| 2 | Экстрагент | Вода очищенная | Спирт этиловый 40% |
| 3 | Соотношение сырья и экстрагента | 1:10 | 1:14 |
| 4 | Степень измельченности сырья, мм | от 1 до 3 | 2 |
| 5 | Температура экстракции, °C | 75 | 55 |
| 6 | Продолжительность контакта фаз в минутах: | ||
| - первый контакт | 30 | 120 | |
| - второй контакт | 30 | 90 | |
| - третий контакт | 30 | 60 | |
| 7 | Отстаивание при +5°C, 3 суток | - | + |
| 8 | Выход целевого продукта, % | 20 | 28 |
| 9 | Содержание в экстракте сухом суммы флавоноидов, % | 5,12 | 6,83 |
| 10 | Содержание в экстракте сухом суммы фенолкарбоновых кислот, % | - | 7,54 |
| 11 | Содержание в экстракте сухом дубильных веществ, % | - | 14,31 |
| 12 | Фармакологическое действие | ||
| - противовоспалительное | + | + | |
| - мочегонное | + | + | |
| - антиоксидантное | + |
Способ получения средства, обладающего противовоспалительной, мочегонной и антиоксидантной активностью, включающий измельчение побегов спиреи иволистной, представляющих собой смесь листьев, цветков и веточек не толще 3 мм, до частиц размером 2,0 мм, их трехкратную экстракцию методом дробной мацерации 40% этиловым спиртом в соотношении сырье - экстрагент 1:14, при температуре 55°C, перемешивание при настаивании, при этом первый контакт фаз - 120 минут, далее извлечение сливают, проводят еще две экстракции, заливая этиловый спирт в объеме, равном слитому извлечению, второй контакт фаз - 90 минут, третий контакт фаз - 60 минут; извлечения объединяют, отстаивают в течение суток, фильтруют, сгущают, сепарируют, сушат.