Применение 2-морфолино-5-фенил-6н-1,3,4-тиадизин, гидробромида в качестве средства, изменяющего суммарную мощность спектра вариабельности сердечного ритма и обладающего антибрадикардическими свойствами
Иллюстрации
Показать всеИзобретение относится к области профилактической медицины, отдельных специальных разделов клинической медицины и к области биологически активных соединений. Предложено применение гидробромида 2-морфолино-5-фенил-6H-1,3,4-тиадизина в качестве средства, изменяющего суммарную мощность спектра вариабельности сердечного ритма и обладающего антибрадикардическими свойствами. Технический результат: снижение в несколько раз мощности высокочастотной (HF-компонент) составляющей спектра сердечного ритма, а также снижение коэффициента вариации кардиоинтервалов за счет снижения регуляторного влияния парасимпатической нервной системы на ритмику сердца. Эффект изобретения может быть использован при необходимости повышения частоты сердечных сокращений (ЧСС) в случае его быстрого понижения, которое может представлять прямую опасность для жизни человека из-за высокого риска внезапной остановки сердца. 8 ил.
Реферат
Изобретение относится к области профилактической медицины, отдельных специальных разделов клинической медицины и к области биологически активных соединений. Эффект изобретения может быть использован при необходимости повышения частоты сердечных сокращений (ЧСС) в случае его быстрого понижения.
Брадикардия является, чаще всего, результатом первичного органического поражения синусного и атриовентрикулярного узлов при ишемической болезни сердца, артериальной гипертонии, миокардитах, пороках сердца, после операций на открытом сердце. Также брадикардия может быть обусловлена экстракардиальными факторами, такими как нарушение вегетативной иннервации, повышение активности блуждающего нерва или чувствительности синусного узла к его влиянию, в частности у спортсменов, отек головного мозга, заболевания гортани, при высокой чувствительности синокаротидной области, ситуационными стрессовыми состояниями, сопровождающимися болью, страхом. Брадикардия возникает при метаболическом дистресс-синдроме и при нарушениях гемостаза, на фоне гиперкалиемии, гиперкальциемии, гипотиреозе, а также при применении лекарственных средств, урежающих частоту сердечных сокращений, таких как сердечные гликозиды (дигоксин), антиаритмические препараты: блокаторы быстрых натриевых каналов (новокаинамид), блокаторы β-адренорецепторов (анаприлин) и блокаторы медленных кальциевых каналов (верапамил).
Известны лекарственные препараты, повышающие ЧСС, которые применяются в клинике - адреналин, коринфар (Corinfar, Pliva Hrvatska), эуфиллин [Регистр Лекарственных средств России РЛС. Энциклопедия лекарств. - 15-й вып. / Гл. ред. Г.Л. Вышковский. - М.: РЛС - 2007, 2006].
Технический результат настоящего изобретения заключается в расширении арсенала средств, обладающих быстрым и выраженным антибрадикардическим действием.
Технический результат изобретения достигается тем, что в качестве фармакологического средства, обладающего антибрадикардическими свойствами свойствами, применяют 2-морфолино-5-фенил-6H-1,3,4-тиадизин, гидробромид.
Объектом изобретения являются антибрадикардические свойства 2-морфолино-5-фенил-6H-1,3,4-тиадизина, гидробромида (формула I).
Формула I
Ранее для 2-морфолино-5-фенил-6H-1,3,4-тиадизина, гидробромида были описаны антикоагулянтные и антиагрегатные свойства (Патент РФ №2259371 (2005)). Однако антибрадикардические свойства препарата выявлены впервые.
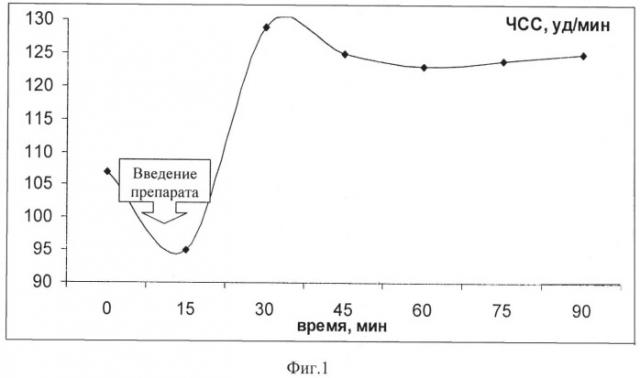
Анализ показателей вариабельности сердечного ритма (ВСР) в эксперименте на собаках выявил увеличение к 30-й минуте наблюдения показателя ЧСС (фиг.1), сохранявшегося до 90 минуты наблюдения. Одновременно отмечалось снижение линейных и нелинейных показателей ВСР, в том числе коэффициента вариации кардиоинтервалов и общей суммарной мощности спектра сердечного ритма (фиг.2), что говорит о снижении экстракардиальных влияний на сердце. Анализ полученных материалов свидетельствует, что выявленное явление происходит за счет ослабления ваготонической модуляции сердечного ритма, что проявляется в снижении мощности высокочастотной (HF-компонент) составляющей спектра сердечного ритма (фиг.3). Эффект увеличения ЧСС может быть использован для коррекции состояний, сопровождающихся брадикардией, которая возникает вследствие нарушения ритмопродуцирующей активности синусного узла и может представлять прямую опасность для жизни человека из-за высокого риска внезапной остановки сердца, развития обморочных состояний и сопровождаться фатальными аритмиями из нижележащих отделов проводящей системы сердца, которые перестают контролироваться импульсами синусного узла.
Эксперименты проведены на 8 беспородных собаках массой 20-25 кг, животных брали в опыт после адаптационного периода, препарат вводили в эффективном количестве, наибольший эффект наблюдали при введении препарата в диапазоне 46-54 мг/кг массы тела.
В первую фазу эксперимента собак наркотизировали золетилом в дозе 10 мг/кг веса животного. После этого производили установку катетеров длиной 20 см в яремную артерию и сонную вену с целью последующего забора артериальной и венозной крови. В катетеры по всей длине вводили раствор гепарина (в соотношении 1:5 с 0,9% раствором NaCl) для предотвращения тромбирования канала катетера. После выхода животного из наркотического сна перед началом 2 фазы эксперимент производили установку датчиков дыхания, датчиков для измерения температуры тела, датчиков для измерения ЭКГ. Послеоперациониый период составлял 48 часов.
При анализе показателей частотных характеристик сердечного ритма было выявлено, что к 30-й минуте эксперимента у животных наблюдалось незначительное увеличение частоты сердечных сокращений, сохранявшееся до конца эксперимента (фиг.1). В «0» точке значения ЧСС составили 107 уд/мин, к 30-й минуте ЧСС возросло до 129 уд/мин.
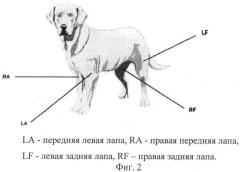
После взвешивания и катетеризации на животное накладывали электроды для регистрации электрокардиограммы. Места присоединения электродов для лучшего контакта с кожей подбривались, затем зажимы типа «крокодил» (с предварительным помещением на место контакта электродного геля) располагали на животное в соответствии со стандартной схемой (фиг.2 LA - передняя левая лапа, RA - правая передняя лапа, LF - левая задняя лапа, RF - правая задняя лапа).
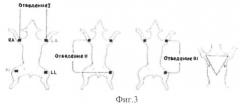
Ритмограмму получали путем 5-минутной регистрации электрокардиограммы в стандартных биполярных отведениях по Энтховену (I, II, III) от конечностей (фиг.3) с помощью электрокардиографа компьютерного «Поли-Снектр-8/Е» (ООО «Нейрософт». Россия, г.Иваново).
После регистрации электрокардиограммы в «0» точке, которая являлась контрольной, ЭКГ регистрировали на 15-й минуте (после введения препарата) и затем каждые 15 минут до окончания эксперимента. После проверки ритмограмм на наличие артефактов производился расчет показателей ВСР при помощи приложения «Поли-Спектр-Ритм», включавший в себя: среднее значение ЧСС, среднее значение R-R интервала, математическое отклонение (S), коэффициента вариации, вариационного размаха R-R-интервалов (Δx), коэффициента асимметрии распределения кардиоинтервалов (As) и эксцесса (Ex), моды (Mo) - величины наиболее часто встречающихся R-R интервалов, амплитуду моды (AMo) - процент встречаемости R-R-интервалов модального диапазона. Также производили расчет следующих спектральных показателей волновой сруктуры сердечного ритма: суммарная мощность спектра (TF), мощность в диапазоне очень низких частот (VLF), мощность в диапазоне низких частот (LF), мощность в диапазоне высоких частот (HF), отношение мощности низких частот к мощности высоких (LF/HF), частоту максимума мощности в диапазоне LF (frLF), частоту максимума мощности в диапазоне HF (frHF).
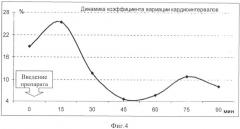
При анализе показателей частотных характеристик сердечного ритма было выявлено, что после введения препарата у животных наблюдалось снижение коэффициента вариации кардиоинтервалов (фиг.4). В «0» точке значения коэффициента вариации составили 18,9%, к 30-й минуте этот показатель снизился до 11,7%, минимальные значения наблюдались на 45-й минуте - 4,57%.
Аналогичная динамика наблюдалась для показателя суммарной мощности спектра вариабельности сердечного ритма (TF), отражающего суммарный уровень активности регуляторных систем (фиг.5). В «0» точке общая мощность спектра сердечного ритма составляла 19372 мс2, к 30-й минуте эксперимента она понизилась до 6255 мс2, минимальные значения наблюдались на 45-й минуте - 587 мс2.
Абсолютные значения высокочастотной составляющей спектра сердечного ритма (HF-компонент), отражающей модулирующее влияние парасимпатического отдела нервной системы, и низкочастотной области спектра сердечного ритма (LF-компонент), обусловленной вспышками симпатической вазомоторной активности и колебаниями ритма артериального давления, имели аналогичную динамику (фиг.6 и фиг.7).
Следует отметить, что если мощность LF-компонента спектра вариабельности сердечного ритма после подъема-снижения к 75-й минуте возвращались к исходным значениям до введения препарата, то мощность высокочастотного компонента у экспериментального животного оставалась сниженной в несколько раз. Все это отражалось на динамике соотношений низкочастотного и высокочастотного компонента (фиг.8), что свидетельствует о смещении вегетативного баланса в сторону увеличения вклада симпатической нервной системы.
Таким образом, установлено, что введение препарата вызывает снижение суммарных нейрогуморальных влияний на ритмику сердца, что обеспечивается понижением регуляторного влияния парасимпатической нервной системы.
Применение 2-морфолино-5-фенил-6H-1,3,4-тиадизина, гидробромида в качестве средства, изменяющего суммарную мощность спектра вариабельности сердечного ритма и обладающего антибрадикардическими свойствами.