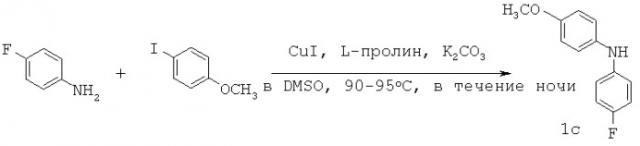
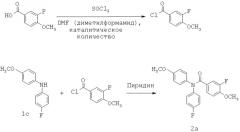
Лиганды рецепторов эстрогенов и способы их применения
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к урологии, и может быть использовано для лечения распространенного рака предстательной железы у субъекта мужского пола. Для этого вводят терапевтически эффективное количество соединения формулы IV или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации:
Способ обеспечивает эффективное лечение, подавление, снижение частоты возникновения, ослабление тяжести или ингибирование распространенного рака предстательной железы, а также паллиативное лечение распространенного рака предстательной железы. 1 н. и 11 з.п. ф-лы, 21 табл., 20 пр., 23 ил.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам уменьшения уровней тестостерона путем уменьшения уровней лютеинизирующего гормона (LH) или независимо от уровней LH у субъекта мужского пола и к способам лечения, подавления, снижения частоты возникновения, ослабления тяжести или ингибирования распространенного рака предстательной железы и паллиативного лечения распространенного рака предстательной железы.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Эстрогены относятся к группе эндогенных и синтетических гормонов, которые важны и используются для поддержания тканей и костей. Эстрогены являются эндокринными регуляторами клеточных процессов, вовлеченных в развитие и поддержание репродуктивной системы. Общепризнана роль эстрогенов в репродуктивной биологии, предупреждении постменопаузальных приливов и предупреждении постменопаузального остеопороза. Важнейшим эндогенным человеческим эстрогеном является эстрадиол, и он обнаружен как у женщин, так и у мужчин.
В проявлении биологических действий эстрогенов и антиэстрогенов участвуют два различных подтипа внутриклеточных рецепторов, рецептор эстрогена альфа (ERα) и рецептор эстрогена бета (ERβ). Обычно эндогенные эстрогены представляют собой сильнодействующие активаторы обоих рецепторных подтипов. Например, эстрадиол действует в качестве агониста ERα во многих тканях, включая ткани молочной железы, костной, сердечно-сосудистой и центральной нервной систем. Обычно селективные модуляторы рецепторов эстрогенов (SERM) в разных тканях действуют по-разному. Например, SERM может быть антагонистом ERα в молочной железе, но может быть частичным агонистом ERα в матке, костной и сердечнососудистой системах. Соответственно, соединения, которые действуют в качестве лигандов рецепторов эстрогенов, полезны в лечении ряда состояний и расстройств.
Рак предстательной железы является одним из наиболее часто диагностируемых типов некожного рака у мужчин в США и второй наиболее общей причиной смерти от рака, и в этом году ожидается более 180000 новых случаев и почти 29000 смертельных исходов. Пациентов с диагнозом распространенный рак предстательной железы подвергают антиандрогенной терапии (ADT), обычно либо посредством агонистов рилизинг-фактора лютеинизирующего гормона (LHRH), либо посредством билатеральной орхиэктомии. В результате антиандрогенной терапии уменьшается не только уровень тестостерона, но также понижаются уровни эстрогена, поскольку эстроген получается в результате ароматизации тестостерона, уровни которого истощаются в результате ADT. Дефицит эстрогенов, индуцированный антиандрогенной терапией, вызывает значительные побочные эффекты, которые включают приливы, гинекомастию и масталгию, потерю костной массы, ухудшение качества и прочности костей, остеопороз и опасные для жизни переломы, неблагоприятные изменения липидов и более частые случаи сердечнососудистого заболевания и инфаркта миокарда, депрессии и других изменений настроения. Считается, что многие побочные эффекты ADT, обусловленные дефицитом эстрогенов, опосредуются ERα.
Лейпролид ацетат (Lupron®) представляет собой синтетический нонапептидный аналог природного гонадотропин-рилизинг гормона (GnRH или LH-RH). Лейпролид ацетат является суперагонистом LH-RH, который в конечном счете подавляет секрецию LH, происходящую в гипофизе. Лейпролид ацетат действует в качестве сильнодействующего ингибитора секреции гонадотропина, вызывая подавление овариального и тестикулярного стероидогенеза. Введение лейпролида ацетата людям сначала вызывает повышение уровней лютеинизирующего гормона (LH) и фолликулостимулирующего гормона (FSH) в кровотоке, приводящее к временному повышению уровней гонадных стероидов (тестостерона и дигидротестостерона у мужчин и эстрона и эстрадиола у женщин в предменопаузальный период). Однако продолжительное введение лейпролида ацетата приводит к уменьшению уровней LH и FSH. У мужчин содержание тестостерона уменьшается до уровней, соответствующих медицинской кастрации (ниже 50 нг/дл). У женщин в предменопаузальный период содержание эстрогенов уменьшается до постменопаузальных уровней. Тестостерон представляет собой известный стимул для злокачественных клеток предстательной железы. Таким образом, подавление секреции тестостерона или ингибирование действий тестостерона является необходимым компонентом терапии рака предстательной железы. Лейпролид ацетат при лечении рака предстательной железы можно использовать для подавления LH, что выражается в уменьшении и снижении уровней тестостерона в сыворотке крови до уровней, соответствующих медицинской кастрации.
Перед тем, как ввести агонисты LHRH, достигали уровней тестостерона, соответствующих медицинской кастрации, повышая эстрогенную активность в гипофизе посредством эстрогенов, преимущественно диэтилстильбэстрола (DES). В равной степени DES был эффективен в качестве агониста LHRH при подавлении тестостерона до уровней, соответствующих медицинской кастрации. У пациентов, подвергнутых лечению с использованием DES, не было приливов или потери костной массы, но наблюдалась гинекомастия в большей степени, чем при проведении ADT с использованием агонистов LHRH. К сожалению, применение высокоэффективных чистых эстрогенов, подобных DES и эстрадиолу, очень часто ассоциировано с высоким риском серьезных сердечно-сосудистых и тромбоэмболических осложнений, которые ограничивают их клиническое применение.
Соединения по данному изобретению уменьшают уровни тестостерона до уровней, соответствующих медицинской кастрации, что может быть полезно для лечения рака предстательной железы, в то же время предупреждая повышенный риск тромботических событий и не вызывая потери костной массы, приливов и/или гинекомастии.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения формулы I-XII, которое изложено в данном описании ниже.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения формулы I-XII, которое изложено в данном описании ниже, причем такое снижение общего тестостерона в сыворотке крови происходит путем уменьшения уровней лютеинизирующего гормона в сыворотке крови.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения формулы I-XII , которое изложено в данном описании ниже, причем такое снижение общего тестостерона в сыворотке не зависит от уменьшения уровней лютеинизирующего гормона в сыворотке
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения формулы I-XII , которое изложено в данном описании ниже, где указанное введение указанных соединений формулы I-XII предупреждает возникновение или приводит к лечению побочных эффектов, связанных с проведением антиандрогенной терапии (ADT), при этом указанный субъект имеет рак предстательной железы.
В одном из воплощений согласно данному изобретению предложен способ антиандрогенной терапии для субъекта, включающий введение терапевтически эффективного количества соединения формулы I-XII, которое изложено в данном описании ниже. В другом воплощении указанный субъект имеет рак предстательной железы.
В одном из воплощений согласно данному изобретению предложен способ лечения, подавления, снижения частоты возникновения, ослабления тяжести или ингибирования распространенного рака предстательной железы, включающий введение терапевтически эффективного количества соединения формулы I-XII, которое изложено в данном описании ниже.
В одном из воплощений согласно данному изобретению предложен способ паллиативного лечения распространенного рака предстательной железы, включающий введение терапевтически эффективного количества соединения формулы I-XII, которое изложено в данном описании ниже.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Признаваемый изобретением объект указан особо и заявлен отчетливо в заключительной части данного описания. Тем не менее, данное изобретение, как в отношении организации, так и способа действия, вместе с его задачами, признаками и преимуществами лучше всего может быть понято со ссылкой на следующее далее подробное описание при его рассмотрении вместе с прилагаемыми графическими материалами, в которых:
на Фиг.1 представлены уровни тестостерона (непрерывная линия) и андрогенов в целом (пунктирная линия) в сыворотке крови у интактных самцов макак после ежесуточного перорального (п/о) введения Соединения IV в дозе 30 мг/кг (первая доза в 0-е сутки) (см. Пример 8);
на Фиг.2 представлены уровни тестостерона у интактных крыс, обработанных Соединением IV (0,3; 1; 10; 30 мг/кг). Iозначает Р<0,05 в сравнении с интактными контролями, обработанными разбавителем. Величины BLOQ (ниже предела количественного определения) представлены графически с пределом количественного определения 0,08 нг/мл (см. Пример 9);
на Фиг.3 представлено ингибирующее влияние Соединения IV на активность фермента 17β-HSD5 (см. Пример 12);
на Фиг.4 представлена агрегация человеческих тромбоцитов in vitro в присутствии DES, 17β-эстрадиола (Е2) и Соединения IV. Обогащенную тромбоцитами плазму (PRP) инкубировали вместе с разбавителем, Е2, DES или Соединением IV в течение 30 секунд, после чего индуцировали агрегацию, используя 0,3 единицы тромбина. Мониторинг агрегации проводили в течение 5 минут и выражали в процентном отношении к контролю - разбавителю (см. Пример 13);
Фиг.5. Типичная схема синтеза для получения Соединений II-XII (см. Пример 1);
Фиг.6. Схема синтеза для получения Соединения IV (см. Пример 2);
Фиг.7. Схема синтеза для получения Соединения VI (см. Пример 3);
Фиг.8. Схема синтеза для получения Соединений IX и Х (см. Пример 5);
на Фиг.9 представлены уровни тестостерона у интактных крыс, обработанных Соединением IV в дозировках 3 мг/кг, 10 мг/кг и 300 мг/кг, через 24 ч, 72 ч и 168 ч (см. Пример 9);
на Фиг.10 представлены уровни LH (Фиг.10А), уровни FSH (Фиг.10 В), уровни тестостерона (Фиг.10С), уровни массы предстательной железы (Фиг.10D), уровни массы семенных пузырьков (Фиг.10Е) и массы леватора (Фиг.10F) у интактных и орхиэктомированных (ORX) крыс, обработанных Соединением IV в дозировках 0,3 мг/кг, 1 мг/кг, 3 мг/кг, 10 мг/кг и 30 мг/кг. Iозначает Р<0,05 в сравнении с интактными контролями, обработанными разбавителем. Oозначает Р<0,05 в сравнении с ORX-контролями, обработанными разбавителем. Величины BLOQ представлены графически с пределом количественного определения 0,08 нг/мл (см. Пример 9);
на Фиг.11 представлен размер предстательной железы у интактных и подвергнутых ORX крыс после введения Соединения IV (Фиг.11А) и DES (Фиг.11В) в различных дозировках (см. Пример 15);
на Фиг.12 представлены различия между DES и Соединением IV; DES дает перекрестную реакцию с глюкокортикоидным рецептором (GR), тогда как Соединение IV нет (Фиг.12А); DES дает перекрестную реакцию с андрогенным рецептором (AR). Он слабо стимулирует и слабо ингибирует действие AR (т.е. является частичным агонистом/антагонистом), тогда как Соединение IV нет (Фиг.12В); DES устраняет трансактивацию рецепторов, родственных рецептору эстрогена, (ERR), тогда как Соединение IV нет (Фиг.12С) (см. Пример 15);
на Фиг.13 представлено влияние Соединения IV в дозировках 5 мг/кг, 10 мг/кг, 15 мг/кг и 30 мг/кг на ослабление приливов в модели отмены морфина. N=7 животных на одну группу. 17β-E2 использовали в дозе 5 мг/кг в 100%-ом DMSO (диметилсульфоксиде) (см. Пример 14);
на Фиг.14 представлено дозозависимое уменьшение массы тела (кг) макак (~20% при дозе 100 мг/кг) после введения Соединения IV в течение 91 суток. Не наблюдали никаких признаков гинекомастии или гиперэстрогении (см. Пример 16);
на Фиг.15 представлено дозозависимое уменьшение уровня тестостерона в сыворотке крови (нг/мл) у макак после ежесуточного перорального введения Соединения IV в сравнении с положительным контролем (агонистом LHRH). Пунктирная линия указывает на уровень тестостерона у химически кастрированных пациентов, а жирная пунктирная линия указывает на уровень тестостерона у хирургически кастрированных макак (см. Пример 16);
на Фиг.16 представлена зависимость уровня антигена предстательной железы (PSA) (нг/мл) от дозы у макак после введения Соединения IV в исходный момент и на 28-е сутки. Обработка Соединением IV значительно уменьшала уровни PSA (см. Пример 16);
на Фиг.17 представлена зависимость объема предстательной железы, измеренного с использованием трансректальной ультрасонографии (TRUS), от дозы у макак в сравнении с положительным контролем (агонистом LHRH) после введения Соединения IV, для 6-й недели (см. Пример 16);
на Фиг.18 представлена зависимость массы органов (предстательной железы, семенных пузырьков и семенников) от дозы у макак после введения Соединения IV в процентном отношении к контролю на 90-е сутки (Фиг.18А). Масса предстательной железы у макак при вскрытии на 13-е сутки после ежесуточного перорального введения Соединения IV (Фиг.18В) (см. Пример 16);
на Фиг.19 представлена зависимость средних уровней общего тестостерона (нмоль/л) от дозы у людей в период между 1-ми и 11-ми сутками после введения Соединения IV (100 мг, 300 мг, 600 мг и 1000 мг) (см. Пример 17);
на Фиг.20 представлена зависимость средних уровней LH (МЕ(международные единицы)/л) от дозы у людей в период между 1-ми и 10-ми сутками после введения Соединения IV (100 мг, 300 мг, 600 мг и 1000 мг) (см. Пример 17);
на Фиг.21 представлена зависимость средних уровней свободного тестостерона (пг/мл) от дозы у людей в период между 1-ми и 10-ми сутками после введения Соединения IV (100 мг, 300 мг, 600 мг и 1000 мг) (см. Пример 17);
на Фиг.22 представлена зависимость средних уровней PSA (мкг/л) от дозы у людей в период между между 1-ми и 10-ми сутками после введения Соединения IV (100 мг, 300 мг, 600 мг и 1000 мг) (см. Пример 17);
на Фиг.23 представлена зависимость уровней тестостерона (нг/мл) от дозы у интактных крыс через 14 суток восстановления после введения Соединения IV. Iозначает Р<0,05 в сравнении с интактными контролями (см. Пример 10).
Следует иметь в виду, что для простоты и ясности иллюстрации, элементы, показанные на графических материалах, не обязательно должны быть представлены в масштабе. Например, размеры некоторых элементов могут быть преувеличены по сравнению с другими элементами для ясности. Кроме того, там, где это целесообразно, номера позиций для обозначения соответствующих или аналогичных элементов могут повторяться среди графических материалов.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
В следующем далее подробном описании изложены многочисленные характерные подробности в целях обеспечения всестороннего понимания изобретения. Однако специалистам в данной области понятно, что настоящее изобретение может быть реализовано на практике без этих характерных подробностей. В других случаях подробно не описаны хорошо известные способы, методики и компоненты, чтобы не загромождать настоящее изобретение.
В одном из воплощений, соединения, которые изложены в данном описании, и/или композиции, содержащие эти соединения, могут быть использованы для снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола.
В одном из воплощений, соединения, которые изложены в данном описании, и/или композиции, содержащие эти соединения, могут быть использованы для снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, причем такое снижение общего тестостерона в сыворотке происходит путем уменьшения уровней лютеинизирующего гормона (LH) в сыворотке.
В одном из воплощений, соединения, которые изложены в данном описании, и/или композиции, содержащие эти соединения, могут быть использованы для снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, причем такое снижение общего тестостерона в сыворотке не зависит от уменьшения уровней лютеинизирующего гормона в сыворотке.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, представленного структурой формулы I:
где
Y представляет собой С(O) или СН2;
R1, R2 независимо представляют собой водород, галоген, гидроксил, алкокси, циано, нитро, CF3, N(R)2, сульфонамид, SO2R, алкил, галогеноалкил, арил, O-Alk-NRaRe или O-Alk-гетероцикл, в котором гетероцикл представляет собой 3-7-членное замещенное или незамещенное гетероциклическое кольцо, возможно ароматическое;
R3, R4 независимо представляют собой водород, галоген, гидроксиалкил, гидроксил, алкокси, циано, нитро, CF3, NHCOR, N(R)2, сульфонамид, SO2R, алкил, галогеноалкил, арил или защищенный гидроксил;
R представляет собой алкил, водород, галогеноалкил, дигалогеноалкил, тригалогеноалкил, CH2F, CHF2, CF3, CF2CF3, арил, фенил, галоген, алкенил, CN, NO2 или ОН;
R5 и R6 независимо представляют собой водород, фенил, алкильную группу из 1-6 атомов углерода, 3-7-членный циклоалкил, 3-7-членный гетероцикл, 5-7-членный арил; или R5 и R6 образуют 3-7-членное кольцо вместе с атомом азота;
j и k независимо равны 1-4;
Alk представляет собой линейный алкил из 1-7 атомов углерода, разветвленный алкил из 1-7 атомов углерода или циклический алкил из 3-8 атомов углерода.
В дополнительных воплощениях способов, изложенных в данном описании, соединение формулы I представлено формулой IA:
где R1, R2, R3, R4, j и k такие, как определено для формулы I.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, представленного соединением формулы II:
.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, представленного соединением формулы III:
.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения или его изомера, фармацевтического продукта, фармацевтически приемлемой соли, полиморфа, гидрата или любой их комбинации, представленного соединением формулы IV:
.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, представленного соединением формулы V:
.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, представленного соединением формулы VI:
.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, представленного соединением формулы VII:
.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, представленного соединением формулы VIII:
.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови путем уменьшения уровней лютеинизирующего гормона (LH) у субъекта мужского пола, имеющего рак предстательной железы, включающий введение терапевтически эффективного количества соединения или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, представленного соединением формулы IX:
.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, представленного соединением формулы X:
.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, представленного соединением формулы XI:
.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, представленного соединением формулы XII:
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения формулы IA, I-XII или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации. В другом воплощении субъект мужского пола имеет рак предстательной железы. В другом воплощении общий тестостерон в сыворотке крови снижен до уровня меньше примерно 100 нг/дл. В другом воплощении общий тестостерон в сыворотке крови снижен до уровня меньше примерно 50 нг/дл. В другом воплощении концентрация общего тестостерона в сыворотке крови снижена до уровня меньше примерно 25 нг/дл.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения формулы IA, I-XII или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, причем такое снижение общего тестостерона в сыворотке происходит путем уменьшения уровней лютеинизирующего гормона (LH) в сыворотке. В другом воплощении субъект мужского пола имеет рак предстательной железы. В другом воплощении общий тестостерон в сыворотке крови снижен до уровня меньше примерно 100 нг/дл. В другом воплощении общий тестостерон в сыворотке крови снижен до уровня меньше примерно 50 нг/дл. В другом воплощении концентрация общего тестостерона в сыворотке крови снижена до уровня меньше примерно 25 нг/дл.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней свободного тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения формулы IA, I-XII или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, причем такое снижение свободного тестостерона в сыворотке происходит путем уменьшения уровней лютеинизирующего гормона (LH) в сыворотке. В другом воплощении субъект мужского пола имеет рак предстательной железы.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения формулы IA, I-XII или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, причем такое снижение общего тестостерона в сыворотке не зависит от уменьшения уровней лютеинизирующего гормона (LH) в сыворотке. В другом воплощении субъект мужского пола имеет рак предстательной железы. В другом воплощении общий тестостерон в сыворотке крови снижен до уровня меньше примерно 100 нг/дл. В другом воплощении общий тестостерон в сыворотке крови снижен до уровня меньше примерно 50 нг/дл. В другом воплощении концентрация общего тестостерона в сыворотке крови снижена до уровня меньше примерно 25 нг/дл.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней свободного тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества соединения формулы IA, I-XII или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации, причем такое снижение уровней свободного тестостерона в сыворотке не зависит от уменьшения уровней лютеинизирующего гормона в сыворотке. В другом воплощении субъект мужского пола имеет рак предстательной железы.
В одном из воплощений согласно данному изобретению предложены способы снижения уровней общего тестостерона в сыворотке крови или уровней свободного тестостерона в сыворотке крови у субъекта мужского пола, причем указанный субъект мужского пола имеет рак предстательной железы. В другом воплощении указанный субъект имеет распространенный рак предстательной железы.
В одном из воплощений уменьшение концентраций тестостерона в сыворотке крови является обратимым и после лечения соединениями по изобретению наблюдается возврат к уровням исходного момента времени.
В другом воплощении концентрации тестостерона в сыворотке крови являются обратимыми после лечения Соединением IV, согласно Фиг.23 и Примеру 10.
В одном из воплощений согласно данному изобретению предложены способы снижения уровней общего тестостерона в сыворотке крови у субъекта мужского пола, включающие введение терапевтически эффективного количества соединения формулы IA, I-XII или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации. В другом воплощении общий тестостерон в сыворотке крови снижен до уровня меньше примерно 100 нг/дл. В другом воплощении общий тестостерон в сыворотке крови снижен до уровня меньше примерно 50 нг/дл. В другом воплощении общий тестостерон в сыворотке крови снижен до уровня меньше примерно 25 нг/дл. В другом воплощении общий тестостерон в сыворотке крови снижен до уровня меньше примерно 75 нг/дл. В другом воплощении общий тестостерон в сыворотке крови снижен примерно до уровня в диапазоне от 75 нг/дл до 100 нг/дл. В другом воплощении общий тестостерон в сыворотке крови снижен примерно до уровня в диапазоне от 50 нг/дл до 75 нг/дл. В другом воплощении общий тестостерон в сыворотке крови снижен примерно до уровня в диапазоне от 40 нг/дл до 50 нг/дл. В другом воплощении концентрация общего тестостерона в сыворотке крови снижена примерно до уровня в диапазоне от 25 нг/дл до 50 нг/дл. В другом воплощении общий тестостерон в сыворотке крови снижен примерно до уровня в диапазоне от 40 нг/дл до 60 нг/дл.
Уровни тестостерона в сыворотке крови могут быть измерены в виде уровней "свободного" (то есть биодоступного и несвязанного) или в виде "общего" тестостерона (включая процентную долю тестостерона, связанного с белком и недоступного). Мужчины старше 40 лет, у которых нет рака предстательной железы, демонстрируют низкие уровни тестостерона, соответствующие уровню общего тестостерона менее 250 нг/дл (<8,7 нмоль/л) или уровню свободного тестостерона менее 0,75 нг/дл (<0,03 нмоль/л).
В одном из воплощений среди способов по данному изобретению предложен способ снижения уровней общего и/или свободного тестостерона в сыворотке крови независимо от уменьшения уровней лютеинизирующего гормона (LH) или путем уменьшения уровней LH у субъекта мужского пола, имеющего рак предстательной железы. В другом воплощении изменения уровней тестостерона будут представлять собой уменьшение относительно уровня перед лечением. В другом воплощении уровень общего тестостерона в сыворотке крови снижен до величины меньше 100 нг/дл. В другом воплощении общий тестостерон в сыворотке крови снижен до уровня меньше 50 нг/дл. В другом воплощении общий тестостерон в сыворотке крови снижен до уровня меньше 25 нг/дл. В другом воплощении уровень свободного тестостерона снижен до величины меньше 2 нг/дл. В другом воплощении уровень свободного тестостерона снижен до величины меньше 1 нг/дл. В другом воплощении уровень свободного тестостерона снижен до величины меньше 0,5 нг/дл. В другом воплощении уровень свободного тестостерона снижен до величины меньше 0,25 нг/дл.
Способы определения уровней свободного тестостерона в сыворотке крови и уровней общего тестостерона в сыворотке крови включают мониторинг уровней тестостерона в продолжение периода лечения посредством проведения анализа крови. Общий тестостерон представляет собой комбинацию циркулирующего в кровотоке тестостерона, связанного с белками-носителями (альбумином, SHBG (глобулин, связывающий половые гормоны (от англ. sex hormone-binding globulin), транскортином, трансферрином), и свободного/несвязанного гормона. На уровни общего тестостерона могут влиять различные факторы, включая уровень белка в крови, который транспортирует этот гормон в организме, возраст, наличие ожирения и помехи, ассоциируемые с обычно используемыми методами тестирования.
Способы, пригодные для измерения свободного тестостерона (FT), могут быть сложными (равновесный диализ и расчет свободного тестостерона (CFT)) или простыми (имеющийся в продаже набор для определения FT "Coat-A-Count") с использованием аналогичного меченого вещества. В другом воплощении измерения уровней общего тестостерона и свободного тестостерона в сыворотке крови можно достичь путем одновременного измерения общего тестостерона и SHBG (например, используя набор для подсчета результатов иммунорадиометрического анализа (от англ. immunoradiometric assay) Irma-Count от DPC (Diagnostic Products Corporation)) и затем расчета свободного тестостерона (CFT). В другом воплощении измерение общего тестостерона и свободного тестостерона находится в компетенции специалиста в данной области.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона в сыворотке крови или уровней свободного тестостерона в сыворотке крови у субъекта мужского пола, включающий введение терапевтически эффективного количества комбинации одной или более чем одной другой формы ADT и соединения формулы IA, I-XII или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации. В другом воплощении снижение общего или свободного тестостерона в сыворотке крови происходит путем уменьшения уровня лютеинизирующего гормона (LH) в сыворотке крови. В другом воплощении снижение уровней общего или свободного тестостерона в сыворотке крови не зависит от уменьшения уровней лютеинизирующего гормона в сыворотке крови.
Способы по данному изобретению включают введение комбинации других форм ADT и соединения по изобретению. В одном из воплощений другие формы ADT включают применение агониста LHRH. В другом воплощении агонистом LHRH является лейпролид ацетат (Lupron® (US 5480656; US 5575987; 5631020; 5643607; 5716640; 5814342; 6036976; все они включены в данное описание посредством ссылки) или гозерелин ацетат (Zoladex®) (US 7118552; 7220247; 7500964; все они включены в данное описание посредством ссылки). В одном из воплощений другие формы ADT включают применение антагониста LHRH. В другом воплощении антагонистом LHRH является дегареликс. В одном из воплощений другие формы ADT включают применение антиандрогенов. В другом воплощении антиандрогенами являются бикалутамид, флутамид, финастерид, дутастерид, MDV3100, нилутамид, хлормадинон или любая их комбинация.
В одном из воплощений способы по данному изобретению включают введение терапевтически эффективного количества антиандрогена и соединения по изобретению. В одном из воплощений способы по данному изобретению включают введение терапевтически эффективного количества агониста LHRH и соединения по изобретению. В одном из воплощений способы по данному изобретению включают введение терапевтически эффективного количества антиандрогена, агониста LHRH и соединения по изобретению.
В одном из воплощений согласно данному изобретению предложен способ снижения уровней общего тестостерона и/или уровней свободного тестостерона в сыворотке крови путем уменьшения уровней лютеинизирующего гормона (LH) или независимо от уменьшения уровней лютеинизирующего гормона у субъекта мужского пола, имеющего рак предстательной железы, с целью проведения антиандрогенной терапии (ADT), включающий введение терапевтически эффективного количества соединения формулы IA, I-XII. В другом воплощении этим соединением является Соединение IV.
В другом воплощении согласно данному изобретению предложен способ антиандрогенной терапии (ADT) субъекта, включающий введение терапевтически эффективного количества соединения формулы IA, I-XII или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации. В другом воплощении указанный субъект имеет рак предстательной железы. В другом воплощении этим соединением является Соединение IV.
В другом воплощении ADT применяют для лечения рака предстательной железы, для замедления прогрессирования рака предстательной железы или для предупреждения и/или лечения рецидива рака предстательной железы.
В одном из воплощений согласно данному изобретению предложен способ лечения рака предстательной железы, замедления прогрессирования рака предстательной железы, предупреждения и/или лечения рецидива рака предстательной железы, включающий введение соединения по изобретению. В другом воплощении введение соединения по изобретению в комбинации с аналогами LHRH, обратимыми антиандрогенами (такими как бикалутамид или флутамид), антиэстрогенами, противораковыми лекарственными средствами, ингибиторами 5-альфа-редуктазы, ингибиторами ароматазы, прогестинами, селективными модуляторами андрогеновых рецепторов (SARM) или аге