Способ прогнозирования ранней постинфарктной стенокардии у пациентов с острым инфарктом миокарда с подъемом сегмента st в госпитальном периоде
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к кардиологии и касается прогнозирования ранней постинфарктной стенокардии (РПИС) у пациентов с острым инфарктом миокарда с подъемом сегмента ST в госпитальном периоде. Для этого осуществляют анализ клинических данных и параметров липидного профиля в первые сутки от начала заболевания. Риск развития РПИС прогнозируют по формуле:P=-3,238+0,01·КДО+0,049·ФВ-0,532·СЖК+0,002·анти омЛПНП+0,001·ПВ-1,129·ХС ЛПВП,где КДО - конечный диастолический объем, ФВ - фракция выброса левого желудочка, СЖК - свободные жирные кислоты, анти омЛПНП - антитела к окислительно-модифицированным липопротеинам низкой плотности, ПВ - пероксид водорода, ХС ЛПВП - холестерин липопротеинов высокой плотности. При значениях Р меньших 0,606 и максимально приближенных к центроиду - 0,080 у пациента прогнозируют РПИС. Способ обеспечивает повышение достоверности индивидуального прогнозирования РПИС в первые сутки от начала заболевания, что, в свою очередь, позволяет максимально рано проводить соответствующую корригирующую терапию. 2пр., 2 таб.
Реферат
Изобретение относится к области медицины, а именно к кардиологии, и может быть использовано для прогнозирования ранней постинфарктной стенокардии у пациентов в госпитальном периоде острого инфаркта миокарда с подъемом сегмента ST.
Инфаркт миокарда с подъемом сегмента ST остается одной из наиболее актуальных проблем современной кардиологии, на протяжении многих десятилетий являясь лидером в причинах смертности населения от сердечно-сосудистых заболеваний. Согласно современным представлениям у 20-60% больных инфарктом миокарда с подъемом сегмента ST отмечается развитие ранней постинфарктной стенокардии (РПИС), которая увеличивает риск рецидива инфаркта миокарда, фатальных нарушений ритма, острой левожелудочковой недостаточности, внезапной смерти [Арутюнов Г.П. с соавт., 2005]. Развитие ранней постинфарктной стенокардии связывают с рецидивирующей ишемией миокарда. В исследованиях последних лет показано, что для больных инфарктом миокарда с подъемом сегмента ST, осложненным развитием ранней постинфарктной стенокардии, характерны многососудистое поражение коронарных артерий, развитие реокклюзии инфаркт-связанной коронарной артерии, дистальная эмболизация тромботическими массами с развитием окклюзии коллатерального кровотока и нарушением микроциркуляции. При этом своевременное выявление факторов риска развития ранней постинфарктной стенокардии в значительной степени позволяет своевременно коррегировать тактику ведения данной категории пациентов и снизить риск фатальных осложнений.
Одним из путей повышения эффективности прогнозирования развития и течения острых коронарных событий является поиск и использование диагностических показателей, наиболее точно характеризующих риск возникновения ранней постинфарктной стенокардии.
Для диагностики РПИС существует ряд методов разной сложности, среди которых наибольшую известность получил способ прогнозирования по уровню гомоцистеина (Люсов В.А. Значение гипергомоцистеинемии для риска неблагоприятных исходов инфаркта миокарда / В.А. Люсов, А.Ю. Лебедева, К.В. Михайлова // Четвертая Московская ассамблея «Здоровье столицы» - 2005). В основе способа лежит определение содержания гомоцистеина в 1-е сутки инфаркта миокарда иммуноферментным методом с использованием набора фирмы «Axis - ShieldAS» (Норвегия). К недостаткам известного способа относится его низкая прогностическая достоверность - 66%.
Известен способ диагностики РПИС у больных острым инфарктом миокарда по уровню нитрита азота (NO2), который реализуется посредством систематического определения нитрита в сыворотке крови больных инфарктом миокарда (Пат. 2335773 Рос. Федерация : МПК G01N 33/84. Способ диагностики ранней постинфарктной стенокардии у больных острым инфарктом миокарда [Текст] / В.Р. Вебер, К.Р. Карибаев, Б.А. Дикалов, И.Е. Айманов; заявитель и патентообладатель ГОУ ВПО «Новгородский государственный университет им. Я. Мудрого» (RU). - №2007103036/15; заявл. 25.01.07; опубл. 10.10.08, бюл. 28. - 4 с.), при этом увеличение показателя более 2,15 мкг/мл прогнозирует начало развития РПИС. Данный метод позволяет с большей достоверностью прогнозировать РПИС, однако к его недостаткам можно отнести отсутствие статистических доказательств получения пороговой концентрации нитрита азота (NO2) равной 2,15 мкг/мл, а именно автор не приводит данных о чувствительности, специфичности метода, не указывает площадь под ROC-кривой, значения 95% доверительного интервала и отношения шансов. Кроме того, на уровень нитрита азота (NO2) в крови может оказывать влияние прием лекарственных препаратов группы нитратов (нитроглицерин) больными ИМ, поскольку возможно НАД·Н2-зависимое восстановление нитрата до нитрита, катализируемое нитратредуктазой.
Известен способ прогнозирования РПИС на основании метода нормирования интенсивных показателей (Пирназаров М.М. Математическое прогнозирование ранней постинфарктной стенокардии / М.М. Пирназаров, Ф.Х. Турсунов // Лiки Украïни. - 2008. - №9. - С.70-73). В способе использованы разработанные прогностические матрицы по данным анамнеза, клинической симптоматике и данным ЭКГ. Прогностическая матрица включает все отобранные факторы риска с их градацией и значениями интегрированного показателя от силы влияния отдельного фактора (X), показателя относительного риска по каждому фактору (R) и их сумму по комплексу факторов (RN), а также нормирующую величину - средний показатель частоты РПИС по данным всего исследования (N). Полученные суммарные значения минимальных и максимальных значений прогностических индексов позволили выявить диапазоны риска РПИС и выделить три категории - «благоприятный прогноз», «внимание», «неблагоприятный прогноз».
Однако данный метод учитывает лишь клинико-анамнестические факторы и данные ЭКГ и не оценивает роль лабораторных маркеров, ориентированных на патофизиологические аспекты заболевания. Изменение содержания таких маркеров в клетках и крови пациентов является отражением внутриклеточных повреждений с нарушением клеточного гомеостаза. Недоучет патофизиологических факторов на наш взгляд можно отнести к недостаткам данного метода.
Наиболее близким к заявляемому является способ прогнозирования риска развития РПИС у больных инфарктом миокарда с подъемом сегмента ST (Бобровская Е.Е. Предикторы ранней постинфарктной стенокардии у больных инфарктом миокарда с подъемом сегмента ST: автореф. дисс. канд. мед. наук: 14.01.05/Е.Е. Бобровская; Санкт-Петербург. ФГУ «Федеральный центр сердца крови и эндокринологии им. В.А. Алмазова» Минздравсоцразвития РФ. - С-Пб., 2011. - 20 с.). При этом в группу признаков, достоверно определяющих высокий относительный шанс развития РПИС, вошли анамнестические и клинические признаки, данные инструментального обследования, носительство у пациента II генотипа АСЕ гена. Из лабораторных маркеров прогностическими предикторами являются - уровень лейкоцитов ≥14*109, содержание C-реактивного белка ≥10 мг/л; уровень фибриногена ≥5 г/л, глюкозы ≥8 ммоль/л и тропонина I≥2 нг/мл. Данные лабораторные показатели оценивают в первые 6 часов от начала острого инфаркта миокарда с элевацией сегмента ST. Кроме того, дополнительно на вторые сутки от начала заболевания оценивают концентрацию глюкозы (≥6,2 ммоль/л) и холестерина (≥7 ммоль/л).
Недостатком способа является использование разных временных интервалов для определения параметров, влияющих на риск развития РПИС: клинические признаки, данные инструментального обследования и лабораторные маркеры оцениваются в первые часы инфаркта миокарда, в то же время диагностической значимостью обладает уровень холестерина и глюкозы, оцененный на вторые сутки от развития заболевания. Наличие разных временных интервалов оказывает влияние на скорость принятия решения о стратификации пациента в группу риска. Кроме того, к недостаткам прототипа можно отнести сложность методики определения носительства II генотипа АСЕ гена, проведение которой требует наличия специального технического оснащения лаборатории и обученного персонала. Проведение данной методики является к тому же длительной и дорогостоящей процедурой.
Техническим результатом предложенного изобретения является повышение достоверности персонифицированного прогнозирования развития ранней постинфарктной стенокардии у пациентов с острым инфарктом миокарда с подъемом сегмента ST в раннем госпитальном периоде, при этом прогноз осуществляют уже на первые сутки от начала заболевания, что позволяет максимально рано проводить коррегирующие мероприятия.
Технический результат достигается за счет того, что в сыворотке крови больного определяют концентрации параметров липидного профиля и показателей про-/антиоксидантной систем, ориентированных на патофизиологические аспекты заболевания в 1-е сутки острого инфаркта миокарда (ИМ) с элевацией сегмента ST, а вероятный риск рассчитывают с помощью диагностической модели.
Для определения прогностически значимых критериев ранней постинфарктной стенокардии, на базе ФГБУ «НИИ КПССЗ» СО РАМН, проведено исследование, включающее 133 пациента (90 мужчин и 43 женщины) в возрасте 60,25±1,12 лет с диагнозом острый ИМ с элевацией сегмента ST. У 28 пациентов за период госпитализации была диагностирована ранняя постинфарктная стенокардия. На основании этого пациенты были разделены на две группы. В первую группу вошли 105 больных ИМ без осложненного течения раннего госпитального периода, во вторую - 28 пациентов с осложненным течением ИМ, кроме того, анализ маркеров РПИС проводили и в контрольной группе, состоящей из 33 человек без заболеваний сердечно-сосудистой системы, сопоставимых по возрасту и полу.
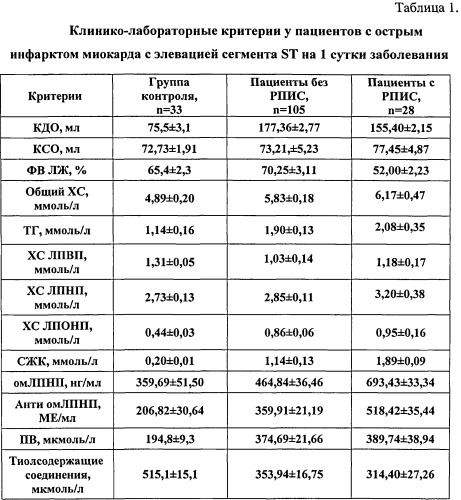
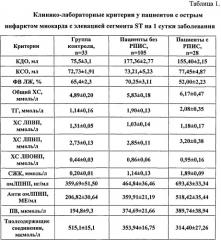
В рамках настоящего исследования в анализ вошли ряд клинических данных, таких как конечный диастолический объем (КДО), конечный систолический объем (КСО), фракция выброса левого желудочка (ФВ ЛЖ) и 12 биохимических маркеров: традиционные параметры липидного профиля крови - общий холестерин (ОХС), триглицериды (ТГ), холестерин липопротеинов высокой плотности (ХС ЛПВП), холестерин липопротеинов низкой плотности (ХС ЛПНП), холестерин липопротеинов очень низкой плотности (ХС ЛПОНП), свободные жирные кислоты (СЖК), окислительно-модифицированные ЛПНП (омЛПНП), антитела к омЛПНП (анти омЛПНП), пероксид водорода (ПВ), тиолсодержащие соединения плазмы крови (табл. 1).
При этом пациенты с ранней постинфарктной стенокардией характеризовались более высоким содержанием свободных жирных кислот - в 1,7 раза, окислительно-модифицированных липопротеинов низкой плотности - 1,5 раза и антител к окислительно-модифицированным липопротеинам низкой плотности - 1,4 раза по сравнению с пациентами с неосложненным течением инфаркта миокарда.
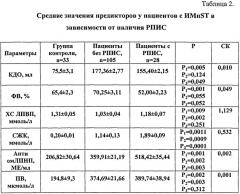
Далее с использованием дискриминантного анализа были отобраны наиболее значимые критерии и определены оптимальные комбинации переменных, определяющие прогноз развития ранней постинфарктной стенокардии у пациентов в первые сутки инфаркта миокарда с подъемом сегмента ST. На основании полученных данных была предложена диагностическая модель, включающая следующие информационные параметры: СЖК, антитела к омЛПНП, пероксид водорода, ХС ЛПВП, а также конечный диастолический объем и фракцию выброса левого желудочка (табл.2).
Примечание: СК - стандартизованный коэффициент. P1 - статистически значимые различия пациентов без РПИС с группой контроля; P2 - статистически значимые различия пациентов с РПИС с группой контроля; P3 - статистически значимые различия параметров между группами.
Для полученных значений переменных рассчитаны стандартизованные коэффициенты (СК), при этом чем больше СК, тем больше вклад соответствующей переменной в дискриминацию совокупностей.
Прогноз вероятного риска развития РПИС (РПИС есть) или его отсутствие (РПИС нет) в первые сутки острого инфаркта миокарда осуществляли на основании формулы канонической линейной дискриминантной функции
P=-3,238+0,01·КДО+0,049·ФВ-0,532·СЖК+0,002·анти
омЛПНП+0,001·ПВ-1,129·ХС ЛПВП
При этом значения функции (центроиды) для группы пациентов «РПИС есть» равно -0,080, а для пациентов группы «РПИС нет» 1,292.
Полученные значения функции (центроиды) были расположены на координатной прямой, середина расстояния между центроидами равна 0,606 и является точкой разделения принадлежности пациента к группе риска.
Таким образом, на основании значения Р, рассчитанного для пациента в первые сутки острого инфаркта миокарда, и приближенности его к центроиду соответствующего кластера делают вывод о наличии или отсутствии риска РПИС. Соответственно при значениях Р, меньших точки разделения кластеров 0,606 и максимально приближенных к центроиду -0,080, делают вывод о вероятном риске развития ранней постинфарктной стенокардии.
Способ позволяет с высокой достоверностью выявлять риск развития ранней постинфарктной стенокардии у пациентов на первые сутки острого инфаркта миокарда с элевацией сегмента ST. Операционные характеристики предложенного способа демонстрируют высокую репрезентативность: чувствительность составила 70,7%, специфичность - 80,8%.
Ниже представлены примеры осуществления способа.
Пример 1.
Пациент Г., 63 года. Госпитализация 12.05.10 г. Диагноз: Q-образующий ИМ передней стенки ЛЖ. Анамнез отягощен АГ и гиперхолестеринемией, клиникой стенокардии III ФК. ИМ и ОНМК в анамнезе отсутствуют. Семейный анамнез отягощен ИБС. Сопутствующей патологии не выявлено. Параметры структурно-функционального состояния ЛЖ: ФВ - 50,93%, КДО - 154,10 мл, КСО - 73,55 мл.
Данные лабораторного обследования на 1-е сутки ИМ: ОХС - 4,82 ммоль/л, ТГ - 1,32 ммоль/л, ХС ЛПВП - 1,33 ммоль/л, ХС ЛПНП - 2,67 ммоль/л, ХС ЛПОНП - 0,71 ммоль/л, Апо В - 1,29 г/л, Апо А1 - 1,27 г/л, Апо В/Апо А1 - 1,02, СЖК - 1,44 ммоль/л, омЛПНП - 399,35 нг/мл, антитела к омЛПНП - 398,22 МЕ/мл, пероксид водорода - 297,02 мкмоль/л, тиолсодержащие соединения - 293,11 мкмоль/л.
P=-3,238+0,010·154,10+0,049·50,93-
0,532·1,44+0,002·398,22+0,001·297,02-1,129·1,33=-0,368
С учетом того, что полученное значение Р ближе к центроиду -0,080 и меньше чем 0,606 сделан вывод, что у пациента присутствует риск РПИС. В течение госпитального периода состояние пациента ухудшилось, диагностирована ранняя постинфарктная стенокардия.
Пример 2.
Пациент С., 59 лет. Госпитализация 19.06.10 г. Диагноз: Q-образующий ИМ передней стенки ЛЖ. Анамнез отягощен АГ и гиперхолестеринемией, клиникой стенокардии I ФК. ИМ и ОНМК в анамнезе отсутствуют. Семейный анамнез отягощен ИБС. Сопутствующей патологии не выявлено. Параметры структурно-функционального состояния ЛЖ: ФВ - 67,73%, КДО - 165,65 мл, КСО - 76,13 мл.
Данные лабораторного обследования на 1-е сутки ИМ: ОХС - 5,04 ммоль/л, ТГ - 1,17 ммоль/л, ХС ЛПВП - 1,21 ммоль/л, ХС ЛПНП - 2,55 ммоль/л, ХС ЛПОНП - 0,68 ммоль/л, Апо В - 1,31 г/л, Апо A1 - 1,29 г/л, Апо В/Апо А1 - 1,02, СЖК - 0,58 ммоль/л, омЛПНП - 379,37 нг/мл, антитела к омЛПНП - 329,14 МЕ/мл, пероксид водорода - 279,20 мкмоль/л, тиолсодержащие соединения - 305,51 мкмоль/л.
P=-3,238+0,010·165,65+0,049·67,73-
0,532·0,58+0,002·329,14+0,001·279,20-1,129·1,21=1,012
Полученное значение P больше чем 0,606 (точки разделения между группами) и ближе к центроиду 1,292, что позволяет сделать вывод об отсутствии у данного пациента риска развития ранней постинфарктной стенокардии. В последующем госпитальный период протекал без осложнений, пациент выписан в удовлетворительном состоянии.
Способ прогнозирования ранней постинфарктной стенокардии у пациентов с острым инфарктом миокарда с подъемом сегмента ST в госпитальном периоде, включающий анализ клинических данных и параметров липидного профиля в первые сутки от начала заболевания, отличающийся тем, что вероятный риск развития РПИС прогнозируют по формулеP=-3,238+0,01·КДО+0,049·ФВ-0,532·СЖК+0,002·антиомЛПНП+0,001·ПВ-1,129·ХС ЛПВП,где КДО - конечный диастолический объем, ФВ - фракция выброса левого желудочка, СЖК - свободные жирные кислоты, анти омЛПНП - антитела к окислительно-модифицированным липопротеинам низкой плотности, ПВ - пероксид водорода, ХС ЛПВП - холестерин липопротеинов высокой плотности, при этом пациента относят к группе «РПИС есть», если значение Р менее 0,606 и максимально приближено к центроиду -0,080, и к группе «РПИС нет», если Р более 0,606 и максимально приближено к центроиду 1,292.