Способ интраоперационной визуализации патологических очагов
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к хирургии и диагностическим методам исследования, в частности к интраоперационной визуализации. Осуществляют адресную доставку в патологические очаги конъюгатов наноразмерных антистоксовых фосфоров (НАФ) с молекулами, селективно связывающимися с целевой биоструктурой, подлежащей визуализации. Проводят облучение патологического очага инфракрасным излучением в диапазоне 975-980 нм. Проводят интраоперационную визуализацию люминесценции поверхностных и приповерхностных патологических очагов невооруженным глазом в синем спектральном диапазоне. Осуществляют глубокое оптическое зондирование с помощью оптического зонда для регистрации патологических очагов, расположенных на глубине, преимущественно, в инфракрасном спектральном диапазоне. Способ обеспечивает высокую чувствительность дифференцировки патологических очагов от нормальных тканей, высокую разрешающую способность визуализации; позволяет дифференцировать поверхностные и приповерхностные патологические очаги невооруженным глазом, а патологические очаги, расположенные на глубине, с помощью оптического зонда. 3 з.п. ф-лы, 3 пр., 7 ил.
Реферат
Область техники, к которой относится изобретение.
Изобретение относится к медицине, а именно к хирургии и диагностическим методам исследования, в частности к интраоперационной визуализации, и раскрывает метод применения люминесцентной нанотехнологии для инспекции биоткани, что включает в себя ее прямую визуализацию, т.е. визуализацию посредством невооруженного человеческого глаза, и оптическое диагностическое зондирование.
Уровень техники.
Оптическое зондирование биологических тканей представляет собой совокупность неинвазивных, т.е. не требующих нарушения целостности исследуемых структур, технологий, направленных на получение информации о структуре и функциональном состоянии тканей и органов и основанных на исследовании особенностей взаимодействия света с биологическими объектами. В ряду недавних достижений следует отметить технологию оптической диффузионной томографии, позволяющей осуществлять мониторинг физиологической активности ткани посредством измерения уровня оксигенации крови; неинвазивно измерять уровень билирубина у новорожденных и т.д. [2]. Данная технология обладает неоспоримыми преимуществами: высокой информативностью в отношении структурно-функционального статуса исследуемого органа или ткани, инструментальной простотой, неинвазивностью, экономичностью. Зондирование позволяет получать данные о состоянии ткани на глубине до нескольких сантиметров от поверхности [3]. Диагностические процедуры с использованием оптической диффузионной томографии хорошо воспринимаются и легко переносятся пациентами. Одной из важных сфер применения оптической диффузионной томографии является зондирование молочных желез, позволяющее диагностировать, определять размеры, пространственное положение и границы опухоли [4]. Молочная железа освещается широкополосным световым источником, отклик биоткани регистрируется оптическим оптоволоконным зондом, после чего анализируется спектральный состав полученного сигнала. Сравнение результатов анализа с теоретическими моделями светорассеяния и светопоглощения биологической ткани позволяет приблизительно воссоздать архитектонику патологического очага, оценить глубину его залегания, размеры, а также вычислить такие важные физиологические параметры, как кровенаполнение и плотность. Однако слабыми местами технологии являются низкое пространственное разрешение, что обусловлено физическими механизмами генерации и регистрации сигнала, а также неспецифичностью диагноза, т.е. невозможностью получить однозначное заключение о виде патологического образования.
Очевидным способом улучшения точности при дифференцировании и определении границ здоровой и патологической ткани является маркирование патологических структур люминесцентными (или флуоресцентными) материалами, часто именуемыми молекулярными зондами. Молекулярный зонд имеет две ключевые компоненты: контрастную и таргетную. Примером контрастной компоненты молекулярного зонда могут служить флуоресцентные органические красители, например флуоресцеин, широко используемый для визуализации кровотока в сосудах глазного дна. Спектрально-селективная регистрация позволяет усилить сигнал от красителя, посредством уменьшения вклада фоновой аутофлуоресценции ткани в получаемое изображение, тем самым улучшив точность определения границ маркированного патологического очага. Примерами таргетной компоненты молекулярного зонда могут служить антитела, пептиды или метаболиты [2]. Контрастная и таргетная компоненты молекулярного зонда спаиваются (соединяются) воедино с использованием процесса конъюгации, делая молекулярный зонд селективным, а диагностику - специфичной. Таким образом, достигается специфическое выявление патологически измененных тканевых элементов (клеток и тканей, отличающихся от здоровых по набору антигенных детерминант).
В последнее время наблюдается повышение востребованности методики интраоперационной визуализации, что подтверждается серией патентов и недавних публикаций [14, 21, 22]. Согласно описанной методике флуоресцентные молекулярные зонды вводятся модельному животному. Резекция тканей оперируемого животного при подсвечивании операционного поля выявляет область локализации опухолевого очага. Подбор молекулярного зонда и подсветки позволяет хорошо различать границы патологических очагов при полноценном освещении хирургического операционного поля. Подобная методика также описана в [23].
Существующие методики флуоресцентной диагностики в реальном времени обладают существенным общим недостатком: чувствительность и разрешающая способность визуализации патологических очагов по-прежнему остается невысокой; в то же время, именно точность локальной диагностики в значительной мере определяет исход операции, общую успешность лечения и прогноз.
Прямая визуализация является общепринятым в диагностической и хирургической практике методом инспекции биоткани. Осмотр патологически измененных участков ткани, сопоставление их со здоровыми тканями и анализ патологических изменений на основе известных в диагностической практике признаков до сих пор является золотым стандартом диагностики. В частности, метод прямой визуализации предназначен для прецизионного выявления патологически измененных тканей, например опухолевых очагов, располагающихся вблизи поверхности исследуемого органа, и особенно полезен во время хирургической процедуры удаления опухоли. Улучшение точности и специфичности локализации патологического очага посредством применения люминесцентных нанотехнологий является предметом данного изобретения.
Раскрытие изобретения.
Задачей настоящего изобретения является обеспечение повышения успешных результатов хирургического лечения и улучшения дальнейшего прогноза течения заболеваний.
Поставленная задача решается за счет достижения технического результата, заключающегося в обеспечении при проведении диагностических исследований, а особенно при проведении хирургических операций, возможности дифференцирования поверхностных и приповерхностных патологических очагов от нормальных, здоровых тканей невооруженным глазом, а структур, расположенных на глубине, - с помощью оптического зонда; с обеспечением высокой чувствительности такой дифференцировки и высокой разрешающей способности визуализации.
Указанный технический результат достигается в способе интраоперационной визуализации патологически измененных клеток, тканей и/или субклеточных структур невооруженным глазом в видимом спектральном диапазоне и их глубокого оптического зондирования с помощью оптического зонда, преимущественно, в инфракрасном спектральном диапазоне, включающем
- адресную доставку в патологические очаги конъюгатов наноразмерных антистоксовых фосфоров (НАФ) с молекулами, селективно связывающимися с целевой биоструктурой, подлежащей визуализации;
- облучение патологического очага инфракрасным излучением в диапазоне 975-980 нм;
- визуализацию люминесценции патологически измененных клеток, тканей и/или субклеточных структур поверхностных и приповерхностных патологических очагов невооруженным глазом в видимом диапазоне, а также регистрацию патологических очагов, расположенных на глубине, преимущественно, в инфракрасном спектральном диапазоне.
Кроме того, технический результат может быть достигнут при проведении in vitro или in vivo диагностики путем визуализации патологически измененных клеток, тканей и/или субклеточных структур невооруженным глазом в видимом спектральном диапазоне и их глубокого оптического зондирования с помощью оптического зонда, преимущественно, в инфракрасном спектральном диапазоне, включающем
- адресную доставку в патологические очаги конъюгатов наноразмерных антистоксовых фосфоров (НАФ) с молекулами, селективно связывающимися с целевой биоструктурой, подлежащей визуализации;
- облучение патологического очага инфракрасным излучением в диапазоне 975-980 нм;
- визуализацию люминесценции патологически измененных клеток, тканей и/или субклеточных структур поверхностных и приповерхностных патологических очагов невооруженным глазом в видимом диапазоне, а также регистрацию патологических очагов, расположенных на глубине, преимущественно, в инфракрасном спектральном диапазоне.
В качестве НАФ могут быть использованы, например, неорганический нанокристаллический матрикс NaYF4, солегированный ионами иттербия (Yb) и эрбия (Er) - NaYF4:Yb:Er, или NaYF4:Yb:Tm, где Er заменен тулием (Tm).
Использование при проведении диагностических исследований, в том числе во время хирургических операций, визуализации поверхностных и приповерхностных патологических очагов невооруженным глазом, т.е. без применения дополнительных визуализирующих оптических устройств, с использованием биокомплексов наноразмерных антистоксовых фосфоров (НАФ), обеспечивает целый ряд преимуществ. Эти преимущества связаны, прежде всего, с отсутствием необходимости использования отсекающих фильтров, т.е. фильтров, разделяющих сигнал флюоресценции от сигнала накачки, поскольку в данном случае именно сам глаз выполняет роль фильтрующего устройства, в связи с тем, что глаз человека способен воспринимать лишь излучение в видимом диапазоне, а для возбуждения излучения НАФ (т.е. в качестве сигнала накачки) используют излучение инфракрасного диапазона. Также, глаз осуществляет функции сканирования изображаемого поля, оптической настройки на резкость, яркость и т.д. и анализ изображения, позволяющий прецизионную колокализацию сигнала НАФ и патологически измененных структур, подлежащих операционному воздействию. Помимо этого, отсутствие необходимости использования при проведении хирургических операций дополнительных визуализирующих оптических устройств обеспечивает удобство проведения операции, а также снижает расходы на оборудование, что, в свою очередь, снижает себестоимость операции. В то же время, благодаря адресной доставке в патологические очаги биокомплексов НАФ, селективно связывающихся с целевой биоструктурой, подлежащей визуализации, обеспечивается высокая чувствительность дифференцировки нормальных, здоровых тканей и патологических очагов, а также высокая разрешающая способность визуализации (вплоть до субмиллиметровых диапазонов - 0,1-1 мм), что, в свою очередь, обеспечивает высокую эффективность и точность диагностики (визуализации) патологических очагов, позволяя достичь значительного повышения успеха лечения и дальнейшего прогноза заболевания. Дополнительные преимущества, оказывающие значительное влияние на успех лечения, обеспечиваются благодаря возможности визуализации патологических очагов, расположенных на глубине, с использованием методики получения изображения с помощью оптических зондов, преимущественно, в инфракрасном диапазоне.
Подробное описание изобретения.
Оригинальность настоящего изобретения заключается в соединении двух взаимоисключающих способов инспекции биоткани, а именно прямой зрительной визуализации и глубокого оптического зондирования (имиджинга). Первый способ полагается на маркирование биоткани контрастными агентами, проявляющимися в видимом световом диапазоне, т.е. от 400 нм до 700 нм, в то время как второй способ требует контрастных агентов в инфракрасном диапазоне 700 нм - 1300 нм, так называемом «окне прозрачности биологической ткани» (см. Рис.1 и 2). Совмещение свойств двух контрастных агентов, реализуемое посредством использования инновационных люминесцентных наноматериалов (например, наноразмерных антистоксовых фосфоров, или НАФ), создающих контраст в обоих спектральных диапазонах, позволяет реализовать новый комплексный тип инспекции (живой) биоткани, маркированной НАФ. Принципиально новый характер инспекции, например, проявляется в возможности одновременной инспекции как приповерхностных (визуализация), так и глубоких (оптическое зондирование) слоев биоткани. Примером востребованности прямой визуализации с последующим контрольным оптическим зондированием операционного поля на глубину до 1 см является интраоперационная инспекция поверхностных очагов патологически измененной ткани.
Настоящее изобретение основано на объединении технологий, относящихся к трем группам: 1. Методы синтеза биокомплексов антистоксовых нанофосфоров [5-8]; 2. Методы и технические решения в области оптического зондирования или оптической томографии [2, 9-11]; 3. Методические решения в области специфической визуализации биоткани с использованием люминесцентных зондов (12-14). Объединение этих трех направлений, обладающее новыми качествами и позволяющее достичь нового неожиданного технического результата, представляет предмет данного изобретения.
Краткое описание чертежей
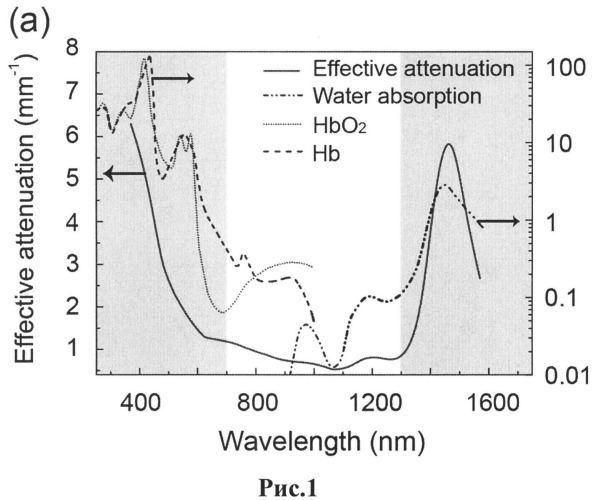
Рис.1. Оптический спектр эффективной экстинкции живой кожной ткани (сплошная линия), доминантными компонентами которой являются поглощение воды (Н2О, штрихпунктирная линия), гемоглобина (Hb, жирная пунктирная линия), оксигемоглобина (HbO2, нежирная пунктирная линия) и белков (не показано). Оптическое рассеивание биоткани было также учтено. Спектральный диапазон окна прозрачности биологической ткани находится в области от 700 нм до 1300 нм и обозначен на рисунке площадью, свободной от серого цвета.
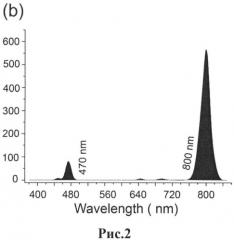
Рис.2. Спектры люминесценции наноматериала NaYF4:Yb:Tm.
Рис.3 Схематическое представление интраоперационной диагностической процедуры в случае рака яичника, выполняемой с использованием биоконъюгированных люминесцентных молекулярных зондов. Вид операционного поля: (а) непосредственное наблюдение невооруженным глазом; (b) поверхностная визуализация опухолевых очагов с помощью люминесцентных молекулярных зондов при использовании подсветки (серые пятна); (с) изображение опухолевого очага (более светлое пятно), расположенного на глубине до 1 см от поверхности, получаемое с помощью оптического томографа использованием невидимой инфракрасной подсветки. Предполагается, что препарат на основе биокомплексов НАФ локализован в опухоли (с). Пациенту вводится препарат, содержащий люминесцентные молекулярные зонды, биоконъюгированные с направляющими биомолекулами (антителами к антигенам опухолевой ткани). Последующее оптическое зондирование выявляет распространение опухоли в глубину. Адаптировано из работы [1].
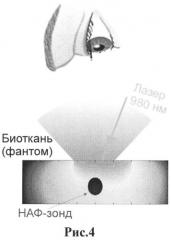
Рис.4. Схематическая диаграмма прямой визуализации НАФ-зонда, находящегося в приповерхностном слое фантома биоткани. Ожидается, что синее излучение (474 нм) от НАФ зонда на основе туллия будет заметным для глаза (хирурга) при подсветке инфракрасным (ИК) лазером.
Рис.5. Схематическая диаграмма оптоволоконного оптического зонда, моделирующего методику интраоперационной процедуры визуализации и оптического зондирования патологического очага, залегающего на глубине до 1 см в фантоме биоткани. Оптическая система представляет собой оптоволоконный зонд, в центральную жилу которого вводится ИК-излучение для возбуждения НАФ-зонда. Возбужденный люминесцентный сигнал в ИК-диапазоне (796 нм) распространяется в мутной поглощающей среде биоткани с минимальными потерями и регистрируется сверхчувствительным фотодетектором после предварительной спектральной фильтрации.
Суть изобретения раскрывается посредством анализа распространения света через живую биологическую ткань, ключевые особенности которого представлены на Рис.1. Очевидно, что видимый световой диапазон, т.е. от 400 нм до 700 нм, является гораздо менее предпочтительным спектральным диапазоном в сравнении с инфракрасном диапазоном, 700 нм-1300 нм, иногда именуемым «окном прозрачности биологической ткани» (см. Рис.1). Действительно, свет эффективно поглощается и рассеивается в видимом диапазоне. Отметим, что человеческое зрение, ответственное за прямую визуализацию, находится в пределах видимого светового диапазона. Стало быть, прямая визуализация биологической ткани с прецизионным (субмиллиметровым) определением границ патологических очагов ограничивается субмиллиметровыми глубинами, которые можно назвать приповерхностными слоями биологической ткани. Получается, что прямая визуализация с применением молекулярных зондов со спектром поглощения и испускания в ультрафиолетовом и видимом диапазонах не позволяет зондирование на диагностически важных глубинах (здесь, именуемого глубоким зондированием, т.е. до 1 см) в контексте интраоперационной процедуры. Вместе с этим, инфракрасные оптические зонды, подходящие для глубокого оптического зондирования, не подходят для прямой визуализации, даже если находятся в приповерхностных слоях биоткани - человеческий глаз (в частности, глаз хирурга) не восприимчив к ИК-свету.
В настоящем изобретении предлагается новый тип молекулярного зонда, имеющего спектральные полосы излучения как в видимом, так и в ИК-диапазонах, как это, например, показано на Рис.2. Это позволяет проводить инспекцию биологической биоткани как посредством прямой визуализации с возможностью прецизионного определения границ патологического очага, так и с помощью инструмента оптического зондирования, позволяющего инспекцию биоткани на глубине до 1 см.
В результате становится возможной методика прямой визуализации и оптического зондирования биологической ткани, содержащей патологические очаги, маркированные биоконъюгатами (биокомплексами) особого класса наноразмерных фосфоров (НАФ-зонды или БиоНАФ), как это схематически представлено на Рис.2. Избирательно накапливаясь в патологически измененных участках, БиоНАФ делают пораженные структуры легко отличимыми от окружающей здоровой ткани. Медицинский оператор получает возможность непосредственно, в реальном времени, четко дифференцировать зону поражения, что в обычных условиях бывает затруднительно.
Осуществление изобретения
Как уже указывалось выше, раскрываемое изобретение опирается на технологию люминесцентных материалов, важным примером которой являются антистоксовые нанофосфоры (НАФ) [5-8]. НАФ представляют собой нанокристаллы, обладающие уникальными оптическими свойствами: они отвечают на воздействие ИК-излучения люминесценцией в видимом (400-700 нм) и ИК (700-900 нм) диапазонах в «окне оптической прозрачности» биотканей (т.н. антистоксовая люминесценция), как это, например, показано на рис.2b. Помимо этого, НАФ, пригодные для использования в настоящем изобретении, должны обладать, по меньшей мере, фотостабильностью, химической инертностью и механической стабильностью, а также отсутствием токсичности для биологических клеток, тканей и организмов.
В качестве НАФ могут быть использованы, например, неорганический нанокристаллический матрикс NaYF4, солегированный ионами иттербия (Yb) и эрбия (Er) - NaYF4:Yb:Er, или NaYF4:Yb:Tm, где Er заменен тулием (Tm). Размер НАФ, пригодных для использования в настоящем изобретении, составляет в 7 - 100 нм, наиболее предпочтительный размер НАФ - 40-60 нм. Существуют НАФ с разными молярными соотношениями Yb и Er, от полной замены ионов иттрия (Y) ионами иттербия в матриксе нанокристалла до нескольких молярных процентов. Молярные соотношения Er и Tm варьируются от 0,01 до 10%. Наиболее оптимальным соотношением солегирующих элементов является 20% Yb и 2% Er в случае NaYF4:Yb:Er и 20% Yb и 0,5% Tm в случае NaYF4:Yb:Tm.
Экспертам в области синтеза и фотофизики антистоксовых нанофосфоров должно быть понятно, что как неорганический нанокристаллический матрикс, так и солегирующие компоненты могут замещаться. Так, нанокристаллический матрикс может быть любым неорганическим кристаллом или аморфным материалом, где эффективность его функционирования определяется возможностью максимальной плотной упаковки солегирующих ионов для обеспечения максимально эффективной передачи энергии возбуждения. Вторым критическим фактором является фононная энергия, поддерживаемая матриксом, которая должна быть минимальной (например, максимальная энергия фононов менее 400 см-1 в случае NaYF4). Солегирующие компоненты могут замещаться широким классом элементов редких земель и лантаноидов, таких как европий, тербий и т.д.
Таким образом, материалы НАФ обладают важными люминесцентными свойствами, позволяющими реализовать как прямую визуализацию, так и оптическое зондирование патологически измененных участков биотканей. Однако применение данных наноматериалов требует создания биосовместимых комплексов (биокомплексов НАФ), обладающих полной функциональностью молекулярных зондов и способных селективно связываться с целевой биоструктурой (мишенью), подлежащей визуализации. Биокомплексы НАФ представляют собой конъюгаты НАФ с молекулами, селективно связывающимися с целевой биоструктурой, например в качестве таких молекул могут использоваться антитела, чувствительные к целевому антигену. В качестве таких антигенов могут выступать антигенные детерминанты опухолевых клеток, например, рецептор класса epithelial growth factor HER2/neu. Также возможно использование лигандов в виде коротких белков (пептидов), способных к целевому связыванию с раковыми клетками. Примером такого пептида может служить соматостатин SST2. В случае визуализации других структур, например нейронных клеток, возможно использование таких лигандов, как энкефалин, который обладает высокой аффинностью к опиоидным рецепторам. В качестве целевой биоструктуры (мишени) могут быть выбраны, например, опухолевые клетки, воспалительные, фиброзные структуры, нервные волокна, кровеносные сосуды, патогены и т.д.
Методы синтеза биокомплексов НАФ (конъюгатов НАФ с биомолекулами) хорошо известны в настоящее время (см., например, 5 - 8), и включают в себя неорганический синтез собственно наночастиц НАФ, функционализацию их поверхности для придания устойчивости в водных и биосовместимых растворах, а также прочную, желательно, ковалентную, привязку направляющего целевого агента в виде биомолекулы.
В зависимости от локализации целевой биоструктуры биокомплексы НАФ могут быть введены в организм с использованием как парентеральных, так и энтеральных путей введения, в том числе, но не ограничиваясь ими, путем введения внутривенно, подкожно, а также посредством поверхностной аппликации.
Визуализация операционного поля с помощью НАФ-зондов предпочтительно осуществляется следующим образом. Биологическая ткань с НАФ-зондом, селективно связавшимся с целевой биоструктурой, облучается светом ИК-лазера накачки в диапазоне 975-980 нм, либо распределенным по всей тестируемой поверхности образца, либо посредством сканирования узконаправленного лазерного пучка по поверхности в растровом режиме (так называемый метод летающей точки), которые хорошо известны в уровне техники (см., например, 11). Схематическая диаграмма метода визуализации НАФ-зонда показана на Рис.4. Важно отметить, что люминесцентные наночастицы (нанокристаллы НАФ), находящиеся в поверхностном и приповерхностном слоях (на глубине не более 50 мкм), открытом во время операции, эффективно возбуждаются лазерным светом накачки, который не успевает рассеяться в приповерхностном слое биологической ткани.
Специалисту в данной области техники понятно, что оптимальное построение систем возбуждения и детектирования свечения НАФ позволит подавить все фоновые засветки от биологической ткани, включая рассеивание цельной крови и аутофлуоресценцию эндогенных флуорофоров.
Как хорошо видно на Рис.1, свет люминесценции нанокристаллов НАФ имеет две спектральные компоненты, синюю и инфракрасную. Синяя компонента подходит для целей визуализации, что также наглядно понятно из Рис.1. Заметим также, что НАФ-зонд в приповерхностном слое хорошо локализуется, как это наглядно продемонстрировано на Рис.4, где форма зонда хорошо распознаваема через слаборассеивающую среду биоткани, что реалистично воспроизводит рассеивающие свойства приповерхностного слоя.
Оптическое зондирование на глубине более 50 мкм, вплоть до глубины 1 см, осуществляется посредством оптического томографа, схематическая диаграмма которого показана на Рис.5. Предпочтительная конфигурация оптического зонда представляет собой оптоволоконный пучок, центральная жила которого зарезервирована под гибкую доставку излучения ИК-лазера (975-980 нм) к поверхности исследуемого объекта. Множество окружающих центральную жилу многомодовых оптических волокон используется для сбора люминесцентного излучения от НАФ-зонда, выходящего на поверхность биоткани или биологического фантома [2]. Люминесцентное излучение, доставленное оптическим волокном к дальнему терминалу зонда, собирается, фильтруется и регистрируется фотоприемником. Как правило, спектральный диапазон чувствительности фотоприемников захватывает как видимую, так и ИК-области спектра, что делает оптический зонд чувствительным к видимому и ИК люминесцентному сигналу от НАФ. В силу того, что применение оптического зондирования предполагается после удаления хорошо визуализируемых патологически измененных структур, сигнал люминесценции НАФ из глубины более 100 мкм включает в себя преимущественно ИК-компоненту, тогда как видимая компонента существенно ослаблена из-за рассеивания и поглощения биоткани.
Распределение интенсивности люминесценции на единицу площади записывается компьютером с целью пространственной локализации зонда посредством компьютерного анализа распределения. Сравнение экспериментально полученного распределения с распределением, смоделированным численными методами, позволяет решить обратную задачу локализации НАФ-зонда вместе с оценкой концентрации антистоксовых нанофосфоров (НАФ-зондов) [см. Рис.5 нижняя панель]. Важно заметить, что схема регистрации (Рис.5) рассчитана на ИК спектральную компоненту НАФ зонда на основе NaYF4:Yb:Tm. Как было отмечено ранее, ИК-излучение распространяется в поглощающей и рассеивающей среде биоткани с минимальными потерями и является идеальным выбором для оптической томографии.
В рамках подтверждения возможности осуществления раскрываемого способа визуализации патологических очагов и достижения указанного технического результата нами были проведены следующие эксперименты, которые продемонстрировали высокую чувствительность и разрешающую способность такой визуализации:
В первом эксперименте нами была продемонстрирована возможность сверхчувствительной регистрации НАФ в толще биоткани на примере детектирования одиночной наночастицы через 250 мкм слой крови. Изучалась возможность регистрации частиц НАФ, скрытых в толще биологической ткани, которая в данной работе была представлена слоем гомогенизированной крови. Была продемонстрирована возможность сверхчувствительной регистрации и оптического имиджинга одиночной наночастицы NaYE4:Yb:Er размером 70 нм через слой 0,25 мм гомогенизированной крови, которая является сильно поглощающим биологических слоем в видимом диапазоне. Эксперименты проводились с использованием эпилюминесцентного оптического микроскопа. На основании представленных экспериментальных данных была проведена оценка чувствительности регистрации одиночной наночастицы НАФ в живой биологической ткани, которая оказалась равной 400 мкм.
Во втором эксперименте нами была продемонстрирована адресная доставка поверхностно-модифицированных и биоконъюгированных НАФ к клеткам рака молочной железы. Оптический имиджинг этих маркированных клеток через фантом биологической ткани, воспроизводящей основные оптические свойства ткани молочной железы, продемонстрировал возможность их регистрации через 1,5 мм ткани. В данном эксперименте мы оценивали чувствительность оптического зондирования рака молочной железы в живой биоткани. Была проведена количественная диагностика коэффициента конверсии НАФ, используемых для маркирования раковых клеток, которая оказалась равной 2% в пересчете на мощность излученного сигнала люминесценции на мощность поглощенного излучения на 975-980 нм. Также биокомплексы НАФ были сконъюгированы с целевыми биомолекулами, мини-антителами scFv4D5, имеющими высокую аффинность к рецепторами HER2/neu раковых клеток, в частности аденокарсиномы SK-BR-3. Была продемонстрирована адресная доставка биокомплексов НАФ к клеточным культурам, и специфичность доставки подтверждена высоким контрастом иммобилизации комплексов (10:1) по сравнению с неспецифической доставкой в другие клетки. Чувствительность регистрации таким образом маркированных клеток была исследована с помощью фантома, воспроизводящего основные свойства биоткани, и эпилюминесцентного микроскопа. На основании полученных экспериментальных данных было проведено теоретическое моделирование, которое показало, что маркированные клетки (около 100 клеток в поле зрения имиджинговой системы) с плотностью частиц 3000 НАФ на клетку будут регистрироваться с глубины 5 мм в живой ткани молочной железы.
В следующем эксперименте мы продемонстрировали возможность визуализации НАФ в приповерхностных слоях ткани. В данном эксперименте были проведены теоретические оценки чувствительности регистрации рака молочной железы, маркированной биокомплексами НАФ (аналогично работе 2) с помощью человеческого глаза. В модели использовалось направленное лазерное излучение 975-980 нм в пределах разрешенных доз лазерного излучения, которое освещало клетки рака молочной железы, маркированные биокомплексами НАФ и залегающие на глубине живой ткани молочной железы. Оценки проводились с учетом чувствительности человеческого глаза в т.н. фотопическом режиме (дневном зрении), а также с учетом параметров сбора света люминесценции НАФ. Было получено, что глаз хирурга сможет надежно видеть раковый очаг с глубины 50 мкм.
Данные примеры не являются ограничивающими; другие воплощения в рамках данного изобретения также могут быть осуществлены специалистами в данной области техники.
Практически полное подавление послесвечения живой ткани, минимальное поглощение и рассеивание света накачки/излучения БиоНАФ, а также эффективное связывание БиоНАФ исключительно с целевыми антигенами обеспечивает высокую чувствительность и специфичность предлагаемых диагностических технологий. Все это делает методику чрезвычайно привлекательной для применения в медицинской практике, а также в биомедицинских исследованиях. Предлагаемый метод может быть использован в практике интраоперационной хирургии опухолей, воспалений, фиброзов, туберкулеза и других заболеваний. Иммуноморфологическое экспресс-выявление антигенов в рамках интраоперационной методики также возможно.
Ожидается, что недорогая чувствительная методика интраоперационной визуализации и оптического зондирования патологических очагов ткани найдет широкое применение в лечебных клиниках, диагностических центрах и исследовательских лабораториях. Совместимость технологии с практикуемой зрительной оценкой патологий облегчит ее внедрение, в то время как неинвазивное глубокое зондирование улучшит результат операции. Широко используемые томографы, включая FT, МРТ, ПЭТ, остаются дорогостоящими и часто лишенными специфичности, обеспечиваемой предлагаемой технологией. Это формирует нишу технологии, как доступной и высокочувствительной интраоперационной экспресс-диагностики опухолей, воспалительных и фиброзно-склеротических процессов, туберкулеза, очаговых инфекций и т.п., когда доступ к пораженным органам ограничен, а фактор времени критичен.
Литература
1. Van Dam GM, Themelis G, Crane LMA, Harlaar NJ, Pleijhuis RG, Kelder W, Sarantopoulos A, de Jong JS, Arts HJG, van der Zee AGJ, Bart J, Low PS, Ntziachristos V. Intraoperative tumor-specific fluorescence imaging in ovarian cancer by folate receptor-alpha targeting: first in-human results. Nat Med 2011; 17(10):1315-U1202.
2. Leblond F, Davis SC, Valdes PA, Pogue BW. Pre-clinical whole-body fluorescence imaging: Review of instruments, methods and applications. Journal of Photochemistry and Photobiology B-Biology 2010; 98(l):77-94.
3. Weissleder R. A clearer vision for in vivo imaging. Nature Biotechnology 2001; 19(4):316-317.
4. Soliman H, Gunasekara A, Rycroft M, Zubovits J, Dent R, Spayne J, Yaffe MJ, Czarnota GJ. Functional Imaging Using Diffuse Optical Spectroscopy of Neoadjuvant Chemotherapy Response in Women with Locally Advanced Breast Cancer. Clinical Cancer Research 2010; 16(9):2605-2614.
5. Schwartz JT, Christopher A.; Nano-particle surface modification. USA. 2009.
6. Ju Y, Shan J; Synthesis of bio-functionalized rar-eearth doped upconverting nanophosphors. USA. 2009.
7. Ju Y, Shan J; he trustees of princeton university, assignee, synthesis of bio-functionalized rare earth doped upconverting nanophosphors. 2009.
8. Cao TY, Yang Y, Gao YA, Zhou J, Li ZQ, Li FY. High-quality water-soluble and surface-functionalized upconversion nanocrystals as luminescent probes for bioimaging. Biomaterials 2011; 32(ll):2959-2968.
9. Ntziachristos V, Weissleder R; The General Hospital Corporation, assignee. Fluorescence-mediated molecular tomography. USA. 2008.
10. Fortier S, Leblond F; Art Advanced Research Technologies Inc., assignee. Fluorescence tomography using line-by-line forward model. USA. 2010.
11. Kobayashi H, Kosaka N, Ogawa M, Morgan NY, Smith PD, Murray CB, Ye XC, Collins J, Kumar GA, Bell H, Choyke PL. In vivo multiple color lymphatic imaging using upconverting nanocrystals. Journal of Materials Chemistry 2009; 19(36):6481-6484.
12. В.Б. Л, ГЛ. К; ОПТИЧЕСКИЙ ИНТРОСКОП. Russian Federation. 2002.
13. Van Dam GMT, George / Crane, Lucia M A / Harlaar, Niels J / Pleijhuis, Rick G / Kelder, Wendy / Sarantopoulos, Athanasios / (…) / Ntziachristos, Vasilis. Intraoperative tumor-specific fluorescence imaging in ovarian cancer by folate receptor-±targeting: first in-human results. Nature Medicine 2011; 17(10):1315-1319.
14. Keereweer S, Kerrebijn JDF, van Driel P, Xie BW, Kaijzel EL, Snoeks TJA, Que I, Hutteman M, van der Vorst JR, Mieog JSD, Vahrmeijer AL, van de Velde CJH, de Jong RJB, Lowik С Optical Image-guided Surgery-Where Do We Stand? Molecular Imaging and Biology 2010; 13(2):199-207.
15. Kim WJ, Nyk M, Prasad PN. Color-coded multilayer photopatterned microstructures using lanthanide (III) ion co-doped NaYF(4) nanoparticles with upconversion luminescence for possible applications in security. Nanotechnology 2009; 20(18).
16. Sandnes B, Keif ТА, Liu H, Zvyagin AV. Retroemission by a glass bead monolayer for high-sensitivity, long-range imaging of upconverting phosphors. Optics Letters 2011; 36(15):3009-3011.
17. Wang F, Deng R, Wang J, Wang Q, Han Y, Zhu H, Chen X, Liu X. Tuning upconversion through energy migration in corea€"shell nanoparticles. Nat Mater 2011; 10(12):968-973.
18. Zhan QQ, Qian J, Liang HJ, Somesfalean G, Wang D, He SL, Zhang ZG, Andersson-Engels S. Using 915 nm Laser Excited Tm(3+)/Er(3+)/Ho(3+)-Doped NaYbF4 Upconversion Nanoparticles for in Vitro and Deeper in Vivo Bioimaging without Overheating Irradiation. Acs Nano 2011; 5(5):3744-3757.
19. Vinegoni С, Razansky D, Hilderbrand SA, Shao FW, Ntziachristos V, Weissleder R. Transillumination fluorescence imaging in mice using biocompatible upconverting nanoparticles. Optics Letters 2009; 34(17):2566-2568.
20. Xiong LQ, Yang TS, Yang Y, Xu CJ, Li FY. Long-term in vivo biodistribution imaging and toxicity of polyacrylic acid-coated upconversion nanophosphors. Biomaterials; 31(27):7078-7085.
21. Frangioni JV. New technologies for human cancer imaging. J Clin Oncol 2008; 26(24):4012-4021.
22. Weissleder R, Pittet MJ. Imaging in the era of molecular oncology. Nature 2008; 452(7187)580-589.
23. Stratonnikov AA, Ermishova NV, Meerovich GA, Kudashev BV, Vakulovskaya EG, Loschenov VB. Simultaneous measurement of photosensitizer absorption and fluorescence in patients undergoing photodynamic therapy. Optical Biopsy Iv. Volume 4613, Proceedings of the Society of Photo-Optical Instrumentation Engineers (Spie). 2002:162-173.
1. Способ интраоперационной визуализации патологических очагов невооруженным глазом в синем спектральном диапазоне и их глубокого оптического зондирования с помощью оптического зонда, преимущественно, в инфракрасном спектральном диапазоне, включающий- адресную доставку в патологические очаги конъюгатов наноразмерных антистоксовых фосфоров (НАФ) с молекулами, селективно связывающимися с целевой биоструктурой, подлежащей визуализации;- облучение патологического очага инфракрасным излучением в диапазоне 975-980 нм;- визуализацию люминесценции поверхностных и приповерхностных патологических очагов невооруженным глазом в синем спектральном диапазоне, а также регистрацию патологических очагов, расположенных на глубине, преимущественно, в инфракрасном спектральном диапазоне.
2. Способ по п. 1, отличающийся тем, что в качестве НАФ используют неорганический нанокристаллический матрикс NaYF4, солегированный ионами иттербия (Yb) и эрбия (Er), NaYF4:Yb:Er или NaYF4:Yb:Tm, где Er заменен тулием Tm.
3. Способ по любому из пп. 1-2, отличающийся тем, что невооруженным глазом осуществляют визуализацию патологических очагов, расположенных на глубине не более 50 мкм.
4. Способ по любому из пп. 1-2, отличающийся тем, что глубокое оптическое зондирование в инфракрасном диапазоне осуществляют для обнаружения патологических очагов, расположенных на глубине более 50 мкм, с возможностью достижения глубины зондирования 1 см.