Способ оценки суммарного риска развития нежелательных сердечно-сосудистых событий у пациентов с недифференцированными формами наследственных нарушений соединительной ткани
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к кардиологии и профилактической медицине, и может быть использовано для дифференциации пациентов с наследственными нарушениями соединительной ткани в группу риска развития нежелательных сердечно-сосудистых событий с целью индивидуализации планирования и осуществления профилактических мероприятий. Определяют возраст пациента и выявляют наличие диспластических изменений в органах, присваивают выявленным изменениям прогностические коэффициенты, причем при наличии: кожных проявлений присваивают коэффициент «+6», флебопатии - «+6», патологии позвоночных артерий - «+2», наследственных нарушений соединительной ткани со стороны 3 и более органов - «+2», а менее 3 - «-4», полностью разомкнутого Виллизиева круга - «+7», двустворчатого аортального клапана - «+16», если возраст пациента составляет до 30 лет включительно присваивают прогностический коэффициент «+6», а более 30 лет - «-3». Полученные коэффициенты суммируют и при достижении значения «+13» определяют принадлежность пациента к группе риска. Способ позволяет с высокой точностью у пациентов с недифференцированными формами наследственных нарушений соединительной ткани определить индивидуальный суммарный риск развития нежелательных сердечно-сосудистых событий. 4 табл.
Реферат
Изобретение относится к медицине, а именно к кардиологии и профилактической медицине, и может быть использовано для дифференциации пациентов с наследственными нарушениями соединительной ткани в группу риска развития нежелательных сердечно-сосудистых событий с целью индивидуализации планирования и осуществления профилактических мероприятий. Для оценки суммарного риска нежелательных сердечно-сосудистых событий применяется расчет суммарного прогностического коэффициента с порогом дифференциации в группу риска +13 исходя из допустимого уровня α (ошибка первого рода) 0,05 (5%), β (ошибка второго рода) - 0,05 (5%). Способ позволяет осуществлять оптимальную дифференциацию пациентов в группу риска развития нежелательных сердечно-сосудистых событий.
Изобретение может быть использовано в кардиологии, терапии для определения тактики ведения пациентов с наследственными нарушениями соединительной ткани на основе оценки индивидуального суммарного риска развития нежелательных сердечно-сосудистых событий.
Известно, что проявления наследственных нарушений соединительной ткани (синоним - «дисплазия соединительной ткани» [1]) вследствие всеобъемлющего распространения соединительной ткани полиорганны и включают, в частности, сердечно-сосудистые синдромы - клапанный синдром (пролапсы и/или миксоматозная дегенерация клапанов), сосудистый синдром (расширение и аневризмообразование артерий различного типа - аневризма аорты, расширение конуса легочной артерии, аневризмы церебральных артерий, патологическая извитость магистральных артерий головы и висцеральных артерий; варикозное расширение вен), аритмический синдром (нарушения функции синоатриального узла, экстрасистолия, пароксизмальные нарушения ритма) [1-5]. Указанные проявления могут нести непосредственную угрозу жизни и здоровью пациентов вследствие прогрессирующего течения и развития осложнений, таких как разрывы аневризм или спонтанная диссекция артериальных сосудов различной локализации (развитие артериальных кровотечений, субарахноидальных кровоизлияний), отрыв хорд левого желудочка, жизнеугрожающие нарушения ритма, внезапная смерть [2, 6-8]. Формирование указанных нежелательных событий наиболее изучено в группе пациентов с синдромными формами наследственных нарушений соединительной ткани - синдроме Марфана, Элерса-Данло, Лойе-Дитца и др. [7, 9-12]. Известно, что недифференцированные формы наследственной патологии соединительной ткани проявляются развитием тех же сердечно-сосудистых синдромов с повышением в сравнении с общей популяцией частоты ранней и внезапной смерти [1-3].
В кардиологии наиболее известен способ оценки прогноза развития фатальных и нефатальных сердечно-сосудистых событий у пациентов с артериальной гипертензией (SCORE), который учитывает клинические характеристики пациентов (пол, возраст (начиная с 40 лет и старше), статус курения, уровень холестерина, уровень артериального давления) [13]. Данный способ является близким заявляемому по общей сущности (использует клинические характеристики пациента и основной патологии) и результату (стратификация риска с формирование отдельных групп пациентов) и выбран в качестве прототипа. Недостатком данного способа является то, что метод ориентирован на пациентов со сформировавшейся сердечно-сосудистой патологией (артериальная гипертензия) и рассчитан на популяцию пациентов старше 40 лет. В то же время у пациентов с недифференцированными формами наследственной патологией соединительной ткани развитие нежелательных сердечно-сосудистых событий вследствие прогредиентного течения диспластического процесса может происходить спонтанно (в отсутствие явных признаков патологии, лежащей в основе развития осложнения) либо в исходе асимптомного течения указанной патологии преимущественно в молодом возрасте [1-3, 14, 15]. В известной отечественной и зарубежной литературе отсутствуют способы оценки суммарного риска развития нежелательных сердечно-сосудистых событий у пациентов с недифференцированным формами наследственных нарушений соединительной ткани.
Задачей изобретения является повышение эффективности способа оценки суммарного риска развития нежелательных сердечно-сосудистых событий в группе пациентов с недифференцированными формами наследственных нарушений соединительной ткани.
Предложен способ оценки суммарного риска развития нежелательных сердечно-сосудистых событий у пациентов с недифференцированными формами наследственных нарушений соединительной ткани: наличие суммарного прогностического коэффициента +13 указывает на риск развития нежелательных сердечно-сосудистых событий в указанной группе пациентов.
Новым в предлагаемом способе является то, что у пациентов с недифференцированными формами наследственных нарушений соединительной ткани осуществляется индивидуальная оценка суммарного риска развития нежелательных сердечно-сосудистых событий на основе расчета и оценки прогностического коэффициента: при значении прогностического коэффициента +13 пациент относится к группе риска.
Применение данных оценки риска позволяет формировать сравнительно однородные по прогнозу группы пациентов, оптимизировать алгоритм диагностических процедур, оценивать течение диспластического процесса, рационально организовывать профилактические мероприятия и долгосрочное лечение, а также анализировать эффективность лечебно-профилактических вмешательств. Следовательно, индивидуальная оценка риска, основанная на клинических характеристиках пациента, является практическим выражением персонифицированного подхода к ведению пациентов указанной группы, что позволяет подойти к решению следующих задач:
- с использованием комплексной оценки клинических характеристик обосновать новый более эффективный подход к прогнозированию течения наследственной патологии соединительной ткани;
- оптимизировать подходы к предупреждению инвалидизации и ранней смертности при недифференцированных формах наследственной патологии соединительной ткани, основанные на принципе стратификации риска.
Отличительные признаки проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области и неочевидные для специалиста. Идентичной совокупности признаков в проанализированной литературе не обнаружено. Предлагаемое изобретение может быть использовано в здравоохранении.
Исходя из вышеизложенного, следует считать изобретение соответствующим условиям патентоспособности "Новизна", "Изобретательский уровень", "Промышленная применимость".
Способ осуществляется следующим образом.
Обследовано 549 пациентов в возрасте 18-45 лет, имеющих признаки наследственных нарушений соединительной ткани (ННСТ): 330 (60,11%) мужчин и 219 (39,89%) женщин. К основным проявлениям ННСТ относили следующие клинические признаки: со стороны костно-мышечной системы - идиопатический сколиоз или кифосколиоз грудного и/или поясничного отделов позвоночника, гиперлордоз поясничного отдела позвоночника, гиперкифоз грудного отдела позвоночника, синдром прямой спины, спондилолистез, крыловидные лопатки, идиопатические деформации грудной клетки (воронкообразная, килевидная), долихостеномелия, арахнодактилия, идиопатическая варусная или вальгустная деформация голеней, плоскостопие продольное и/или поперечное, полая стопа, гипермобильность суставов, пронация стоп, расширение пупочного кольца, паховая, вентральная грыжа; со стороны сердечно-сосудистой системы - пролапсы и/или миксоматозная дегенерация клапанов сердца, расширение/аневризма/диссекция артерий (аорта, легочня артерия, артерии головы и шеи, брюшной полости), флебопатия, варикозное расширение вен (нижних, верхних конечностей, таза), гипоплазия и/или патологическая извитость артерий (артерии головы и шеи, висцеральные и пр.), идиопатическая гипотензия; со стороны желудочно-кишечного тракта - рефлюксная болезнь, птоз желудка и/или кишечника, долихосигма; со стороны дыхательной системы - трахеобронхомаляция, трахеобронхомегалия, спонтанный идиопатический пневмоторакс, идиопатические апикальные буллы, гипервентиляционный синдром; со стороны мочеполовой системы - нефроптоз, пролапс генитальный; глазные проявления - нарушения рефракции, вывих/подвывих хрусталика, голубые склеры; кожные проявления - тонкая кожа, келоидные рубцы, симптом «папиросной бумаги», атрофические стрии, гиперэластичная (гиперрастяжимая) кожа. Оценка наличия ННСТ проводилась с расчетом диагностического коэффициента по Яковлеву В.М., Нечаевой Г.И. (1994 г.) [15].
Средний возраст в группе составил 23,51±8,67 (95%ДИ 22,78-24,24). Представленность диспластических изменений в наблюдаемой группе пациентов характеризовалась доминированием проявлений со стороны костно-мышечного аппарата и сердечно-сосудистой системы (табл. 1).
В среднем проявления дисморфогенеза соединительной ткани (синоним ННСТ) регистрировались со стороны одновременно трех указанных выше систем органов, включая орган зрения и кожу (3,06±0,93). При оценке признаков ННСТ в соответствие с Национальными рекомендациями [1] с наибольшей частотой регистрировались следующие фенотипы: повышенная диспластическая стигматизация/повышенная преимущественно висцеральная диспластическая стигматизация (59,19%), синдром ПМК (28,23%).
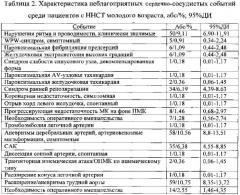
Средняя длительность наблюдения общей группы пациентов с ННСТ составила 7,49±3,44 лет (95%ДИ 7,21-7,79). Средний возраст в группе на контрольном визите - 31,01±8,58 лет (95%ДИ 30,29-31,73). В изучаемой группе у 156 пациентов (28,42%; 95%ДИ 24,72-32,43) в возрасте 18-45 лет было зафиксировано 217 неблагоприятных события, связанные с патологией сердца и/или сосудов (табл. 2).
Средний возраст манифестации неблагоприятного сердечно-сосудистого события (НССС) - 27,95±8,14 лет (95%ДИ 26,66-29,24). Для последующего анализа пациенты были разделены на группы: группа 1 (ННСТ с развитием нежелательных сердечно-сосудистых событий) и группа 2 (ННСТ без нежелательных сердечно-сосудистых событий). Общепопуляционные факторы риска (артериальная гипертензия, курение, злоупотребление алкоголем, тяжелый физический труд) регистрировались в группе пациентов с НССС (группа 1) и группе пациентов без НССС (группа 2) с одинаковой частотой: 15,38% (n=24; 95%ДИ 10,29-22,22) и 10,18% (n=40; 95%ДИ 7,46-13,71), соответственно (χ2 2,04; df 1; р=0,1537). В группе с НССС было значимо больше мужчин 66,67% (n=104; 95%ДИ 58,62-73,88%) и 57,51% (n=226; 95%ДИ 52,45-62,43%), соответственно в группе I и группе II (χ2 3,91; р=0,048). В группе 1 значимо чаще встречались MAP и пороки развития сердца и висцеральных сосудов (97,44% и 62,85%), соответственно; χ2 67,27; df 1; р=0,000). В группе 1 суммарный диагностический коэффициент (ДК) был значимо выше, чем в группе 2 (36,10±13,02 и 25,96±8,09; критерий Баренса-Фишера 9,059; р=0,000). Оценка признаков ННСТ в группах позволила выделить отдельные перспективные для включения в прогностический алгоритм проявления. Принимая во внимание только те признаки, которые значимо различались между группами, мы оценили показатель информативности и рассчитали прогностические коэффициенты для определения суммарного риска развития нежелательных сердечно-сосудистых событий. Оценка информативности и расчет прогностического коэффициента признака с построением суммарных прогностических таблиц проводилась с использованием метода Кульбака и неоднородной последовательной статистической процедуры распознавания [16], соответственно:
величина информативности I диапазона i признака j равна:
I ( x j i ) = Д К ( x j i ) 1 2 [ P ( x j i A ) − P ( x j i B ) ] ,
где ДК - диагностический коэффициент;
Д К ¯ ( x j i ) = 10 log P ¯ ( x j i / A ) P ¯ ( x j i / B ) ,
где P ¯ ( x i j / A ) и P ¯ ( x i j / B ) - средневзвешенные частости признака.
За минимальную информативность для включения признака в прогностическую таблицу принимали I (xj)=0.5 (табл. 3).
Учитывая значимость оцениваемого фактора - развитие НССС, величину пороговых сумм прогностических коэффициентов (ПК) рассчитывали исходя из допустимого уровня α (ошибка первого рода) 0,05 (5%), β (ошибка второго рода) - 0,05 (5%): +13 (гипотеза/заболевание А) и - 13 (гипотеза/заболевание В).
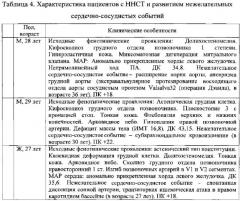
Предлагаемый способ оценки риска был реализован в группе пациентов с ННСТ (n=65; средняя длительность наблюдение 2,5 года). После анализа ПК пациенты были разделены на 2 группы: группа 1 (ПК≥13; n=27), группа 2 (ПК<13; n=38). За указанное время наблюдения в группе 1 зарегистрировано 3 нежелательных сердечно-сосудистых события (11,11%, 95%ДИ 2,91-30,30): расширение корня аорты, n=2; расширение восходящей аорты, n=1; спонтанная диссекция сонной артерии, транзиторная ишемическая атака в правом каротидном бассейне, n=1; 2 мужчин (табл. 4).
В группе 2 нежелательных явлений не зарегистрировано (0,00%; 95%ДИ 0,0-11,43). Группы значимо различались (χ2 49,80; df 1; р=0,000) по исходам наблюдения. Таким образом, предлагаемый способ оценки суммарного риска развития нежелательных сердечно-сосудистых событий продемонстрировал свою эффективность.
Предлагаемый способ оценки суммарного риска нежелательных сердечно-сосудистых событий применен у 65 пациентов молодого возраста с недифференцированными формами наследственных нарушений соединительной ткани и позволяет повысить эффективность оценки риска нежелательных сердечно-сосудистых событий у пациентов указанной группы.
Источники информации
1. Наследственные нарушения соединительной ткани в кардиологии. Диагностика и лечение. Российские рекомендации (I пересмотр). - Российский кардиологический журнал №1 (99), 2013, приложение 1. - 32 с.
2. Яковлев В.М., Нечаева Г.И., Бакулина Е.Г. Основы клинической диагностики дисплазии соединительной ткани: руководство для практического врача. - Ставрополь: АГРУС, 2011. - 408 с.
3. Кадурина Т.И., Горбунова В.Н. Дисплазия соединительной ткани. Руководство для врачей. - СПб.: Элби-СПб, 2009. - 704 с.
4. Isolated mitral valve prolapse is an independent predictor of aortic root size in a general population. J.R. Matos-Souza, M.E. Fernandes-Santos, E.L. Hoehne et al. Eur J Echocardiogr. 2010. V. 11(3). P. 302-305.
5. Incidence of Aortic Root Dilatation in Pectus Excavatum and Its Association With Marfan Syndrome. D. Rhee, D. Solowiejczyk, K. Altmann, A. Prakash et al. Arch Pediatr Adolesc Med. 2008. V. 162(9). P. 882-885.
6. Caglayan A.O., Dundar M. Inherited diseases and syndromes leading to aortic aneurysms and dissections. European Journal of Cardio-thoracic Surgery. 2009. V. 35. P. 931-940.
7. Vanakker O.M., Hemelsoet D., Paepe A.De. Hereditary Connective Tissue Diseases in Young Adult Stroke: A Comprehensive Synthesis. Stroke Res Treat. 2011; ID 712903, 18 p. http://dx.doi.org/10.4061/2011/712903.
8. Familial Cervical Artery Dissections Clinical, Morphologic, and Genetic Studies. Martin J.J., Hausser I., Lyrer P. et al. Stroke. 2006. V. 37. P. 2924-2929.
9. Aburawi E.H., O′Sullivan J. Relation of aortic root dilatation and age in Marfan′s syndrome. Eur. Heart J. 2007. V. 28. P. 376-379.
10. Guidelines on the management of valvular heart disease (version 2012). The Joint Task Force on the Management of Valvular Heart Disease of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). Eur. Heart J. 2012. V. 33. P. 2451-2496.
11. Guidelines for the Diagnosis and Management of Patients With Thoracic Aortic Disease. 2010 ACCF/AHA/AATS/ACR/ASA/SCA/SCAI/SIR/STS/SVM. Circulation. 2010. V. 121. P. e266-e369.
12. Executive summary: HRS/EHRA/APHRS expert consensus statement on the diagnosis and management of patients with inherited primary arrhythmia syndromes. S.G. Priori, A.A. Wilde, M. Horie et al. Europace. 2013. V. 15. P. 1389-1406.
13. 2013 ESH/ESC Guidelines for the management of arterial hypertension: the Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). Mancia G., Fagard R., Narkiewicz K. et al. J. Hypertension 2013. V. 31(7). P. 1281-1357.
14. Методология курации пациентов с дисплазией соединительной ткани семейным врачом в аспекте профилактики ранней и внезапной смерти. Г.И. Нечаева, В.П. Конев, И.А. Викторова и др. - Российские медицинские вести, 2004, №3, с. 25-32.
15. Яковлев В.М., Нечаева Г.И. Кардио-респираторные синдромы при дисплазии соединительной ткани. Омск: ОГМА, 1994. - 217 с.
16. Гублер Ε.В. Применение непараметрических критерией статистики в медико-биологических исследованиях / Е.В. Гублер, А.А. Генкин. - Ленинград: Медицина, 1973. - 141 с.
Способ оценки суммарного риска нежелательных сердечно-сосудистых событий у пациентов с недифференцированными формами наследственных нарушений соединительной ткани, отличающийся тем, что определяют возраст пациента и выявляют наличие диспластических изменений в органах, присваивают выявленным изменениям прогностические коэффициенты, причем при наличии кожных проявлений присваивают коэффициент «+6», флебопатии - «+6», патологии позвоночных артерий - «+2», наследственных нарушений соединительной ткани со стороны 3 и более органов - «+2», а менее 3 - «-4», полностью разомкнутого Виллизиева круга - «+7», двустворчатого аортального клапана - «+16», если возраст пациента составляет до 30 лет включительно присваивают прогностический коэффициент «+6», а более 30 лет - «-3», далее полученные коэффициенты суммируют и при достижении значения «+13» определяют принадлежность пациента к группе риска.