Pde10 ингибиторы и содержащие их композиции и способы
Иллюстрации
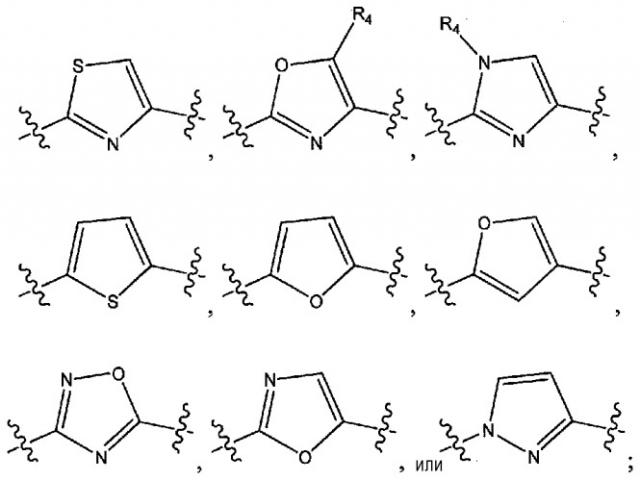
Показать всеИзобретение относится к соединениям формулы (I) и их фармацевтически приемлемым солям, где А является тиазолилом, оксазолилом, тиенилом, фурилом, имидазолилом, пиразолилом или оксадиазолилом (структуры которых приведены в п.1 формулы изобретения), R1 представляет собой C1-6алкил; R2 представляет собой (i) фенил, замещенный галогеном; C1-6алкилом, необязательно замещенным морфолином или C1-6диалкиламино; C1-6алкокси, необязательно замещенным галогеном; или гетероциклилом, где гетероциклильный заместитель выбран из морфолина; пиразолила, необязательно замещенного C1-6алкилом; пиперидинила; пирролидинила; оксадиазолила, замещенного C1-6алкилом; фурила, замещенного C1-6алкилом; диоксидоизотиазолидинила; триазолила; тетразолила, замещенного C1-6алкилом, тиадиазолила, замещенного C1-6алкилом; тиазолила, замещенного C1-6алкилом; пиридила; или пиразинила; (ii) замещенный или незамещенный гетероциклил, выбранный из хинолинила; пиридила, замещенного C1-6алкокси или морфолинилом; или бензо [d] [1, 2, 3] триазолила, замещенного C1-6алкилом; R3 представляет собой фенил, замещенный 2 или 3 заместителями, выбранными из галогена; C1-6алкила; C1-6алкокси, необязательно замещенного галогеном; гидроксигруппой; циано; или -C(=O)ORa, где Ra представляет собой фенил; R4 представляет собой водород, C1-6алкил или C1-6галогеналкил. Также изобретение относится к фармацевтической композиции, содержащей соединения формулы (I), способу ингибирования PDE10, способу лечения неврологических расстройств и к промежуточным соединениям: 2-(4-хлор-3,5-диметоксифенил)фурану и 4-(5-метил-1,3,4-тиадиазол-2-ил)бензальдегиду. Технический результат - соединения формулы (I) в качестве ингибиторов PDE10. 6 н. и 33 з.п. ф-лы, 13 ил., 2 табл., 77 пр.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка заявляет приоритет в соответствии с 35 U.S.C. §119(e) предварительной патентной заявкой США № 61/313544, поданной 12 марта 2010, и предварительной патентной заявкой США № 61/430841, поданной 7 января 2010, данные заявки включены в настоящее описание полностью с помощью ссылки.
УРОВЕНЬ ТЕХНИКИ
Область техники, к которой относится настоящее изобретение
В общем, настоящее изобретение относится к соединениям, обладающим активностью в качестве PDE10 ингибиторов, и к содержащим их композициям, а также способам лечения различных заболеваний путем введения данных соединений нуждающемуся в этом теплокровному животному.
Описание родственного уровня техники
Фосфодиэстеразы циклических нуклеотидов (PDE) представлены большим суперсемейством ферментов. Известно, что PDE имеют модульное строение, с консервативным каталитическим доменом, близким к карбоксильному концу, и регуляторными доменами или мотивами, часто вблизи аминоконца. В настоящее время PDE суперсемейство включает более двадцати различных генов, разделенных на одиннадцать PDE семейств (Lugnier, C., "Cyclic nucleotide phosphodiesterase (PDE) superfamily: a new target for the development of specific therapeutic agents". Pharmacol Ther. 2006 Mar; 109(3):366-98).
О недавно описанной PDE, PDE10, одновременно сообщалось тремя независимыми группами (Fujishige et al., "Cloning and characterization of a novel human phosphodiesterase that hydrolyzes both cAMP and cGMP (PDE10A)", J Biol Chem 1999, 274:18438-18445; Loughney et al., "Isolation and characterization of PDE10A, a novel human 3',5'-cyclic nucleotide phosphodiesterase," Gene 1999, 234:109-117; Soderling et al., "Isolation and characterization of a dual-substrate phosphodiesterase gene family: PDE10A", Proc Natl Acad Set USA 1999, 96:7071-7076). PDE10 обладает способностью гидролизовать и цАМФ, и цГМФ; однако, K m для цАМФ составляет приблизительно 0,05 мкМ, тогда как K M для цАМФ составляет 3 мкМ. Кроме того, V max для цАМФ гидролиза в пять раз меньше, чем для цГМФ. Из-за данной кинетики цГМФ гидролиз PDE10 эффективно ингибируется цАМФ in vitro, предполагая, что PDE10 может функционировать как цАМФ-ингибированная цГМФ фосфодиэстераза in vivo. В отличие от PDE8 или PDE9, PDE10 ингибируется IBMX с IC50 (концентрация, ингибирующая 50%) 2,6 мкМ (см. Soderling and Beavo, "Regulation of cAMP and cGMP signaling: new phosphodiesterases and new functions", Current Opinion in Cell Biology, 2000, 12:174-179).
PDE10 содержит два аминоконцевых домена, которые являются аналогичными цГМФ-связывающим доменам PDE2, PDE5 и PDE6, которые представляют собой домены, консервативные для широкого спектра белков. Из-за большой консервативности данного домена в настоящее время его называют GAF доменом (для GAF белков: цГМФ связывающие фосфодиэстеразы; аденилатциклаза цианобактерии Anabaena; и транскрипционный регулятор fh1A Escherichia coli). Хотя в PDE2, PDE5 и PDE6 GAF домены связывают цГМФ, это, вероятно, не основная функция данного домена во всех случаях (например, считается, что E. coli не синтезирует цГМФ). Интересно, что in vitro исследования связывания PDE10 показывают константу диссоциации (Kd) для цГМФ связывания, значительно большую 9 мкМ. Поскольку считается, что in vivo концентрации цГМФ не достигают таких больших значений в большинстве клеток, по-видимому вероятно, что либо сродство PDE10 к цГМФ увеличивается регуляцией, либо первичная функция GAF домена в PDE10 может быть несколько отличной от цГМФ связывания.
Повсеместно ведется поиск ингибиторов PDE семейства ферментов для широкого диапазона показаний терапевтических применений. Описанные в литературе терапевтические применения PDE ингибиторов включают аллергию, обструктивное заболевание легких, гипертонию, рак почки, стенокардию, сердечную недостаточность, депрессию и эректильную дисфункцию (WO 01/41807 A2). Другие ингибиторы PDE описывают для лечения ишемических заболеваний сердца (патент США № 5693652). Более конкретно, ингибиторы PDE10 описывают как пригодные для лечения определенных неврологических и психических расстройств, включая, болезнь Паркинсона, болезнь Хантингтона, шизофрению, бредовые расстройства, психоз, вызванный употреблением наркотиков, и панические и обсессивно-компульсивные расстройства (патентная заявка США № 2003/0032579). Было показано, что PDE10 присутствует при высокой концентрации в нейронах в областях мозга, которые тесно связаны со многими неврологическими и психиатрическими расстройствами. Посредством ингибирования PDE10 активности концентрации цАМФ и цГМФ увеличиваются в нейронах, и способность данных нейронов правильно функционировать посредством этого улучшается. Таким образом, считается, что ингибирование PDE10 является пригодным для лечения широкого диапазона заболеваний или расстройств, для которых было бы полезно увеличивать концентрации цАМФ и цГМФ в нейронах, включая те неврологические, психотические, тревожные расстройства и/или двигательные расстройства, которые упомянуты выше.
Тогда как успех был достигнут относительно ингибирования PDE10, в данной области еще остается необходимость в ингибиторах PDE10, а также необходимость лечения различных заболеваний и/или состояний, для которых могло бы быть полезно данное ингибирование.
КРАТКОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Вкратце, настоящее изобретение, в общем, относится к соединениям, которые обладают активностью в качестве PDE10 ингибиторов, а также способам их получения и применения, и к содержащим их фармацевтическим композициям.
В одном варианте осуществления соединения имеют следующую общую структуру (I):
включая их фармацевтически приемлемые соли, стереоизомеры, сольваты и пролекарства, в которых A, R1, R2 и R3 такие, как определено ниже.
Соединения настоящего изобретения можно применять в широком диапазоне терапевтических применений и их можно применять для лечения широкого диапазона заболеваний или расстройств, для которых было бы полезно увеличение концентрации цАМФ и цГМФ, особенно в нейронах, включая (но не ограничиваясь) неврологические расстройства, такие как психотические расстройства, тревожные расстройства, двигательные расстройства и/или неврологические расстройства, такие как болезнь Паркинсона, болезнь Хантингтона, болезнь Альцгеймера, энцефалит, фобия, эпилепсия, афазия, паралич Белла, церебральный паралич, нарушения сна, боль, синдром Туретта, шизофрения, бредовые расстройства, биполярные расстройства, посттравматические стрессовые расстройства, психоз, вызванный употреблением наркотиков, панические расстройства, обсессивно-компульсивные расстройства, синдром дефицита внимания, расстройство социального поведения, аутизм, депрессия, деменция, когнитивные расстройства, эпилепсия, бессонница и рассеянный склероз.
Способы настоящего изобретения включают введение эффективного количества соединения вышеуказанной структуры, обычно в виде фармацевтической композиции, нуждающемуся в этом млекопитающему, включая человека. Таким образом, в следующем варианте осуществления описывают фармацевтические композиции, содержащие одно или более соединений вышеуказанной структуры в комбинации с фармацевтически приемлемым носителем или разбавителем.
Данные и другие аспекты настоящего изобретения будут очевидны со ссылкой на следующее подробное описание. С этой целью в настоящем описании указаны различные ссылки, которые описывают более подробно определенную вспомогательную информацию, методики, соединения и/или композиции, и каждая из ссылок вводится в настоящее описание полностью с помощью ссылки.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
ФИГ.1 показывает, что соединение 1-1 настоящего изобретения (Пример 1), введенное внутрибрюшинной инъекцией, значительно снижает гиперактивность у мышей в модели психоза, вызванного психостимулятором (PCP), при сравнении с контролем с носителем.
ФИГ.2 показывает, что соединение 1-1 настоящего изобретения (Пример 1), введенное пероральным способом введения, значительно снижает гиперактивность у мышей в модели психоза, вызванного психостимулятором (PCP), при сравнении с контролем с носителем.
ФИГ.3 показывает, что соединение 2-1 настоящего изобретения (Пример 2), введенное внутрибрюшинной инъекцией, значительно снижает гиперактивность у мышей в модели психоза, вызванного психостимулятором (PCP), при сравнении с контролем с носителем.
ФИГ.4 показывает, что соединение 2-1 настоящего изобретения (Пример 2), введенное пероральным способом введения, значительно снижает гиперактивность у мышей в модели психоза, вызванного психостимулятором (PCP), при сравнении с контролем с носителем.
ФИГ.5 показывает, что соединение 2-1 настоящего изобретения (Пример 2) значительно снижает условную реакцию избегания (CAR) у мышей, подготовленных в CAR модели психоза при сравнении с контролем с носителем.
ФИГ.6 показывает, что соединение 11-1 настоящего изобретения (Пример 11), введенное внутрибрюшинной инъекцией, значительно снижает гиперактивность у мышей в модели психоза, вызванного психостимулятором (PCP), при сравнении с контролем с носителем.
ФИГ.7 показывает, что соединение 34-1 настоящего изобретения (Пример 34) значительно снижает условную реакцию избегания (CAR) у мышей, подготовленных в CAR модели психоза при сравнении с контролем с носителем.
ФИГ.8 показывает, что соединение 36-1 настоящего изобретения (Пример 36) значительно снижает условную реакцию избегания (CAR) у мышей, подготовленных в CAR модели психоза при сравнении с контролем с носителем.
ФИГ.9 показывает, что соединение 47-1 настоящего изобретения (Пример 47) значительно снижает условную реакцию избегания (CAR) у мышей, подготовленных в CAR модели психоза при сравнении с контролем с носителем.
ФИГ.10 показывает, что соединение 61-1 настоящего изобретения (Пример 61) значительно снижает условную реакцию избегания (CAR) у мышей, подготовленных в CAR модели психоза при сравнении с контролем с носителем.
ФИГ.11 показывает, что соединение 63-1 настоящего изобретения (Пример 63) значительно снижает условную реакцию избегания (CAR) у мышей, подготовленных в CAR модели психоза при сравнении с контролем с носителем.
ФИГ.12 показывает, что соединение 49-1 настоящего изобретения (Пример 49) значительно снижает условную реакцию избегания (CAR) у мышей, подготовленных в CAR модели психоза при сравнении с контролем с носителем.
ФИГ.13 показывает, что соединение 65-10 настоящего изобретения (Пример 65, таблица 1) значительно снижает условную реакцию избегания (CAR) у мышей, подготовленных в CAR модели психоза при сравнении с контролем с носителем.
ПОДРОБНОЕ ОПИСАНИЕ
Как упоминается выше, в общем, настоящее изобретение относится к соединениям, пригодным в качестве PDE10 ингибиторов, а также способам их получения и применения и к содержащим их фармацевтическим композициям.
В одном варианте осуществления PDE10 ингибиторы имеют следующую структуру (I):
или их фармацевтически приемлемая соль, стереоизомер, сольват или пролекарство,
в которой:
A представляет собой:
или
R1 представляет собой C1-6алкил, C1-6галогеналкил, C1-6аралкил, арил, -(CH2)nO(CH2)mCH3 или -(CH2)nN(CH3)2;
R2 представляет собой (i) замещенный или незамещенный арил или (ii) замещенный или незамещенный гетероциклил;
R3 представляет собой замещенный или незамещенный арил;
R4 представляет собой водород, C1-6алкил или C1-6галогеналкил;
n равно 1, 2, 3, 4, 5 или 6; и
m равно 0, 1, 2, 3, 4, 5 или 6.
Как используется в настоящем описании, вышеуказанные термины имеют следующие значения:
"Амино" относится к -NH2 радикалу.
"Циано" относится к -CN радикалу.
"Гидрокси" или "гидроксил" относится к -OH радикалу.
"Имино" относится к =NH заместителю.
"Нитро" относится к -NO2 радикалу.
"Оксо" относится к =O заместителю.
"Тиоксо" относится к =S заместителю.
"C1-6алкил" относится к линейному или разветвленному, нециклическому или циклическому, ненасыщенному или насыщенному алифатическому углеводородному радикалу, содержащему от 1 до 6 атомов углерода. Примеры насыщенных алкилов с прямой цепью включают метил, этил, н-пропил, н-бутил, н-пентил, н-гексил и подобные; тогда как насыщенные разветвленные алкилы включают изопропил, втор-бутил, изобутил, трет-бутил, изопентил и подобные. Примеры насыщенных циклических алкилов включают циклопропил, циклобутил, циклопентил, циклогексил и подобные; тогда как ненасыщенные циклические алкилы включают циклопентенил и циклогексенил и подобные. Ненасыщенные алкилы содержат, по меньшей мере, одну двойную или тройную связь между соседними атомами углерода (называемые "алкенил" или "алкинил" соответственно). Примеры алкенилов с прямой или разветвленной цепью включают этиленил, пропиленил, 1-бутенил, 2-бутенил, изобутиленил, 1-пентенил, 2-пентенил, 3-метил-1-бутенил, 2-метил-2-бутенил, 2,3-диметил-2-бутенил и подобные; тогда как примеры алкинилов с прямой или разветвленной цепью включают ацетиленил, пропинил, 1-бутинил, 2-бутинил, 1-пентинил, 2-пентинил, 3-метил-1-бутинил и подобные.
"C1-6алкилен" или "C1-6алкиленовая цепь" относится к прямой или разветвленной двухвалентной углеводородной цепи, присоединяющей остаток молекулы к радикалу, состоящей только из атомов углерода и водорода, которая является насыщенной или ненасыщенной (т.е. содержит одну или более двойных и/или тройных связей), и содержащей от одного до шести атомов углерода, например метилен, этилен, пропилен, н-бутилен, этенилен, пропенилен, н-бутенилен, пропинилен, н-бутинилен и подобные. Алкиленовую цепь присоединяют к остатку молекулы через одинарную или двойную связь и к радикалу через одинарную или двойную связь. Положения присоединения алкиленовой цепи к остатку молекулы и к радикалу можно осуществлять через один атом углерода или любые два атома углерода в цепи.
"C1-6алкокси" относится к радикалу формулы -ORa, где Ra представляет собой алкильный радикал, как определено выше, например метокси, этокси и подобные.
"Арил" относится к углеводородной кольцевой системе, включающей водород, 6-18 атомов углерода и, по меньшей мере, одно ароматическое кольцо. Арильный радикал может представлять собой моноциклическую, бициклическую, трициклическую или тетрациклическую кольцевую систему, которая может содержать конденсированные или мостиковые кольцевые системы. Арильные радикалы включают, но не ограничиваются ими, арильные радикалы, полученные из ацеантрилена, аценафтилена, ацефенантрилена, антрацена, азулена, бензола, хризена, фторантена, флуорена, as-индацена, s-индацена, индана, индена, нафталина, феналена, фенантрена, плеиадена, пирена и трифенилена.
"C1-6аралкил" обозначает радикал формулы -Rb-Rc, где Rb представляет собой алкиленовую цепь, как определено выше, и Rc представляет собой один или более арильных радикалов, как определено выше, например бензил, дифенилметил и подобные.
"Циклоалкил" или "карбоциклическое кольцо" относится к стабильному неароматическоу моноциклическому или полициклическому углеводородному радикалу, состоящему только из атомов углерода и водорода, который может содержать конденсированные или мостиковые кольцевые системы, содержащие от трех до пятнадцати атомов углерода, предпочтительно содержащие от трех до десяти атомов углерода, и который может быть насыщенным или ненасыщенным и присоединенным к остатку молекулы одинарной связью. Моноциклические радикалы включают, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Полициклические радикалы включают, например, адамантил, норборнил, декалинил, 7,7-диметил-бицикло[2,2,1]гептанил и подобные.
"Гало" или "галоген" относится к брому, хлору, фтору или йоду.
"C1-6галогеналкил" относится к C1-6алкильному радикалу, как определено выше, который замещен одним или более галогеновыми радикалами, как определено выше, например трифторметил, дифторметил, трихлорметил, 2,2,2-трифторэтил, 1,2-дифторэтил, 3-бром-2-фторпропил, 1,2-дибромэтил и подобные.
"Гетероцикл" или "гетероциклил" относится к 4-7-членному моноциклическому или 7-10-членному бициклическому, гетероциклическому кольцу, который является либо насыщенным, ненасыщенным, либо ароматическим, и который содержит от 1 до 4 гетероатомов, независимо выбранных из азота, кислорода и серы, и в котором гетероатомы азота или серы могут быть необязательно окислены, и гетероатом азота может быть необязательно кватернизирован, включая бициклические кольца, в которых любой из вышеуказанных гетероциклов конденсирован с бензольным кольцом. Гетероцикл может быть присоединен через любой гетероатом или атом углерода. Ароматический гетероцикл называют в настоящем описании "гетероарил", и он включает (но не ограничивается) фурил, бензофуранил, тиофенил, бензотиофенил, пирролил, индолил, изоиндолил, азаиндолил, пиридил, хинолинил, изохинолинил, оксазолил, изоксазолил, бензоксазолил, пиразолил, имидазолил, бензимидазолил, тиазолил, бензотиазолил, изотиазолил, пиридазинил, пиримидинил, пиразинил, триазинил, циннолинил, фталазинил, оксадиазолил, тиадиазолил, бензизоксазолил, триазолил, тетразолил, индазолил и хиназолинил. В добавление к перечисленным выше гетероарилам, гетероциклы также включают морфолинил, пирролидинонил, пирролидинил, пиперидинил, пиперазинил и подобные. Кроме того, гетероциклы также включают бензотиофен-2-ил, 2,3-дигидробензо-1,4-диоксин-6-ил, бензо-1,3-диоксол-5-ил и подобные.
Термин "замещенный", как применяют в настоящем описании (например, в контексте замещенного гетероциклила или замещенного арила), обозначает то, что, по меньшей мере, один атом водорода замещен заместителем. "Заместители" в контексте настоящего изобретения включают галоген, гидрокси, оксо, циано, нитро, имино, тиоксо, амино, алкиламино, диалкиламино, алкил, алкокси, алкилтио, галогеналкил, арил, аралкил, гетероарил, гетероарилалкил, гетероцикл и гетероциклалкил, а также -NRaRb, -NRaC(=O)Rb, -NRaC(=O)NRaNRb, -NRaC(=O)ORb, - NRaSO2Rb, -C(=O)Ra, -C(=O)ORa, -C(=O)NRaRb, -OC(=O)NRaRb, -ORa, -SRa, -SORa, -S(=O)2Ra, -OS(=O)2Ra, -S(=O)2ORa, =NSO2Ra и -SO2NRaRb. В вышеуказанных заместителях Ra и Rb в данном контексте могут быть одинаковыми или различными и независимо представлять собой водород, алкил, галогеналкил, циклоалкил, арил, аралкил, гетероциклил. Кроме того, вышеуказанные заместители могут быть дополнительно замещены одним или более из указанных выше заместителей.
В следующих вариантах осуществления структуры (I) соединение имеет следующую структуру (I-A):
В других следующих вариантах осуществления структуры (I) соединение имеет следующую структуру (I-B):
В других следующих вариантах осуществления структуры (I) соединение имеет следующую структуру (I-С):
В других следующих вариантах осуществления структуры (I) соединение имеет следующую структуру (I-D):
В других следующих вариантах осуществления структуры (I) соединение имеет следующую структуру (I-E):
В других следующих вариантах осуществления структуры (I) соединение имеет следующую структуру (I-F):
В других следующих вариантах осуществления структуры (I) соединение имеет следующую структуру (I-G):
В других следующих вариантах осуществления структуры (I) соединение имеет следующую структуру (I-H):
В других следующих вариантах осуществления структуры (I) соединение имеет следующую структуру (I-I):
В других следующих вариантах осуществления структуры (I), в частности структурах (I-B) и (I-C), R4 представляет собой водород или R4 представляет собой C1-6алкил (такой как, например, метил).
В других следующих вариантах осуществления структуры (I) R1 представляет собой C1-6алкил (такой как, например, R1 представляет собой метил или этил).
В других следующих вариантах осуществления структуры (I) R3 представляет собой замещенный или незамещенный фенил (такой как, например, 4-бром-3,5-диметоксифенил, 4-хлор-3,5-диметоксифенил или 3,4,5-триметоксифенил).
В других следующих вариантах осуществления структуры (I) R2 представляет собой замещенный или незамещенный арил, такой как замещенный или незамещенный фенил. В более конкретных вариантах осуществления, в которых R2 представляет собой замещенный фенил, R2 представляет собой фенил, замещенный C1-6алкокси, или R2 представляет собой фенил, замещенный замещенным или незамещенным гетероциклилом (такой как, например, 4-(5-метил-1,3,4-оксадиазол-2-ил)фенил, 4-(5-метил-1,3,4-тиадиазол-2-ил)фенил или 4-морфолинофенил).
В других следующих вариантах осуществления структуры (I) R2 представляет собой замещенный или незамещенный гетероциклил.
Соединения настоящего изобретения можно обычно применять в виде свободной кислоты или свободного основания. Альтернативно, соединения настоящего изобретения можно применять в виде солей присоединения кислоты или основания. Соли присоединения кислоты свободных аминосоединений настоящего изобретения можно получить способами, хорошо известными в данной области техники, и их можно получить из органических и неорганических кислот. Подходящие органические кислоты включают малеиновую, фумаровую, бензойную, аскорбиновую, янтарную, метансульфоновую, уксусную, трифторуксусную, щавелевую, пропионовую, винную, салициловую, лимонную, глюконовую, молочную, миндальную, коричную, аспарагиновую, стеариновую, пальмитиновую, гликолевую, глютаминовую и бензолсульфоновую кислоты. Подходящими неорганическими кислотами являются хлороводородная, бромоводородная, серная, фосфорная и азотная кислота. Соли присоединения основания включают те соли, которые образуются с карбоксилатным анионом, и включают соли, полученные с органическими и неорганическими катионами, такие как соли, выбранные из солей щелочных и щелочноземельных металлов (например, лития, натрия, калия, магния, бария и кальция), а также аммониевым ионом и его замещенными производными (например, дибензиламмоний, бензиламмоний, 2-гидроксиэтиламмоний и подобные). Таким образом, предполагается, что термин "фармацевтически приемлемая соль" структуры (I) включает любую и все приемлемые солевые формы.
Кроме того, пролекарства также включены в контекст настоящего изобретения. Пролекарства представляют собой любые ковалентно-связанные носители, которые высвобождают соединение структуры (I) in vivo при введении данного пролекарства пациенту. Пролекарства обычно получают модификацией функциональных групп таким способом, чтобы данная модификация расщеплялась, или обычными способами или in vivo, давая исходное соединение. Пролекарства включают, например, соединения настоящего изобретения, в которых гидрокси, амино или сульфгидрильная группа соединены с любой группой, которая при введение пациенту расщепляется, образуя гидрокси, амино или сульфгидрильную группы. Таким образом, типичные примеры пролекарств включают (но не ограничиваются ими) ацетатные, формиатные и бензоатные производные спиртовой и аминовой функциональной группы соединения структуры (I). Далее, в случае карбоновой кислоты (-COOH) можно применять эфиры, такие как метиловый эфир, этиловый эфир и подобные.
Предусматривается, что настоящее изобретение, описанное в настоящем описании, также включает все фармацевтически приемлемые соединения структуры (I), изотопно меченные одним или более атомами, замещенными атомами, имеющими различный атомный вес и массовое число. Примеры изотопов, которые можно вводить в описанные соединения, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора, хлора и йода, такие как 2H, 3H, 11C, 13C, 14C, 13N, 15N, 15O, 17O, 18O, 31P, 32P, 35S, 18F, 36Cl, 123I и 125I соответственно. Данные радиомеченные соединения могут быть пригодны для того, чтобы помочь определить или измерить эффективность соединений, характеризуя, например, место или способ действия, или связывающую способность фармакологически важного места действия. Определенные изотопно-меченные соединения структуры (I), например соединения с введенным радиоактивным изотопом, являются пригодными для исследований распределения в тканях лекарственного средства и/или субстрата. Радиоактивные изотопы тритий, т.е. 3H, и углерод-14, т.е. 14C, являются особенно пригодными для данной цели из-за легкости введения и готовых способов детекции. Замещение более тяжелыми изотопами, такими как дейтерий, т.е. 2H, может давать определенные терапевтические преимущества, являющиеся результатом большей метаболической стабильности, например увеличения in vivo периода полураспада или снижения требуемых доз, и, следовательно, оно может быть предпочтительным в некоторых обстоятельствах. Замещение позитронно-активными изотопами, такими как 11C, 18F, 15O и 13N, может быть пригодным в исследованиях с помощью позитронно-эмиссионной томографии (PET) для изучения степени занятости рецептора субстратом. Изотопно-меченные соединения структуры (I) обычно можно получить общепринятыми способами, известными специалисту в данной области техники, или способами, аналогичными способам, описанным в примерах, как указано ниже, применяя подходящий изотопно-меченный реагент вместо немеченого реагента, применяемого ранее.
Что касается стереоизомеров, соединения структуры (I) могут содержать хиральные центры и могут существовать в виде рацематов, рацемических смесей и в виде индивидуальных энантиомеров или диастереомеров. Все данные изомерные формы включены в объем настоящего изобретения, включая их смеси. Кроме того, некоторые кристаллические формы соединений структуры (I) могут существовать в виде полиморфов, которые включены в объем настоящего изобретения. Кроме того, некоторые соединения структуры (I) могут также образовывать сольваты с водой или другими органическими растворителями. Аналогично, данные сольваты включены в объем настоящего изобретения.
В другом варианте осуществления настоящего изобретения описывают фармацевтические композиции, содержащие одно или более из соединений структуры (I). Для целей введения соединения настоящего изобретения можно формулировать в виде фармацевтических композиций. Фармацевтические композиции настоящего изобретения содержат одно или более из соединений настоящего изобретения и фармацевтически приемлемый носитель и/или разбавитель. PDE10 ингибитор присутствует в композиции в количестве, которое является эффективным для лечения конкретного заболевания, т.е. в количестве, достаточном для достижения требуемого PDE10 ингибирования, и предпочтительно с приемлемой токсичностью для теплокровного животного. Обычно фармацевтические композиции настоящего изобретения могут содержать PDE10 ингибитор в количестве от 0,1 мг до 250 мг на одну дозу, в зависимости от пути введения, и более обычно от 1 мг до 60 мг. Подходящие концентрации и дозы может легко определить специалист в данной области техники.
В общих чертах, стандартная дневная доза может находиться в диапазоне от приблизительно 1 мкг/кг до 100 мг/кг, предпочтительно 0,01-100 мг/кг, более предпочтительно 0,1-70 мг/кг, в зависимости от типа и тяжести заболевания, например, одним или более отдельными введениями. Для повторяющегося введения в течение нескольких дней или более в зависимости от заболевания лечение осуществляют до требуемого подавления возникающих симптомов заболевания. Однако могут быть пригодны другие режимы дозирования. Прогресс данной терапии может быть отслежен стандартными способами и анализами. Характеристики единичных лекарственных форм настоящего изобретения определяются и непосредственно зависят от уникальных характеристик активного соединения и конкретного терапевтического эффекта, которого требуется достичь, и ограничений, присущих области составления композиций активного соединения для лечения индивидов.
Фармацевтически приемлемый носитель и/или разбавители являются известными специалисту в данной области техники. Что касается композиций, полученных в виде жидких растворов, приемлемые носители и/или разбавители включают соляной раствор и стерильную воду и могут необязательно содержать антиоксиданты, буферы, бактериостаты и другие стандартные добавки. Композиции можно также формулировать в виде пилюль, капсул, гранул или таблеток, которые содержат в добавление к PDE10 ингибитору разбавители, диспергирующие агенты и поверхностно-активные вещества, связующие и смазывающие вещества. Кроме того, специалист в данной области техники может формулировать PDE10 ингибитор подходящим способом и согласно принятой практике, такой как та, что описана в Remington's Pharmaceutical Sciences, Gennaro, Ed., Mack Publishing Co., Easton, PA 1990.
В другом варианте осуществления настоящее изобретение относится к способу лечения заболевания, такого как (но не ограничиваясь ими) психотические расстройства, тревожные расстройства, двигательные расстройства и/или неврологические расстройства, такие как болезнь Паркинсона, болезнь Хантингтона, болезнь Альцгеймера, энцефалит, фобия, эпилепсия, афазия, паралич Белла, церебральный паралич, нарушения сна, боль, синдром Туретта, шизофрения, бредовые расстройства, биполярные расстройства, посттравматические стрессовые расстройства, психоз, вызванный употреблением наркотиков, панические расстройства, обсессивно-компульсивные расстройства, синдром дефицита внимания, расстройства социального поведения, аутизм, депрессия, деменция, когнитивные расстройства, эпилепсия, бессонница и рассеянный склероз, как описано выше. Данные способы включают введение соединения настоящего изобретения теплокровному животному в количестве, достаточном для лечения заболевания. В данном контексте "лечить" включает профилактическое введение. Данный способ включает системное введение PDE10 ингибитора настоящего изобретения, предпочтительно в виде фармацевтической композиции, как обсуждается выше. Как применяют в настоящем изобретении, системное введение включает пероральные и парентеральные способы введения, включая подкожное, внутримышечное, внутричерепное, внутриглазничное, офтальмологическое, внутрижелудочковое, интракапсулярное, внутрисуставное, интраспинальное, интрацистернальное, внутрибрюшинное, интраназальное, аэрозолем, внутривенное, внутрикожное, ингаляционное, трансдермальное, трансмукозальное и ректальное введение.
Что касается перорального введения, подходящие фармацевтические композиции PDE10 ингибиторов включают порошки, гранулы, пилюли, таблетки и капсулы, а также жидкости, сиропы, суспензии и эмульсии. Данные композиции могут также содержать ароматизаторы, консерванты, суспендирующие агенты, загустители и эмульгаторы и другие фармацевтически приемлемые добавки и наполнители. Что касается парентерального введения, соединения настоящего изобретения могут быть получены в виде водных инъецируемых растворов, которые могут содержать, кроме PDE10 ингибитора, буферы, антиоксиданты, бактериостаты и другие добавки и вспомогательные вещества, обычно применяемые в данных растворах. Композиции настоящего изобретения можно доставлять в системе доставки для обеспечения замедленного высвобождения или повышенного поглощения или активности терапевтического соединения, такой как липосомальная или гидрогельная система для инъекции, микрочастицы, наносистема или мицелловая система для пероральной или парентеральной доставки, или капсула с поэтапным высвобождением для пероральной доставки.
В качестве дополнительного преимущества настоящего изобретения ожидается, что у соединений структуры (I) будут отсутствовать или снижены метаболические побочные эффекты, связанные с общепринятыми противопсихотическими препаратами, в частности инцидента терапевтически вызванного ожирения. Например, продолжительное применение оланзапина (Zyprexa®), наиболее часто прописываемого лекарственного препарата для лечения шизофрении, и родственных нестандартных протиопсихотических препаратов, связано со значительными метаболическими побочными эффектами, включая ожирение и связанные с ним заболевания, такие как диабет.
У животных субхроническое лечение оланзапином стимулирует потребление пищи и увеличивает вес тела, также как у человека. Кроме того, оланзапин резко снижает концентрацию лептина в крови. Лептин представляет собой гормон сытости, получаемый в адипозных тканях, и снижение концентрации лептина стимулирует аппетит. Существует теория, что оланзапин может стимулировать потребление пищи, по меньшей мере, частично снижением концентрации лептина. Однократное введение оланзапина также изменяет ответную реакцию животного на концентрацию глюкозы и инсулина в тестах толерантности к глюкозе, что может также быть напрямую связано с эффектом оланзапина на потребление пищи и увеличение массы тела. Исследование острого эффекта PDE10 ингибиторов настоящего изобретения на метаболизм, такой как изменения, связанные с лептином, инсулином и глюкозой в процессе метаболизма в стандартных животных моделях, а также хронического эффекта PDE10 ингибиторов настоящего изобретения на потребление пищи, вес тела и энергетический гомеостаз, в сравнении с оланзапином должно обосновать фармацевтическое преимущество PDE10 ингибиторов в качестве антипсихотических препаратов с точки зрения побочных эффектов.
Композиции настоящего изобретения можно вводить в комбинации с одним или более дополнительными терапевтическими агентами, в комбинации с или путем одновременного или последовательного введения. Подходящие дополнительные агенты (т.е. вспомогательные вещества) могут включать стандартные противопсихотические препараты, которые блокируют допаминовые D2-рецепторы и серотониновые 5HT2 рецепторы, например галоперидол, флуфеназин, хлорпромазин и нестандартные противопсихотические препараты, например клозапин, оланзапин, рисперидон, кветиамин, зипразидог.
Соединения настоящего изобретения могут быть проанализированы для определения их IC50 величин посредством модификации двухстадийного способа Thompson и Appleman (Biochemistry 10; 311-316; 1971). Вкратце, цАМФ дополняют (3H)цАМФ и выдерживают с PDE10 и различными концентрациями соединений структуры (I). После подходящего периода выдерживания реакцию прекращают нагреванием. Затем смесь подвергают обработке фосфатазой змеиного яда. Фосфатаза гидролизует любой АМФ в смеси, но оставляет непрореагировавший цАМФ незатронутым. Таким образом, выделением цАМФ из смеси и определением ее концентрации (радиографией) можно определить процент ингибирования. IC50 величины можно рассчитать проведением эксперимента при различных концентрациях, применяя стандартные графические способы. Подробное описание данного способа, применяемого для анализов IC50, приведено в следующих примерах. В связи с этим PDE10 ингибиторы настоящего изобретения обладают IC50 100 мкМ или меньшей, обычно меньшей чем 10 мкМ и обычно меньшей чем 1 мкМ.
Соединения настоящего изобретения можно получить известными способами органического синтеза, включая способы, описанные подробно в следующих примерах. Следующие примеры приведены с целью иллюстрации, а не ограничения.
ПРИМЕРЫ
ПРИМЕР 1
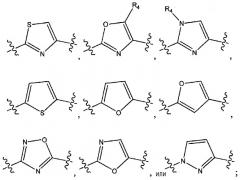
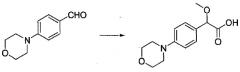
1-(4-(4-БРОМ-3,5-ДИМЕТОКСИФЕНИЛ)ТИАЗОЛ-2-ИЛ)-2-МЕТОКСИ-2-(4-МОРФОЛИНОФЕНИЛ)ЭТАНОН
В колбу, высушенную в сушильном шкафу, загружали 4-(4-морфолинил)бензальдегид (10,1 г, 53 ммоль), безводный метанол (60 мл) и безводный диоксан (60 мл),