Состав для стабилизации липидов к окислению
Иллюстрации
Показать всеИзобретение относится к области пищевой технологии, а именно к способам защиты липидов, масел, жиров от окисления и окислительной деструкции. В качестве антиоксиданта используют 2-гидрокси-1-(N-4′-гидроксифенил)бензкарбамид (осалмид, оксафенамид), добавляемый в количестве 0,01-0,14% от массы липидов. Изобретение направлено на расширение ассортимента эффективных синтетических антиоксидантов, достижение высоких эффектов ингибирования при меньших концентрациях антиоксиданта. 2 табл., 2 пр.
Реферат
Изобретение относится к области пищевой технологии, а именно к способам защиты липидов, масел, жиров от окисления и окислительной деструкции, и может быть использовано в пищевой, косметической и химико-фармацевтической промышленности для получения стабильных липидосодержащих пищевых добавок (нутрицевтиков), лечебно-косметических средств и лекарственных препаратов.
Для торможения процессов окисления применяют антиоксиданты (ингибиторы окисления), которые находят все более широкое применение для предотвращения окислительных превращений липидов и содержащих их препаратов in vitro, а также in vivo в комплексной терапии широкого круга заболеваний / Герчук М.П. Антиокислители в пищевой промышленности // Журн. Всесоюз. хим. общества им. Д.И. Менделеева. - 1960. - N. 4. - С. 395-402. Авакумов В.М., Ковлер М.А., Крутикова - Львова Р.П. Лекарственные средства метаболической терапии на основе витаминов и ферментов (Обзор) // Вопросы мед. ХИМИИ. - 1992. - Т. 38. - N 4. - С. 14-21. Дурнев А.Д., Середенин С.В. Антиоксиданты как средства защиты генетического аппарата // Хим.-фарм. журн. - 1990. - N 2. - С. 92-100/. Таким образом, антиоксиданты, присутствующие в лекарственном или косметическом препарате, являются не только действующим началом этих средств, но могут значительно тормозить их окисление в процессе длительного хранения, способствуя сохранению в нативном состоянии легкоокисляемых биологически активных компонентов. Известны составы для стабилизации липидов к окислению различного происхождения путем введения антиоксидантов токоферолов /US №2564106, кл. 252-404, опубликованный 14.08.1951/, нафтолов и фенолов / Эмануэль Н.М., Лясковская Ю.Н. Торможение процессов окисления жиров. М.: Пищепромиздат, 1961. - 360 с. /.
В качестве прототипа выбран состав для стабилизации липидов к окислению с помощью введения токоферолов /Патент США №2564106, кл. 252-404, опубликованный 14.08.1951/. Указанный состав тормозит процесс окисления липидов за счет антиоксидантного действия ингибитора природного происхождения α-токоферола (6-гидрокси-2,5,7,8-тетраметил-2-фитил-хромана, витамина Е). Известно, что α-токоферол характеризуется чрезвычайно высокой константой скорости реакции с пероксильными радикалами k7=(3,3-3,5)×106 M-1×c-1 /Бурлакова Е.Б., Крашаков С.А., Храпова Н.Г. Кинетические особенности токоферолов как антиоксидантов. Черноголовка, 1992. - 56 с./.
Недостатком этого состава является сложный механизм действия α-токоферола в липидных субстратах, его участие не только в реакциях обрыва цепей, но и реакциях продолжения цепей, что приводит к снижению антиоксидантной активности α-токоферола и промотированию процесса окисления.
Предлагаемое соединение 2-гидрокси-1-(N-4′-гидроксифенил)бензкарбамид (осалмид, оксафенамид), производное салициловой кислоты и пара-аминофенола, применяется как желчегонное средство. Соединение проявляет активность с пероксильными радикалами с константой скорости реакции k7=6,86×104 M-1×c-1 и обладает дополнительно способностью непосредственно взаимодействовать с гидропероксидами, разрушая их без образования свободных радикалов, что не наблюдается в присутствии α-токоферола /Перевозкина М.Г. Кинетика и механизм ингибирующего действия производных фенозана, салициловой кислоты и их синергических смесей с α-токоферолом и фосфолипидами. Автореф. дис.… канд. хим. наук. Тюмень. - 2003. 28 с./. Разрушение гидропероксидов под влиянием 2-гидрокси-1-(N-4′-гидроксифенил)бензкарбамида, в свою очередь, является причиной выигрыша в периодах индукции. Для предлагаемого синтетического антиоксиданта имеет место положительная корреляционная связь между концентрацией и величиной ингибирующего эффекта, что не наблюдается для α-токоферола, указанная зависимость имеет экстремальный характер и при высоких концентрациях антиоксидантное действие α-токоферола сменяется на проантиоксидантное. Дополнительно 2-гидрокси-1-(N-4′-гидроксифенил)бензкарбамид обладает фотостабилизирующим действием, способен поглощать УФ-излучение в диапазоне 301-305 нм, опасным для развития рака кожи, что может использоваться в косметической промышленности /Поротов Л.Г., Сторожок Н.М., Перевозкина М.Г. Кинетические исследования антиоксидантного и фотостабилизирующего действия осалмида - нового амидного производного салициловой кислоты // Сб. докл. всерос. науч. конф. молодых ученых и II школа им. Академика Н.М. Эмануэля «Окисление, окислительный стресс, антиоксиданты». Москва. (1-3 июня). 2006. С. 131-133/.
Задачей заявляемого изобретения является разработать состав для стабилизации липидов к окислению с помощью антиоксиданта, обладающего высокой ингибирующей активностью и фотостабилизирующим действием в процессе окислительной деструкции природных липидов.
Технический результат - простой состав, не требующий больших материальных затрат, основанный на способности низкотоксичного антиоксиданта 2-гидрокси-1-(N-4′-гидроксифенил)бензкарбамида взаимодействовать с пероксильными радикалами и разрушать продукты окислительной деструкции липидов (гидропероксиды) нерадикальным путем, поглощать УФ-излучение в диапазоне 301-305 нм и обладать фотостабилизирующим действием.
Технический результат достигается тем, что к липидам добавляют в качестве антиоксиданта 2-гидрокси-1-(N-4′-гидроксифенил)бензкарбамид в количестве 0,01-0,14% от массы липидов.
Сущность изобретения заключается в использовании по новому назначению 2-гидрокси-1-(N-4′-гидроксифенил)бензкарбамида (осалмида, оксафенамида), химическая структура соединения представлена ниже
Антиоксидантную активность (АОА) тестировали волюмометрическим методом поглощения кислорода в модифицированной установке типа Варбурга при окислении этилолеата (ЭО) в присутствии водного раствора триметилцетиламмоний бромида (ЦТМАБ) в качестве поверхностно-активного вещества (ПАВ) в концентрации 1×10-3 Μ, с добавками водного раствора хлорида меди (II) в концентрации 2×10-3 Μ при t=(60±0,2)°С. Соотношение воды и липидов составляло 3:1, общий объем пробы 4 мл /Ушкалова В.Н., Перевозкина М.Г., Барышников Э.В. Разработка способа тестирования средств антиоксидантотерапии // В сб.: Свободно-радикальное окисление липидов в эксперименте и клинике. Тюмень, Из-во Тюм. ГУ. - 1997. - С. 77-82. Патент RU 2322658, опубл. 20.04.2008 г. Бюл. №11/.
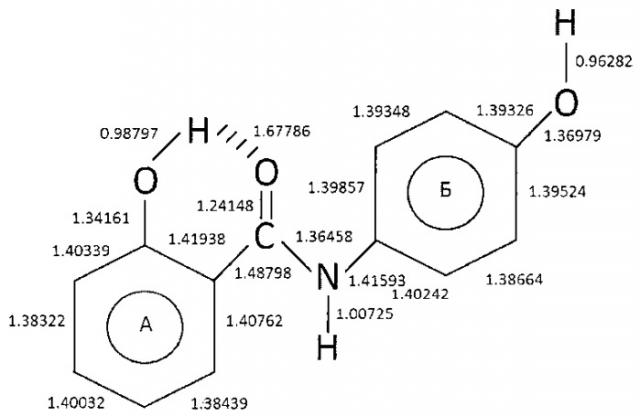
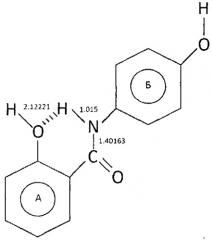
При помощи компьютерной программы Current Gaussian 09 Revision D.01 были рассчитаны длины связей между атомами в молекуле осалмида, возможность образования внутримолекулярной водородной связи (ВВС), дипольные моменты (µ) и энергии активации молекул (Еа). Показано, что длина связи О-Н в ароматическом кольце А соединения (0,98787×10-10 м) больше, чем длина связи О-Н в кольце Б (0,96282×10-10 м) (см. схему: Длины связей между атомами в молекуле осалмида). Наиболее активными О-Н группами в реакциях с пероксильными радикалами являются гидроксильные группы из кольца А. Длина ВВС между группами О-Н…О=С составляла (1,67786×10-10 м). Длина связи C-N в молекуле осалмида составляла (1,36458×10-10 м). Дипольный момент и энергия активации молекулы осалмида составляет 2,6778 D и - 782,6772869 кДж/моль соответственно. Показано, что осалмид не образует ВВС между группами Ν-Η…О-Н, по расчетам длина связи будет составлять 2,12221×10-10 м (см. схему), а дипольный момент µ=3,3548 D, поэтому существование такой молекулы не является оптимальным.
В качестве критериев оценки антиоксидантных свойств соединений использовали - периоды индукции, начальные и максимальные скорости окисления. Графическим методом определяли величину периода индукции (τi), представляющей собой отрезок оси абсцисс, отсекаемый перпендикуляром, опущенным из точки пересечения касательных, проведенных к кинетической кривой. Эффективность торможения процесса окисления липидного субстрата определяется совокупностью реакций ингибитора и обозначает его антиоксидантную активность, количественно определяемой по формуле АОА=τi-τS/τS, где τS и τi - периоды индукции окисления субстрата в отсутствие и в присутствии исследуемого антиоксиданта (АО) соответственно. Критерием антиоксидантного действия служили начальная (Wo2нач) и максимальная (Wo2max) скорости процесса окисления в присутствии и в отсутствии антиоксиданта. Скорость инициирования определяли уравнением Wi=f[InH]/τi, где f - стехиометрический коэффициент ингибирования, [InH] - концентрация реперного ингибитора, τi - период индукции.
Кинетику накопления гидропероксидов в модельном субстрате исследовали в условиях аутоокисления методом обратного йодометрического титрования в среде хлорбензола при t=(60±0,2)°C. Навеску окисляемого модельного субстрата растворяли в смеси ледяной уксусной кислоты и хлороформа в соотношении 3:2, добавляли насыщенный на холоде иодид калия, смесь перемешивали и оставляли в темноте. Через равные промежутки времени отбирали пробы и определяли в них перекисное число: ; где а - объем Na2S2O3, пошедший на титрование пробы; b - объем Na2S2O3, пошедший на титрование контрольного опыта; d - масса навески субстрата окисления.
Сущность изобретения иллюстрируется следующими примерами.
Пример 1
Берут 1 г (точная навеска) этилолеата (ЭО) и помещают в манометрическую ячейку, добавляют 2-гидрокси-1-(N-4′-гидроксифенил)бензкарбамид в количестве 0,03% от массы липидов, добавляют водный раствор хлорида меди (II) в концентрации в пробе 2×10-3 Μ, водный раствор цетилтриметиламмония бромида (ЦТМАБ) в концентрации в пробе 1×10-3 М, доводят водой до общего объема пробы 4 мл. Поглощение кислорода оценивают волюмометрическим методом в термостатированной установке типа Варбурга при температуре t=(60±0,2)°C при перемешивании на магнитной мешалке. Измеряют объем (мм3) поглощенного кислорода во времени, строят график в координатах dV/dt. Графическим методом из кинетических кривых определяют величину периода индукции (τi). Из наклона кинетических кривых определяют начальную (WO2нач2.) и максимальную (WO2мах) скорости окисления липидного субстрата в контрольном опыте и с добавками антиоксидантов. Показатели сравнивают с прототипом.
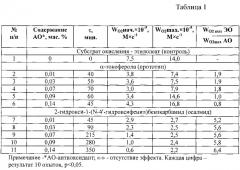
Кинетические параметры окисления этилолеата (ЭО) в водно-липидной среде в присутствии 2×10-3 Μ CuCl2 в зависимости от концентрации 2-гидрокси-1-(N-4′-гидроксифенил)бензкарбамида и α-токоферола (прототип), Wi=6,7×10-5 М×c-1, t=60°С.
Пример 2
Берут 10 г (точная навеска) линолевой кислоты (ЛК), добавляют 2-гидрокси-1-(N-4′-гидроксифенил)бензкарбамид в количестве 0,03% от массы липидов, перемешивают магнитной мешалкой в светонепроницаемой термостатированной ячейке при температуре t=(60±0,2)°C. Через равные промежутки времени отбирают пробы и определяют в них перекисное число (ПЧ).
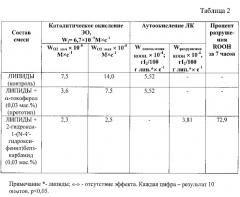
Величины начальной, максимальной скоростей поглощения кислорода при каталитическом окислении этилолеата (ЭО), разрушения гидропероксидов при аутоокислении линолевой кислоты (ЛК) в присутствии 2-гидрокси-1-(N-4′-гидроксифенил)бензкарбамида и α-токоферола (прототип), t=60°С.
Состав для стабилизации липидов к окислению, включающий антиоксидант, отличающийся тем, что в качестве антиоксиданта используют 2-гидрокси-1-(N-4′-гидроксифенил)бензкарбамид (осалмид, оксафенамид), добавляемый в количестве 0,01-0,14% от массы липидов.