Способ получения средства на основе гликозилированных полипептидов
Иллюстрации
Показать всеИзобретение относится к фармацевтической промышленности, а именно к способу получения средства на основе гликозилированных полипептидов, обладающего противовоспалительным действием. Способ получения средства на основе гликозилированных полипептидов из отходов переработки промысловых морских ежей Strongylocentrotus droebachiensis, обладающего противовоспалительным действием. Способ включает экстракцию внутренностей морских ежей этиловым спиртом, отделение экстракта на сепараторе или центрифуге, его упаривание, фильтрацию концентрата, гель-хроматографирование, отделение фракции с молекулярной массой 5,5-7,0 кДа и ее высушивание, при определенных условиях. Получаемое средство обладает выраженным противовоспалительным действием. Вышеописанный способ позволяет повысить чистоту гликозилированных полипептидов. 2 н. и 1 з.п. ф-лы, 4 табл., 1 ил., 4 пр.
Реферат
Изобретение относится к технологии переработки природных объектов и касается способа получения средства на основе гликозилированных полипептидов из отходов переработки промысловых морских ежей Strongylocentrotus droebachiensis.
Биологическое разнообразие Мирового океана представляет практически неограниченный источник для поиска новых биологически активных соединений. Вещества, выделенные из морских животных, водорослей и бактерий, обладают широким спектром биологической активности, включая антибактериальную, антикоагулянтную, противовоспалительную, антиаллергическую, противогрибковую, антитромбоцитарную, иммуномодулирующую, противоопухолевую, проапоптотическую и другие активности.
Морские беспозвоночные являются одним из перспективных объектов мирового промысла: на их долю приходится до 8,5% улова. Известно около 800 видов съедобных морских беспозвоночных, которые широко используются для приготовления пищевой, технической, кормовой продукции, а также в лечебно-профилактических целях [Справочник по химическому составу и технологическим свойствам водорослей, беспозвоночных и морских млекопитающих / под ред. В.П. Быкова. - М.: Изд-во ВНИРО, 1999. - 262 с.].
При экстракции тканей моллюсков выделяют уникальные компоненты, обладающие противоопухолевой активностью. Экстракт из двустворчатого моллюска мерценарии способен ингибировать рост злокачественных новообразований. Диализированный экстракт из тканей мерценарии в эксперименте in vitro подавлял рост саркомы 180 и саркомы Кребса [Пат. US 3655875, 11.04.1972].
Известен способ получения углевод-белкового комплекса, обладающего противоопухолевой и иммуностимулирующей активностью, получаемого из мантии приморского гребешка с использованием экстракции физраствором с последующим диализом и высушиванием [Пат. RU 2121844, опубл. 20.11.1998]. Известна биологически активная добавка к пище, представляющая собой гидролизат из отходов разделки морского гребешка.
Предложен также способ получения биологически активной добавки путем кислотного гидролиза отходов разделки морского гребешка. После гидролиза проводят нейтрализацию и упаривание массы. Затем осуществляют охлаждение и повторную нейтрализацию массы. Готовый гидролизат отделяют от осадка [Пат. RU 2192149 C1, опубл. 10.11.2002].
Морские ежи являются типичными представителями беспозвоночных и источником ряда интересных биологически активных веществ [Воробьев В.В. Создание биоактивных фармакологических субстанций и лекарственных средств из морских гидробионтов // Вестник биотехнол. - 2009. - Т.4, №1. - С.33-38].
По данным Y. Nishida et al. (2007) в органах пищеварительного тракта морского ежа содержится большое количество веществ белковой природы с широким диапазоном молекулярных масс, в том числе и низкими молекулярными массами в области 10 кДа [Nishida Y., Suzuki K., Kumagai Y. et al. Isolation and primary structure of a cellulase from the Japanese sea urchin Strongylocentrotus nudus // Biochimie. - 2007. - Vol.89, N8. - P.1002-1011].
Известен способ получения гликопептида, обладающего противовоспалительным действием, из ткани желудочно-кишечного тракта животных, включающий механическую очистку сырья, замораживание, измельчение, экстракцию раствором уксусной кислоты, фильтрацию, обработку фильтрата ацетоном, лиофилизацию полученного осадка, содержащего целевой продукт, растворение его в дистиллированной воде с последующей дополнительной очисткой [SU 1697315 A1, опубл. 10.04.1999].
Известен пептидный конъюгат, содержащий гликозилированный пептид, который ковалентно связан с фрагментом полиэтиленгликоля (ПЭГ) через интактную гликозильную связывающую группу. Изобретение обеспечивает получение нового химического соединения, содержащего разветвленную молекулу ПЭГ, сиалильную связывающую группу и пептид с пониженной антигенностью [RU 2460543 C2, опубл. 10.09.2012].
Известен способ получения биологически активных веществ гликопептидной природы путем обработки культуральной жидкости молочнокислых бактерий кислыми протеолитическими ферментами, последующее разделение центрифугированием культуральной жидкости на биомассу и молочную сыворотку, которые обрабатывают раздельно. Молочную сыворотку разделяют ультрафильтрацией на высокомолекулярную и низкомолекулярную фракции. Высокомолекулярную фракцию молочной сыворотки лиофилизируют. Низкомолекулярную фракцию молочной сыворотки выпаривают и получают молочную кислоту и ее соли. Биомассу суспендируют в аммиачной воде и разделяют центрифугированием на жидкую фазу и твердую. Жидкую фазу концентрируют ультрафильтрацией. К полученному концентрату добавляют раствор уксусно-кислого цинка с получением цинксодержащего комплекса. Твердую фазу (биомассу) для разрушения клеточных стенок подвергают обработке ультразвуком или обработке «замораживание-размораживание». Затем кипятят, охлаждают, добавляют лизоцим и гидролизуют. Гидролизат подкисляют уксусной кислотой и разделяют на твердую и жидкую фазы центрифугированием. Твердую фазу, полученную из гидролизата, высушивают и получают препарат, содержащий остатки клеточных стенок и нерастворенный гликопептид. Жидкую фазу, полученную из гидролизата, фракционируют ультрафильтрацией на высокомолекулярную фракцию и низкомолекулярную фракцию. Полученную высокомолекулярную фракцию лиофилизируют с получением препарата, содержащего лизоцим и высокомолекулярный гликопептид. Низкомолекулярную фракцию хроматографируют, фильтруют, упаривают и лиофилизируют с получением препарата [RU 2304167 C2, опубл. 10.08.2007].
Известный способ описывает получение продукта, содержащего гликопептиды из клеток молочно-кислых бактерий. Однако в ходе технологической обработки биомассу молочнокислых бактерий для разрушения клеточных стенок подвергают воздействию ультразвуком или обработке "замораживание-размораживание", кипячению и обработке лизоцимом, после чего из суспензии лизоцимного гидролизата отделяют водонерастворимые гликопептиды методами микро-, ультра-, нанофильтрации и хроматографией. Применение водонерастворимых гликопептидов ограничивает их применение и биодоступность. Кроме того требуется значительное количество вспомогательных веществ для растворения подобных соединений и повышения их биодоступности.
Известна биологически активная добавка к пище, представляющая спиртовой экстракт из внутренностей кукумарии японской, содержащая тритерпеновые гликозиды, гексозамины и минеральные вещества и обладающая антиоксидантной, иммуномодулирующей, цитостатической активностью [ТУ 9265-075-00472021-96].
Известен способ лабораторно-аналитического получения пептидов из морских ежей Echinus esculentus L. путем экстракции ацетоном, упаривания, разделения на комплекте из пяти патронов С18 Sep-Paks (Waters, Milford, MA, USA) последовательным элюированием 20%, 40%, 60% и 80% ацетонитрила (ACN) в 0,1% TFA. Далее 50 мкл образцов, полученных при элюировании 20%, 40%, 60% и 80% ACN в TFA, анализировали на наличие SALMFamide пептидов с использованием радиоиммуноанализа. Sep-Pak элюаты, содержащие SALMFamide пептиды, наносили на колонку С8 (Brownlee RP300, Perkin-Elmer, Boston, MA, USA; 2.1 mm × 220 mm) и элюировали методом ВЭЖХ смесью 0-80% ACN/TFA при скорости 0,5 мл/мин в течение 30 мин. Фракции на анализ SALMFamide-подобной иммунореактивности отбирали через каждые 0,5 мин [Elphick M.R., Thorndyke M.C. Molecular characterization of SALMFamide neuropeptides in sea urchins // J Exp Biol, 2005, Vol.208, P.4273-4282].
Однако известный способ является лабораторно-аналитическим. SALMFamide пептиды, обладающие иммунореактивностью, были выделены в виде фракций методом многостадийной ВЭЖХ с целью установления их генома. Получить данным способом пептиды в количестве, достаточном для подтверждения его активности, не предоставляется возможным.
Известен способ выделения fasciclin I-подобного белка с молекулярной массой 33 кДa из гонад морского ежа Strongylocentrotus intermedius с использованием гидрофобной хроматографии и гельфильтрации [Sato K., Nishi N., Nomizu M. Characterization of a fasciclin I-like protein with cell attachment activity from sea urchin Strongylocentrotus intermedius) ovaries // Arch Biochem Biophys, 2004, Vol.424(1), P.1-10].
Однако известный способ позволяет выделить негликозилированный белок с молекулярной массой 33 кДa из гонад морских ежей Strongylocentrotus intermedius, а не низкомолекулярный гликозилированный полипептид.
Наиболее близким к заявляемому способу по технической сущности является способ получения средства, содержащего 10-15% пептидов, 35-45% аминокислот, 4-8% фосфолипидов и микроэлементы и получаемого после отделения гонад из морских ежей, заключающийся в извлечении внутренностей, их экстракции этиловым спиртом в соотношении 1:1-3 при температуре от 0 до плюс 10°C в течение от 2 ч до 10 суток, отделении жидкой части с получением водно-спиртового экстракта, отгонке спирта, высушивании [Пат. RU 2481119 C1, опубл. 10.05.2013].
Недостатком данного способа является получение комплексного препарата, в состав которого входят как низкомолекулярные олигопептиды, аминокислоты и минеральные вещества, так и полипептиды. Кроме этого, в спиртовой экстракт переходит значительное количество соединений липидной природы, которые в процессе высушивания соосаждаются на поверхности, происходит процесс "залипания" полученного продукта и быстрое его окисление.
Задачей данного изобретения является получение средства на основе гликозилированного полипептида с сохранением его нативных свойств, увеличение чистоты и стабильности конечного продукта.
Эта задача решена тем, что в известном способе, включающем извлечение внутренностей морских ежей, их экстракцию этиловым спиртом в соотношении 1:1-3 при температуре от 0 до плюс 10°С в течение от 2 ч до 10 суток, отделение жидкой части с получением водно-спиртового экстракта, отгонку спирта, высушивание сырья, согласно изобретению свежие, замороженные или сушеные внутренности морских ежей, заливают этиловым спиртом при соотношении сырье:экстрагент 1:1-1:3, суспензию инкубируют при температуре от 0 до плюс 10°C в течение от 2 ч до 10 суток, осадок отделяют на сепараторе или центрифуге, упаривают экстракт до 1/50-1/70 объема, концентрат пропускают через фильтр с размером пор 1 кДa, подвергают гель-хроматографии, отделяют фракцию с молекулярной массой 5,5-7,0 кДа, отделенную фракцию, содержащую гликозилированный полипептид, высушивают.
Технический результат, обеспечиваемый изобретением, заключается в повышении степени очистки гликозилированного полипептида.
Отличительными признаками в способе-прототипе и заявляемом способе являются:
- концентрирование по молекулярной массе и отсечение соединений с молекулярной массой менее 5,5 кДа и более 7,0 кДа;
- фракционирование и выделение гликозилированного полипептида с использованием гель-хроматографии.
Использование совокупности этих отличительных признаков позволяет повысить чистоту целевого продукта, поскольку при концентрировании с использованием мембран с пределом 1 кДа позволяет избавиться от микроэлементов, аминокислот и олигопептидов. Дальнейшее фракционирование методом гель-фильтрации позволяет получить гликозилированный полипептид высокой степени чистоты.
Изобретение иллюстрируется следующими примерами.
Пример 1.
К 1 кг внутренностей морских ежей добавляют 2,5 л 95% спирта этилового, экстрагируют при 5°C в течение 7 суток, фильтруют. Полученную жидкую часть концентрируют до 1/50 первоначального объема на вакуумном испарителе и далее концентрат для удаления микроэлементов, аминокислот, олигопептидов фильтруют на фильтре типа Amicon Ultra-15 1K - 1000 NMWL размером пор 1 кДа до конечной концентрации 1 мг/мл. Концентрацию пептидов определяют по методике Варбурга и Кристиана, основанной на измерении оптических плотностей раствора при длинах волн 280 нм и 260 нм и дальнейшем вычислении концентрации пептидов. После стадии концентрирования полученный экстракт очищают от других примесей методом гель-хроматографии, используя Sephadex молекулярные сита. Полученную жидкую часть высушивают. В результате получают около 0,55 г сухого очищенного средства на основе гликозилированных полипептидов с молекулярной массой 5,5-7,0 кДа.
Содержание в нем галактозы 30-35%, фукозы 1,4-1,6%, степень сульфатирования 0,90-0,10%.
Пример 2. Определение гликозилированных полипептидов с помощью ВЭЖХ анализа на колонке с обращенной фазой.
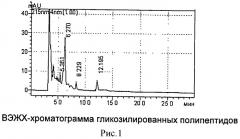
Средство на основе гликозилированного полипептида анализируют методом ВЭЖХ на колонке Jupiter C18 300A, размер частиц 5 мкм, 4,6×250 мм в изократическом режиме элюирования с использованием 3% ацетонитрила: 97% 0,03% раствор трифторуксусной кислоты (ТФУ). Детектирование при длине волны 215 нм (Рис.1).
По результатам количественной оценки методом внутренней нормализации доминирующим является компонент со временем удерживания около 6,27 мин. Его содержание около 80,0%.
Пример 3. Противовоспалительное действие на экспериментальной модели острого бронхита у крыс.
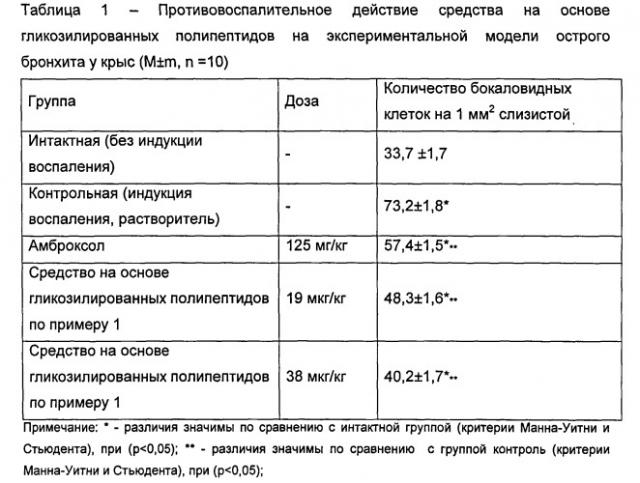
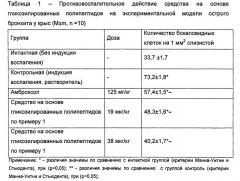
Острый бронхит моделировали введением формалина в носовые ходы крыс [Руководство по проведению доклинических исследований лекарственных средств под ред. Миронова А.Н. - Часть первая. - М.: Гриф и К, 2012. - 944 с.]. Индукцию острого воспаления вызывали введением эндотрахеально 1% раствора формалина крысам в 1-й день исследования. Средство на основе гликозилированных полипептидов и препарат сравнения амброксол (Амбробене, раствор для приема внутрь и ингаляций, Ratiopharm GmbH, Германия) вводили ингаляционно в течение 7 дней после индукции патологии. Растворителем служила вода для инъекций. Эффективность препаратов оценивали по выраженности гистологических изменений ткани легкого (Таблица 1).
При гистологической оценки ткани легкого было установлено, что средство по примеру 1 в дозах 19 и 38 мкг/кг обладает выраженным противовоспалительным эффектом, что выражалось снижением инфильтрации слизистой и подслизистой оболочек бронхов, а также значимым уменьшением на 34 и 45% количества бокаловидных клеток по сравнению с контрольной группой. У большинства животных, получавших средство на основе гликозилированного полипептида по примеру 1 в дозах 19 и 38 мкг/кг, выявили наиболее легкий вариант патологии - поствоспалительную гиперплазию бокаловидных клеток. Эффективность применения средства по примеру 1 в обоих дозах была сопоставима с эффективностью препарата сравнения амброксолом.
Пример 4. Противовоспалительное действие на модели хронической обструктивной болезни легких у крыс.
Хроническую обструктивную болезнь легких (ХОБЛ) моделировали ежедневным окуриванием крыс табачным дымом в резервуарах курительной машины в течение 28 дней [Groneberg D.A., Fan Chung K. Models of chronic obstructive pulmonary disease // Respir Res. 2004; 5(1): 18]. Индукцию хронического воспаления вызывали путем ежедневного помещения в течение 6 часов животных в резервуар курительной машины, где создавали концентрации никотина 28 мг/кг и смолы 357,6 мг/кг. Были исследованы группы: интактная - без патологии, без лечения; контрольная - с патологией, без лечения; группа, получающая препарат сравнения амброксол на фоне патологии; 3 группы, получающие средство на основе гликозилированных полипептидов по примеру 1, в 3-х дозах на фоне патологии. Препараты вводили ежедневно ингаляционно с 14 по 28 день исследования. Оценку эффективности препаратов проводили по степени изменения антиоксидантного статуса (восстановленный глутатион, малоновый диальегид (МДА) плазмы крови) (Таблица 2), изменению количества лейкоцитов в бронхоальвеолярном лаваже (таблица 3) и выраженности гистологических изменений ткани легкого (Таблица 4).
Применение средства на основе гликозилированных полипептидов по примеру 1 на фоне ХОБЛ защищало бронхи от негативного воздействия табачного дыма, снижало степень выраженности воспаления и оказывало антиоксидантное действие. На фоне применения средства по примеру 1 на 28 день развития патологии у животных отмечалось увеличение концентрации восстановленного глутатиона на 43-44% и снижение уровня МДА на 34-45% относительно контрольной группы.
На фоне развившейся патологии наблюдали статистически значимое увеличение количества лейкоцитов в бронхоальвеолярном лаваже в 2 раза по сравнению с интактной группой. Применение средства на основе гликозилированного полипептида в 3-х дозах, также как и препарата сравнения в течение 14 дней приводило к снижению количества лейкоцитов.
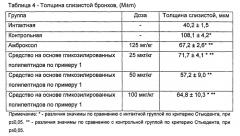
При оценке степени выраженности воспалительных изменений ткани легких было установлено (Таблица 4), что применение средства по примеру 1 приводило к выраженному уменьшению процессов инфильтрации слизистой и подслизистой оболочек, полному отсутствию экссудата в просвете бронхов или снижению количества экссудата, содержащего единичные макрофаги. Таблица 4 - Толщина слизистой бронхов, (M±m)
При гистологическом исследовании было выявлено снижение толщины слизистой бронхов в группе, получавшей средство по примеру 1, на 34-47% относительно контрольной группы животных, что свидетельствует о выраженном уменьшении воспалительной гиперплазии эпителия бронхов. Все эффекты средства на основе гликозилированного полипептида по примеру 1 были сопоставимы с препаратом сравнения амброксолом.
1. Способ получения средства на основе гликозилированных полипептидов, обладающего противовоспалительным действием, включающий экстракцию внутренностей морских ежей Strongylocentrotus droebachiensis этиловым спиртом при соотношении сырье:экстрагент 1:1-1:3 при температуре от 0 до плюс 10°C в течение от 2 ч до 10 суток, отделение экстракта на сепараторе или центрифуге, его упаривание до 1/50-1/70 объема, фильтрацию концентрата через фильтр с размером пор 1 кДа для удаления микроэлементов, аминокислот, олигопептидов, гель-хроматографирование концентрата, отделение фракции с молекулярной массой 5,5-7,0 кДа и ее высушивание.
2. Способ по п.1, отличающийся тем, что используют свежие, замороженные или сушеные внутренности морских ежей.
3. Средство на основе гликозилированных полипептидов, полученное способом по п.1, обладающее противовоспалительным действием.