Биоактивное гидрогелевое раневое покрытие
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к хирургии. Описано биоактивное раневое покрытие на основе гидрогелевого нанокомпозита, которое содержит антимикробный и антиоксидантный компоненты: модифицированный серебром монтмориллонит и фуллеренол, направленные на оптимизацию течения раневого процесса, профилактику развития и подавление раневой инфекции. Раневое покрытие может быть использовано для лечения огнестрельных ран, ран при тяжелой механической травме, неинфицированных и инфицированных ран, в том числе гнойных и длительно незаживающих, гранулирующих ран после глубоких термических, химических и лучевых ожогов, в комплексном лечении трофических язв и пролежней в стационарных, амбулаторных и полевых условиях. Раневое покрытие эластично, не фрагментируется при выполнении перевязок, что облегчает уход за раной. Высокая сорбционная способность матрицы раневого покрытия, в том числе по отношению к крупномолекулярным компонентам раневого экссудата, обеспечивает быструю элиминацию раневого ложа. Использование гидрогелевого, т.е. обладающего высокой степенью гидратации, раневого покрытия соответствует современному принципу ведения раны во влажной среде и обеспечивает оптимальные условия для ранней активации репаративных процессов. 5 ил., 2 табл., 4 пр.
Реферат
Изобретение относится к медицине, а именно к хирургии, предназначено для местного лечения ран в воспалительной фазе раневого процесса. Биоактивное раневое покрытие на основе гидрогелевого нанокомпозита содержит комплекс биоактивных препаратов для оптимизации течения раневого процесса, профилактики развития и подавления раневой инфекции. Раневое покрытие может быть использовано для лечения огнестрельных ран, ран при тяжелой механической травме, неинфицированных и инфицированных ран, в том числе гнойных и длительно незаживающих, гранулирующих ран после глубоких термических, химических и лучевых ожогов, в комплексном лечении трофических язв и пролежней в стационарных, амбулаторных и полевых условиях.
Известны отечественные покрытия на основе альгината натрия, являющегося гидрогелем природного происхождения: «Колетекс-гель-ДНК», содержащие деринат (дезоксирибонуклеат натрия), а также «Колетекс-гель-ДНК-Л» - деринат и лидокаин. Рекомендовано применять указанные покрытия для профилактики и лечения лучевых реакций и повреждений слизистых оболочек (полости рта и ротоглотки, мочевого пузыря, прямой кишки, влагалища и т.д.) в процессе и/или после проведения лучевой терапии, а также для лечения длительно незаживающих ран и трофических язв, бытовых ожогов [патент РФ 2483755, ООО «Колетекс», 2006]. Однако слабая ранозаживляющая активность и отсутствие антимикробного действия значительно снижают возможность широкого применения данных гидрогелей в медицинской практике.
Известно перевязочное средство, содержащее полимерную пленку с нанесенным на ее поверхность слоем полимерного гидрогеля. Пленка выполнена из биосовместимого оптически прозрачного полимера со сквозными отверстиями диаметром D=0,01-3,0 мкм и плотностью N=(103=109)1/см2, а в качестве полимерного гидрогеля нанесен гидрогель на основе хитозана. Перевязочное средство препятствует проникновению к ране микроорганизмов, обеспечивает бактериостатическое действие в ране, позволяет визуально следить за процессами, протекающими в ране, и удобно прикрепляется к раневой поверхности [патент РФ 2270646, ООО «Фолиум», 2006].
Общими недостатками представленных покрытий являются относительно низкая сорбционная емкость, значительное снижение прочности матрицы при набухании, отсутствие поглощающей способности по отношению к крупномолекулярным компонентам раневого экссудата и микрофлоре.
Наиболее близким к заявленному изобретению являются синтетические гидрогелевые покрытия торговой марки «АППОЛО-ПАК-АМ», «АППОЛО-ПАК-АИ», созданные на основе сополимера акриламида и акриловой кислоты с включением антисептиков мирамистина или йодовидона и местного анестетика анилокаина. Гидрогели также обладают незначительной сорбционной способностью 2-3 г/г. Покрытия содержат антимикробный и обезболивающий препараты, но не содержат антиоксидантных средств, что значительно снижает их эффективность при выраженном воспалительном процессе [ТУ 9393-002-42965160-2009, ООО «ТД «АППОЛО», 2009; http://www.appolo.ru/products/gidrogelevaya-produktsiya/povyazka-ranozazhivlyayushchaya-appolo.html#документы]. Существенным конструктивным недостатком этих гелей является то, что значительная часть геля, при вскрытии упаковки, остается на внутренней поверхности (более 50%), а не переносится на рану с сеткой-носителем. Указанные раневые покрытия имеют низкие показатели pH в пределах 5,5-6,0, что в условиях местного тканевого ацидоза также снижает их эффективность.
Таким образом, необходимость разработки способов иммобилизации биоактивных компонентов в матрицу-носитель на основе гидрогелей различной химической природы, обеспечивающих пролонгированный выход последних в раневое ложе, при сохранении их высокой сорбционной способности и механической прочности, остается актуальной.
Технической задачей и положительным результатом настоящего изобретения является получение биоактивного гидрогелевого раневого покрытия, содержащего патогенетически обоснованный комплекс лечебных препаратов, местное применение которого позволит оптимизировать течение раневого процесса, сократить сроки заживления, предотвратить развитие осложнений.
Указанная задача решена с помощью создания на основе гидрогелевого нанокомпозита раневого покрытия, содержащего биоактивные компоненты: антимикробный - модифицированный серебром монтмориллонит (Ag-MMT) и антиоксидантный - фуллеренол.
Поставленная задача и технический (социальный) результат достигаются за счет того, что биоактивное гидрогелевое раневое покрытие содержит в своей основе сополимер акриловой кислоты и акриламида, при этом в состав сополимера включен наполнитель-модификатор модифицированный серебром монтмориллонит, позволяющий получать гидрогелевый нанокомпозит с интеркалированной структурой, обладающий антимикробным действием, иммобилизация в сополимер на этапе синтеза фуллеренола придает покрытию антиоксидантное действие.
Биоактивное гидрогелевое раневое покрытие характеризуется тем, что для получения однородной структуры полимерной матрицы раневого покрытия и обеспечения оптимального, дозированного и пролонгированного, антимикробного действия используют высокодисперсную фракцию модифицированного серебром монтмориллонита с диаметром частиц менее 0,25 мм.
Биоактивное гидрогелевое раневое покрытие характеризуется также тем, что концентрация биоактивных компонентов в матрице составляет, масс.%:
| модифицированный серебром монтмориллонит | 2,0-5,0 |
| фуллеренол | 1,0-2,0 |
Это раневое покрытие обладает высокой степенью гидратации, соответствует современным требованиям ведения раны и обеспечивает оптимальные условия для более ранней активации репаративных процессов, сводя к минимуму воспалительную фазу участка повреждения. Это позволяет осуществить более раннее восстановление жизнедеятельности поврежденного органа.
Гидрогелевые матрицы раневых покрытий синтезировали путем взаимодействия нейтрализованной акриловой кислоты (АК) и акриламида (АА) с N,N′-метилен-бис-акриламидом (МБАА) в качестве сшивающего агента в присутствии окислительно-восстановительной системы «персульфат аммония - тетраметилэтилендиамин (ТМЭД)». Предварительно очищенную акриловую кислоту растворяли в воде в концентрации 30 мас.%. Ее нейтрализацию проводили раствором бикарбоната натрия (NaHCO3) под контролем pH-метрии. Предварительно рассчитанный объем раствора NaHCO3 постепенно добавляли до установления показателя pH смеси в пределах 7,0-7,5. Реакция нейтрализации сопровождается выделением большого количества углекислого газа, поэтому после ее завершения смесь выдерживали в течение 5-10 минут. Затем в смесь добавляли расчетное количество АА, МБАА, ТМЭД и воды. Смесь тщательно перемешивали до полного растворения всех компонентов с последующим повторным контролем показателя pH. После этого смесь охлаждали до температуры 5-10°C с целью предотвращения спонтанной полимеризации. После охлаждения в смесь вводили расчетное количество персульфата аммония, тщательно перемешивали и заливали в химически чистую форму.
Введение биоактивных наполнителей - водного раствора фуллеренола и модифицированного серебром монтмориллонита - проводили на этапе синтеза гидрогелевого полимера, добиваясь равномерного раскрытия слоистых структур и распределения монтмориллонита в полимере использованием ультразвукового диспергатора. Таким образом, получали биоактивные раневые покрытия, представляющие собой нанокомпозиты с интеркалированной структурой вследствие внедрения цепей акриламидного полимера в межпакетное пространство частиц монтмориллонита.
Разработка и практическое применение гидрогелевых раневых покрытий особенно актуальна в свете современного принципа ведения раны во влажной среде. Высокая степень влагосодержания гидрогелей способствует размягчению некротических образований за счет регидратации тканей, что облегчает их механическое удаление. Создание в ране влажной среды обеспечивает оптимальные для заживления раны условия и, как следствие, способствует ускорению процессов гранулирования и эпителизации. Гидрогелевые полимеры являются пластичными и хорошо моделируются на ранах со сложным рельефом, не обладают адгезией даже при длительном нахождении на раневой поверхности и легко удаляются без риска ее травматизации. При этом значительная сорбционная способность гидрогелей способствует элиминации раневой поверхности от некротизированных тканей, микробных клеток, избытков раневого отделяемого.
Известно, что фуллеренол наряду с другими водорастворимыми кластерами фуллерена C60 (C60/ПВП и C60/Tween 80) проявляет антиоксидантные свойства при концентрации 0,01%. Применение водного раствора фуллеренола при раневом процессе будет способствовать стабилизации собственной системы антиоксидантной защиты, тормозить развитие свободнорадикального перекисного окисления липидов, клеточных и капиллярных мембран, предотвращая повреждение клеток и тканей, ограничивая распространение воспалительных изменений и вторичного некроза тканей, а за счет усиления фагоцитарной активности макрофагов способствовать повышению неспецифического иммунитета. Парентеральное введение фуллеренола не проявляет острой токсичности, не влияет на морфофункциональное состояние внутренних органов, метаболизм и не вызывает патологической реакции системы кроветворения.
Известно, что серебро обладает широким спектром антибактериального действия, воздействует также на рост дрожжей, плесневых грибов. Свидетельства о выявлении резистентных к серебру микроорганизмов имеют спорадический характер, что особенно актуально на фоне возросшей устойчивости к другим традиционным антисептикам. Наиболее перспективным для иммобилизации на раневые покрытия являются наноразмерные частицы серебра (AgNPs - ArgentumNanoParticles), обеспечивающие дозированный и пролонгированный антимикробный эффект. Ограниченное межслоевое пространство монтмориллонита, являясь специфическим «нанореактором», может быть использовано для выращивания и доставки наноразмерных частиц серебра.
Доклинические испытания, а именно эффективность местного применения сетчатого биоактивного раневого покрытия, устанавливали экспериментальным путем на животных (крысах-самцах линии Wistar).
Примеры доклинических испытаний
Пример 1. Биосовместимость раневого покрытия изучена на модели кожно-плоскостных условно асептических ран у 20 крыс. В послеоперационном периоде клинических признаков воспалительно-дегенеративных изменений в ране не отмечено. По данным гистоморфологического исследования на 7 сутки установлена классическая картина неосложненного регенеративного процесса, что позволило сделать вывод о биосовместимости и биоинертности раневого покрытия.
Пример 2. Для определения способности раневого покрытия подавлять рост бактериальной флоры на границе контакта с раневой поверхностью установлены показатели их бактериостатического действия, а также минимальная ингибирующая концентрация (МИК) Ag-MMT в их составе.
Значения МИК Ag-MMT в составе матриц раневых покрытий на основе ДЦСХ, воздействующей на референтные и госпитальные штаммы микроорганизмов, установили на уровне 0,1 масс.% и 0,2 масс.%. соответственно.
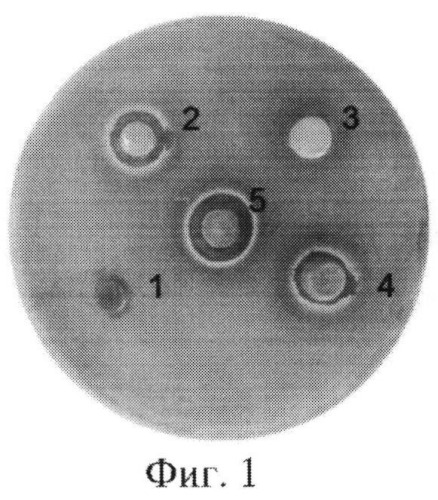
Результаты испытаний приведены в таблице 1 и на фиг.1 - P.aeruginosa, фиг.2 - E.coli, фиг.3 - MRSA (концентрация Ag-MMT в полимере, масс.%: 1-1%, 2-2%, 3-3%, 4-5%, 5-10%).
| Таблица 1 | ||||||
| Оценка бактериостатического действия раневых покрытий по зонам задержки роста микроорганизмов, мм | ||||||
| Содержание Ag-MMT, масс.%Штаммы микроорганизмов | 1 | 2 | 3 | 5 | 10 | |
| Референтные | E.coli | 3,2±1,3 | 10,4±3,32 | 30,7±2,04 | 34,3±2,87 | 36,8±3,11 |
| S.aureus | 0 | 2,4±0,56 | 8,6±2,73 | 15,7±2,64 | 27,6±3,15 | |
| P.aeruginosa | 2,2±0,65 | 8,3±1,16 | 27,5±3,22 | 31±2,65 | 32,8±2,81 | |
| Ассоциация | 0 | 5,46±1,71 | 17,4±2,57 | 25,3±2,46 | 31,4±3,4 | |
| Госпитальные | K.pneumoniae | 3,6±1,06 | 12,6±1,55 | 18,46±2,3 | 20,33±3,48 | 24,1±3,01 |
| P.aeruginosa | 0 | 2,4+1,08 | 7,4+1,65 | 15,45±2,53 | 21,3±2,75 | |
| MRSA | 0 | 0,26±0,05 | 3,76±1,45 | 12,6±1,54 | 18,89±2,55 |
Пример 3. По результатам оценки способности разработанного покрытия подавлять рост раневой микрофлоры установлено значимое снижение уровня бактериальной обсемененности инфицированных ран, а также возможность сравнительно длительного его поддержания ниже критического уровня (103 КОЕ) за счет пролонгированного антимикробного действия. Эффективное подавление раневой инфекции, являющейся ведущим патогенетическим звеном осложненного течения раневого процесса, должно способствовать сокращению сроков заживления ран (фиг.4 - биоактивное гидрогелевое раневое покрытие, фиг.5 - асептическая марлевая повязка).
Иммобилизация Ag-MMT в качестве антимикробного компонента биоактивного раневого покрытия на основе гидрогелевого нанокомпозита в минимальной концентрации 2 мас.% позволяет получать значимый бактериостатический эффект in vitro и поддерживать уровень бактериального обсеменения раны ниже 103 (КОЕ) на протяжении 5-7 суток in vivo.
Пример 4. По данным планиметрического исследования, представленным в таблице 2, установлено, что местное применение биоактивного гидрогелевого раневого покрытия предупреждает осложненное течение раневого процесса, позволяет сократить сроки заживления ран при лечении гранулирующих ран после глубоких ожогов и инфицированных кожно-плоскостных ран на 15-20%.
| Таблица 2 | ||||||||
| Показатели планиметрического исследования заживления ран, % | ||||||||
| Опытные группыСрок наблюдения | Гранулирующие раны после глубоких ожогов | Инфицированные кожно-плоскостные раны | ||||||
| Контроль | Опыт | Контроль | Опыт | |||||
| 1 | 2 | 1 | 2 | 1 | 2 | 1 | 2 | |
| 5 сутки | 20,8±1,1 | 4,2±0,2 | 27,4±0,8* | 5,5±0,1* | 29,4±1,4* | 5,8±0,4* | 43,4±0,2* | 8,7±0,3* |
| 10 сутки | 42,3±2,1 | 4,2±0,1 | 63,2±1,3* | 6,3±0,3* | 58,2±0,4* | 5,8±0,6* | 89,5±2,1* | 8,9±0,5* |
| 15 сутки | 68,1±1,3 | 4,5±0,3 | 98,7±0,6* | 6,6±0,6* | 95,3±0,3* | 6,3±0,3* | - | - |
| 20 сутки | 99,3±0,3 | 4,9±0,2 | - | - | - | - | - | - |
| Срок заживления | 20,0±0,4 | 15,8±0,7* | 16,0±0,4 | 13,4±0,3* | ||||
| Примечание к таблице 2: | ||||||||
| 1 - уменьшение площади раневой поверхности в процентном отношении к начальным размерам раны; | ||||||||
| 2 - скорость заживления (%/день). | ||||||||
| * Различия с контролем достоверны при p<0,05. |
Биоактивное гидрогелевое раневое покрытие, содержащее в своей основе сополимер акриловой кислоты и акриламида, отличающееся тем, что на этапе синтеза в состав сополимера включены два компонента: модифицированный серебром монтмориллонит в виде высокодисперсной фракции с диаметром частиц менее 0,25 мм в концентрации 2,0-5,0 мас.%, позволяющий получать в качестве полимерной матрицы покрытия гидрогелевый нанокомпозит с однородной интеркалированной структурой, придающий покрытию дозированное и пролонгированное антимикробное действие; и фуллеренол в концентрации 1,0-2,0 мас.%, придающий покрытию антиоксидантное действие.