Способ оценки антиагрегантной функции эндотелия
Иллюстрации
Показать всеИзобретение относится к медицине и может быть применено в практическом здравоохранении для повышения точности диагностики и снижения риска тромботических, геморрагических и тромбоэмболических осложнений. В исследуемых объемах крови до и после локальной гипоксии определяют интенсивность контактной коагуляции (ИКК), далее определяют время от начала исследования (t0) до достижения максимального снижения амплитуды вязкоупругих свойств крови (t1) после локальной гипоксии и при уменьшении значения ИКК на 30% и более и одновременном увеличении значения t1 на 30% и более антиагрегантную функцию эндотелия оценивают как нормальную, а при возрастании ИКК или отсутствии ее изменений и одновременном увеличении значения t1 менее чем на 30% или отсутствии увеличения t1 антиагрегантную функцию эндотелия оценивают как сниженную. Применение предлагаемого способа позволяет повысить точность диагностики антиагрегантной функции эндотелия за счет уменьшения механического воздействия на форменные элементы крови, сократить время и стоимость исследования. 5 ил., 1 табл., 4 пр.
Реферат
Изобретение относится к медицине, конкретно к способам диагностики эндотелиальной дисфункции.
Под эндотелиальной дисфункцией понимается дисбаланс медиаторов, обеспечивающих в норме оптимальное течение всех эндотелий-зависимых процессов [1]. Эндотелиальная дисфункция приводит к преобладанию вазоконстрикции, пролиферативных процессов, тромбогенного потенциала, снижению тромборезистентности сосудистой стенки [2, 3].
Очевидно, что генерализованная реакция эндотелия при его дисфункции, в отличие от апо-/паракринной при физиологических условиях, формирует существенные предпосылки для развития «Вирховской триады», инициирующей широкий спектр тромботических, геморрагических и тромбоэмболических осложнений в различных участках сосудистого русла [4].
Известные способы диагностики эндотелиальной дисфункции основаны на определении эндотелиальных маркеров, среди множества которых важнейшими являются повышенные уровни: PAI-I, оксида азота, простагландина 12, протеинов S и С, антитромбина III, т.е. факторов, напрямую принимающих участие в функции гемостаза [5, 6]. Такая диагностика эндотелиальной дисфункции в отношении получения информации о результирующей функции системы - гемостатическом потенциале - интегративной активности сосудисто-тромбоцитарного, коагуляционного, противосвертывающего и фибринолитического звеньев системы гемостаза, определяющих во временном срезе реологические свойства крови и возможность ограничения экстравазации ее клеточного и жидкостного компонентов при ее повреждении, фрагментарна и априори не позволяет отразить все нюансы изменений гемостаза [7].
Кроме того, для осуществления большинства способов диагностики эндотелиальной дисфункции требуется наличие лаборатории, оборудованной необходимым оборудованием, соответствующих реактивов и специально обученного персонала. Развернутое же исследование достаточно громоздко и трудоемко, требует больших количеств крови обследуемого, недостаточно оперативно и носит преимущественно исследовательский, а не прикладной характер [8, 9]. С этой точки зрения стремление к более экономному, целенаправленному и оперативному исследованию эндотелиальной дисфункции вполне понятно и оправданно.
Известен способ диагностики состояния эндотелия по данным исследования маркеров эндотелиальной дисфункции с использованием пробы с постокклюзионной вазодилатацией плечевой артерии. Больным определяли показатели, отражающие функциональное состояние эндотелия сосудов: количество десквамированных эндотелиоцитов (ДЭ) в крови. Также определяли концентрацию фактора Виллебранда методом иммуноферментного анализа с использованием моноклональных антител, уровень фибриногена плазмы крови - гравиметрическим методом. С целью оценки функции эндотелия всем больным была выполнена проба с постокклюзионной вазодилатацией (ПОВД) плечевой артерии (ПА). Признаком выраженной дисфункции эндотелия считали сужение диаметра ПА [10].
Данный способ является наиболее близким к предлагаемому по технической сущности и достигаемому результату и выбран в качестве прототипа.
Однако данный способ диагностики имеет ряд недостатков: данная методика достаточно трудоемкая, занимает значительное количество времени, а также немаловажную роль играет субъективность оценки регистрируемых изменений, не позволяющая судить, в общем, об эндотелиальной дисфункции на начальном этапе гемокоагуляции и сопровождающаяся травматизацией форменных элементов.
Задачей изобретения является повышение точности исследования эндотелиальной дисфункции у больных путем регистрации в режиме реального времени нарушений начального этапа гемокоагуляции в исследуемых микрообъемах крови без травматизации форменных элементов крови за счет уменьшения механического воздействия на них.
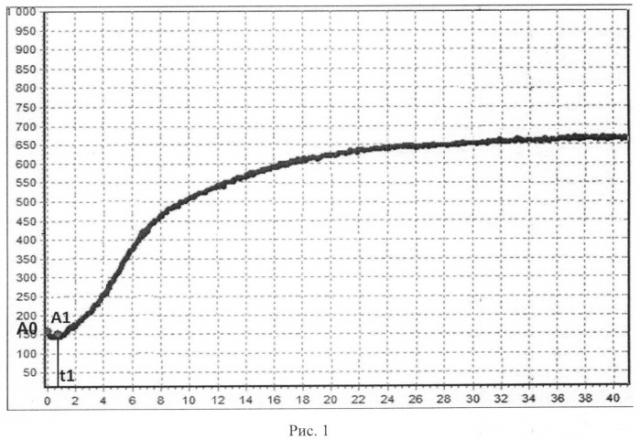
Поставленная задача решается путем регистрации в режиме реального времени нарушений начального этапа гемокоагуляции в исследуемых объемах крови, для чего до и после локальной гипоксии определяют интенсивность контактной коагуляции (ИКК) - частного от деления разницы амплитуд начального значения вязкоупругих свойств крови в точке t0 (А0) и максимального ее снижения за время t1 (A1) на временной интервал t1 (ИКК=А0-А1/t1) (рис.1), далее определяют динамику времени от начала исследования t0 до достижения максимального снижения амплитуды вязкоупругих свойств крови t1 на графиках до и после локальной гипоксии, и при увеличении значения t1 на 30% и более и одновременном уменьшении значения ИКК на 30% и более антиагрегантную функцию эндотелия оценивают как нормальную; при увеличении значения t1 менее чем на 30% или при отсутствии увеличения t1, а также при возрастании ИКК или отсутствии изменений ИКК антиагрегантную функцию эндотелия оценивают как сниженную.
Новым в предлагаемом способе является оценка антиагрегантной функции эндотелия по величинам значений ИКК и t1 и при увеличении значения t1 после локальной гипоксии на 30% и более и одновременном уменьшении значения ИКК на 30% и более антиагрегантную функцию эндотелия оценивают как нормальную; при увеличении значения t1 менее чем на 30% или при отсутствии увеличения t1, а также при возрастании ИКК или отсутствии изменений ИКК антиагрегантную функцию эндотелия оценивают как сниженную.
Оценка гемостатического потенциала цельной крови в режиме «point-of-care test» позволяет оценить всю совокупность взаимодействия элементов системы регуляции агрегатного состояния крови в условиях влияния не избегаемого стрессора - стандартизированной контактной активации. Действительно, проба цельной крови, содержащая аликвоты продуцентов эндотелия (ряд из которых реализуют эффекты в ограниченном временно интервале от 1 до 30 с), форменные элементы крови и плазменные факторы гемостаза, используемая для оперативного анализа, позволяет получать объективную информацию о «временном срезе» состояния гемостатического потенциала и состоятельности функции эндотелия. В связи с этим системный характер эндотелиальной дисфункции должен вызывать реакцию гемостатического потенциала на всех этапах формирования поперечно сшитого фибрина, а для оценки гемостатического потенциала должен использоваться чувствительный «глобальный» тест и обязательно в режиме «point-of-care test».
Техническим результатом предлагаемого изобретения является повышение точности за счет уменьшения механического воздействия на форменные элементы крови, сокращение времени исследования, невысокая стоимость исследования. Немаловажную роль играет невысокая стоимость расходных материалов и самого исследования, для которого не нужно большого количества крови обследуемого. Также предлагаемый способ достаточно прост в выполнении и не требует наличия специальной лаборатории.
Существенные признаки предлагаемого изобретения проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области, и неочевидны для специалиста. Идентичной совокупности признаков не обнаружено в исследованной патентной и научно-медицинской литературе. Предлагаемый способ может быть применен в практическом здравоохранении для точной постановки диагноза.
Исходя из вышеизложенного, следует считать предлагаемое изобретение соответствующим условиям патентоспособности «новизна», «изобретательский уровень», «промышленная применимость».
Изобретение будет понятно из следующего описания и приложенных к нему рисунков:
На рис.1 показан алгоритм определения и расчета интенсивности контактной коагуляции: А0 - начальное значение амплитуды в момент времени t0, в о.е.
t1 - период реакции (время от начала исследования до достижения максимального снижения амплитуды низкочастотной пьезотромбоэластографии - А1, в мин),
А1 - максимальное снижение амплитуды за время «t1» (период реакции), в о.е.
ИКК=(А1-А0)/t1.
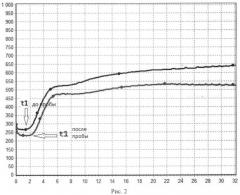
На рис.2 изображен график исследования пациентки А.
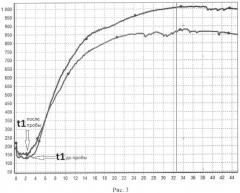
На рис.3 изображен график исследования пациентки М.
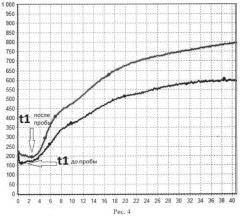
На рис.4 изображен график исследования пациента К.
На рис.5 изображен график исследования пациентки Б.
Данные, полученные в результате исследования, отражены в таблице.
Способ осуществляют следующим образом: определяют агрегатное состояние цельной крови, которую забирают у пациента из локтевой вены дважды, до и после пробы с локальной гипоксией (наложение жгута), трехкомпонентным силиконовым шприцем с резиновой манжетой одного объема - 2,0 мл, без наложения жгута. Заполняют разовую кювету 0,45 мл цельной крови, которая находится в термостате, и начинают исследование на аппаратно-программном комплексе АРП-01 «Меднорд». В основу анализа низкочастотной пьезотромбоэластографии положены изменения относительных значений вязкоупругих свойств крови, происходящих во время коагуляции: за период - «повреждение сосудистой стенки - достижение максимальной плотности сгустка в процессе его полимеризации и ретракции». Динамика исследуемого процесса - переход крови в ходе коагуляции от жидкого состояния в твердое - определяется изменениями агрегатного состояния последней и регистрируется в виде интегрированной кривой линии, каждая точка которой определяется состоянием системы в определенный момент времени исследования. Принципиально новым отличием данного способа является оценка интенсивности контактной коагуляции (ИКК), которая определяется как частное от деления разницы амплитуд начального значения вязкоупругих свойств крови в момент времени t0 (А0) максимального ее снижения за время t1 (А1) на период ретракции t1. (А0-A1)/t1 (рис.1). Таким образом, с помощью данного показателя оценивают антиагрегантную функцию эндотелия в I и II фазы коагуляции (этап предварительно зарождающегося сгустка).
Пример 1. Пациентка А., 37 лет. Диагноз: Беременность 32 недели. Острый флеботромбоз глубоких вен правой голени, верифицированный ультрасонографией вен нижних конечностей. Поступила с жалобами на чувство тяжести в ногах и незначительную отечность; болезненность по ходу сосудов; болезненность при пассивном тыльном сгибании стопы (возникает боль по задней поверхности голени, отдающая в подколенную ямку); тянущие боли по внутренней поверхности бедра и стопы. Данные обследования: артериальное давление систолическое - 130 мм рт.ст., диастолическое - 80 мм рт.ст.
При оценке антиагрегантного состояния функции эндотелия получены t1 до проведения пробы 1,4 и после 1,0; то есть зарегистрировано уменьшение t1 на 30%, и возросла ИКК с 20 до 60 (рис.2).
В результате проведенного исследования установлено снижение антиагрегантной функции эндотелия - дисфункция эндотелия, подтвержденная оценкой маркеров эндотелиальной активации до и после проведения пробы: фактор Виллебранда - 8,62/8,90 МЕ/мл, NO - 92/84 мкмоль/л.
Пример 2. Пациентка М., 52 года. Диагноз: Варикозное расширение вен левой нижней конечности, первичное заболевание. Рефлюкс по большой подкожной и перфорантной вене бедра, верифицированный ультрасонографией вен нижних конечностей. Поступила с жалобами на наличие варикозно измененных вен на левой нижней конечности, отеки дистальных отделов голени, боли и тяжесть в икроножных мышцах во второй половине дня. Данные обследования: артериальное давление систолическое - 125 мм рт.ст., диастолическое - 85 мм рт.ст.
При оценке антиагрегантного состояния функции эндотелия зарегистрировано t1 до локальной гипоксии 2,15 и после 2,25, то есть отсутствие изменения t1, и возросла ИКК с 27 до 31 (рис.3).
В результате проведенного исследования установлено нарушение антиагрегантной функции эндотелия, т.е. дисфункция эндотелия, подтвержденная оценкой маркеров эндотелиальной активации до и после проведения пробы: фактор Виллебранда - 8,84/9,15 МЕ/мл, NO - 67/54 мкмоль/л.
Пример 3. Пациент К., 43 года. Диагноз: ВСД по смешанному типу. Поступил с жалобами на нестабильность артериального давления; учащенное сердцебиение; периодически беспокоящую головную боль и головокружение. Данные обследования: артериальное давление систолическое - 120 мм рт.ст., диастолическое - 75 мм рт.ст.
При оценке антиагрегантного состояния функции эндотелия t1 увеличилась с 0,6 до 2,5 после проведения пробы локальной гипоксии, и зарегистрировано уменьшение ИКК с 90 до 10,4 (рис.4).
В результате антиагрегационная функция эндотелия оценивается как нормальная, подтвержденная оценкой маркеров эндотелиальной активации до и после проведения пробы: фактор Виллебранда - 0,94/1,52 МЕ/мл, NO - 120/145 мкмоль/л.
Пример 4. Пациентка Б., 41 год, практически здоровая. Данные обследования: артериальное давление систолическое - 120 мм рт.ст., диастолическое - 80 мм рт.ст.
При оценке антиагрегантного состояния функции эндотелия получены результаты: t1 до пробы 0,6 и после пробы 3,2, то есть зарегистрировано увеличение t1 более чем на 30%, ИКК уменьшилась с 58 до 15 (рис.5).
В результате антиагрегационная функция эндотелия оценивается как нормальная, подтвержденная оценкой маркеров эндотелиальной активации до и после проведения пробы: фактор Виллебранда - 0,61/0,92 МЕ/мл, NO - 83/92 мкмоль/л.
| Ф.И.О. | Показатели |
| Пациентка А., 37 лет. | t1 (до пробы)=1,4; t1 (после пробы)=1,0; |
| ИКК (до пробы)=20; ИКК (после пробы)=60 | |
| фактор Виллебранда - 8,62/8,90 МЕ/мл, NO - 92/84 мкмоль/л | |
| Пациентка М., 52 года. | t1 (до пробы)=2,15; t1 (после пробы)=2,25; |
| ИКК (до пробы)=27; ИКК (после пробы)=31 | |
| фактор Виллебранда - 8,84/9,15 МЕ/мл, NO - 67/54 мкмоль/л | |
| Пациент К., 43 года. | t1 (до пробы)=0,6; t1 (после пробы)=2,5 |
| ИКК (до пробы)=90; ИКК (после пробы)=10,4 | |
| фактор Виллебранда - 0,94/1,52 МЕ/мл, NO - 120/145 мкмоль/л. | |
| Пациентка Б., 41 год. | t1 (до пробы)=0,6; t1 (после пробы)=3,2; |
| ИКК (до пробы)=58; ИКК (после пробы)=15 | |
| фактор Виллебранда - 0,61/0,92 МЕ/мл, NO - 83/92 мкмоль/л |
Предлагаемый в качестве изобретения способ применен у 48 пациентов и позволяет повысить точность диагностики антиагрегантной функции эндотелия за счет уменьшения механического воздействия на форменные элементы крови, сократить время и стоимость исследования.
Список литературы
1. Bdolah Y., Karumanchis A., Sacha B.P. Recent advances in understanding of preeclampsia. Review Created Med J 2005; 46: 5: - p.728-736.
2. Bretelle F., Sabatier F. Et al. New insight in physiopathology of preeclampsia and intra-uterine growth retardation: role of inflammation. GynecObstetFertil 2004; 32:6: - p.482-489.
3. Davidson J.M., Homuth V., Jeyabalan A. et al. New aspects in the patophysiology of preeclampsia. J Am SocNephrol 2004; 25: - p.2440-2448.
4. Клименкова В.Ф., Бочков Ю.А., Шписман М.Н., Тютрин И.И. Выявление тромбоопасности как раннего маркера гестоза методом низкочастотной пьезотромбоэластографии // Фундаментальные исследования. - 2012. - №8 (часть 2). - с.330-333.
5. Зайнулина М.С., Петрищев Н.Н. Эндотелиальная дисфункция и ее маркеры при гестозе. Журнал акушерство и женские болезни 1997; I: С.59-61.
6. Мозговая Е.В., Печерина Л.В., Сепиашвили Л.А., Опыт применения антикоагулянтной терапии в акушерстве с целью коррекции эндотелиальной дисфункции при гестозе. / Дисфункция эндотелия. Причины, механизмы, фармакологическая коррекция, под редакцией Петрищева Н.Н.; - СПб.: изд. СПбГМУ, 2003. - С.83-97.
7. Соловьев М.А., Удут В.В, Тютрин И.И., Клименкова В.Ф. Новая технология диагностики и мониторинга критических нарушений гемостаза / Медико-биологические и социально-психологические проблемы безопасности в чрезвычайных ситуациях, 2013. №4. - стр.55-60.
8. Карпищенко А.И. Медицинские лабораторные технологии и диагностика: Справочник. Медицинские лабораторные технологии / Под ред. проф. А.И. Карпищенко. - СПб.: Интермедиа, 1999. - с.243-284.
9. Кишкун А.А. Руководство по лабораторным методам диагностики. - М.: ГЭОТАР. - Медиа, 2007. - с.310-340.
10. Асташев П.Е., Гудымович В.Г. Маркеры эндотелиальной дисфункции как прогностический признак течения внутрисердечного инфекционного процесса // Вестник Национального медико-хирургического Центра им. Н.И. Пирогова. - 2011, т.6, №3. с.4-5.
Способ оценки антиагрегантной функции эндотелия путем исследования системы регуляции агрегатного состояния крови, которое проводят дважды до и после ишемической пробы, отличающийся тем, что в исследуемых объемах крови до и после локальной гипоксии определяют интенсивность контактной коагуляции, (ИКК), далее определяют время от начала исследования (t0) до достижения максимального снижения амплитуды вязкоупругих свойств крови (t1) после локальной гипоксии и при уменьшении значения ИКК на 30% и более и одновременном увеличении значения t1 на 30% и более антиагрегантную функцию эндотелия оценивают как нормальную, а при возрастании ИКК или отсутствии ее изменений и одновременном увеличении значения t1 менее чем на 30% или отсутствии увеличения t1 антиагрегантную функцию эндотелия оценивают как сниженную.