Состав для стабилизации липидов к окислению
Иллюстрации
Показать всеИзобретение относится к области пищевой технологии, а именно к способам защиты липидов, масел, жиров от окисления и окислительной деструкции. Состав для стабилизации липидов, включает α-токоферол и бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфидпри следующих соотношениях компонентов в смеси, масса в %: α-токоферол 3,0-90,9,бис-3-(4′-гидрокси-3′,5′-дитрет-бутилфенил)пропил сульфид 3,0-9,1, добавляемых в концентрации 0,03-0,45% от массы липидов. Изобретение позволяет повысить ингибирующий эффект при наименьших концентрациях антиоксиданта. 2 табл., 3 пр.
Реферат
Изобретение относится к области пищевой технологии, а именно к способам защиты липидов, масел, жиров от окисления и окислительной деструкции и может быть использовано в пищевой, косметической и химико-фармацевтической промышленности для получения стабильных липидосодержащих пищевых добавок (нутрицевтиков), лечебно-косметических средств и лекарственных препаратов.
Известны способы стабилизации липидов различного происхождения к окислению путем введения антиоксидантов: токоферолов [SU №2564106, 1951], аскорбиновой кислоты и ее производных [GB 2123024А, 1984], нафтолов и фенолов [Эмануэль Н.М., Лясковская Ю.Н. Торможение процессов окисления жиров, Москва, Пищепромиздат, 1961].
Во всем мире ведется целенаправленный отбор полифункциональных стабилизаторов, лекарств антиоксидантного действия, синергических смесей. Использование синергических смесей позволяет получать высокоэффективные композиции, простые по составу и доступные для практического применения, при этом снижается количество антиоксиданта.
Известен состав для стабилизации липидов, включающий следующие компоненты, масса в %:
| α-токоферол (или α-токоферола ацетат) | 2,4-80,0 |
| бензафлавин | 2,3-76,9 |
| лецитин | 8,3-93,8, |
добавляемых в концентрации 0,4-5,2% от массы липидов (RU 2077558, опубл. 20. 04. 1997 г.).
Указанный состав тормозит процесс окисления липидов за счет антиоксидантного действия ингибиторов природного происхождения α-токоферола (6-гидрокси-2,5,7,8-тетраметил-2-фитил-хромана, витамина Е), бензафлавина (аналога витамина В2) и лецитина (яичного фосфатидилхолина). В составе указанной композиции бензафлавин и лецитин проявляют по отношению к α-токоферолу или α-токоферола ацетату синергическое действие. Однако практическое применение указанной синергической смеси затруднено в силу многокомпонентности ее состава, отсутствия промышленного производства бензафлавина, дороговизны препаратов, получаемых в экспериментальном производстве.
Задачей заявляемого изобретения является экономия использования дорогостоящих соединений, достижение ингибирующего эффекта меньшим количеством антиоксиданта.
Техническим результатом изобретения является упрощение состава и повышение его ингибирующего эффекта при наименьших концентрациях антиоксидантов.
Указанный технический результат достигается тем, что в составе для стабилизации липидов, включающем α-токоферол, особенностью является то, что вместо бензафлавина и лецитина используют бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид при следующих соотношениях компонентов в смеси, масса в %:
| α-токоферол | 3,0-90,9, |
| бис-3-(4′-гидрокси-3′,5′-дитрет- | |
| бутилфенил)пропил сульфид | 3,0-9,1, |
добавляемых в концентрации 0,03-0,45% от массы липидов.
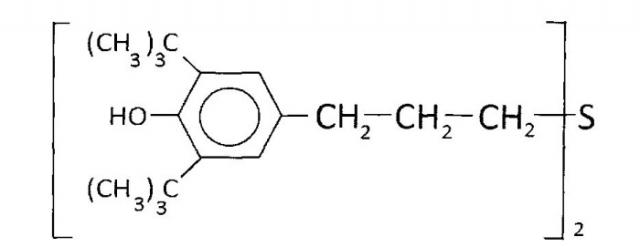
Предлагаемое соединение бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид (СО-3) было синтезировано в Новосибирском Институте органической химии им. Н.Н. Ворожцова СО РАН с целью расширения ассортимента нетоксичных биологически активных ингибиторов окисления. Химическая структура соединения представлена ниже:
Соединение не обладает местным и общетоксическим действием, не оказывает влияния на эмбриогенез и развитие потомства. Токсичность (ЛД50) бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида составляет более 10000 мг/кг. (Толстикова Т.Г., Долгих М.П., Сорокина И.В., Крысин А.П. Острая токсичность ряда новых производных 1,6-дитрет-бутилфенола. В сб. материалов «Биоантиоксидант». Научный вестник мед.акад. - Тюмень. - 2003. С.77-80.)
(Воевода Т.В., Толстикова Т.Г., Сорокина И.В. Изучение токсического действия фенольного антиоксиданта СО-3 в субхроническом эксперименте // Экспериментальная и клиническая фармакология. - 2000. - Т.63. - №4. - С.57-60.)
(Орлова Т.Н., Толстикова Т.Г., Сорокина И.В. Фармакокинетика нового фенольного антиоксиданта СО-3 //. Химико-фармацевтический журнал. - 2000. - Т.34. - №9. - С.9-11.)
(Зенков Н.К., Кандалинцева Н.В., Ланкин В.З., Фенольные биоантиоксиданты, СО РАМН, Новосибирск - 2003. - 328 С.) Серосодержащие аналоги фенолов в последнее время представляют большой интерес, вызванный их способностью эффективно тормозить окисление по нескольким механизмам.
(Перевозкина М.Г., Гуреева Н.В., Сторожок Н.М. Антиоксидантная активность новых серусодержащих фенолов // В сб.: Современные методы исследования в медицине и фармации. Казань. - 2002. - 29-30.)
Предлагаемое соединение бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид проявляет активность в реакции с пероксидными радикалами с константой скорости реакции К7=1,30×104 М-1×с-1, и обладает дополнительно способностью непосредственно. взаимодействовать с гидропероксидами, разрушая их без образования свободных радикалов до 41,4%, что не наблюдается в присутствии α-токоферола. Разрушение гидропероксидов под влиянием заявляемого соединения, в свою очередь, является причиной выигрыша в периодах индукции и обеспечения высокой эффективности соединения по сравнению с прототипом.
Эффективность стабилизаторов оценивалась несколькими независимыми методами (Сторожок Н.М. Межмолекулярные взаимодействия компонентов природных липидов в процессе окисления. Дис.… д-ра хим. наук. М.: Институт биохимической физики им. Н.М. Эмануэля РАН, 1996. С.360.) (Цепалов В.Ф., Харитонова А.А., Гладышев Г.П. и др. Определение констант скорости и коэффициентов ингибирования фенолов-антиоксидантов с помощью модельной цепной реакции // Кинетика и катализ. - 1977. - Т.18. - вып.5. - С.1261-1267.)
- изучалась кинетика поглощения кислорода при инициированном окислении липидных субстратов в присутствии предлагаемого состава и прототипа;
- тестировалась кинетика накопления первичных продуктов окисления - гидропероксидов методом йодометрического титрования (ПЧ) при аутоокислении липидов при повышенных температурах (60±0,2°C).
Изучение кинетики поглощения кислорода проводилось волюмометрическим методом в установках типа Варбурга при инициированном окислении липидов в присутствии инициатора азобисизобутиронитрила (АИБН) в концентрации 3 мМ при температуре 60±0,2°C. Кинетику накопления гидропероксидов в модельном субстрате исследовали в условиях аутоокисления методом обратного йодометрического титрования в неводной среде. Навеску окисляемого модельного субстрата растворяли в смеси ледяной уксусной кислоты и хлороформа в соотношении 3:2, добавляли насыщенный на холоду иодид калия, смесь перемешивали и оставляли в темноте. Через равные промежутки времени отбирали пробы и определяли в них перекисное число: П Ч = 0,1269 × ( a − b ) d ; где а - объем Na2S2O3, пошедший на титрование пробы; b - объем Na2S2O3, пошедший на титрование контрольного опыта; d - масса навески субстрата окисления.
Эффективность совместного ингибирующего действия смеси количественно характеризовали абсолютным значением разности (Δτ) периодов индукции окисления метилолеата (МО) в присутствии композиции антиоксидантов (АО) (τΣ) и простой суммы индивидуальных компонентов (Στi) (аддитивное действие) (Δτ=τΣ-Στi), либо выражали в относительных единицах - (Δτ/Στi)×100%. Выполнение неравенства τΣ>Στi свидетельствовало о проявлении синергизма в совместном действии компонентов, а τΣ<Στi - об эффекте антагонизма.
Критерием антиоксидантного действия служили начальная (Wo2нач) и максимальная (Wo2max) скорости процесса окисления в присутствии и в отсутствии антиоксиданта. Эффективность стабилизации окисления определяли также по величине WO2max (мо)/WO2max (MO+AO), количественно характеризующей степень уменьшения скорости поглощения кислорода в присутствии метилолеата (МО) и метилолеата с добавками антиоксидантов (МО+АО).
Изучение ингибирующего действия смесей α-токоферола с бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфидом с постоянными концентрациями α-токоферола показало, что зависимость периодов индукции от концентрации бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида носит экстремальный характер с максимумом в области 2×10-4 моль/л (0,03% от массы липидов). Диапазон эффективных концентраций соответствовал (1,0-3,0)×10-4 моль/л, что составляет (0,01-0,04)% от массы липидов. Диапазон эффективных концентраций смесей α-токоферола с бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфидом с постоянными концентрациями бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида соответствовал (0,1-3,0)×10-3 моль/л, что составляет (0,01-0,41)% от массы липидов.
Сущность изобретения иллюстрируется следующими примерами:
1. Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0044 г (0,04%) смеси α-токоферола с бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфидом. Стабилизирующая комбинация содержит 0,0034 г α-токоферола, 0,0010 г бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида, что составляет соответственно 0,03% и 0,01% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %:
| α-токоферол | 71,4 |
| бис-3-(4′-гидрокси-3′,5′-дитрет- | |
| бутилфенил)пропил сульфид | 28,6 |
2. Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0064 г (0,06%) смеси α-токоферола с бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфидом. Стабилизирующая комбинация содержит 0,0034 г α-токоферола, 0,0030 г бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида, что составляет соответственно 0,03% и 0,03% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %:
| α-токоферол | 55,6 |
| бис-3-(4′-гидрокси-3′,5′-дитрет- | |
| бутилфенил)пропил сульфид | 44,4 |
3. Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0078 г (0,08%) смеси α-токоферола с бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфидом. Стабилизирующая комбинация содержит 0,0068 г α-токоферола, 0,0010 г бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида, что составляет соответственно 0,07% и 0,01% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %:
| α-токоферол | 83,3 |
| бис-3-(4′-гидрокси-3′,5′-дитрет- | |
| бутилфенил)пропил сульфид | 16,7 |
Наибольшую эффективность по сравнению с прототипом проявляет смесь, включающая 92,6% α-токоферола и 7,4% бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида, добавляемая в концентрации 0,34% и 0,03% соответственно от массы липидов, максимально достигаемый ингибирующий эффект составляет 1970 мин, соотношение компонентов смеси 12,5:1, при этом эффективность предлагаемой смеси выше эффективности прототипа на 40%.
Было установлено, что эффективность синергизма при совместном использовании α-токоферола и бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида в субстратах составляет от (40-60)%, тогда как для прототипа эффективность смесей изменялась в пределах (16,7-20,0)% (табл.1). (Примечание - ∗АО-антиоксидант; «-« - отсутствие эффекта. Каждая цифра - результат 10 опытов, р<0,05).
При изучении кинетики накопления гидропероксидов было показано, что в опытах с концентрацией 83,3% α-токоферола и 16,7% бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида в концентрации 0,14% и 0,03% от массы липидов соответственно, процент разрушения гидропероксидов составляет 41,4%, что не наблюдается в присутствии прототипа (табл.2). (Примечание ∗ - липиды; «-« - отсутствие эффекта. Каждая цифра - результат 10 опытов, р<0,05).
Предлагаемый состав, включающий α-токоферол и бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид, достигает эффекта ингибирования окисления липидов при низких концентрациях компонентов смеси по сравнению с прототипом. Сочетание в одной композиции ингибиторов, действующих на разные элементарные реакции сложного окислительного процесса, а также присутствие эффекта синергизма антиоксидантов, позволяет увеличить ингибирующую способность смеси и эффективно тормозить окисление полиненасыщенных субстратов.
| Таблица 1 | ||||||||
| Состав модельной системы | Содержание АО∗, мас.% | Оценка эффективности (по периодам индукции), мин | Оценка эффективности (по скорости окисления) | |||||
| τиндАО, мин | Στi, мин | τΣ, мин | Δτ, мин | (Δτ/Στi)×100% | Wo2max×10-7, М×c-1 | W O 2 ( M O ) W O 2 ( M O + A O ∗ ) | ||
| Метилолеат | 0 | - | - | - | - | - | 8,0 | - |
| Индивидуальный α-токоферол | 0,01 | 75 | 0 | 0 | 0 | 0 | 6,5 | 1,2 |
| 0,03 | 160 | 0 | 0 | 0 | 0 | 6,4 | 1,3 | |
| 0,08 | 400 | 0 | 0 | 0 | 0 | 6,4 | 1,3 | |
| 0,14 | 600 | 0 | 0 | 0 | 0 | 6,4 | 1,3 | |
| Индивидуальный бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид | 0,01 | 130 | 0 | 0 | 0 | 0 | 7,8 | 1,0 |
| 0,03 | 250 | 0 | 0 | 0 | 0 | 7,5 | 1,1 | |
| 0,05 | 450 | 0 | 0 | 0 | 0 | 6,6 | 1,2 | |
| 0,08 | 780 | 0 | 0 | 0 | 0 | 6,6 | 1,2 | |
| 0,11 | 920 | 0 | 0 | 0 | 0 | 6,6 | 1,2 | |
| ПРОТОТИП | ||||||||
| Смесь с соотношением 23,1% α-токоферола и 19,2% бензафлавина и 57,7% лецитина | ||||||||
| α-токоферол | 1,01 | 300 | 300 | 350 | 50 | 16,7 | 4,9 | 1,6 |
| Бензафлавин | 0,41 | - | ||||||
| Лецитин | 1,08 | - | ||||||
| Смесь с соотношением 23,3% α-токоферола и 23,3% бензафлавина и 53,4% лецитина | ||||||||
| α-токоферол | 0,78 | 450 | 450 | 540 | 90 | 20 | 4,3 | 1,9 |
| Бензафлавин | 0,41 | - | ||||||
| Лецитин | 0,84 | - | ||||||
| Смесь с соотношением 17,7% α-токоферола и 20,6% бензафлавина и 61,7% лецитина | ||||||||
| α-токоферол | 0,34 | 980 | 980 | 1140 | 60 | 6,1 | 2,4 | 3,3 |
| Бензафлавин | 0,20 | - | ||||||
| Лецитин | 0,50 | - | ||||||
| ЗАЯВЛЯЕМЫЙ СОСТАВ |
| Смесь с соотношением 83,3% α-токоферола и 16,7% бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида | ||||||||
| α-токоферола | 0,14 | 600 | 850 | 1240 | 390 | 45,9 | 3,8 | 2,1 |
| бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид | 0,03 | 250 | ||||||
| Смесь с соотношением 71,4% α-токоферола и 28,6% бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида | ||||||||
| α-токоферола | 0,03 | 160 | 290 | 310 | 20 | 6,9 | 4,2 | 1,9 |
| бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид | 0,01 | 130 | ||||||
| Смесь с соотношением 55,6% α-токоферола и 44,4% бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида | ||||||||
| α-токоферола | 0,03 | 190 | 440 | 620 | 180 | 40,9 | 3,4 | 2,4 |
| бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид | 0,03 | 250 | ||||||
| Смесь с соотношением 83,3% α-токоферола и 16,7% бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида | ||||||||
| α-токоферола | 0,07 | 350 | 480 | 520 | 40 | 8,3 | 3,7 | 2,2 |
| бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид | 0,01 | 130 | ||||||
| Смесь с соотношением 88,2% α-токоферола и 11,8% бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида |
| α-токоферола | 0,10 | 450 | 580 | 630 | 50 | 8,6 | 3,4 | 2,4 |
| бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид | 0,01 | 130 | ||||||
| Смесь с соотношением 90,9% α-токоферола и 9,1% бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида | ||||||||
| α-токоферола | 0,14 | 600 | 730 | 820 | 90 | 12,3 | 3,7 | 2,2 |
| бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид | 0,01 | 130 | ||||||
| Смесь с соотношением 92,6% α-токоферола и 7,4% бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида | ||||||||
| α-токоферола | 0,34 | 980 | 1230 | 1970 | 740 | 60,2 | 2,1 | 3,8 |
| бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид | 0,03 | 250 | ||||||
| Смесь с соотношением 71,4% α-токоферола и 28,6% бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида | ||||||||
| α-токоферола | 0,07 | 350 | 600 | 860 | 260 | 43,3 | 3,9 | 2,1 |
| бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид | 0,03 | 250 |
Таблица 2
| № п/п | Состав смеси | Инициированное окисление, Wi=4,2×10-8 М-1×с-1 | Аутоокисление МО | Процент разруше ния ROOH за 7 часов | ||
| WO2 нач×10-7 М-1с | WO2 max×10-7 М-1с | Wнакопления ROOH.×10-4; гI2/100 г лип.*×с-1 | Wразрушения ROOH×10-4; гI2/100 г лип.*×с-1 | |||
| 1 | МО (контроль) | 1,9 | 8,0 | 8,7 | - | - |
| 2 | МО + Смесь с соотношением 83,3% α-токоферола (0,14 мас.%) и 16,7% бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфида (0,03 мас.%) | 0,6 | 3,8 | 1,8 | 41,4 | |
| 3 | МО + Смесь с соотношением 17,7% α-токоферола (0,34 мас.%) и 20,6% бензафлавина (0,20 мас.%) и 61,7% лецитина (0,50 мас.%) | 0,7 | 2,4 |
Состав для стабилизации липидов к окислению, включающий α-токоферол и синергист антиоксиданта, отличающийся тем, что в качестве синергиста антиоксиданта используют бис-3-(4′-гидрокси-3′,5′-дитретбутилфенил)пропил сульфид при следующих соотношениях компонентов в смеси, масса в %:
| α-токоферол | 3,0-90,9 |
| бис-3-(4′-гидрокси-3′,5′-дитрет- | |
| бутилфенил)пропил сульфид | 3,0-9,1, |