Способ получения n-(4-бромфенил)-n-(2-адамантил)амина (бромантана)
Иллюстрации
Показать всеИзобретение относится к усовершенствованному способу получения N-(4-бромфенил)-N-(2-адамантил)амина (бромантана), который обладает психостимулирующим и иммунопротекторным действием. Способ осуществляется по следующей схеме:
Согласно способу смесь адамантанона, броманилина и монооксида углерода подвергают взаимодействию в условиях, катализируемых солями или карбонилами металла, выбранными из группы, включающей родий, рутений, иридий, кобальт, железо. Взаимодействие проводят при повышенном давлении и при нагревании в присутствии осушителя в полярном протонном или апротонном растворителе, выбранном из группы тетрагидрофуран, ацетонитрил, этилацетат. Мольное соотношение адамантанона, пара-броманилина и катализатора составляет 1,0-1,1:1,0:0,01-0,05. Предпочтительно способ осуществляют при давлении СО 5-100 атм и температуре 25-200°C. В качестве катализатора желательно использовать RuCl3·3H2O, димер диацетата родия, карбонил кобальта, хлорид иридия (III), карбонил железа. Способ позволяет упростить процесс за счет осуществления его в одну стадию с выходом целевого продукта до 95%, устраняет необходимость удаления большого количества непрореагировавших реагентов. 7 з.п. ф-лы, 1 табл., 10 пр.
Реферат
Изобретение относится к органической химии, а именно к аминопроизводным адамантана, в частности к получению N-(4-бромфенил)-N-(2-адамантил)амина (бромантана), соединения, обладающего психостимулирующим и иммунопротекторным действием. N-(4-бромфенил)-N-(2-адамантил)амин является активным веществом таких известных фармацевтических препаратов, как бромантан и ладастен (Ladasten®).
Указанные препараты обладают широким спектром биологического действия, в частности стимулирующими и анксиолитическими свойствами, основным фармакологическим эффектом является стимулирующее влияние на центральную нервную систему, которое проявляется в повышении физической и умственной работоспособности, замедлении развития утомления и ускорении восстановления после интенсивных физических и психических нагрузок. Определенную роль в реализации фармакологического действия бромантана играют его антирадикальные и мембранопротекторные свойства [Методы исследования и фармакологической коррекции физической работоспособности человека. / Под ред. И.Б. Ушакова, М., Медицина, 2007; Морозов И.С., Петров В.И., Сергеева С.А. Фармакология адамантанов. - Волгоград: ВМА, 2001; Патент РФ №2175229, A61K 31/35; A61P 25/22 (1999); Б.И. №30; Сюняков С.А., Гришин С.А., Телешова Е.С., Незнамов Г.Г., Середенин С.Б. Результаты пилотного клинического исследования Ладастена, Экспериментальная и клиническая фармакология, 2006, 69 (4), с.10-15)].
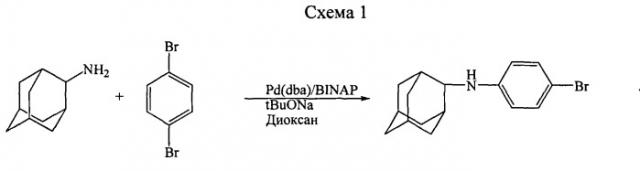
Известен способ получения N-(4-бромфенил)-N-(2-адамантил)амина, заключающийся в аминировании пара-дибромбензола адамантан-2-амином в присутствии палладиевых катализаторов и фосфорсодержащих сокатализаторов [Аверин А.Д., Улановская М.А., Ковалев В.В., Буряк А.К., Орлинсон Б.С., Новаков И.А., Белецкая И.П. Палладий-катализируемое аминирование адамантан-1- и -2-аминами изомерных дигалогенбензолов. ЖОрХ, 46(1), 2010, с.64-72].
Способ обладает рядом недостатков: выход целевого продукта не превышает 57%, необходимо использовать большое количество палладиевого катализатора (4 мол.%) и дорогостоящий сокатализатор.
Известны способы получения N-(4-бромфенил)-N-(2-адамантил)амина (бромантана), основанные на восстановительном аминировании адамантанона по реакции Лейкарта-Валлаха, где исходный адамантанон подвергают взаимодействию с пара-броманилином в муравьиной кислоте [SU Авт. свид. СССР №860446, C07C 211/00, A61K 31/136, А61Р 25/26, (1993), опубл. 30.11.1993; RU Патент РФ №1601978, 1995; И.С. Морозов, Н.В. Климова, Л.Н. Лаврова, Н.И. Авдюнина, Б.М. Пятин, B.C. Троицкая, Н.П. Быков. N-адамантилпроизводные ароматических аминов. Сообщение I. Синтез и нейротропная активность N-адамант-2-ил)анилинов. Хим.-фарм. ж., 1998, 32(1), 3)].
Один из вышеуказанных способов получения N-(4-бромфенил)-N-(2-адамантил)амина включает взаимодействие адамантанона с 99% муравьиной кислотой и пара-броманилином и последующую обработку образующегося формильного производного 15% соляной кислотой [SU Авт. свид. СССР №860446, C07C 211/00, A61K 31/136, А61Р 25/26, (1993), опубл. 30.11.1993]. Мольное соотношение реагентов: пара-броманилин : муравьиная кислота : адамантанон составляет 2:2:1. Выход целевого продукта составляет 80%. Т.пл. 100-102°C (абсолютный этанол). Недостатком способа является использование 2-кратного избытка токсичного броманилина и муравьиной кислоты, что требует тщательной и трудоемкой очистки целевого продукта.
Известный способ получения ряда N-(адамант-2-ил)анилинов, в том числе N-(4-бромфенил)-N-(2-адамантил)амина [И.С. Морозов, Н.В. Климова, Л.Н. Лаврова, Н.И. Авдюнина, Б.М. Пятин, B.C. Троицкая, Н.П. Быков. N-адамантилпроизводные ароматических аминов. Сообщение I. Синтез и нейротропная активность N-адамант-2-ил)анилинов. Хим.-фарм. ж., 1998, 32(1), с.3], восстановительным аминированием адамантанона осуществляют кипячение адамантанона с соответствующим анилином в муравьиной кислоте при мольном соотношении указанных веществ 1:2:4 соответственно (Схема 2).
Способ состоит из 3 стадий: на стадии (1) образуется формильное производное, которое гидролизуют соляной кислотой на стадии (2) и на стадии (3) образовавшийся гидрохлорид целевого продукта превращают в основание. В случае получения бромантана (R=R′=Н, R″=Br) образующийся после гидролиза на стадии (2) технический гидрохлорид отделяют фильтрацией, суспендируют в растворе едкого натра и получают целевой продукт в виде основания, которое очищают кристаллизацией из этанола. Т.пл. 107-109°C. Выход основания не указан, выход гидрохлорида 95,8%.
Недостатками способа является его многостадийность и необходимость использования большого избытка реагентов.
Еще один из вышеуказанных способов получения N-(4-бромфенил)-N-(2-адамантил)амина восстановительным аминированием адамантанона осуществляют кипячением смеси адамантанона, пара-броманилина и муравьиной кислоты при мольном соотношении реагентов 1:2-3:3-4 соответственно [RU Патент РФ №1601978, C07C 211/49, A61K 31/135, (1995), опубл. 27.10.1995].
Способ состоит из 3 вышеуказанных стадий (Схема 2). В качестве реагента используют 80-85% муравьиную кислоту, после кипячения смеси адамантанона, пара-броманилина и муравьиной кислоты в течение нескольких часов избыток муравьиной кислоты отгоняют, поднимают температуру реакционной смеси до 110-130°C и продолжают реакцию до содержания адамантанона 1-2%, затем гидролизуют образующийся формамид в присутствии соляной кислоты при температуре кипения реакционной смеси, полученный гидрохлорид целевого продукта превращают в основание обработкой водным раствором гидроокиси натрия, и очищают основание перекристаллизацией из изопропанола и дополнительным переосаждением водой из изопропанола. Выход целевого продукта 97,3-97,8%. Т.пл. 108-109°C.
Данный способ представляется наиболее эффективным и по некоторым существенным признакам является наиболее близким к заявляемому способу, поэтому он был выбран в качестве прототипа.
Недостатками способа-прототипа являются наличие нескольких стадий, необходимость использования 2-4-кратного избытка реагентов (амина и муравьиной кислоты соответственно), что требует дополнительных трудоемких операций для очистки целевого продукта и удаления непрореагировавших веществ, при этом используется большое количество кислот и оснований, которые также необходимо регенерировать или удалять в виде отходов.
Таким образом, существует потребность в простом с технологической точки зрения и экономичном способе получения бромантана, применимого в промышленности для производства этого препарата.
Задачей настоящего изобретения является разработка простого одностадийного способа получения N-(4-бромфенил)-N-(2-адамантил)амина из доступного сырья, пригодного для использования в промышленности.
Поставленная задача решается заявляемым способом получения N-(4-бромфенил)-N-(2-адамантил)амина из адамантанона и пара-броманилина, который состоит в том, что смесь адамантанона, пара-броманилина и монооксида углерода подвергают взаимодействию, катализируемому солями или карбонилами металла, выбранного из группы, включающей родий, рутений, иридий, кобальт и железо, причем взаимодействие проводят при повышенном давлении и при нагревании в присутствии осушителя в полярном протонном или апротонном растворителе, выбранном из группы: тетрагидрофуран, ацетонитрил, этилацетат, при этом мольное соотношение адамантанона, пара-броманилина и катализатора составляет 1,0-1,1: 1,0:0,01-0,05 (Схема 3). Способ осуществляют при давлении СО 5-100 атм и температуре 25-200°C, в качестве осушителя используют молекулярные сита.
Заявляемый способ осуществляют в одну стадию: смесь адамантанона, пара-броманилина, раствора катализатора, монооксида углерода и осушителя выдерживают при повышенном давлении и при нагревании в течение 11-24 часов. Газообразные продукты легко удаляют из реакционной смеси известными приемами и подвергают регенерации, очистке или утилизации. После удаления газообразных веществ получают целевой продукт-сырец с выходом 79-95%, перекристаллизацией которого из ацетонитрила или изопропанола получают очищенный бромантан, т.пл. 108-109°C. Способ включает минимальное количество операций: загрузка реагентов в реактор, нагревание, извлечение целевого продукта и его очистка.
Таким образом, заявляемый способ позволяет получать целевой продукт в одну стадию с высоким выходом. Использование почти эквимолярных количеств исходных адамантанона и пара-броманилина делает менее трудоемкой очистку целевого продукта, устраняет необходимость удаления больших количеств непрореагировавших реагентов и минимизирует количество отходов. Удаляемый из реакционной смеси СО можно превращать в СО2 по известной технологии (на палладиевом катализаторе). Таким образом, заявляемый способ является весьма перспективным с экологической точки зрения. Способ включает минимальное количество операций: загрузка реагентов в реактор, нагревание, извлечение целевого продукта и его очистка.
Способ основан на реакции восстановительного аминирования адамантанона, причем восстановителем в данном случае является монооксид углерода. Известно, что монооксид углерода является потенциальным восстановителем, но область применения этого восстановителя до сих пор ограничивалась в основном неорганической химией, в частности металлургией, где его применяют для восстановления оксидов металлов. В органической химии известно использование монооксида углерода в качестве восстановителя только для восстановления ароматических нитрогрупп. Другие примеры применения СО в качестве восстановителя в органическом синтезе до сих пор не были известны. Неожиданно оказалось, что СО является эффективным восстановителем в реакции восстановительного аминирования адамантанона, что позволило получить целевой бромантан в одну стадию с высоким выходом (см. примеры 1-10 и таблицу).
Исходные вещества, растворители и реагенты, необходимые для осуществления заявляемого способа, производятся промышленностью и являются коммерчески доступными.
Изобретение иллюстрируется конкретными примерами его осуществления, приведенными ниже.
Спектры 1Н ЯМР записаны на ЯМР-спектрометрах «BrukerAvance 300» и «BrukerAvance 400». Химические сдвиги приведены в м.д. относительно тетраметилсилана, откалиброванные на соответствующий пик растворителя.
Пример 1
В бюкс помещают 0,52 г (3 ммоль) пара-броманилина, 3,2 мл раствора хлорида рутения в ацетонитриле, содержащего 16 мг RuCl3·3H2O (0,06 ммоль), 292 мг молекулярных сит (MS 4Å), 0,5 г (3,3 ммоль) адамантанона. Бюкс помещают в автоклав Parr объемом 100 мл, закрывают автоклав и трижды набирают по 10 атмосфер монооксида углерода с последующим сбросом давления. После чего набирают 30 атмосфер СО и автоклав выдерживают в печи при температуре 140°C в течение 11 часов. Затем автоклав охлаждают, давление сбрасывают и вынимают бюкс, в котором находится продукт-сырец в виде белого кристаллического вещества (0,88 г, выход >95%), его перекристаллизовывают из ацетонитрила, отфильтровывают и дополнительное количество чистого продукта выделяют из маточника на хроматографической колонке с силикагелем. Выход очищенного продукта 82%. Т.пл. 108-109°C.
1Н NMR (300 MHz, CDCl3) δ 7.23 (д, J=8.6 Гц, 2Н), 6.48 (д, J=8.6 Гц, 2Н), 4.06 (с, J=98.0 Гц, 1H), 3.49 (с, 1Н), 1.80 (м, 15Н).
Примеры 2-10 осуществляют по методике, аналогичной описанной в примере 1. Результаты представлены в приведенной ниже таблице.
Заявляемый способ обладает следующими преимуществами по сравнению с известными аналогами: (i) целевой продукт получают в одну стадию; (ii) избыток СО легко удаляют стандартными приемами; и, если необходимо, СО превращают в СО2 по известной технологии; (iii) использование почти эквимолярных количеств исходных адамантанона и пара-броманилина и небольшие количества катализатора, что упрощает очистку целевого продукта, устраняет необходимость удаления больших количеств непрореагировавших реагентов и минимизирует количество отходов, поэтому способ перспективен с точки зрения охраны окружающей среды.
Техническим результатом изобретения является новый малоотходный способ получения бромантана, который позволяет получать целевой продукт в одну стадию с высоким выходом.
1. Способ получения N-(4-бромфенил)-N-(2-адамантил)амина из адамантанона и пара-броманилина, отличающийся тем, что смесь адамантанона, пара-броманилина и монооксида углерода подвергают взаимодействию, катализируемому солями или карбонилами металла, выбранными из группы, включающей родий, рутений, иридий, кобальт, железо, причем взаимодействие проводят при повышенном давлении и при нагревании в присутствии осушителя в полярном протонном или апротонном растворителе, выбранном из группы тетрагидрофуран, ацетонитрил, этилацетат, при этом мольное соотношение адамантанона, пара-броманилина и катализатора составляет 1,0-1,1:1,0:0,01-0,05.
2. Способ по п.1, отличающийся тем, что его осуществляют при давлении СО 5-100 атм.
3. Способ по п.1, отличающийся тем, что его осуществляют при температуре 25-200°C.
4. Способ по п.1, отличающийся тем, что в качестве катализатора используют RuCl3·3H2O.
5. Способ по п.1, отличающийся тем, что в качестве катализатора используют димер диацетата родия.
6. Способ по п.1, отличающийся тем, что в качестве катализатора используют карбонил кобальта.
7. Способ по п.1, отличающийся тем, что в качестве катализатора используют хлорид иридия (III).
8. Способ по п.1, отличающийся тем, что в качестве катализатора используют карбонил железа.