Композиции и способы лечения рака
Иллюстрации
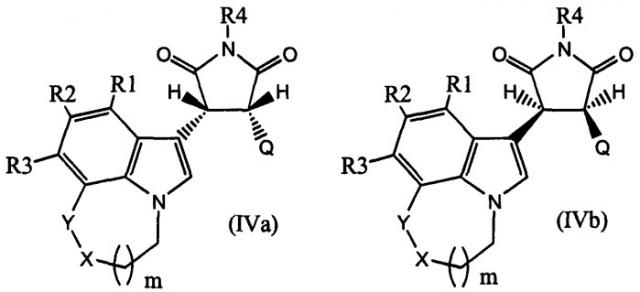
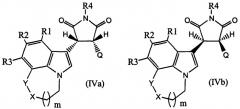
Показать всеИзобретение относится к пирролохинолинилпирролидин-2,5-дионам формулы IVa, IVb, Va или Vb, обладающих свойствами ингибитора роста раковых клеток, к фармацевтической композиции на их основе и к способу лечения с их использованием. В общих формулах IVa, IVb, Va, Vb R1, R2 и R3 означают водород, F, Cl, Br, I, -(С1-С6) алкил, CF3, -О-(C1-С6) алкил, или -OCF3; R4 означает водород, - (C1-С6) алкил или -CH2R7; R7 означает -О-Р(=O)(OH)2, -O-Р(=O)(-ОН)(-O-(C1-C6) алкил), -O-Р(=O)(-O-(C1-C6)алкил)2, -O-Р(=O)(-ОН)(-O-(СН2)-фенил), -O-Р(=O)(-O-(СН2)-фенил)2, группы карбоновой кислоты, группы аминокарбоновой кислоты или пептид; Q представляет собой арил, гетероарил, -О-арил, -S-арил, -О-гетероарил или -S-гетероарил; X означает -(СН2)- или -(NH)-; Y означает -(СН2)- или связь; где указанные арильная, гетероарильная, -О-арильная, -S-арильная, -О-гетероарильная и -S-гетероарильная группы могут быть замещены одним или несколькими заместителями, и m равно 1 или 2. 3 н. и 23 з.п. ф-лы, 2 табл., 12 ил., 88 пр.
Реферат
По данной заявке испрашивается приоритет по предварительной заявке на патент США No. 60/650951, поданной 9 февраля 2005 г., содержание которой включено в данное описание посредством ссылки во всей совей полноте.
Рак представляет собой вторую ведущую причину смертности в Соединенных Штатах Америки за исключением только сердечных заболеваний (Cancer Facts и Figures 2004, American Cancer Society, Inc.). Несмотря на недавние успехи в диагностике и лечении рака, излечение возможно с помощью хирургии и лучевой терапии при раннем выявлении рака, но существующая в настоящее время лекарственная терапия при метастатических заболеваниях большей частью является полумерой и редко предлагает длительные средства излечения. Даже при наличии новых химиотерапевтических средств, поступающих на рынок, сохраняется необходимость в новых лекарственных средствах, эффективных при монотерапии или в комбинации с существующими агентами в качестве первой терапии, а также в качестве вторичной и третичной терапии при лечении резистентных опухолей.
Раковые клетки по определению являются гетерогенными. Например, в рамках единственной ткани или типа клеток множество мутационных «механизмов» может приводить к развитию рака. По существу гетерогенность часто существует между раковыми клетками, полученными из опухолей одной и той же ткани и одного и того же типа, возникших у различных индивидуумов. Часто наблюдаемые мутационные «механизмы», связанные с некоторыми видами рака, могут различаться между одним и другим типами тканей (например, часто наблюдаемые мутационные «механизмы», приводящие к раку толстой кишки, могут отличаться от часто наблюдаемых «механизмов», приводящих к лейкозу). По этой причине часто трудно предсказать, будет ли конкретный вид рака давать ответную реакцию на определенный химиотерапевтический агент (Cancer Medicine, 5th Edition, Bast et al. eds., B.C. Decker Inc., Hamilton, Ontario).
Рак молочной железы представляет собой наиболее часто диагностируемый не кожный вид рака у женщин и расценивается как второй по числу смертей от рака у женщин после рака легких (Cancer Facts and Figures 2004, American Cancer Society, Inc.). Варианты выбора лечения при раке молочной железы в настоящее время включают хирургию, лучевую терапию и химиотерапию/гормональную терапию с использованием таких агентов, как тамоксифен, ингибиторы ароматазы, Herceptin® (трастузумаб), Taxol® (паклитаксель), циклофосфамид, метотрексат, доксорубицин (адриамицин) и 5-фторурацил. Несмотря на улучшения в диагностике рака и терапевтическом лечении, рост заболеваемости раком молочной железы продолжает увеличиваться с 1980-х годов. В 2004 г. ожидается примерно 215000 новых случаев возникновения рака молочной железы у женщин и примерно 1450 новых случаев рака молочной железы у мужчин (там же). Соответственно необходимы новые соединения и способы лечения рака молочной железы.
Компоненты клеточного сигнального пути трансдукции, которые регулируют рост и дифференциацию нормальных клеток, могут, при нарушении регуляции, приводить к развитию клеточного пролиферативного нарушения и рака. Мутации в клеточных сигнальных белках могут приводить к тому, что такие белки будут экспрессироваться или активироваться на неподходящих уровнях или в неподходящее время во время клеточного цикла, что, в свою очередь, может приводить к неконтролируемому росту клеток или изменениям в свойствах присоединения клетка-клетка. Например, нарушение регуляции рецепторных тирозинкиназ в результате мутации, перегруппировки генов, генной амплификации и сверхэкспресии как рецептора, так и лиганда, влечет за собой развитие и прогрессирование рака у людей.
Рецепторная тирозинкиназа c-Met является единственным известным высокоаффинным рецептором фактора роста гепатоцитов (HGF), также известного, как фактор рассеяния. Связывание HGF с межклеточным лиганд-связывающим доменом c-Met приводит к мультимеризации рецептора и фосфорилированию множества остатков тирозина во внутриклеточной части c-Met. Активация c-Met приводит к связыванию и фосфорилированию переходных белков, таких как Gab-1, Grb-2, Shc и c-Cbl, и последующей активации сигнальных трансдукторов, таких как PI3K, PLC-γ, STAT, ERK1 и 2 и FAK. c-Met и HGF экспрессируются во множестве тканей и их экспрессия обычно ограничивается главным образом клетками эпителиального и мезенхимального происхождения, соответственно. c-Met и HGF аномально регулируются при раке человека и могут вносить свой вклад в нарушение регуляции роста клеток, распространение опухолевых клеток и инвазию опухоли во время прогрессирования и метастазов заболевания (см., например, Journal of Clinical Investigation 109: 863-867 (2002) и Cancer Cell pp 5-6 July 2004). c-Met и HGF экспрессируются в большой степени относительно окружающих тканей при многочисленных видах рака и их экспрессия коррелирует с плохим прогнозом для пациента (см., например, Journal of Cellular Biochemistry 86: 665-677 (2002); Int. J. Cancer (Pred. Oncol.) 74: 301-309 (1997); Clinical Cancer Research 9: 1480-1488 (2003) и Cancer Research 62: 589-596 (2002)). Не связываясь с какой-либо теорией, c-Met и HGF могут защищать опухоли от клеточной смерти, индуцированной агентами, повреждающими ДНК, и как таковые могут вносить вклад в устойчивость опухолей к химиотерапии. Не ограничиваясь какой-либо теорией, ингибиторы c-Met могут быть полезными в качестве терапевтических агентов при лечении пролиферативных нарушений, включая рак молочной железы (см., например, Cancer and Metastasis Reviews 22: 309-325 (2003)).
Процитированные выше ссылки не признаются как являющиеся прототипом заявляемого изобретения.
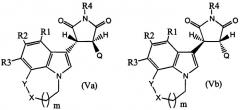
Настоящее изобретение относится к соединениям пирролохинолинилпирролидин-2,5-диона формулы IVa, IVb, Va или Vb, и к способам получения соединений формулы IVa, IVb, Va и Vb,
где:
R1, R2 и R3 независимо выбирают из группы, состоящей из водорода, F, Cl, Br, I, ─NR5R6, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, замещенного ─O─(C1─C6)алкила, ─O─(C3─C9)циклоалкила и замещенного ─O─(C3─C9)циклоалкила, арила, гетероарила, гетероциклила;
R4 независимо выбирают из группы, состоящей из водорода, ─(C1─C6)алкила, ─CH2R7;
R5, R6 независимо выбирают из группы, состоящей из водорода и ─(C1─C6)алкила;
R7 независимо выбирают из группы, состоящей из ─O─P(=O)(OH)2, ─O─P(=O)(─OH)(─O─(C1─C6)алкил), ─O─P(=O)(─O─(C1─C6)алкил)2, ─O─P(=O)(─OH)(─O─(CH2)─фенил), ─O─P(=O)(─O─(CH2)─фенил)2, группы карбоновой кислоты, группы аминокарбоновой кислоты и пептида;
Q выбирают из группы, состоящей из арила, гетероарила, ─O─арила, ─S─арила, ─O─гетероарила и ─S─гетероарила;
X выбирают из группы, состоящей из ─(CH2)─, ─(NR8)─, S и O;
R8 независимо выбирают из группы, состоящей из водорода, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила и ─O─(C1─C6)алкила, ─C(=O)─O─(C1─C6)алкила и замещенного ─C(=O)─O─(C1─C6)алкила;
Y выбирают из группы, состоящей из ─(CH2)─ или связи;
где указанные арильная, гетероарильная, ─O─арильная, ─S─арильная, ─O─гетероарильная и ─S─гетероарильная группы могут быть замещены одним или несколькими заместителями, независимо выбранными из группы, состоящей из F, Cl, Br, I, ─NR5R6, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, замещенного ─O─(C1─C6)алкила, ─O─(C3─C9)циклоалкила, замещенного ─O─(C3─C9)циклоалкила, ─арила, ─арил─(C1─C6)алкила, ─арил─O─(C1─C6)алкила, ─O─арила, ─O─(C1─C4)алкиларила, гетероарила, гетероциклила, ─O─(C1─C4)алкилгетероцикла и ─(S(=O)2)─(C1─C6)алкила; и
m равно 1 или 2.
В одном из вариантов осуществления R4 представляет собой ─CH2R7, и R7 представляет собой ─O─P(=O)(OH)2, ─O─P(=O)(─OH)(─O─(C1─C6)алкил), ─O─P(=O)(─O─(C1─C6)алкил)2, группу карбоновой кислоты, группу аминокарбоновой кислоты или пептид.
В одном из вариантов осуществления X выбирают из группы, состоящей из ─(NR8)─, S и O.
В одном из вариантов осуществления m равно 2,
В предпочтительном варианте осуществления соединения пирролохинолинилпирролидин-2,5-диона выбирают из группы, состоящей из (+)-цис-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона, (-)-цис-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона, (+)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона и (-)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона. В следующем предпочтительном варианте осуществления соединение представляет собой (-)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-дион.
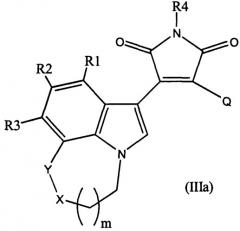
Настоящее изобретение также относится к соединениям пирролохинолинилпиррол-2,5-диона формулы IIIa и их синтезу.
где:
R1, R2 и R3 независимо выбирают из группы, состоящей из водорода, F, Cl, Br, I, ─NR5R6, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, замещенного ─O─(C1─C6)алкила, ─O─(C3─C9)циклоалкила и замещенного ─O─(C3─C9)циклоалкила, арила, гетероарила, гетероциклила;
R4 независимо выбирают из группы, состоящей из водорода, ─(C1─C6)алкила, ─CH2R7;
R5, R6 независимо выбирают из группы, состоящей из водорода и ─(C1─C6)алкила;
R7 независимо выбирают из группы, состоящей из ─O─P(=O)(OH)2, ─O─P(=O)(─OH)(─O─(C1─C6)алкил), ─O─P(=O)(─O─(C1─C6)алкил)2, ─O─P(=O)(─OH)(─O─(CH2)─фенил), ─O─P(=O)(─O─(CH2)─фенил)2, группы карбоновой кислоты, группы аминокарбоновой кислоты и пептида;
Q выбирают из группы, состоящей из арила, гетероарила, ─O─арила, ─S─арила, ─O─гетероарила и ─S─гетероарила, при условии, что когда R4 представляет собой водород, (C3-C4)циклоалкил или (C1-C4)алкил, Q не является 3-индолилом или замещенным 3-индолилом;
X выбирают из группы, состоящей из ─(CH2)─, ─(NR8)─, S и O;
R8 независимо выбирают из группы, состоящей из водорода, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, ─C(=O)─O─(C1─C6)алкила и замещенного ─C(=O)─O─(C1─C6)алкила;
Y выбирают из группы, состоящей из ─(CH2)─ или связи;
где указанные арильная, гетероарильная, ─O─арильная, ─S─арильная, ─O─гетероарильная и ─S─гетероарильная группы могут быть замещены одним или несколькими заместителями, независимо выбранными из группы, состоящей из F, Cl, Br, I, ─NR5R6, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, замещенного ─O─(C1─C6)алкила, ─O─(C3─C9)циклоалкила, замещенного ─O─(C3─C9)циклоалкила, ─арила, ─арил─(C1─C6)алкила, ─арил─O─(C1─C6)алкила, ─O─арила, ─O─(C1─C4)алкиларила, гетероарила, гетероциклила, ─O─(C1─C4)алкилгетероцикла и ─(S(=O)2)─(C1─C6)алкила; и
m равно 1 или 2,
при условии, что соединения, в которых R1, R2, R3, R4 являются водородом, Q представляет собой 5-членный гетероарил с одним атомом азота, гетероарил, конденсированный с бензогруппой, Х представляет собой (СН2)-, Y представляет собой связь, и m равно 1 или 2.
Настоящее изобретение также относится к фармацевтической композиции, содержащей одно или несколько соединений формулы IIIa, IVa, IVb, Va или Vb и один или несколько фармацевтически приемлемых носителей или эксципиентов. Настоящее изобретение также относится к фармацевтической композиции, содержащей соединение формулы IIIa, IVa, IVb, Va или Vb и один или несколько фармацевтически приемлемых носителей или эксципиентов.
Настоящее изобретение относится к способу лечения клеточного пролиферативного нарушения, причем указанный способ включает введение нуждающемуся в этом субъекту терапевтически эффективного количества соединения формулы IIIa, IVa, IVb, Va или Vb или его фармацевтически приемлемой соли, или пролекарства, метаболита, аналога или производного в сочетании с фармацевтически приемлемым носителем, где указанное клеточное пролиферативное нарушение подвергается лечению.
В одном из вариантов осуществления клеточное пролиферативное нарушение представляет собой рак.
Настоящее изобретение также относится к способу модулирования активности c-Met, включающему контактирование клетки с эффективным количеством соединения формулы IIIa, IVa, IVb, Va или Vb или его фармацевтически приемлемой соли, или пролекарства, метаболита, аналога или производного, где указанное контактирование приводит к указанному модулированию активности c-Met.
В одном из вариантов осуществления модулирование заключается в ингибировании.
В одном из вариантов осуществления соединение модулирует активность c-Met без существенного модулирования указанной активности протеинкиназы С.
Настоящее изобретение также относится к способу селективного ингибирования активности c-Met в отсутствие ингибирования протеинкиназы С, включающему контактирование клетки с эффективным количеством соединения формулы IIIa, IVa, IVb, Va или Vb или его фармацевтически приемлемой соли, или пролекарства, метаболита, аналога или производного, где указанное контактирование приводит к указанному селективному ингибированию указанной активности c-Met без ингибирования указанной активности протеинкиназы С.
Настоящее изобретение также относится к способу селективного индуцирования клеточной смерти предраковых клеток или раковых клеток, включающему контактирование клетки с эффективным количеством соединения формулы IIIa, IVa, IVb, Va или Vb или его фармацевтически приемлемой соли, или пролекарства, метаболита, аналога или производного, где указанное контактирование приводит к указанному селективному индуцированию клеточной смерти указанных предраковых клеток или указанных раковых клеток.
Кроме того, настоящее изобретение относится к способу лечения рака, включающему селективное модулирование активности c-Met или обеих, без существенного модулирования активности протеинкиназы С.
Далее настоящее изобретение относится к способу скрининга соединений-кандидатов для лечения рака, включающему контактирование клетки с соединением-кандидатом, измерение активности c-Met, измерение активности протеинкиназы С и выбор соединения-кандидата, способного селективно ингибировать активность c-Met без существенного ингибирования активности протеинкиназы С, где указанное соединение-кандидат, способное селективно ингибировать активность c-Met без существенного ингибирования активности протеинкиназы С, представляет собой соединение-кандидат для лечения рака. В одном из вариантов осуществления активность протеинкиназы C измеряют in vitro.
Другие отличительные признаки и преимущества настоящего изобретения будут очевидны из приведенного дополнительного описания, включая различные примеры. Приведенные примеры иллюстрируют различные компоненты и методики, полезные при практическом осуществлении настоящего изобретения. Примеры не ограничивают заявляемого изобретения. На основании настоящего описания специалист в данной области сможет идентифицировать и использовать другие компоненты и методики, полезные при практическом осуществлении настоящего изобретения.
Краткое описание рисунков
На фиг.1 представлены химические структуры (±)-цис-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона и (±)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона.
На фиг.2 показано действие (±)-цис-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона или (±)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона на выживание клеток MDA-MB-231 или Paca-2 in vitro.
На фиг.3 показано действие (-)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона или (+)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона на выживание клеток MDA-MB-231 in vitro.
На фиг.4 показано действие (±)-цис-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона или (±)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона на активность протеинкиназы C in vitro.
На фиг.5 показано ингибирование фосфорилирования c-Met и фосфорилирования ERK1/2 с помощью (-)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона или (+)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона.
На фиг.6 показано действие (±)-цис-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона или (±)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона, вводимого индивидуально в дозе 160 мг/кг, на рост гетеротрансплантированных опухолей рака молочной железы MDA-MB-231 у не имеющих вилочковой железы голых самок мышей.
На фиг.7 показано действие (±)-цис-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона или (±)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона, вводимого индивидуально в дозе 80 мг/кг, на рост гетеротрансплантированных опухолей рака молочной железы MDA-MB-231 у не имеющих вилочковой железы голых самок мышей.
На фиг.8 показано действие (-)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона на индуцирование апоптоза раковых клеток.
На фиг.9 показано действие (-)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона, ингибирующее метастатическую инвазию раковых клеток.
На фиг.10 показано действие (-)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона на гетеротрансплантированной модели рака молочной железы.
На фиг.11 показано действие (-)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона на гетеротрансплантированной модели рака толстой кишки.
На фиг.12 показано действие (-)-транс-3-(5,6-дигидро-4H-пирроло[3,2,1-ij]хинолин-1-ил)-4-(1H-индол-3-ил)пирролидин-2,5-диона на гетеротрансплантированной модели рака поджелудочной железы.
1. Пирролохинолинилпиррол-2,5-дионы и пирролохинолинилпирролидин-2,5-дионы
Настоящее изобретение относится к соединениям пирролохинолинилпиррол-2,5-диона формулы III и IIIa и их синтезу
где:
R1, R2 и R3 независимо выбирают из группы, состоящей из водорода, F, Cl, Br, I, ─NR5R6, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, замещенного ─O─(C1─C6)алкила, ─O─(C3─C9)циклоалкила и замещенного ─O─(C3─C9)циклоалкила, арила, гетероарила, гетероциклила;
R4 независимо выбирают из группы, состоящей из водорода, ─(C1─C6)алкила, ─CH2R7;
R5, R6 независимо выбирают из группы, состоящей из водорода и ─(C1─C6)алкила;
R7 независимо выбирают из группы, состоящей из ─O─P(=O)(OH)2, ─O─P(=O)(─OH)(─O─(C1─C6)алкил), ─O─P(=O)(─O─(C1─C6)алкил)2, ─O─P(=O)(─OH)(─O─(CH2)─фенил), ─O─P(=O)(─O─(CH2)─фенил)2, группы карбоновой кислоты, группы аминокарбоновой кислоты и пептида;
Q выбирают из группы, состоящей из арила, гетероарила, ─O─арила, ─S─арила, ─O─гетероарила и ─S─гетероарила;
X выбирают из группы, состоящей из ─(CH2)─, ─(NR8)─, S и O;
R8 независимо выбирают из группы, состоящей из водорода, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, ─C(=O)─O─(C1─C6)алкила и замещенного ─C(=O)─O─(C1─C6)алкила;
Y выбирают из группы, состоящей из ─(CH2)─ или связи;
где указанные арильная, гетероарильная, ─O─арильная, ─S─арильная, ─O─гетероарильная и ─S─гетероарильная группы могут быть замещены одним или несколькими заместителями, независимо выбранными из группы, состоящей из F, Cl, Br, I, ─NR5R6, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, замещенного ─O─(C1─C6)алкила, ─O─(C3─C9)циклоалкила, замещенного ─O─(C3─C9)циклоалкила, ─арила, ─арил─(C1─C6)алкила, ─арил─O─(C1─C6)алкила, ─O─арила, ─O─(C1─C4)алкиларила, гетероарила, гетероциклила, ─O─(C1─C4)алкилгетероцикла и ─(S(=O)2)─(C1─C6)алкила; и
m равно 1 или 2,
Для соединения формулы IIIa Q выбирают из группы, состоящей из арила, гетероарила, ─O─арила, ─S─арила, ─O─гетероарила и ─S─гетероарила, при условии, что когда R4 представляет собой водород, (C3-C4)циклоалкил или (C1-C4)алкил, Q не является 3-индолилом или замещенным 3-индолилом.
Настоящее изобретение также относится к соединениям пирролохинолинилпирролидин-2,5-диона формулы IVa, IVb, Va или Vb и к способам получения соединений формулы IVa, IVb, Va и Vb,
где:
R1, R2 и R3 независимо выбирают из группы, состоящей из водорода, F, Cl, Br, I, ─NR5R6, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, замещенного ─O─(C1─C6)алкила, ─O─(C3─C9)циклоалкила и замещенного ─O─(C3─C9)циклоалкила, арила, гетероарила, гетероциклила;
R4 независимо выбирают из группы, состоящей из водорода, ─(C1─C6)алкила, ─CH2R7;
R5, R6 независимо выбирают из группы, состоящей из водорода и ─(C1─C6)алкила;
R7 независимо выбирают из группы, состоящей из ─O─P(=O)(OH)2, ─O─P(=O)(─OH)(─O─(C1─C6)алкил), ─O─P(=O)(─O─(C1─C6)алкил)2, ─O─P(=O)(─OH)(─O─(CH2)─фенил), ─O─P(=O)(─O─(CH2)─фенил)2, группы карбоновой кислоты, группы аминокарбоновой кислоты и пептида;
Q выбирают из группы, состоящей из арила, гетероарила, ─O─арила, ─S─арила, ─O─гетероарила и ─S─гетероарила;
X выбирают из группы, состоящей из ─(CH2)─, ─(NR8)─, S и O;
R8 независимо выбирают из группы, состоящей из водорода, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, ─C(=O)─O─(C1─C6)алкила и замещенного ─C(=O)─O─(C1─C6)алкила;
Y выбирают из группы, состоящей из ─(CH2)─ или связи;
где указанные арильная, гетероарильная, ─O─арильная, ─S─арильная, ─O─гетероарильная и ─S─гетероарильная группы могут быть замещены одним или несколькими заместителями, независимо выбранными из группы, состоящей из F, Cl, Br, I, ─NR5R6, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, замещенного ─O─(C1─C6)алкила, ─O─(C3─C9)циклоалкила, замещенного ─O─(C3─C9)циклоалкила, ─арила, ─арил─(C1─C6)алкила, ─арил─O─(C1─C6)алкила, ─O─арила, ─O─(C1─C4)алкиларила, гетероарила, гетероциклила, ─O─(C1─C4)алкилгетероцикла и ─(S(=O)2)─(C1─C6)алкила; и
m равно 1 или 2.
1.1. Определения
Термин «алкил» относится к радикалам, содержащим углерод и водород и не являющимся ненасыщенными. Алкильные радикалы могут быть линейными или разветвленными. Иллюстративные алкильные радикалы включают, но без ограничения, метил, этил, пропил, изопропил, гексил, трет-бутил, втор-бутил и подобные. Алкильные группы могут быть обозначены с использованием цепи, так, например, (C1-C6)алкильная группа представляет собой алкильную группу, имеющую от одного до шести атомов углерода в линейной или разветвленной алкильной цепи. Замещенные и незамещенные алкильные группы могут независимо представлять собой (C1-C5)алкил, (C1-C6)алкил, (C1-C10)алкил, (C3-C10)алкил или (C5-C10)алкил. Если специально не указано иное, термин «алкил» не включает «циклоалкил».
Термин «циклоалкильная» группа относится к циклической алкильной группе, имеющей указанное число атомов углерода в «кольцевой части», где «кольцевая часть» может состоять из одной или нескольких кольцевых структур, которые являются конденсированными, спиро или мостиковыми кольцевыми структурами. Например, C3-C6 циклоалкильная группа (например, (C3-C6)циклоалкил) представляет собой кольцевую структуру, имеющую от 3 до 6 атомов углерода в кольце. Когда диапазон не указан, циклоалкильная группа имеет от трех до девяти атомов углерода ((C3-C9)циклоалкил) в кольцевой части. Иллюстративные циклоалкильные группы включают, но не ограничиваются ими, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и адамантил. Предпочтительные циклоалкильные группы имеют три, четыре, пять, шесть, семь, восемь, девять или от трех до девяти атомов углерода в кольцевой структуре.
Термины «замещенный алкил» и «замещенный циклоалкил» относятся к алкильным и циклоалкильным группам, как определено выше, замещенным одним или несколькими заместителями, независимо выбранными из группы, состоящей из фтора, арила, гетероарила, ─O─(C1─C6)алкила и ─NR5R6, где R5 и R6 независимо выбирают из группы, состоящей из водорода и ─(C1─C6)алкила.
Термин «арил» относится к ароматической карбоциклической группе, имеющей одно, два или три ароматических кольца. Иллюстративные арильные группы включают, но без ограничения, фенил, нафтил и подобные. Арильные группы включают одно, два или три ароматических кольца, конденсированные с одним или несколькими дополнительными неароматическими карбоциклическими или гетероциклическими кольцами, содержащими 4-9 членов. Примеры конденсированных арильных групп включают бензоциклобутанил, инданил, тетрагидронафтиленил, 1,2,3,4-тетрагидрофенантренил, тетрагидроантраценил, 1,4-дигидро-1,4-метанонафталенил, бензодиоксолил.
Термин «гетероарил» относится к гетероароматической (гетероарильной) группе, имеющей одно, два или три ароматических кольца, содержащие 1-4 гетероатома (таких как азот, сера или кислород) в ароматическом кольце. Гетероарильные группы включают одну, две или три ароматические кольцевые структуры, содержащие 1-4 гетероатома, конденсированные с одним или несколькими дополнительными неароматическими кольцами, содержащими 4-9 членов. Гетероарильные группы, содержащие гетероатом единственного типа в ароматическом кольце, обозначают по типу содержащегося в них гетероатома, так выражения азотсодержащий гетероарил, кислородсодержащий гетероарил и сера-содержащий гетероарил означают гетероароматические группы, содержащие один или несколько атомов азота, кислорода или серы, соответственно. Иллюстративные гетероарильные группы включают, но без ограничения, пиридил, пиримидинил, тиазолил, хинолил, хиназолинил, тиазолил, бензо[b]тиофенил, фуранил, имидазолил, индолил и подобные.
Термины «гетероциклил» или «гетероцикл» относятся к либо насыщенным, либо ненасыщенным стабильным неароматическим кольцевым структурам, которые могут быть конденсированными, спиро- или мостиковыми структурами с образованием дополнительных колец. Каждый гетероцикл состоит из одного или нескольких атомов углерода и от одного до четырех гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы. «Гетероциклил» или «гетероцикл» включают стабильные неароматические 3-7-членные моноциклические гетероциклические кольцевые структуры и 8-11-членные бициклические гетероциклические кольцевые структуры. Гетероциклильный радикал может быть присоединен через любой эндоциклический атом углерода или азота, что приводит к созданию стабильной структуры. Предпочтительные гетероциклы включают 3-7-членные моноциклические гетероциклы (более предпочтительно 5-7-членные моноциклические гетероциклы) и 8-10-членные бициклические гетероциклы. Примеры таких групп включают пиперидинил, пиперазинил, пиранил, пирролидинил, морфолинил, тиоморфолинил, оксопиперидинил, оксопирролидинил, оксоазепинил, азепинил, изоксозолил, тетрагидропиранил, тетрагидрофуранил, диоксолил, диоксинил, оксатиолил, дитиолил, сульфоланил, диоксанил, диоксоланил, тетрагидрофуродигидрофуранил, тетрагидропиранодигидрофуранил, дигидропиранил, тетрагидрофурофуранил, тетрагидропиранофуран, хинуклидинил (1-азабицикло[2,2,2]октанил) и тропанил (8-метил-8-азабицикло[3,2,1]октанил).
Применительно к заместителю Q, термин «замещенный 3-индолил» относится к 3-индолильной группе, замещенной одним или несколькими заместителями, выбранными из группы состоящей из F, Cl, Br, I, ─NR5R6, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, замещенного ─O─(C1─C6)алкила, ─O─(C3─C9)циклоалкила, замещенного ─O─(C3─C9)циклоалкила, ─арила, ─арил─(C1─C6)алкила, ─арил─O ─(C1─C6)алкила, ─O─арила, ─O─(C1─C4)алкиларила, гетероарила, гетероциклила, ─O─(C1─C4)алкилгетероцикла и ─(S(=O)2)─(C1─C6)алкила; где R5, R6 независимо выбирают из группы, состоящей из водорода и ─(C1─C6)алкила.
Применительно к заместителю R7, термин «группа карбоновой кислоты» относится к группе, имеющей форму ─O─C(=O)─(C1─C6)алкила, ─O─C(=O)─(C3─C9)циклоалкила, ─O─C(=O)─арила, ─O─C(=O)─гетероарила, ─O─C(=O)─гетероцикла, ─O─C(=O)─(C1─C6)алкиларила, ─O─C(=O)─(C1─C6)алкилгетероарила или ─O─C(=O)─(C1─C6)алкилгетероцикла. В «группу карбоновой кислоты» включены группы, имеющие форму ─O─C(=O)─(C1─C6)алкила, ─O─C(=O)─(C3─C9)циклоалкила, ─O─C(=O)─арила, ─O─C(=O)─гетероарила, ─O─C(=O)─гетероцикла, ─O─C(=O)─(C1─C6)алкиларила, ─O─C(=O)─(C1─C6)алкилгетероарила или ─O─C(=O)─(C1─C6)алкилгетероцикла, замещенные одним или несколькими заместителями, независимо выбранными из группы, состоящей из F, Cl, Br, I, ─OH, ─SH, ─NR5R6, ─(C1─C6)алкила, замещенного ─(C1─C6)алкила, ─(C3─C9)циклоалкила, замещенного ─(C3─C9)циклоалкила, ─O─(C1─C6)алкила, замещенного ─O─(C1─C6)алкила, ─S─(C1─C6)алкила, ─O─(C3─C9)циклоалкила, замещенного ─O─(C3─C9)циклоалкила, ─арила, ─O─арила, ─O─(C1─C4)алкиларила, гетероарила, гетероциклила, ─O─(C1─C4)алкилгетероцикла, ─(S(=O)2)─(C1─C6)алкила, ─NH─C(=NH)─NH2 (т.е. гуанидино), ─COOH и ─C(=O)─NR5R6, где R5 и R6 независимо выбирают из группы, состоящей из водорода и ─(C1─C6)алкила. Кроме того, применительно к заместителю R7, термин «группа аминокарбоновой кислоты» относится к группе карбоновой кислоты, включая группы карбоновых кислот, замещенные одним или несколькими вышеуказанными заместителями, которые содержат одну или несколько независимо выбранных аминогрупп типа ─NR5R6, где R5 и R6 независимо выбирают из группы, состоящей из водорода и (C1-C6)алкила.
В одном варианте осуществления данного изобретения R7 представляет собой альфа-амино или иминокислоту, включая, но, не ограничиваясь ими, аланин, аргинин, аспарагин, аспартамовую кислоту, цистеин, глутамин, глутаминовую кислоту, глицин, гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин, валин или их стереоизомерные или рацемические смеси. В другом варианте осуществления данного изобретения R7 представляет собой альфа-амино или иминокислоту, выбранную из группы, состоящей из L-аланина, L-аргинина, L-аспарагина, L-аспартамовой кислоты, L-цистеина, L-глутамина, L-глутаминовой кислоты, L-глицина, L-гистидина, L-изолейцина, L-лейцина, L-лизина, L-метионина, L-фенилаланина, L-пролина, L-серина, L-треонина, L-триптофана, L-тирозина, L-валина.
Применительно к заместителю R7, термин «пептид» относится к дипептиду, трипептиду, тетрапептиду или пентапептиду, который при гидролизе высвобождает две, три, четыре или пять амино или иминокислот (например, пролин), соответственно. Применительно к заместителю R7, пептиды связаны с остатком молекулы через сложноэфирную связь. В одном варианте осуществления пептиды R7 состоят из альфа-амино или иминокислот, включая, но, не ограничиваясь ими, аланин, аргинин, аспарагин, аспартамовую кислоту, цистеин, глутамин, глутаминовую кислоту, глицин, гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин, валин или их стереоизомерные или рацемические смеси, и в более предпочтительном варианте данного варианта осуществления карбоксильная группа присоединена сложноэфирной связью к концевой карбоксильной COOH группе пептида в противоположность карбоксилам боковой цепи. В другом варианте осуществления данного изобретения R7 представляет собой альфа-амино или иминокислоту, выбранную из группы, состоящей из L-аланина, L-аргинина, L-аспарагина, L-аспартамовой кислоты, L-цистеина, L-глутамина, L-глутаминовой кислоты, L-глицина, L-гистидина, L-изолейцина, L-лейцина, L-лизина, L-метионина, L-фенилаланина, L-пролина, L-серина, L-треонина, L-триптофана, L-тирозина, L-валина, и в более предпочтительном варианте данного варианта осуществления карбоксильная группа присоединена сложноэфирной связью к концевой карбоксильной COOH группе пептида в противоположность карбоксилам боковой цепи.
1.2. Предпочтительные соединения
В предпочтительные варианты осуществления включены соединения формулы III, IVa, IVb, Va или Vb, где Q выбирают из группы, состоящей из арила, гетероарила, ─O─арила, ─S─арила, ─O─гетероарила и ─S─гетероарила, при условии, что Q не является 3-индолилом или замещенным 3-индолилом. В других предпочтительных вариантах осуществления Q выбирают из группы, состоящей из арила, гетероарила, ─O─арила, ─S─арила, ─O─гетероарила и ─S─гетероарила, при условии, что когда R4 представляет собой водород, циклоалкил или алкил, Q не является 3-индолилом или замещенным 3-индолилом. В других предпочтительных вариантах осуществления Q выбирают из группы, состоящей из арила, гетероарила, ─O─арила, ─S─арила, ─O─гетероарила и ─S─гетероарила, при условии, что когда R4 представляет собой водород, (C3-C4)циклоалкил или (C1-C4)алкил, Q не является 3-индолилом или замещенным 3-индолилом. В другом предпочтительном варианте осуществления Q представляет собой 3-индолил или замещенный 3-индолил, при условии, что R4 не является водородом, циклоалкилом или алкилом. Еще в одном предпочтительном варианте осуществления Q представляет собой 3-индолил или замещенный 3-индолил, при условии, что R4 не является водородом, (C3-C4)циклоалкилом или (C1-C4)алкилом.
Другие предпочтительные варианты осуществления включают соединения формулы IIIa, IVa, IVb, Va или Vb, где R4 представляет собой ─CH2R7. Данные соединения могут служить пролекарственными формами соответствующих соединений формулы IIIa, IVa, IVb, Va или Vb, где R4 представляет собой Н. Пролекарственная форма расщепляется при гидролизе с высвобождением соответствующего соединения, где R4 представляет собой Н. Гидролиз может протекать ферментативным или неферментативным образом, что приводит к соответствующим гидроксиметиленовым производным, которые при последующем гидролизе приводят к высвобождению соединений,