Состав для стабилизации липидов к окислению
Иллюстрации
Показать всеИзобретение относится к области пищевой технологии, а именно к получению состава, стабилизирующего процесс окисления липидов. Состав для стабилизации, включающий в качестве антиоксиданта 4-(N-ацетил)аминофенол (парацетамол), добавляемый в количестве 0,01-0,08% от массы липидов. Изобретение позволяет получить состав, не требующий больших материальных затрат, основанный на способности низкотоксичного антиоксиданта взаимодействовать с пероксильными радикалами и разрушать продукты окислительной деструкции липидов нерадикальным путем. 3 табл., 3 пр.
Реферат
Изобретение относится к области пищевой технологии, а именно к способам защиты липидов, масел, жиров от окисления и окислительной деструкции, и может быть использовано в пищевой, косметической и химико-фармацевтической промышленности для получения стабильных липидосодержащих пищевых добавок (нутрицевтиков), лечебно-косметических средств и лекарственных препаратов.
Для торможения процессов окисления применяют антиоксиданты (ингибиторы окисления), которые находят все более широкое применение для предотвращения окислительных превращений липидов и содержащих их препаратов in vitro, а также in vivo в комплексной терапии широкого круга заболеваний / Герчук М.П. Антиокислители в пищевой промышленности // Журн. Всесоюз. хим. общества им. Д.И. Менделеева. - 1960. - N. 4. - С.395-402. Авакумов В.М., Ковлер М.А., Кругликова - Львова Р.П. Лекарственные средства метаболической терапии на основе витаминов и ферментов (Обзор)// Вопросы мед. химии. - 1992. - Т.38. - N4. - С.14-21. Дурнев А.Д., Середенин С.В. Антиоксиданты как средства защиты генетического аппарата // Хим. - фарм. журн. - 1990. - N2. - С.92-100 /. Таким образом, антиоксиданты, присутствующие в лекарственном или косметическом препарате, являются не только действующим началом этих средств, но могут значительно тормозить их окисление в процессе длительного хранения, способствуя сохранению в нативном состоянии легкоокисляемых биологически активных компонентов. Известны составы для стабилизации липидов к окислению различного происхождения путем введения антиоксидантов токоферолов / US №2564106, кл. 252-404, опубликованный 14.08.1951 /, нафтолов и фенолов / Эмануэль Н.М., Лясковская Ю.Н. Торможение процессов окисления жиров. - М.: Пищепромиздат, 1961. - 360 с. /.
В качестве прототипа выбран состав для стабилизации липидов с помощью синтетического антиоксиданта дибунола (2,6-дитрет.бутил-4-метилфенола), добавляемого в концентрации 0,02-0,2% от массы липидов / Шмулович В.Г. Применение антиоксидантов в России для стабилизации жиров, пищевых и кормовых продуктов // Вопросы питания. 1994. №1/2. С.42-44 /. Недостатком этого состава является необходимость использования высоких концентраций дибунола, что ведет к отдаленным токсическим последствиям / Зарудий Ф.С., Гильмутдинов Г.З., Зарудий Р.Ф. 2,6-Ди-трет-бутил-4-метилфенол (дибунол, ионол, тонарол) - классический антиоксидант (обзор) // Хим. - фарм. журнал. 2001. Т.35. №3. С.42-48 /.
Предлагаемое соединение 4-(N-ацетил)аминофенол (парацетамол) проявляет активность с пероксильными радикалами с константой скорости реакции k7=4,00×104 М-1×c-1, снижает скорость процесса окисления липидов в 5-10 раз, разрушает продукты окислительной деструкции липидов (гидропероксиды) нерадикальным путем на 60-75%, что не наблюдается в присутствии дибунола. Разрушение гидропероксидов под влиянием 4-(N-ацетил)аминофенола, в свою очередь, является причиной выигрыша в периодах индукции.
Задачей настоящего изобретения является разработать состав для стабилизации липидов к окислению с помощью антиоксиданта, обладающего высокой эффективностью и низкой токсичностью.
Технический результат - простой состав, не требующий больших материальных затрат, основанный на способности низкотоксичного антиоксиданта 4-(N-ацетил)аминофенола взаимодействовать с пероксильными радикалами и разрушать продукты окислительной деструкции липидов (гидропероксиды) нерадикальным путем.
Технический результат достигается тем, что к липидам добавляют в качестве антиоксиданта 4-(N-ацетил)аминофенол в количестве 0,01-0,08% от массы липидов.
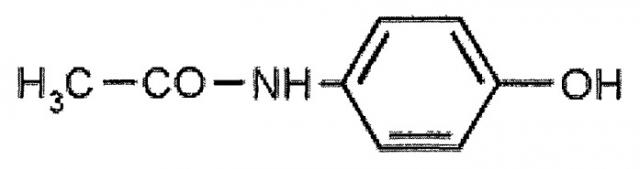
Сущность изобретения заключается в использовании по новому назначению 4-(N-ацетил)аминофенола (парацетамол), химическая структура соединения представлена ниже:
Антирадикальную активность антиоксидантов (АРА) тестировали в системе инициированного окисления этилбензола хемилюминесцентным (ХЛ) методом. Окисление этилбензола проводили в стеклянной ячейке, расположенной в светонепроницаемой камере фотометрической установки, снабженной фотоумножителем ФЭУ-29. Ячейка имеет термостатируемую рубашку. Через ячейку пропускали очищенный от пыли и паров воды воздух. Исследуемое вещество вводили в окислительную ячейку по ходу реакции с помощью шприцевого устройства. Излучаемый свет фокусировался на фотоумножитель с помощью системы сферических зеркал. Окисление инициировалось азо-бис-изобутиронитрилом (АИБН) в концентрации 3×10-3 М при t=(60±0,2)°C. Скорость зарождения свободных радикалов определялась экспериментально с помощь реперного ингибитора - хромана C и составила 2,3×10-8 М×с-1. Для усиления свечения использовался люминофор 9,10-дибромантрацен в концентрации 5×10-4 М, не оказывающий влияния на кинетику окисления. Концентрация ингибитора составляла (1-5)×10-4 М. В ходе эксперимента были получены типичные S-образные кинетические кривые. Основной кинетической характеристикой ХЛ кривых является величина тангенса угла наклона касательной, проведенной в точке перегиба, пропорциональная максимальной скорости расходования антиоксиданта [d(I0/I)/dt]max. Указанную величину использовали для расчетов значения k7 с учетом уравнения [ d ( I 0 / I ) d t ] max = ( 0,22 ± 0,02 ) × k 7 × W i / k 6 , где k6 - константа скорости рекомбинации перекисных радикалов (для этилбензола k6=4,1×108 e-2100/RT).
Антиоксидантную активность (АОА) тестировали волюмометрическим методом поглощения кислорода в модифицированной установке типа Варбурга при окислении метилолеата (МО) в среде инертного растворителя хлорбензола, процесс инициировали за счет термического разложения АИБН в концентрации 3×10-3 М. В качестве критериев оценки антиоксидантных свойств соединений использовали периоды индукции, начальные и максимальные скорости окисления. Графическим методом определяли величину периода индукции (τi), представляющей собой отрезок оси абсцисс, отсекаемый перпендикуляром, опущенным из точки пересечения касательных, проведенных к кинетической кривой. Эффективность торможения процесса окисления липидного субстрата определяется совокупностью реакций ингибитора и обозначает его антиоксидантную активность, количественно определяемую по формуле АОА=τi-τS/τS, где τS и τi - периоды индукции окисления субстрата в отсутствие и в присутствии исследуемого антиоксиданта (АО) соответственно. Критерием антиоксидантного действия служили начальная (WО2 нач) и максимальная (WО2 max) скорости процесса окисления в присутствии и в отсутствие антиоксиданта. Скорость инициирования определяли уравнением Wi=f[InH]/τi, где f - стехиометрический коэффициент ингибирования, [InH] - концентрация реперного ингибитора, τi - период индукции.
Кинетику накопления гидропероксидов в модельном субстрате исследовали в условиях аутоокисления методом обратного йодометрического титрования в среде хлорбензола при t=(60±0,2)°C. Навеску окисляемого модельного субстрата растворяли в смеси ледяной уксусной кислоты и хлороформа в соотношении 3:2, добавляли насыщенный на холоду иодид калия, смесь перемешивали и оставляли в темноте. Через равные промежутки времени отбирали пробы и определяли в них перекисное число: П Ч = 0,1269 × ( a − b ) d ; где a - объем Na2S2O3, пошедший на титрование пробы; b - объем Na2S2O3, пошедший на титрование контрольного опыта; d - масса навески субстрата окисления.
Сущность изобретения иллюстрируется следующими примерами:
Пример 1
Берут 1 г (точная навеска) этилбензола, добавляют 4-(N-ацетил)аминофенол в количестве 0,01% от массы липидов, помещают в ячейку хемилюминометра, добавляют 3×10-3 М азо-бис-изобутиронитрила (АИБН) и перемешивают с использованием магнитной мешалки. Окисление проводят кислородом воздуха при температуре t=(60±0,2)°C. Эффективность действия соединения определяют по значению константы скорости взаимодействия антиоксиданта с пероксильными радикалами k7 и величине стехиометрического коэффициента ингибирования f. В аналогичных условиях определяют эффективность дибунола, выбранного в качестве прототипа (Табл.1).
Показано, что величина антирадикальной активности для 4-(N-ацетил)аминофенола выше в 2,9 раза, чем для прототипа.
Значения константы скорости реакции антиоксидантов с пероксильными радикалами R O 2 •
Wi=2,3×10-8 M×c-1; t=60°
| Таблица 1 | |||
| Название *АО | Содержание *АО, мас.% | k7×104, М-1×c-1 | f |
| Дибунол (2,6-дитрет.бутил-4-метилфенол) (Прототип) | 0,01 | 1,4 | 2,0 |
| 4-(N-ацетил)аминофенол (парацетамол) | 0,01 | 4,0 | 2,4 |
Пример 2
Берут 1 г (точная навеска) метилолеата (МО) и помещают в манометрическую ячейку, добавляют 4-(N-ацетил)аминофенол в количестве 0,03% от массы липидов, 0,5 мл 3×10-3 М инициатора окисления АИБН, доводят хлорбензолом до общего объема пробы 2 мл. Поглощение кислорода оценивают волюмометрическим методом в термостатированной установке типа Варбурга при температуре t=(60±0,2)°C при перемешивании на магнитной мешалке. Измеряют объем (мм3) поглощенного кислорода во времени, строят график в координатах dV/dt. Графическим методом из кинетических кривых определяют величину периода индукции (τi). Из наклона кинетических кривых определяют начальную (WO2 нач) и максимальную (WO2 max) скорости окисления липидного субстрата в контрольном опыте и с добавками антиоксидантов. Показатели сравнивают с прототипом (Табл.2).
Кинетические параметры окисления метилолеата в безводной среде в присутствии 3×10-3 М АИБН в зависимости от концентрации 4-(N-ацетил)аминофенола и дибунола (прототип), Wi=4,2×10-8 М×c-1, t=60°C
| Таблица 2 | |||||
| № п/п | Содержание АО*, мас.% | τ, мин | WO2нач×10-7, М×c-1 | WO2max×10-7, М×c-1 | |
| Субстрат окисления - метилолеат (контроль) | |||||
| 1 | 0 | 0 | 1,90 | 8,00 | 1 |
| Дибунол (прототип) | |||||
| 2 | 0,03 | 190 | 0,68 | 6,3 | 1,3 |
| 3 | 0,05 | 380 | 0,69 | 6,2 | 1,3 |
| 4 | 0,08 | 570 | 0,67 | 6,4 | 1,3 |
| 4-(N-ацетил)аминофенол (парацетамол) | |||||
| 5 | 0,01 | 130 | 0,65 | 1,40 | 5,7 |
| 6 | 0,03 | 220 | 0,57 | 1,30 | 6,2 |
| 7 | 0,05 | 425 | 0,50 | 1,16 | 6,9 |
| 8 | 0,08 | 625 | 0,31 | 0,66 | 12,1. |
Пример 3
Берут 10 г (точная навеска) линолевой кислоты (ЛК), добавляют 4-(N-ацетил)аминофенол в количестве 0,03% от массы липидов, перемешивают магнитной мешалкой в светонепроницаемой термостатированной ячейке при температуре t=(60±0,2)°C. Через равные промежутки времени отбирают пробы и определяют в них перекисное число (ПЧ) (Табл.3).
Величины начальной, максимальной скоростей поглощения кислорода при инициированном окислении метилолеата (МО), разрушения гидропероксидов при аутоокислении линолевой кислоты (ЛК) в присутствии 4-(N-ацетил)аминофенола и дибунола (прототип), t=60°C
| Таблица 3 | |||||
| Состав смеси | Инициированное окисление МО, Wi=4,2×10-8 М×c-1 | Аутоокисление ЛК | Процент разрушения ROOH за 7 часов | ||
| WO2 нач×10-7 М×c-1 | WO2 max×10-7 М×c-1 | W накопления ROOH×10-4; гI2/100 г лип.*×c-1 | W разрушения ROOH×10-4, гI2/100 г лип.*×c-1 | ||
| ЛИПИДЫ (контроль) | 1,90 | 8,00 | 5,52 | - | - |
| ЛИПИДЫ + дибунол (0,03 мас.%) (прототип) | 0,68 | 6,3 | 5,52 | - | - |
| ЛИПИДЫ + 4-(N-ацетил)аминофенол (0,03 мас.%) | 0,57 | 1,30 | - | 4,50 | 75,4 |
Состав для стабилизации липидов к окислению, включающий антиоксидант, отличающийся тем, что в качестве антиоксиданта использован 4-(N-ацетил)аминофенол (парацетамол), добавляемый в количестве 0,01-0,08% от массы липидов.