Способ создания биоинженерного каркаса легкого крысы
Иллюстрации
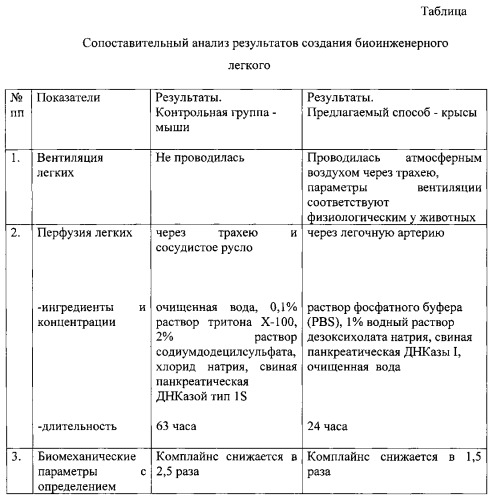
Показать всеИзобретение относится к медицине, а именно к созданию биоинженерного органа, и может быть использовано в трансплантологии. Способ создания биоинженерного каркаса легкого крысы включает перфузию легкого детергентно-энзиматическим методом, контроль качества каркаса гистологическим исследованием. На фоне постоянной соответствующей физиологическим параметрам вентиляции легких атмосферным воздухом через трахею в течение 24 часов осуществляют через легочную артерию перфузию легких путем последовательного воздействия децеллюляризирующих растворов. Для этого с равной продолжительностью воздействия используют фосфатный буфер, 1% водный раствор дезоксихолата натрия, свиную панкреатическую ДНКазу I, очищенную воду. После чего для обеспечения качества последующей рецеллюляризации с помощью колориметрического метода подтверждают биосовместимость созданного каркаса легкого, жизнеспособность, а также сохранность его архитектоники путем определения его биомеханической прочности на растяжение и сжатие, фиксируя легочный комплайнс. Способ обеспечивает сохранение структуры матрикса легкого и его качества, исключает риск контаминации. 1 табл.
Реферат
Предлагаемое изобретение относится к медицине, а именно к регенеративной медицине, и может быть использовано в клеточной биологии, молекулярной биологии, торакальной хирургии для создания биоинженерного органа в качестве трансплантата.
Трансплантация органов является эффективным методом лечения пациентов, страдающих заболеваниями в терминальной стадии, но, к сожалению, она связана с постоянным недостатком донорских органов, необходимостью пожизненной иммуносупрессивной терапии, имеет высокий процент смертности, а также по этическим соображениям пересадка органов не проводится во многих странах [Fuchs J.R. et al., 2001]. Это вызывает потребность в новых способах лечения для восстановления или замещения поврежденных органов и тканей, что позволит избежать сложностей, связанных с аллогенной трансплантацией. Многообещающей стратегией в репарации или замещении поврежденных органов и тканей является тканевая инженерия [Ott Н.С.et al., 2008]. Тканевая инженерия включает в себя разработку и модификацию биологических (природных) или искусственных каркасов (носителей), а также оценку и поддержание жизнеспособности клеток или тканей, взаимодействующих с ними. С целью исключения иммунных реакций биологические каркасы должны быть децеллюляризированы, но при этом сохранять исходную структуру ткани и внеклеточного матрикса (ВКМ). Известно, что децеллюляризация - это процесс, направленный на удаление клеток из ткани с сохранением ВКМ и трехмерности структуры органа [Ott Н.С.et al., 2008; Badylak S.F. et al., 2011]. Исследования по созданию естественных каркасов методом децеллюляризации ведутся для следующих органов: трахеи, пищевода, сердца, легких, скелетной мышцы, диафрагмы и др. [Atala А., 2009; Ott Н.С.et al., 2008; Badylak S.F. et al., 2011; Conconi M.T. et al., 2005; Macchiarini P. et al., 2008].
С учетом высокой смертности от хронических заболеваний дыхательной системы, весьма актуальной является разработка способа создания биоинженерного легкого.
В частности, известен способ децеллюляризации органокомплекса легких мыши [Price А.Р., England К.А. et al. Development of a decellularized lung bioreactor system for bioengineering the lung: the matrix reloaded. Tissue Eng. Part A 2010; 16: 2581-91]. Протокол включает в себя перфузию легких мыши через трахею и сосудистое русло очищенной водой, детергентами и ферментами: 0,1% раствором тритона Х-100, 2% раствором содиумдодецилсульфата, хлоридом натрия, свиной панкреатической ДНКазой типа 1S в течение 63 часов. Контроль качества полученного каркаса определяли гистологическими методами и регистрацией эластических свойств.
Основными недостатками данного способа являются повреждение гистологической структуры альвеол легких вследствие перфузии через дыхательные пути и воздействия высоких концентраций детергентов, а также длительность проведения децеллюляризации, повышающая риск бактериальной контаминации. Способ предусматривает контроль получаемого биоинженерного каркаса легкого только по данным гистологического исследования и по оценке эластических свойств каркаса. Также в данном протоколе децеллюляризацию проводят на модели легких мыши, что, в связи с физиологическими отличиями животных, не может транслироваться на модель крысы без изменений и дополнений.
За ближайший аналог принят способ проведения децеллюляризации легких крысы [Ott Н.С., Clippinger В., Conrad С.et al. Regeneration and orthotopic transplantation of a bioartificial lung. Nat. Med. 2010; 16: 927-33], заключающийся в проведении физиологической ретроградной перфузии легких через легочную артерию фосфатным буфером (PBS) с добавлением гепарина и антибиотиков, деионизированной водой и растворами детергентов: 0,1% содиумдодецилсульфата и тритона Х-100 в течение 72 часов. Контроль качества проводился путем гистологического исследования, анализа морфологической структуры и механических свойств полученного каркаса.
Основным недостатком данного способа является длительность проведения децеллюляризации, создающая угрозу бактериальной контаминации каркаса.
Задачи: максимальное сохранение гистологической структуры внеклеточного матрикса легкого, обеспечение щадящего режима обработки биологического материала, снижение концентраций детергентов, физиологическая вентиляция легких, снижение времени экспозиции растворов и вероятности бактериальной контаминации получаемого каркаса, т.е. повышение качества получаемого биоинженерного материала и обеспечение контроля его качества.
Сущностью предложенного изобретения является то, что на фоне постоянной соответствующей физиологическим параметрам вентиляции легких атмосферным воздухом через трахею перфузию легочной артерии в течение 24 часов осуществляют путем последовательного воздействия через легочную артерию децеллюляризирующих растворов: фосфатного буфера; 1% водного раствора дезоксихолата натрия; свиной панкреатической ДНКазы I; очищенной воды с равной продолжительностью приемов воздействия, после чего для обеспечения качества последующей рецеллюляризации с помощью колориметрического метода подтверждают биосовместимость созданного биоинженерного каркаса легкого крысы, жизнеспособность клеток на каркасе, сохранность архитектоники полученного каркаса путем использования методов рутинного гистологического исследования и определения его биомеханической прочности на растяжение и сжатие, фиксируя легочной комплайнс.
Технический результат способа состоит в повышении качества получаемого материала каркаса, отсутствии бактериальной контаминации каркаса, полном нивелировании негативных эффектов известных способов того же назначения. Для достижения указанного результата использовались сниженные концентрации и сокращенное время экспозиции перфузионных растворов, а также применение физиологической вентиляции легких при проведении децеллюляризации (параметры вентиляции соответствуют естественным у животных - крыс). Ранее использовавшиеся протоколы повреждали паренхиму легких и несли высокий риск развития бактериальной контаминации, что крайне неблагоприятно сказывается на качестве полученного каркаса легкого и возможности последующего создания биоинженерного органа. Кроме того, способ предусматривает контроль качества получаемого биоинженерного каркаса легкого на жизнеспособность, совместимость, адекватность трансплантата планируемому реципиенту.
Способ создания биоинженерного легкого крысы осуществляют следующим образом: проводят забор органокомплекса «сердце-легкие» после эвтаназии крысы с соблюдением этических норм, фиксируют органокомплекс в биореакторе, выполняют децеллюляризацию легких детергентно-энзиматическим методом в течение 24 часов на фоне постоянной вентиляции трахеи атмосферным воздухом путем последовательного воздействия децеллюляризирующих растворов: фосфатного буфера; 1% водного раствора дезоксихолата натрия (неионного детергента щадящего действия, разрушающего клеточные мембраны и способствующего лизису клеток для получения каркаса легкого); свиной панкреатической ДНКазы I; очищенной воды с равной продолжительностью воздействия. Контроль качества полученного биоинженерного каркаса осуществляют методами рутинного гистологического исследования и определения предельных биомеханических параметров на растяжение и сжатие для подтверждения сохранности архитектоники внеклеточного матрикса легких и отсутствия клеточных элементов на легочном каркасе, а также использованием регистрации биомеханических данных с целью обеспечения соответствия биомеханических свойств имплантата реципиенту дополнительной регистрацией легочного комплайнса при моделировании физиологических условий для установления сохранной способности легких к растяжению и сжатию. Определение легочного комплайнса включает в себя регистрацию величин дыхательного объема, давления плато, пикового дыхательного объема легких, давление в легочной артерии и грудной полости. Жизнеспособность клеток на полученном каркасе определяют путем колориметрического анализа с использованием ХТТ-реагента в целях установления биосовместимости полученного каркаса и проведения последующих экспериментов по рецеллюляризации. Колориметрический анализ проводится согласно рекомендациям в инструкции производителя.
Способ апробирован в течение 2 лет на биологическом материале (органокомплекс «сердце-легкие») экспериментальных животных (крысах). Результаты полностью подтвердили решаемые задачи. Получены естественные матриксы органов с сохранным внеклеточным матриксом и отсутствием клеточных структур.
Данный способ создания биоинженерного легкого использован в эксперименте на 30 крысах-самцах линии Lewis. Выполнены забор и фиксация в биореакторе органокомплекса «сердце-легкие» с последующей децеллюляризацией легких по предлагаемому способу. Пример: забор органокомплекса «сердце-легкие» проведен у крысы-самца линии Lewis весом 200 г после проведенной эвтаназии передозировкой наркотических средств в соответствии с этическими требованиями. Органокомплекс фиксирован в биореакторе. Начата децеллюляризация легких: на фоне постоянной вентиляции трахеи атмосферным воздухом в течение 24 часов проводили последовательную перфузию легочной артерии децеллюляризирующими растворами: фосфатным буфером; 1% водным раствором дезоксихолата натрия; свиной панкреатической ДНКазой I; очищенной водой с равной продолжительностью приемов воздействия. Контроль качества полученного биоинженерного каркаса осуществляли методами рутинного гистологического исследования (окрашивание гематоксилин-эозином, трихромом по Массону, окрашивание по Ван Гизон), а также путем определения предельных биомеханических параметров на растяжение и сжатие с дополнительной регистрацией легочного комплайнса при моделировании физиологических условий. Определение легочного комплайнса включает в себя регистрацию величин дыхательного объема, давления плато, пикового дыхательного объема легких, давление в легочной артерии и грудной полости на всем протяжении децеллюляризации во время моделирования вдоха и выдоха у животного. Жизнеспособность клеток на полученном каркасе определяли путем колориметрического анализа с использованием ХТТ-реагента с целью определения биосовместимости полученного каркаса и проведения последующих экспериментов по рецеллюляризации. Колориметрический анализ проводится согласно рекомендациям в инструкции производителя. В результате экспериментов по децеллюляризации получен каркас легких с сохранением гистологической архитектоники и белков внеклеточного матрикса. Вышеуказанный каркас при проведении колориметрического анализа продемонстрировал биосовместимость и нетоксичность по отношению к клеткам, которым он был засеян.
Способ создания биоинженерного каркаса легкого крысы, включающий перфузию легкого детергентно-энзиматическим методом, контроль качества каркаса гистологическим исследованием, отличающийся тем, что на фоне постоянной соответствующей физиологическим параметрам вентиляции легких атмосферным воздухом через трахею перфузию легочной артерии в течение 24 часов осуществляют путем последовательного воздействия через легочную артерию децеллюляризирующих растворов: фосфатного буфера; 1% водного раствора дезоксихолата натрия; свиной панкреатической ДНКазы I; очищенной воды с равной продолжительностью воздействия, после чего для обеспечения качества последующей рецеллюляризации с помощью колориметрического метода подтверждают биосовместимость созданного биоинженерного каркаса легкого крысы, жизнеспособность, сохранность архитектоники полученного каркаса путем определения его биомеханической прочности на растяжение и сжатие, фиксируя легочный комплайнс.