Аминоамиды в ряду бактериохлорофилла альфа, обладающие фотодинамической активностью, и способ их получения
Иллюстрации
Показать всеИзобретение относится к аминоамидам в ряду бактериохлорофилла а общей формулы:
где n=2,4,8,10, обладающим фотоиндуцированной противоопухолевой активностью, и к способу их получения путем взаимодействия метилового эфира бактериофеофорбида а с диаминоалканом формулы NH2(CH2)nNH2, где n=2, 4, 8, 10, в пиридине. Техническим результатом является получение высокоэффективных фотосенсибилизаторов, аминоамидов в ряду бактериохлорофилла а, на основе бактериохлорина е, обладающих высокой фотоиндуцированной противоопухолевой активностью. 2 н.з. п. ф-лы, 4 ил., 11 пр.
Реферат
Настоящее изобретение относится к химии биологически активных соединений, конкретно к новому классу соединений - аминоамидам бактериохлорофилла а или бактериоаминоамидам, которые имеют интенсивное поглощение в ближней ИК-области, обладают химической и фотостабильностью, а также улучшенными гидрофильными свойствами за счет протонирования терминальной аминогруппы, что позволяет рассматривать их в качестве перспективных фотосенсибилизаторов (ФС) для фотодинамической терапии рака.
В клиниках ряда стран мира (США, Германии, Израиле, Канаде, России и др.) в течение последних 20 лет в онкологии активно применяются методы флуоресцентной диагностики (ФД) и фотодинамической терапии (ФДТ) опухолей, которые основаны на фотофизических и фотохимических эффектах, возникающих при облучении введенных в организм фотосенсибилизаторов светом определенной длины волны. Несомненным преимуществом фотодинамической терапии перед другими консервативными методами лечения злокачественных новообразований является локальность воздействия на опухоль, которая обеспечивается повышенной концентрацией фотосенсибилизатора в опухолевом очаге и направленным световым воздействием.
Клинические испытания метода ФДТ свидетельствуют о его эффективности при тяжелых дисплазиях, начальных поверхностно расположенных опухолях различной локализации у онкологических больных с тяжелой сопутствующей патологией.
Основное ограничение метода ФДТ связано с глубиной его воздействия. Используемые в клинике препараты имеют спектр фотодинамического воздействия с максимумами поглощения в области 630-675 нм. Проницаемость биологических тканей в этом диапазоне незначительна и составляет не более 1 см. Это часто приводит к частичной деструкции опухолевого очага, что впоследствии обусловливает продолженный рост опухоли. К недостаткам фотосенсибилизаторов первого поколения (Фотогем, Россия; Фотофрин, США; Фотосан, Германия) также следует отнести длительное время циркуляции в организме и выраженную кожную фототоксичность.
Создание и внедрение новых фотосенсибилизаторов, поглощающих в дальней красной области спектра - «окне проницаемости» биологических тканей, может расширить сферу применения ФДТ. Поэтому на протяжении последнего десятилетия проводится активный поиск новых высокоэффективных фотосенсибилизаторов, а также изучение их фотоиндуцированной активности in vitro и in vivo. Фотосенсибилизаторы природного происхождения легко выводятся из организма и быстро подвергаются биодеградации, что существенно снижает побочные эффекты ФДТ.
В ряду хлорофилла а исследована фотодинамическая активность хлорина е6 (Хл е6) и его аминоамидного производного (ЭДА-Хл е6), содержащего в положении 13 хлоринового макроцикла остаток этилендиамина [J.Photochem. Photobiol.B: Biol., 1992]. Было показано, что эффективность фототерапии с аминоамидом хлорина е6 значительно выше по сравнению с незамещенным хлорином. В биологических испытаниях на животных-опухоленосителях коэффициент селективности накопления ЭДА-Хл е6 в опухоли составляет 20, тогда как для Хл е6 он не превышает 3, что объясняется высокой аффинностью аминоамидного производного Хл е6 к липопротеинам низкой плотности в кровотоке и направленной доставкой подобных конъюгатов в опухолевую ткань.
Известны фотосенсибилизаторы 1, представляющие собой соли эфиров моноамида хлорина е6. Известен также способ их получения и способ ФДТ, включающий системное введение фотосенсибилизатора и облучение патологического участка оптическим излучением в спектральном диапазоне 655-662 нм. Вышеуказанные фотосенсибилизаторы и способ фотодинамической терапии с их участием являются ближайшими аналогами настоящего изобретения [Патент РФ 2416614].
Однако недостаточная глубина проникновения света в ткани у производных хлорофилла а ограничивает их использование в качестве фотосенсибилизаторов.
Из фотосенсибилизаторов хлоринового ряда в России применяются препараты «Фотодитазин» (662 нм) и «Радахлорин» (662 нм), в Республике Беларусь - «Фотолон» (660 нм), которые являются производными хлорофилла а.
В последние годы активно разрабатываются препараты, имеющие полосы поглощения в спектральной области так называемого «терапевтического окна прозрачности» (700-900 нм), где поглощение света биологическими тканями минимальное. Эти ФС относят к третьему поколению наряду с препаратами, включающими векторные молекулы, наночастицы или липосомы с целью улучшения селективности накопления ФС в опухолевых клетках.
Технический результат изобретения - получение высокоэффективных фотосенсибилизаторов, аминоамидов в ряду бактериохлорофилла а, на основе бактериохлорина е с улучшенными спектральными свойствами, обладающих высокой фотоиндуцированной противоопухолевой активностью в системах in vitro и in vivo, обеспечивающих излеченность животных-опухоленосителей, селективное накопление в опухоли и быстрое выведение из организма млекопитающих.
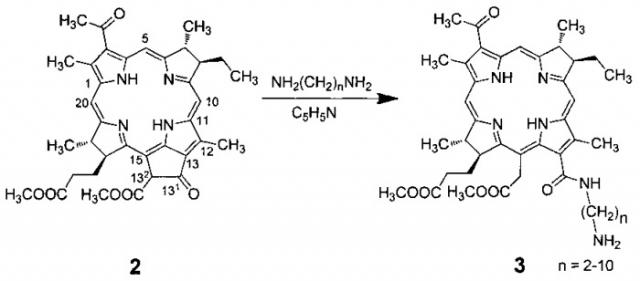
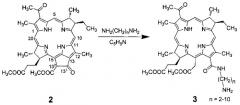
Технический результат достигается обработкой метилового эфира бактериофеофорбида а 2 диаминоалканом формулы NH2(CH2)nNH2, где n=2, 4, 8, 10. Исходный бактериофеофорбид а получают из бактериохлорофилл/каротиноидной смеси, выделенной из биомассы бактерий Rhodobacter Capsulata, путем двухстадийного кислотного гидролиза этой смеси 15% соляной и 80% трифторуксусной кислот. В качестве фотосенсибилизаторов предлагаются бактериоаминоамиды 3 (метиловый эфир 131-(ω-аминоалкилкарбомоил)бактерихлорина е) общей формулы:
Под действием нуклеофилов пентаноновый экзоцикл в бактериофеофорбиде легко раскрывается с разрывом связи С(131)-С(132). Раскрытие экзоцикла обусловлено наличием стерически доступного нуклеофильного центра при атоме углерода С(131). Механизм раскрытия экзоцикла без участия кислорода представляет собой катализируемое основанием нуклеофильное присоединение к 131-карбонильной группе бактериофеофорбида, который трансформируется в соответствующий 131-карбоксамид. Эффективность аминолиза экзоцикла определяется основностью используемого амина и стерическими эффектами при координации нуклеофильного центра 131 с азотсодержащими нуклеофилами.
Реакция протекает по схеме:
Предлагаемый способ заключается в следующем.
К раствору метилового эфира бактериофеофорбида а в пиридине добавляют диаминоалкан формулы NH2(CH2)nNH2, где n=2, 4, 8, 10, в 10-кратном мольном избытке и перемешивают при комнатной температуре в течение 2 часов. За ходом реакции следят по изменениям в спектрах поглощения и хроматографической подвижности. Раскрытие циклопентанонового фрагмента в молекуле бактериофеофорбида сопровождается незначительным гипсохромным смещением длинноволновой полосы поглощения с 760 нм до 754 нм, тогда как хроматографическая подвижность продукта реакции сильно снижается (Rf=0.3) по сравнению с исходным пигментом (Rf=0.7).
Полученный раствор разбавляют хлороформом, к нему добавляют 0.1 N раствор HCl и переносят в делительную воронку. Органический слой отделяют, промывают раствором гидрокарбоната натрия, высушивают сульфатом натрия и упаривают. Продукт перекристаллизовывают из петролейного эфира.
Отличительными признаками заявляемых производных бактериохлорофилла а и способа их получения являются:
1) использование в качестве исходного соединения бактериофеофорбида, что позволяет получать бактериоаминоамиды с поглощением в области 750-755 нм;
2) использование в синтезе бактериоаминоамидов диаминоалканов формулы NH2(CH2)nNH2, где n=2, 4, 8, 10, что позволяет направленно регулировать амфифильные свойства целевых пигментов;
3) наноструктурированная водная дисперсия на основе бактериоаминоамидов химически и фотостабильна;
4) наноструктурированная водная дисперсия на основе бактериоаминоамидов обладает высокой фотоиндуцированной активностью по отношению к опухолевым клеткам человека различного генеза при отсутствии темновой токсичности;
5) наноструктурированная водная дисперсия на основе бактериоаминоамидов при ФДТ приводит к увеличению продолжительности жизни (от 55 до 180%) и излеченности животных (от 30 до 100%);
6) наноструктурированная водная дисперсия на основе бактериоаминоамидов быстро выводится из организма млекопитающих, в том числе из кожи и мышц в течение 72 часов после введения ФС.
Строение полученных соединений доказано электронной, ИК-,1Н ЯМР - спектроскопией, а также подтверждено данными матричной лазерно-активируемой масс-спектрометрии (MALDI).
Оценку фотоиндуцированной активности проводили:
- в системе in vitro на опухолевых клетках человека различного эпителиального происхождения: эпидермоидной карциномы гортаноглотки (НЕр2) и аденокарциномы легкого (А549);
- в системе in vivo на мышах с саркомой 37 (S37).
Предлагаемое изобретение иллюстрируется нижеследующими примерами, но не ограничивается ими.
Пример 1. Получение метилового эфира 131-(4-аминобутилкарбомоил) бактериохлорина е (3, n=4).
К раствору 20 мг (0,03 ммоль) метилового эфира бактериофеофорбида а в 4 мл пиридина прибавляли 0,033 мл (0,3 ммоль) диаминобутана. Полученный раствор перемешивали в течение 6 часов при комнатной температуре. Ход реакции контролировали спектрофотометрически и при помощи тонкослойной хроматографии (ТСХ). Реакционную смесь переносили в делительную воронку, добавляли хлороформ (50 мл) и 0,1N раствор соляной кислоты (100 мл). Органический слой отделяли, промывали водным раствором гидрокарбоната натрия, сушили над безводным сульфатом натрия, упаривали на роторном испарителе при температуре 35-40°C. Продукт очищали с помощью препаративной ТСХ на силикагеле в системе хлороформ-метанол с градиантом концентрации метанола от 0,5 до 40%.
Выход соединения 3 (n=4) составил 19 мг (85%). Электронный спектр, λmax, нм (ε х 10-3, М-1см-1): 400 (100), 522 (55), 754 (68). Масс-спектр (MALDI), m/z:712,3 (М+).
Данные ядерно-магнитного резонанса 1Н ЯМР (300 МГц, CDCl3, δ, м.д.): 9.25 (Н, с, 5-Н), 8.63 (Н, с, 10-Н), 8.46 (Н, с, 20-Н), 5.15 и 4.89 (2Н, д, J=19 Гц, 151-Н), 4.27 (Н, м, 7-Н), 4.16 (Н, м, 18-Н), 4.13 (Н, м, 17-Н), 4.01 (Н, м, 8-Н), 3.62 (3Н, с, 153-Н), 3.55 (3Н, с, 174-Н), 3.40 (3Н, с, 21-Н), 3.10 (3Н, с, 121-Н), 2.92 (3Н, с, 32-Н), 2.47 и 2.19 (2Н, м, 172-Н), 2.31 и 1.93 (2Н, м, 81-Н), 2.03 и 1.77 (2Н, м, 171-Н), 1.74 (3Н, д, J=7 Гц, 71-Н), 1.57 (3Н, д, J=7 Гц, 181-Н), 1.26 (8Н, м, 133-136-Н), 1.04 (3Н, т,J=7Гц, 82-Н).
Протоны при аминогруппах: 6.68 (Н, т, 132-NH), 5,88 (2Н, т, 137-NH), 2.15 (2Н, с, индол).
Пример 2. Получение метилового эфира 131-(2-аминоэтилкарбомоил) бактериохлорина е (3, n=2).
Аналогично пр. 1 реакцию проводили 4 часа.
Выход соединения 3 (n=2) составил 20 мг (93%). Электронный спектр, λmax, нм (ε х 10-3, М-1см-1): 400 (100), 522 (55), 754 (68). Масс-спектр (MALDI), m/z:684,2 (М+).
Пример 3. Получение метилового эфира 131-(8-аминооктилкарбомоил) бактериохлорина е (3, n=8).
Аналогично пр. 1 реакцию проводили 36 часов.
Выход соединения 3 (n=8) составил 16 мг (66%). Электронный спектр, λmax, нм (ε х 10-3, M-1см-1): 400 (100), 522 (55), 754 (68). Масс-спектр (MALDI), m/z:768,7 (М+).
Пример 4. Получение метилового эфира 131-(8-аминодецилкарбомоил) бактериохлорина е (3, n=10).
Аналогично пр. 1, реакцию проводили 48 часов.
Выход соединения 3 (n=10) составил 14 мг (53%). Электронный спектр, λmax, нм (ε х 10-3, М-1см-1): 400 (100), 522 (55), 754 (68). Масс-спектр (MALDI), m/z: 797,0 (М+).
Пример 5. Получение наноструктурированной водной эмульсии метилового эфира 131-(4-аминобутилкарбомоил) бактериохлорина е с использованием Кремофора EL.
Растворяли 5 мг метилового эфира 131-(4-аминобутилкарбомоил) бактериохлорина е в 0.25 мл Кремофора EL. К полученному раствору добавляли 0.9% раствор хлористого натрия до концентрации 1 мг/мл при перемешивании при комнатной температуре. Полученный объем фильтровали через мембранный фильтр «Millipore» с размером пор 0.22 мкм.
Пример 6. Оценка фотостабильности наноструктурированной водной дисперсии метилового эфира 131-(4-аминобутилкарбомоил)бактериохлорина е (3, n=4) на основе Кремофора в бесклеточной среде.
Оценку фотовыцветания проводили в среде Игла MEM, содержащей 10% эмбриональной телячьей сыворотки (ЭТС). Концентрация раствора составляла 7 мкМ. Раствор облучали полихроматическим светом. В качестве источника света использовали галогеновую лампу с широкополосным фильтром КС-13 (λmax≥640 нм) и водным фильтром толщиной 5 см. Световая доза составляла 5 и 10 Дж/см2 при плотности мощности 11,4 мВт/см2. Измерения флуоресценции проводили контактным способом на лазерном спектральном анализаторе «ЛЭСА-06» (ТОО «БиоСпек», Россия) в спектральном диапазоне 649-950 нм. Флуоресценцию возбуждали излучением He-Ne лазера (длина волны генерации 632,8 нм). Спектры флуоресценции регистрировали сразу после приготовления раствора и после облучения.
При облучении красителя не происходит сдвига максимума флуоресценции (λmах=753±3 нм), интенсивность флуоресценции при дозе 10 Дж/см2 снижается не более чем на 15% без изменений в профиле спектра относительно максимального значения, полученного ех tempore, что свидетельствует о его стабильности при воздействии светом (Фиг.1).
Пример 7. Накопление и распределение наноструктурированной водной дисперсии метилового эфира 131-(4-аминобутилкарбомоил)бактериохлорина е (3, n=4) на основе кремофора в клетках А549.
Накопление, распределение и локализация соединений в клетках А549 были изучены методами конфокальной микроскопии и реконструкции спектральных изображений (КОМИРСИ) и лазерной сканирующей конфокальной микроскопии (ЛСКМ).
Конфокальные спектральные изображения клеток, а также спектры флуоресценции калибровочных растворов измеряли с помощью экспериментальной установки для микроспектрального конфокального анализа на основе спектрографа OMARS-89 (Dilor, Франция), микроскопа Olympus ВН-2 (Япония) и предметного столика с электронной системой микропозиционирования (Marzhauser-Wetziar, Германия). В качестве системы детекции использовали прибор с зарядовой связью (1024×256 элементов) с воздушным Пельте охлаждением (Wright Instruments LTD, Англия).
Возбуждение флуоресценции осуществляли, облучая образец лазером с длиной волны 532 нм (12 мкВт). Полученные спектры флуоресценции представлялись в виде суммы модельных спектров: аутофлуоресценции в клетке, базовой линии, обусловленной особенностями прибора и флуоресценции исследуемого соединения, измеренной в 1% CrEL. По полученным спектральным изображениям определяли среднюю интенсивность флуоресценции в цитоплазме клетки. Среднюю цитоплазматическую концентрацию соединения (Сцит) рассчитывали по формуле:
Сцит - (Iцит×Ск×tk)/(Ik×t),
где Iцит, Ik - средняя интенсивность флуоресценции в цитоплазме клетки и интенсивность калибровочного спектра соответственно, Ск - концентрация вещества при снятии калибровочного спектра флуоресценции, t, tk - время накопления спектра в отдельной точке в эксперименте и при измерении калибровочного спектра соответственно.
Коэффициенты накопления (К) рассчитывали по формуле:
К=Сцит/Свнеш,
где Свнеш - концентрация соединения во внешней среде. В каждой выборке обрабатывалось и усреднялось 20-30 клеток.
Внутриклеточное распределение соединений изучали с помощью конфокального лазерного сканирующего микроскопа SP2-4Pi (Leica, Германия). Конфокальные флуоресцентные изображения получали с использованием 100× маслоиммерсионного объектива (планапохромат, числовая апертура 1,46) и лавинного фотодиода в качестве детектора. Латеральное разрешение составляло 0,3 мкм, аксиальное разрешение - 1,5 мкм. Флуоресценцию соединений возбуждали Ar+-лазером (514 нм) и регистрировали в области 700-850 нм.
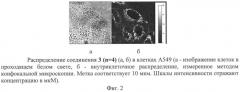
Методом ЛСКМ установлено, что соединение эффективно проникает в клетки А549 и накапливается в цитоплазматической области. Происходит концентрирование в везикулярных клеточных структурах субмикронного размера, а также диффузное окрашивание цитоплазмы, которое усиливается в околоядерной области (Фиг.2). Соединение в ядро клетки не проникает и не накапливается в плазматической мембране.
Согласно результатам микроспектральных исследований внутриклеточные спектры флуоресценции одинаковы по форме и максимуму во всех участках цитоплазматической области и совпадают со спектрами флуоресценции в 1% CrEL. Это позволяет предположить, что данные соединения накапливаются в клетке в липидоподобном окружении.
Нами были определены коэффициенты внутриклеточного накопления (отношение внутриклеточной концентрации соединения к его концентрации в инкубационной среде). При этом клетки инкубировали с соединением 3 (n=4) в концентрации 0,5 мкМ в течение 2 часов. Коэффициент внутриклеточного накопления составляет 65.
Пример 8. Фотоиндуцированная активность наноструктурированной водной дисперсии метилового эфира 131-(4-аминобутилкарбомоил)бактериохлорина е (3, n=4) на основе кремофора в отношении клеток культуры Нер2.
Оценку фотоиндуцированной активности проводили при варьировании концентрации и времени инкубации от 30 минут до 6 часов. Исследования проводили как с удалением фотосенсибилизатора перед облучением, так и без удаления ФС, что позволяет нам также говорить о накоплении красителей в клетке.
Клетки рассеивали в лунки плоскодонного 96-луночного микропланшета (Costar, США) в концентрации 7×104 кл/мл. Соединения вносили через 24 часа после посева клеток, варьируя концентрацию от 8 до 700 нМ. Облучение проводили галогеновой лампой с использованием широкополосного фильтра КС-13 (λmах≥640 нм) и водного фильтра толщиной 5 см. Уровень ингибирования роста клеток в культуре вычисляли по формуле:
ИР(%)=[(Пк-По)/Пк]×100%,
где ИР - ингибирование роста клеток культуры, в процентах;
Пo и Пк - число жизнеспособных клеток, выраженное в единицах оптической плотности, соответственно в опытных (с красителем) и контрольных (без красителя) пробах.
Биологически значимым эффектом считали ингибирование роста культуры на 50% (ИК50).
Выявлено, что краситель 3 (n=4) проявлял максимальную фотоиндуцированную активность относительно клеток культуры Нер2 при 4-часовой инкубации (32±3 нМ), с увеличением времени инкубации до 6 часов величина ИК50 увеличивается (43±2 нМ), что свидетельствует о выведении красителя из клеток (Фиг.3).
Удаление красителя из культуральной среды перед воздействием светом не снижает эффективность фотодинамического воздействия (ИК50=34±3 нМ) (Фиг.3). Это говорит о том, что уже через 2 часа после внесения ФС в культуральную среду фотоиндуцированная активность реализуется преимущественно за счет активации внутриклеточного красителя, что и было доказано методами КОМИРСИ и ЛСКМ.
Таким образом, результаты, полученные in vitro, показывают, что метиловый эфир 131-(4-аминобутилкарбомоил)бактериохлорина е (3, n=4) эффективно накапливается в клетках и обладает высокой фотоиндуцированной активностью в отношении клеток Нер2.
Пример 9. Распределение наноструктурированной водной дисперсии диметилового эфира 131-(4-аминобутилкарбомоил)бактериохлорина е (3, n=4) на основе кремофора в опухоли S37 и флуоресцентная контрастность относительно окружающей ткани.
Оценку распределения ФС в опухолевой и окружающих тканях проводили у мышей с саркомой S37 в интервале от 0 до 72 часов методом ЛФС. Фотосенсибилизатор вводили внутривенно в дозе 5,0 мг/кг. Флуоресценцию регистрировали контактным способом на лазерном спектральном анализаторе для флуоресцентной диагностики опухолей и контроля за ФДТ «ЛЭСА-06».
В опухолевой ткани нормированная флуоресценция ФС достигала максимального значения (10.4±3.1 усл. ед.) через 30 минут и сохраняется на высоком уровне до 2 часов после введения, а затем к 72 часам снижается на 74% от максимального значения. Наиболее высокие уровни нормированной флуоресценции в коже (3.7±0.9 усл. ед.) наблюдаются через 30 минут после введения ФС, в мышце (4.9±0.8 усл. ед.) - через 15-30 минут. Максимальная флуоресцентная контрастность ФС относительно окружающих нормальных тканей кожи регистрировалась через 0.25-2 часа после введения и составляла 2.8±0.5-3.0±0.3 усл. ед., а относительно мышцы - через 30 минут после введения и составляла 2.3±0.5 усл. ед.
Пример 10. Фотоиндуцированная противоопухолевая активность
наноструктурированной водной дисперсии метилового эфира 131-(4-аминобутилкарбомоил)бактериохлорина е (3, n=4) на основе кремофора у животных с саркомой S37.
Исследование фотодинамической терапии с соединением 3 (n=4) в виде наноструктурированной водной дисперсии на основе кремофора проводили у животных с саркомой S37, привитой подкожно с внешней стороны правого бедра мышам BDF1, в зависимости от дозы ФС на 7 сутки после инокуляции опухоли.
В первой, второй и третьей опытных группах животным вводили ФС однократно внутривенно в хвостовую вену в дозах 1.25, 2.5 и 5.0 мг/кг, соответственно. Облучение проводили через 30 минут после введения фотосенсибилизатора. Для облучения использовали светодиодный источник с длиной волны 754±14 нм и плотностью мощности 150 мВт/см2 (плотность энергии 150 Дж/см2). Четвертая группа животных - контрольная без воздействия.
Эффективность ФДТ оценивали, используя общепринятые в экспериментальной онкологии критерии:
- торможение роста опухоли ТРО=[(Vk-Vоп)/Vк]·100%, где Vоп и Vk - объем опухоли в опытной и контрольной группах соответственно;
- увеличение продолжительности жизни УПЖ=[(СПЖоп - СПЖк)/СПЖк]·00%, где СПЖоп и СПЖк - средняя продолжительность жизни в опытной и контрольной группах соответственно;
- критерий излеченности КИ=[Nи/No]·100%, где Nи и No - количество излеченных животных и общее количество животных в опытной группе, соответственно.
Объем опухоли рассчитывали по формуле: V=d1·d2·d3, где d1, d2 и d3 - три взаимно перпендикулярных диаметра опухоли.
Измерение объема опухоли проводили в течение 20 суток после проведенного облучения с помощью электронного цифрового кронциркуля STORMtm 3С301 «Central». За животными наблюдали 120 суток.
В опытных группах в течение суток после облучения у животных образовывался интенсивный отек в зоне воздействия, который сохранялся до 5-10 суток. При использовании соединения 3 (n=4) в дозе 1.25 мг/кг, среднее значение объема опухоли увеличивалось медленно по отношению к объему опухоли контрольной группы. ТРО составило 92.6 - 100%, УПЖ - 170.8%, КИ - 66.7%. Для доз 2.5 и 5.0 мг/кг выявлена еще более высокая эффективность: 100% торможение роста опухоли в течение всего срока наблюдения, 100% излеченность животных в течение 120 суток наблюдения (Фиг.4).
Пример 11. Фармакокинетика наноструктурированной водной дисперсии метилового эфира 131-(4-аминобутилкарбомоил)бактериохлорина е (3, n=4) на основе кремофора у интактных мышей.
Фармакокинетику диметилового эфира 131-(8-аминобутилкарбомоил) бактериохлорина изучали методом ЛФС в органах и тканях интактных мышей в дозе 5.0 мг/кг.
Максимум спектра флуоресценции ФС в тканях животных регистрировали при 753±2 нм. Флуоресцирующая форма фотосенсибилизатора быстро (в течение 15-30 минут) регистрировалась во внутренних органах и тканях организма, преимущественно в печени, затем снижалась с различной скоростью. Максимальная флуоресценция соединения 3 (n=4) в крови определялась сразу после внутривенного введения и в течение 4-х часов снижалась более чем на 95% от максимального значения и через сутки уже не регистрировалась.
Во внутренних органах через 24 часа уровень нормированной флуоресценции снижался в печени на 79%, почках - на 69%, селезенке - на 91% от максимального значения. Флуоресцирующая форма фотосенсибилизатора в дозе 5.0 мг/кг определялась в селезенке до 6 суток, а в почках и печени остаточное количество определялось до 14 суток.
В коже максимальное значение флуоресценции регистрировалось через 30 минут после введения фотосенсибилизатора, затем его нормированная флуоресценция быстро снижалась и через 24 часа составляла 30% от максимального значения и через 72 часа не определялась. Это свидетельствует о быстром элиминировании ФС из кожи. В мышце через 24 часа уровень нормированной флуоресценции также снижался на 62%, в жировой ткани - на 72%. Флуоресцирующая форма ФС определялась в мышце и жировой ткани до 72 часов.
Полученные данные свидетельствуют о быстрой циркуляции метилового эфира 131-(4-аминобутилкарбомоил)бактериохлорина е в организме млекопитающих и его выведении преимущественно через печень с желчью и почки с мочой.
Таким образом, заявляемые аминоамиды бактериохлорина е являются высокоактивными фотосенсибилизаторами нового поколения, поглощающими в ближней ИК-области спектра и обеспечивающими высокую фотоиндуцированную противоопухолевую активность, 100%-ное торможение роста опухоли и 100% излеченность животных за счет селективного накопления в опухоли и быстрого выведения из организма.
1. Аминоамиды в ряду бактериохлорофилла a общей формулы: где n=2, 4, 8, 10, обладающие фотоиндуцированной противоопухолевой активностью.
2. Способ получения аминоамидов по п. 1, включающий обработку метилового эфира бактериофеофорбида а диаминоалканом формулы NH2(CH2)nNH2, где n=2, 4, 8, 10, в пиридине.