ethod of determining gas chromatographic retention indices of o-alkylmethylfluorophosphonate compounds based on 13c nmr data
Иллюстрации
Показать всеИспользование: для определения газохроматографичеких индексов удерживания соединений ряда О-алкилметилфторфосфонатов (ОАМФФ) по данным ЯМР 13С. Сущность изобретения заключается в том, что выполняют построение корреляционных уравнений для известной выборки изомеров и последующее определение значения индексов удерживания неизвестных изомеров по установленной зависимости, при этом в качестве спектральной характеристики используется суммарное значение химических сдвигов ядер 13C атомов углерода, находящихся в разветвлении углеродного скелета О-алкильного радикала рассчитанных по спектрам ЯМР 13C. Технический результат: повышение достоверности и объективности определения газохроматографических индексов удерживания соединений ряда ОАМФФ. 2 ил., 5 табл.
Реферат
Изобретение относится к исследованию или анализу материалов путем определения их химических или физических свойств, конкретно путем разделения на составные части (компоненты) с использованием адсорбции, абсорбции или подобных процессов, например хроматографии или спектроскопии ЯМР 13C.
Изобретение может быть использовано для хроматографической и хроматомасс-спектрометрической идентификации контролируемых соединений ряда O-алкилметилфторфосфонатов (ОАМФФ) в рамках мероприятий по выполнению Конвенции о запрещении разработки, производства, накопления и применения химического оружия и о его уничтожении (далее Конвенция) {Конвенция о запрещении разработки, производства, накопления и применения химического оружия и о его уничтожении. - М.: Комитет по конвенциальным проблемам химического и биологического оружия при Президенте Российской Федерации, 1994 - 133 с.).
Актуальность разработки обусловлена отсутствием полного массива значений индексов удерживания (ИУ) изомеров ОАМФФ, включенных в Список 1 Конвенции и подлежащих контролю в разных матрицах, в том числе в объектах окружающей среды.
Главным требованием к исходным характеристикам для вычисления индексов удерживания является их практическая доступность. В противном случае такие методы будут представлять лишь теоретический интерес. Следовательно, соответствующие алгоритмы должны быть ориентированы на весьма подробные и хорошо систематизированные данные, например на физико-химические константы органических соединений. Из литературных источников известно (Зенкевич И.Г., Кузнецова Л.М. Использование физико-химических констант органических соединений при хромато-масс-спектрометрической идентификации [Текст] // Ж. аналит. Химии. - 1992. - Т.47. - № 6. - С.982-993), что наибольшую точность определения значений газохроматографических индексов удерживания обеспечивает линейное корреляционное уравнение (1), связывающее ИУ с физико-химическими характеристиками:
где - a, b - коэффициенты линейного уравнения;
x - физико-химическая характеристика.
Теоретически обоснованных рекомендаций выбора физико-химических характеристик (x) не существует. В исследовательской практике чаще всего используются температура кипения, летучесть, дипольный момент, коэффициент Генри (Panneerselvam K., Antony М.Р, Srinivasa, T.G., Vasudeva Rao P.R. Estimation of normal boiling points of trialkyl phosphates using retention indices by gas chromatography [Текст] // Thermochimica Acta 2010. - 511. - P.107-111. Сидоров P.И., Романенко Л.С., Резников С.А. Влияние дипольного момента нитроароматических углеводородов на их удерживание в газожидкостной хроматографии [Текст] // ЖФХ. - 1977. - Т.51. - Вып.11. - С.2913-2917. Прудковский А.Г., Долгоносов A.M. Инструмент для оценки индекса Ковача по времени удерживания вещества в газовой хроматографии [Текст] // Ж. Аналит. Химии. - 2008. - Т.63. - №9. - С.935-940).
Способы определения индексов удерживания по физико-химическим константам для соединений класса ОАМФФ характеризуются существенным ограничением, связанным с отсутствием справочных данных. Так, проведенный литературный поиск по физико-химическим константам соединений класса ОАМФФ показал, что объем экспериментальных данных весьма мал, зачастую авторы ограничиваются двумя основными представителями этого класса, такими как зарин и зоман.
Наиболее распространенный способ определения ИУ по температуре кипения для соединений ряда ОАМФФ связан с трудностью точного измерения их температур, поскольку при воздействии высоких температур происходит разложение исследуемого вещества, например разложение зомана начинается от 150°C, а температура кипения находится в диапазоне от 190 до 200°C. При этом требуемая точность определения температуры кипения составляет не более чем ±1-2°C, поскольку при последующем пересчете в ИУ отклонение соответствует 5-10 у.е., что сравнимо с современной межлабораторной воспроизводимостью этих параметров на стандартных неполярных фазах (Зенкевич И.Г. Общие закономерности изменения физико-химических свойств органических соединений в гомологических рядах [Текст]. // Журн. орг. химии. - 2006. - Т.42. - Вып.1. - С.9-20).
К другим методам определения ИУ, основанным на поиске корреляционных уравнений, относятся методы с применением нейронных сетей (Баскин И.И., Зефиров И.Г., Гальберштам Н.М. Нейронные сети как метод поиска зависимостей структура-свойство органических соединений [Текст]. // Успехи химии. - 2003. - Т.72. - №7. - С.706-727) и "Количественного соотношения структура-удерживание" (QSRR - Quantitative Structure-Retention Relationships) (Wang H., Zhang A., Sun C., Wang L. Prediction of gas chromatographic retention indices of organophosphorus compounds by holographic QSRR [Текст] // Chinese Science Bulletin. - 2009. - V.54. - №.4 - P.635-641. Курбатова С.В., Финкельштейн E.E., Колосова Е.А., Карташев А.В., Рашкин С.В. Метод структурной аналогии в исследовании адамантана и его производных [Текст] // Журн. Структ. химии. - 2004. - Т.45. - №1. - С.150-157. Balkrishna R.G. , Rameshwar P., Rajinder K.D., Shankarrao K.S., Rajendra K.S., Balwant S.B., Karumuru M.R. Use of Gas Chromatographic Retention Indices for Quantitative Structure Activity Relationship Studies of DialkyI Phenyl Phosphates [Текст] // Pestic. Sci. - 1990. - 29. - 379-385). Приведенные способы определения ИУ базируются на связи целевого свойства и определенных молекулярных характеристик (топологических, электронных и др.) для соединений рассматриваемой выборки. Однако при реализации данных методов необходимы данные по большой выборке соединений с многообразными разветвлениями углеродного скелета, а для повышения точности расчетов ИУ необходимы дескрипторы, которые должны быть чувствительны к структурной изомеризации.
В настоящее время в хроматографических базах данных представлено незначительное количество изомеров класса ОАМФФ с различными разветвлениями углеродного скелета O-алкильного радикала.
Из многообразия различных методов определения ИУ наиболее близким способом расчета ИУ к предлагаемому является способ, используемый в работе (Vazhev V.V., Aldabergenov M.K. The use of IR spectra for estimating the boiling point and molecular weights of monohydric aliphatic of alcohols [Текст] // Russian journal of applied chemistry. - 2005. - V.78. - №3 - P.453-455). В этой работе определение ИУ одноатомных спиртов основывается на использовании преобразованных ИК-спектров как дескрипторов молекулярной структуры в методе QSPR (QSPR - Quantitative Structure-Property Relationships). Существенным недостатком этого метода является то, что при определении типа структурного изомера ОАМФФ методом ИК-спектроскопии в ИК-спектре данных соединений наблюдается наложение спектральных линий алкильных фрагментов, связанных с атомами фосфора и кислорода. Кроме того, метод ИК-спектроскопии обладает более низкой разрешающей способностью по сравнению, например, со спектроскопией ЯМР, согласно принципу неопределенности Гейзенберга (Fujikawa K. Universally valid Heisenberg uncertainty relation [Текст]. // Physical Review A. - 2012. - V.85. - №6. - P.37-43), что играет большую роль при определении типа структурного изомера. Недостатки использования данных ИК-спектров заметно сказываются на определении ИУ.
До настоящего времени характеристики спектроскопии ЯМР 13C для определения индексов удерживания органических соединений не применялись.
Нами предложен новый подход в применении ЯМР характеристик, таких как значения химических сдвигов ЯМР 13C изомеров ОАМФФ, для определения ИУ исследуемых веществ, поскольку химические сдвиги углеродных атомов чувствительны к изомеризации структуры O-алкильного радикала. Суммарное значение химического сдвига ядер 13C атомов углерода отражает влияние степени разветвленности О-алкильного радикала на электронное строение структурных фрагментов и их взаимное расположение, т.е. зависит от изомерного строения радикала.
Задача настоящего изобретения заключается в разработке способа определения газохроматографических параметров удерживания соединений ряда ОАМФФ по данным химических сдвигов ЯМР 13C.
Решение поставленной задачи предполагает технический результат, заключающийся в повышении достоверности и объективности определения газохроматографических индексов удерживания соединений ряда ОАМФФ.
Поставленная задача решается тем, что в способе определения газохроматографических индексов удерживания соединений гомологического ряда O-алкилметилфторфосфонатов на основе взаимосвязи спектральных и хроматографических характеристик, заключающемся в построении корреляционных уравнений для известной выборки изомеров и последующем определении значения индексов удерживания неизвестных изомеров по установленной зависимости, отличающемся тем, что в качестве спектральной характеристики используется суммарное значение химических сдвигов ядер 13C атомов углерода, находящихся в разветвлении углеродного скелета O-алкильного радикала и рассчитанных по спектрам ЯМР 13C.
Экспериментальные значения ИУ и химических сдвигов были получены на хромато-масс-спектрометре 6890/5973N фирмы Agilent Technologies и на ЯМР-спектрометре модели FT-80 фирмы Varian на частоте 20 МГц. Для разделения компонентов смеси применяли кварцевую капиллярную колонку DB-5HT длиной 30 м, внутренним диаметром 0,25 мм с толщиной фазы 0,1 мкм, со слабополярной неподвижной жидкой фазой (5% фенил - 95% диметилполисилоксан).
Определение химических сдвигов ядер 13C проводилося относительно стандарта, в качестве которого использовался тетраметилсилан.
В предлагаемом изобретении суммарное значение химических сдвигов ЯМР 13C определяется суммой значений химических сдвигов для каждого углеродного атома, находящегося в боковом разветвлении относительно максимальной углеводородной цепи.
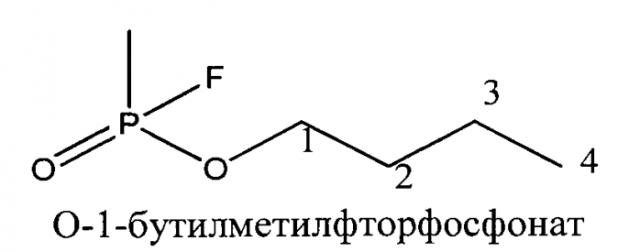
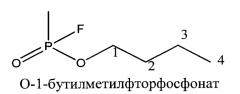
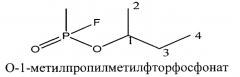
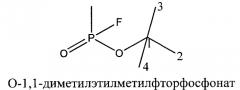
В таблице 1 приведены структурные формулы и названия трех исследуемых изомеров с четырьмя атомами углерода в O-алкильном радикале, а также значения химических сдвигов ядер 13C для каждого углеродного атома.
| Таблица 1 | ||
| Значения химических сдвигов ядер 13C для каждого углеродного атома ОАМФФ в O-алкильном радикале | ||
| Структурная формула и химическое название изомера | Номер атома | Значение химического сдвига ЯМР 13C, δ, м.д. |
| 1 | 66,9 | |
| 2 | 32,3 | |
| 3 | 18,6 | |
| 4 | 13,5 | |
| Суммарное значение химических сдвигов, ΣδC, м.д. | 0,0 | |
| 1 | 77,5 | |
| 2 | 22,9 | |
| 3 | 30,3 | |
| 4 | 9,4 | |
| Суммарное значение химических сдвигов, ΣδC, м.д. | 22,9 | |
| 1 | 77,6 | |
| 2 | 30,5 | |
| 3 | 30,5 | |
| 4 | 30,5 | |
| Суммарное значение химических сдвигов, ΣδC, м.д. | 61,0 |
Приведенные в таблице 1 данные показывают принцип определения суммарного значения химического сдвига. Так, у изомера с н-бутильным O-алкильным радикалом суммарное значение химического сдвига составляет 0 м.д., поскольку у данного радикала отсутствуют разветвления. В то же время у 1-метилпропильного O-алкильного радикала химический сдвиг равен 22,9 м.д. В том случае если в радикале имеется несколько боковых разветвлений относительно углеводородной цепи, химические сдвиги их суммируются. Так, например, у O-третбутильного радикала имеются два углеродных атома в разветвлении. Химические сдвиги ЯМР 13C для каждого углеродного атома равны 30,5 м.д., а суммарное значение составляет 61,0 м.д.
В таблице 2 приведены хроматографические и спектральные данные ОАМФФ с 4 углеродными атомами в O-алкильном радикале, свидетельствующие о возрастании значений ИУ с уменьшением суммарного значения химических сдвигов ΣδC ЯМР 13C у исследуемых изомеров.
| Таблица 2 | ||
| Хроматографические и спектральные данные ОАМФФ с четырьмя атомами углерода в O-алкильном радикале | ||
| Название O-алкильного радикала | Экспериментальное суммарное значение химических сдвигов ΣδC, м.д. | Экспериментальное значение ИУ RiC, у.е. |
| O-третбутил | 61,0 | 850,3 |
| 1-Метилпропил | 22,9 | 918,2 |
| 2-Метилпропил | 18,5 | 935,2 |
| Бутил | 0,0 | 970,1 |
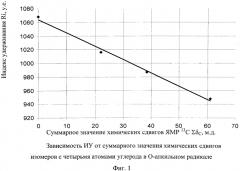
На фигуре 1 представлена корреляционная зависимость между значениями ИУ и суммарного значения химических сдвигов исследуемых изомеров с 4 углеродными атомами в O-алкильном радикале, которая наглядно показывает возрастание значений ИУ с уменьшением суммарного значения химических сдвигов ΣδC ЯМР 13C у изомеров ОАМФФ с 4 углеродными атомами в O-алкильном радикале.
Данная зависимость описывается линейным уравнением (1) с коэффициентом корреляции равным 0,994:
где Ri - значение индекса удерживания, у.е.;
ΣδC - суммарное значение химических сдвигов, м.д.
В таблице 3 приведены экспериментальные и определенные по уравнению (1) значения индексов удерживания. Отклонение определенных значений относительно экспериментальных значений ИУ приведены в последнем столбце таблицы.
Данные, представленные в таблице 3, свидетельствуют о том, что для исследуемых соединений отклонения определенных ИУ от экспериментальных значений не превышают предела межлабораторной воспроизводимости, составляющей ±15 у.е., а среднее значение погрешности составляет 2,9 у.е.
Далее рассмотрим работоспособность предлагаемого способа на примере определения газохроматографических индексов удерживания изомеров ряда ОАМФФ с пятью атомами углерода в O-алкильном радикале по данным ЯМР 13C.
| Таблица 3 | |||
| Экспериментальные и определенные значения ИУ ОАМФФ с четырьмя атомами углерода в O-алкильном радикале | |||
| Название O-алкильного радикала | Индекс удерживания | Отклонение от экспериментального значения, Δ = | R i c − R i p | , у.е. | |
| Экспериментальное значение, Ric, у.е. | Определенные значение по уравнению (1), Rip, у.е. | ||
| O-третбутил | 850,3 | 848,8 | 1,5 |
| 1-Метилпропил | 918,2 | 923,6 | 5,4 |
| 2-Метилпропил | 935,2 | 932,2 | 3,0 |
| Бутил | 970,1 | 968,5 | 1,6 |
| Среднее отклонение от экспериментальных значений | 2,9 |
В таблице 4 приведены хроматографические и спектральные данные изомеров ОАМФФ с пятью углеродными атомами в O-алкильном радикале.
| Таблица 4 | ||
| Хроматографические и спектральные данные изомеров ОАМФФ с пятью углеродными атомами в O-алкильном радикале | ||
| Название O-алкильного радикала | Суммарное значение химического сдвига ΣδC, м.д. | Значение индекса удерживания Ric, у.е. |
| 1,1-Диметилпропил | 61,0 | 948,2 |
| 2,2-Диметилпропил | 53,0 | 967,1 |
| 1,2-Диметилпропил | 38,4 | 987,4 |
| 1-Этилпропил | 26,5 | 1013,5 |
| 1-Метилбутил | 22,0 | 1016,0 |
| 2-Метилбутил | 15,9 | 1032,1 |
| 3-Метилбутил | 20,3 | 1026,2 |
| Пентил | 0,0 | 1067,9 |
На фигуре 2 представлена зависимость ИУ от суммарного значения химических сдвигов ЯМР 13C исследуемых изомеров. Уравнение связи для изомеров с пятью углеродными атомами в O-алкильном радикале имеет следующий вид (2):
где Ri - значение индекса удерживания, у.е.;
ΣδC - суммарное значение химических сдвигов, м.д.
Коэффициент корреляции для данного уравнения равен 0,992.
В таблице 5 приведены экспериментальные и определенные по уравнению (2) значения индексов удерживания. Отклонение определенных значений относительно экспериментальных значений ИУ приведены в последнем столбце таблицы.
| Таблица 5 | |||
| Экспериментальные и определенные значения ИУ изомеров ОАМФФ с пятью углеродными атомами в O-алкильном радикале | |||
| Название O-алкильного радикала | Индекс удерживания | Отклонение от экспериментального значения, Δ = | R i c − R i p | , у.е. | |
| Экспериментальное значение, Ric, у.е. | Определенное значение по уравнению (2), Rip, у.е. | ||
| 1,1-Диметилпропил | 948,2 | 947,6 | 0,6 |
| 2,2-Диметилпропил | 967,1 | 962,8 | 4,3 |
| 1,2-Диметилпропил | 987,4 | 990,5 | 3,1 |
| 1-Этилпропил | 1013,5 | 1013,0 | 0,5 |
| 1-Метилбутил | 1016,0 | 1021,7 | 5,7 |
| 2-Метилбутил | 1032,1 | 1033,3 | 1,2 |
| 3-Метилбутил | 1026,2 | 1025,0 | 1,2 |
| Пентил | 1067,9 | 1063,5 | 4,4 |
| Среднее значение отклонений | 2,6 |
Данные, представленные в таблице 5, показывают, что для исследованных соединений отклонения определенных ИУ от экспериментальных значений не превышают предела межлабораторной воспроизводимости, а среднее значение погрешности составляет для изомеров O-пентила 2,6 у.е.
Заявляемый способ позволяет
- повысить точность определения индексов удерживания структурных изомеров ОАМФФ;
- устанавливать последовательность газохроматографического удерживания изомеров ОАМФФ на слабополярных фазах газохроматографических колонок;
- расширить базы хроматографических аналитических данных для изомеров ОАМФФ.
Способ определения газохроматографических индексов удерживания соединений гомологического ряда О-алкилметилфторфосфонатов на основе взаимосвязи спектральных и хроматографических характеристик, заключающийся в построении корреляционных уравнений для известной выборки изомеров и последующем определении значения индексов удерживания неизвестных изомеров по установленной зависимости, отличающийся тем, что в качестве спектральной характеристики используется суммарное значение химических сдвигов ядер 13C атомов углерода, находящихся в разветвлении углеродного скелета О-алкильного радикала рассчитанных по спектрам ЯМР 13C.