Схема приема ботулотоксина для профилактики хронической мигрени
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к неврологии, и касается профилактики хронической мигрени. Для этого вводят ботулотоксин в фиксированные места лобных мышц, мышц, вызывающих сморщивание кожи, мышц гордецов, затылочные мышцы, височные мышцы, трапециевидные мышцы и шейные околопозвоночные мышцы. Всего 31-39 мест инъекции, по 5 единиц ботулотоксина на 1 инъекцию. При этом общее количество вводимого ботулотоксина составляет 155-195 единиц. Такая схема введения ботулотоксина обеспечивает эффективную профилактику головной боли у больных с хронической мигренью. 4 з.п. ф-лы, 17 ил., 24 табл.
Реферат
Перекрестная ссылка на родственные заявки
[1] Данная заявка претендует на приоритет Предварительной заявки на патент США №61/319230, поданной 30 марта 2010 года, и №61/320667, поданной 2 апреля 2010 года, все из которых полностью включены сюда посредством ссылки.
Область техники
[2] Различные варианты воплощения этого изобретения относятся к лечению различных заболеваний, в частности, к протоколам инъекционного введения ботулинического нейротоксина.
Уровень техники
[3] Известно, что ботулинические токсины можно использовать для лечения разнообразных заболеваний. Примерами такого использования являются: Патент США 5714468 (лечение мигрени), выданный 3 февраля 1998 года; опубликованная Патентная заявка США №2005019132 (лечение головной боли), регистрационный номер 11/039506, поданная 18 января 2005 года; опубликованная Патентная заявка США №20050191320 (лечение MOU), регистрационный номер 10/789180, поданная 26 февраля 2004 года; и Патент США 7811587 (лечение нейропсихиатрических расстройств), выданный 12 октября 2010 года; все полностью включены сюда посредством ссылки.
[4] Примером заболевания, которое можно лечить ботулиническими токсинами, служит хроническая мигрень - приводящая к потере трудоспособности головная боль, поражающая от 1,3% до 2,4% населения и являющаяся наиболее распространенным типом первичной хронической ежедневной головной боли в Соединенных Штатах. Хроническая мигрень связана с физическим страданием, нетрудоспособностью и чрезмерным использованием лекарств, и лишь одна треть из всех пациентов, страдающих хронической мигренью, использует лекарства для профилактики головной боли. Для лечения пациентов, страдающих хронической мигренью, были исследованы лишь несколько вариантов профилактики головной боли. Таким образом, сохраняется потребность в оптимизированных и целевых методологиях лечения этого конкретного недуга, а также в определении специфических и приносящих пользу схем инъекций и дозировки при использовании ботулинических токсинов в лечении хронической мигрени.
[5] Другим патологическим состоянием, которое можно лечить ботулиническим токсином, является головная боль, вызванная чрезмерным использованием лекарственных средств (MOU). Она описана как самоподдерживающийся периодический прием лекарств от головной боли, приводящий к ежедневной или почти ежедневной головной боли с непреодолимым и предсказуемым использованием лекарств, дающих немедленное облегчение. Данные, подтверждающие существование такого патологического состояния как МОН, широко публикуются в медицинской литературе.
Сущность изобретения
[6] В одном из вариантов воплощения этого изобретения представлен способ профилактики головной боли у пациента, страдающего хронической мигренью, состоящий главным образом из местного введения ботулинического нейротоксина в лобную мышцу, сморщиватель, мышцу гордецов, затылочную, височную, трапециевидную и шейные околопозвоночные мышцы пациента, страдающего от мигрени, причем ботулинический нейротоксин вводится в лобную мышцу в количестве примерно двадцати единиц токсина, разделенных между четырьмя местами инъекции; в сморщиватель - в количестве примерно десяти единиц токсина, разделенных между двумя местами инъекции; в мышцу гордецов - в количестве примерно пяти единиц токсина в одно место инъекции; в затылочную мышцу - в количестве от примерно тридцати единиц токсина, разделенных между шестью местами инъекции, до примерно сорока единиц токсина, разделенных между восемью местами инъекции; в височную мышцу - в количестве от примерно сорока единиц токсина, разделенных между восемью местами инъекции, до примерно пятидесяти единиц токсина, разделенных между десятью местами инъекции; в трапециевидную мышцу - в количестве от примерно тридцати единиц токсина, разделенных между шестью местами инъекции, до примерно пятидесяти единиц токсина, разделенных между десятью местами инъекции; и в шейные околопозвоночные мышцы - в количестве примерно двадцати единиц токсина, разделенных между четырьмя местами инъекции, при этом ботулинический нейротоксин вводится в 31-39 мест инъекции.
Краткое описание фигур
[7] Для иллюстрации аспектов и характерных особенностей вариантов воплощения этого изобретения приводятся следующие рисунки.
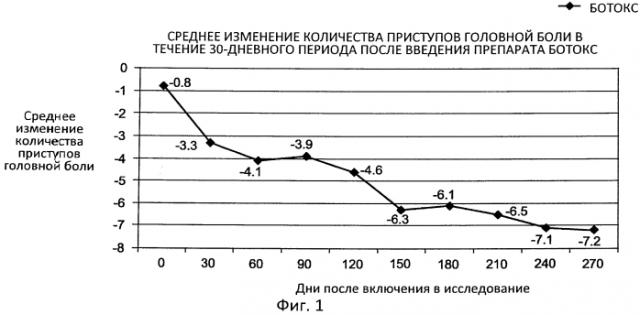
[8] Фигура 1 представляет собой график, демонстрирующий результаты (среднее изменение количества случаев головной боли за тридцать дней) клинического исследования использования препарата БОТОКС® для лечения, среди прочего, мигрени, который показывает, что у пациентов после введения препарата БОТОКС® реже наблюдаются приступы головной боли. Исходя из данных, представленных на Фигурах, пациентам препарат БОТОКС® вводили в 0, 90 и 180 день исследования.
[9] Фигура 2 представляет собой график, демонстрирующий результаты (среднее изменение количества дней одновременного приема пациентами лекарств, облегчающих острую головную боль, за тридцать дней) клинического исследования использования препарата БОТОКС® для лечения, среди прочего, мигрени, который показывает, что пациенты после введения препарата БОТОКС® принимают лекарства для ослабления острой головной боли в течение меньшего количества дней.
[10] На Фигуре 3 представлен график, демонстрирующий сравнение процента пациентов (некоторым из пациентов вводили препарат БОТОКС®, а некоторым - плацебо), которые в течение тридцатидневного периода использовали наркотические лекарственные средства для борьбы с острой головной болью. Фигура 3 показывает сокращение использования наркотических лекарственных средств пациентами, которым вводили препарат БОТОКС®.
[11] Фигура 4 представляет график, который демонстрирует снижение процента пациентов, которые чрезмерно использовали лекарственные средства для борьбы с острой головной болью в течение тридцатидневного периода после введения препарата БОТОКС®.
[12] Фигура 5 представляет график, который демонстрирует снижение процента пациентов, которые чрезмерно использовали триптаны в течение тридцатидневного периода после введения препарата БОТОКС®.
[13] Фигура 6 включает два графика, которые демонстрируют среднее изменение количества приступов головной боли, испытуемых пациентами в течение тридцатидневного периода после введения препарата БОТОКС®, причем либо пациенты не имели MOU («без MOU»; график слева), либо пациенты страдали от MOU (график справа). Критерии «>15 дней и>2 дней/неделю» использовались для того, чтобы определить, страдал ли пациент головной болью, вызванной чрезмерным использованием лекарств. «MOU» и «MOD» являются синонимами. По определению, пациент страдает MOU, если он/она принимает лекарства от острой головной боли в течение 15 и более дней в месяц и по меньшей мере два раза в неделю в течение недели, когда такой пациент испытывает острую головную боль.
[14] Фигура 7 включает два графика, на которых изображено среднее изменение (по сравнению с базовой линией) частоты приступов головной боли в течение 30-дневного периода у пациентов, использовавших (график А) и не использовавших (график В) лекарства для профилактики головной боли при базовой линии, для объединенной группы пациентов. Ордината представляет значения среднего изменения количества приступов головной боли в течение тридцатидневного периода; «n» означает количество пациентов в анализируемой выборке.
[15] Фигура 8 включает два графика, на которых изображено среднее изменение количества приступов головной боли, которые испытывали пациенты в течение тридцатидневного периода после введения препарата БОТОКС®, при этом либо пациенты не использовали одновременно никакие иные средства профилактики головной боли (график слева), либо пациенты не использовали одновременно никакие иные средства профилактики головной боли, но страдали MOU (график справа).
[16] Фигура 9 включает два графика, на которых изображено среднее изменение количества приступов головной боли, которые испытывали пациенты в течение тридцатидневного периода после введения препарата БОТОКС®, при этом пациенты либо не использовали одновременно никакие иные средства профилактики головной боли и не испытывали MOU (график слева), либо пациенты не использовали одновременно никакие иные средства профилактики головной боли, но страдали MOU (график справа).
[17] На Фигуре 10 представлена гистограмма процента пациентов, которые в течение тридцатидневного периода после введения препарата БОТОКС® использовали также опиоиды для борьбы с острой головной болью.
[18] Фигура 11 включает два графика, на которых изображено среднее изменение количества приступов головной боли, которые испытывали пациенты в течение тридцатидневного периода после введения препарата БОТОКС®, при этом пациенты либо чрезмерно использовали триптан (график слева), либо не использовали чрезмерно триптан (график справа).
[19] Фигура 12 включает два графика, на которых изображено среднее изменение по сравнению с базовой линией (после введения препарата БОТОКС®) количества дней использования лекарственных средств против острой головной боли (анальгетиков) пациентами, при этом пациенты либо чрезмерно использовали триптан (график слева), либо не использовали чрезмерно триптан (график справа).
[20] Фигура 13 содержит слева схематическое изображение анатомии мышц человека от левого плеча вверх, а справа - схематическое изображение спины.
[21] Фигура 14 включает два графика, на которых изображено среднее изменение (по сравнению с базовой линией) частоты приступов головной боли в течение 30-дневного периода для пациентов, которые не реагировали на плацебо (А), и пациентов, отреагировавших на плацебо (В).
[22] На Фигуре 15 представлено среднее изменение (по сравнению с базовой линией) частоты приступов головной боли в течение 30-дневного периода для объединенной группы пациентов.
[23] Фигура 16 включает два графика, на которых изображено среднее изменение (по сравнению с базовой линией) количества дней использования анальгетиков для лечения острой головной боли в течение 30-дневного периода для пациентов, использовавших при базовой линии лекарственные средства для профилактики головной боли (А), и пациентов, не использовавших при базовой линии лекарственные средства для профилактики головной боли (В), для объединенной группы пациентов.
[24] Фигура 17 представляет пример фиксированных мест, в которых пациенту вводится ботулинический токсин (на этой Фигуре пациент находится в положении лежа на спине и сидя) в соответствии с одним из вариантов воплощения схемы инъекций.
Описание изобретения
[25] В некоторых вариантах воплощения этого изобретения доза ботулотоксина, используемого в соответствии с вариантами воплощения этого изобретения, является меньшей, чем количество ботулотоксина, которое могло бы использоваться для того, чтобы парализовать мышцу, так как цель способа, согласно вариантам воплощения настоящего изобретения, не парализовать мышцу, а снизить ощущение боли, вызываемое афферентными нейронами, расположенными в мышце или на ней, или в коже, или под кожей.
[26] Здесь используются следующие определения:
[27] «Примерно» означает «приблизительно» или «около» и в контексте с числовыми значениями или диапазоном значений означает ±10% от приведенного или заявленного значения или диапазона.
[28] «Ослабление» означает снижение проявления боли, головной боли или симптома головной боли. Таким образом, ослабление включает некоторое снижение, значительное снижение, почти полное прекращение и полное прекращение. Эффект ослабления может не проявляться клинически в течение 1-7 дней после введения пациенту клостридиального токсина или в течение еще некоторого времени.
[29] «Ботулотоксин» означает ботулинический нейротоксин в виде чистого токсина или комплекса, природного, рекомбинантного или модифицированного токсина, и включает ботулотоксин типа А, типа В, типа С1, типа D, типа Е, типа F и типа G. Как используется здесь термин «ботулотоксин» не включает не нейротоксины, такие как цитотоксичные ботулотоксины С2 и С3.
[30] «Местное введение» означает введение фармацевтического средства в мышцу или вблизи мышцы, или под кожу пациенту несистемным путем. Таким образом, местное введение исключает системные пути введения, такие как внутривенное или оральное введение.
[31] «Периферическое введение» означает введение в место, находящееся в стороне от места проявления симптомов в отличие от «местного введения».
[32] Обозначение «MOU» означает головную боль, вызванную чрезмерным использованием лекарственных средств.
[33] «Лечение» означает ослабление (или прекращение) по меньшей мере одного симптома (такого как, например, головная боль), либо временное, либо постоянное. Лечение может включать профилактическое применение для предотвращения по меньшей мере одного симптома головной боли.
[34] Здесь представлены различные варианты воплощения схемы введения ботулинических нейротоксинов. В некоторых вариантах воплощения этого изобретения способ может включать определенные места инъекции и дозировки ботулотоксина для лечения различных заболеваний, включая, например, хроническую мигрень, MOU, неврологические расстройства и т.п. В определенных вариантах воплощения этого изобретения заболевание можно лечить внутримышечным введением токсина в определенном количестве или диапазоне доз в определенные места верхней части туловища человека. В некоторых вариантах воплощения этого изобретения такие места могут включать, например, голову, шею, одно или два плеча, как спереди, так и сзади. Ботулотоксином может быть ботулотоксин типа А, типа В, типа С1, типа D, типа Е, типа F и типа G или любой их комбинацией. Ботулинический нейротоксин может быть также рекомбинантным ботулиническим нейротоксином, таким как ботулотоксины, производимые Е.coli.
[35] Кроме того, ботулинический нейротоксин может быть модифицированным нейротоксином, таким как ботулинический нейротоксин, в котором по сравнению с природным токсином есть по меньшей мере одна удаленная аминокислота, модифицированная или замененная, либо модифицированный ботулинический нейротоксин может быть рекомбинантным ботулиническим нейротоксином или его производным или фрагментом. В некоторых вариантах воплощения этого изобретения модифицированный токсин обладает измененной способностью адресации на клетки-мишени, как нейронные, так и ненейронные клетки. Такая измененная способность обеспечивается заменой природного домена таргетинга ботулотоксина доменом таргетинга, демонстрирующим селективное связывание с рецептором неботулинического токсина, присутствующего в клетке-мишени неботулинического токсина. Такие модификации домена таргетинга приводят к образованию модифицированного токсина, способного селективно связываться с рецептором неботулинического токсина (целевой рецептор), присутствующим в клетке-мишени неботулинического токсина (переадресация токсина). Модифицированный ботулинический токсин, обладающий таргетинговой активностью по отношению к клеткам-мишеням неботулинического токсина, может связываться с рецептором на клетке-мишени неботулинического токсина, перемещаться в цитоплазму и проявлять свой протеолитический эффект на комплексе мембранных белков SNARE клетки-мишени. По существу, легкая цепь ботулотоксина, содержащая ферментный домен, внутриклеточно доставляется к любой желаемой клетке за счет выбора подходящего домена таргетирования.
[36] Ботулотоксины, предназначенные для использования в этом изобретении, могут храниться в лиофилизированном, высушенном под вакуумом виде в контейнерах под вакуумом или в устойчивых жидкостях. Перед лиофилизацией ботулотоксин можно соединить с фармацевтически приемлемыми вспомогательными веществами, стабилизаторами и/или носителями, такими как, например, альбумин или тому подобное. В вариантах воплощения этого изобретения, содержащих альбумин, последний может быть, например, альбумином из сыворотки человека или т.п. Лиофилизированный материал можно восстановить с помощью подходящей жидкости, такой как, например, раствор соли, вода или т.п., для получения раствора или композиции, содержащей ботулотоксин для введения пациенту.
[37] Количество ботулотоксина, вводимое в соответствии со способом, находящимся в пределах вариантов воплощения этого изобретения, может изменяться в соответствии с конкретными характеристиками боли, для лечения которой предназначен такой ботулотоксин, включая выраженность боли и другие различные переменные, связанные с пациентом, включая размер, вес, возраст и восприимчивость к терапии. В качестве практической рекомендации, как правило, не менее 1 единицы и не более 25 единиц ботулотоксина типа А (такого как препарат БОТОКС) вводятся в одно место инъекции в течение одного сеанса лечения одного пациента. В случае использования ботулотоксина типа А, такого как ДИСПОРТ®, не менее 2 единиц и не более 125 единиц ботулотоксина типа А вводятся в одно место инъекции в течение одного сеанса лечения одного пациента. В случае использования ботулотоксина типа В, такого как МИОБЛОК®, не менее 40 единиц и не более 1500 единиц ботулотоксина типа В вводятся в одно место инъекции в течение одного сеанса лечения одного пациента.
[38] Предпочтительно в случае использования препарата БОТОКС® вводятся не менее 2 единиц и не более 20 единиц ботулотоксина типа А в одно место инъекции в течение одного сеанса лечения одного пациента; в случае использования препарата ДИСПОРТ® не менее 4 единиц и не более 100 единиц вводятся в одно место инъекции в течение одного сеанса лечения одного пациента; и в случае использования препарата МИОБЛОК® не менее 80 единиц и не более 1000 единиц вводятся в одно место инъекции в течение одного сеанса лечения одного пациента.
[39] Более предпочтительно в случае использования препарата БОТОКС® вводятся не менее 5 единиц и не более 15 единиц ботулотоксина типа А; в случае использования препарата ДИСПОРТ® вводятся не менее 20 единиц и не более 75 единиц; и в случае использования препарата МИОБЛОК® не менее 200 единиц и не более 750 единиц вводятся, соответственно, в одно место инъекции в течение одного сеанса лечения одного пациента.
[40] Как правило, общее количество препаратов БОТОКС®, ДИСПОРТ® и МИОБЛОК®, подходящее для введения пациенту в соответствии со способами со настоящему изобретению, описанными здесь, не должно превышать примерно 300 единиц, примерно 1500 единиц или примерно 15000 единиц, соответственно, за один сеанс терапии.
[41] Эффект лечения ботулотоксином может сохраняться от 1 месяца до 5 лет.
[42] Варианты воплощения этого изобретения обеспечивают целевую фиксированную схему инъекций, направленную на определенный набор мышц, с определенным минимальным количеством и объемом инъекций, а также обеспечивают дополнительное/необязательное введение дополнительного ботулотоксина в определенные места выбранных мышц. В одном из вариантов воплощения этого изобретения фиксированная доза (т.е. минимальная дозировка в соответствии с фиксированными количествами и местами, определенными в «Инструкции по медицинскому использованию», вкладываемой в упаковку, или в указаниях по применению препарата) ботулотоксина вводится в лобную мышцу, сморщиватель, мышцу гордецов, затылочную, височную, трапециевидную и шейные околопозвоночные мышцы пациента, и затем переменное дополнительное количество ботулотоксина может быть добавлено для введения в четыре или менее семи участков головы/шеи так, чтобы общее количество введенного ботулотоксина не превышало максимальную общую дозу, указанную в листовке-вкладыше в упаковке или в указаниях по применению препарата, прилагающихся к лекарству, содержащему ботулотоксин. Ботулотоксин может быть выбран из группы, состоящей из ботулотоксинов типа А, В, С, D, Е, F и G. Ботулотоксин типа А является предпочтительным ботулотоксином. Ботулотоксин может вводиться в количестве от 1 единицы до примерно 3000 единиц или от 2 единиц до примерно 2000 единиц, или от 5 единиц до примерно 1000 единиц, или от 10 единиц до примерно 500 единиц, или от 15 единиц до примерно 250 единиц, или от 20 единиц до примерно 150 единиц, или от 25 единиц до примерно 100 единиц, или от 30 единиц до примерно 75 единиц, или от 35 единиц до примерно 50 единиц, или в аналогичном количестве, и ослабление симптомов может продолжаться от 1 месяца до 5 лет.
[43] В одном из вариантов воплощения этого изобретения описывается способ, в котором используется доза и схема инъекций 155 единиц препарата БОТОКС® (как правило, обеспечиваемая в виде 100 единиц нейротоксинового комплекса Clostridium botulinum типа А с 0,5 мг альбумина из сыворотки человека и 0,9 мг натрия хлорида в стерильном лиофилизированном виде для восстановления раствора), вводимого в виде инъекций в 31 фиксированное место в фиксированной дозе (5 единиц) на одну инъекцию, и необязательных 40 единиц, вводимых в не более 8 дополнительных мест инъекции, придерживаясь режима отслеживания боли в рамках цикла лечения (так, чтобы вводилось суммарно не более 195 единиц в не более 39 мест инъекции). Общая доза делится между 7 мышцами головы/шеи, и сеанс лечения повторяется каждые 12 недель.
[44] В одном из вариантов воплощения этого изобретения способ лечения мигрени, такой как, например, хроническая мигрень, может включать введение ботулотоксина в 31 фиксированное место инъекции в семи мышцах головы/шеи. Необязательно можно использовать до 8 дополнительных мест инъекции в трех определенных мышцах, если такие три мышцы являются подгруппой указанных выше семи мышц головы/шеи, придерживаясь режима отслеживания боли для обеспечения гибкости в выборе дозы на мышцу для выбранных трех мышц в соответствии с потребностями пациента. В отдельных вариантах воплощения этого изобретения от минимум 155 единиц ботулотоксина типа А до примерно 195 единиц ботулотоксина типа А вводятся в соответствии с определенной схемой инъекций, представленной здесь.
[45] В определенном варианте воплощения этого изобретения способ лечения хронической мигрени включает этап местного введения ботулинического нейротоксина в лобную мышцу, сморщиватель, мышцу гордецов, затылочную, височную, трапециевидную и шейные околопозвоночные мышцы пациента, страдающего от хронической мигрени, таким образом, чтобы ботулинический нейротоксин вводился в лобную мышцу в количестве примерно двадцати единиц токсина, разделенных между четырьмя местами инъекции, в сморщиватель - в количестве примерно десяти единиц токсина, разделенных между двумя местами инъекции, в мышцу гордецов - в количестве примерно пяти единиц токсина в одно место инъекции, в затылочную мышцу - в количестве от примерно тридцати единиц токсина, которые разделяются между шестью местами инъекции, до примерно сорока единиц токсина, которые разделяются между восемью местами инъекции; в височную мышцу - в количестве от примерно сорока единиц токсина, которые разделяются между восемью местами инъекции, до примерно пятидесяти единиц токсина, которые разделяются между десятью местами инъекции; в трапециевидную мышцу - в количестве от примерно тридцати единиц токсина, которые разделяются между шестью местами инъекции, до примерно пятидесяти единиц токсина, которые разделяются между десятью местами инъекции; и в шейные околопозвоночные мышцы - в количестве примерно двадцати единиц токсина, которые разделяются между четырьмя местами инъекции, так, чтобы общее количество введенного ботулинического нейротоксина было в пределах от примерно 155 единиц до примерно 195 единиц, введенных в 31-39 мест инъекции, соответственно.
[46] В одном аспекте варианты воплощения этого изобретения основываются на обнаружении того, что ботулотоксин может использоваться для лечения пациентов с MOU, как для (а) сокращения количества приступов головной боли, испытываемых пациентом (см. Фигуру 1), так и для (b) сокращения ежедневного использования пациентом лекарств от острой головной боли (Фигура 2). В частности, мы обнаружили (см. Фигуру 3), что ботулотоксин может использоваться для сокращения использования пациентом наркотических обезболивающих лекарственных средств.
[47] Кроме того, мы обнаружили, что пациенты, чрезмерно использующие лекарственные средства для облегчения боли, значительно сокращают использование таких лекарственных средств после лечения ботулотоксином (см. Фигуру 4). Мы также обнаружили значительное сокращение приема триптановых лекарств пациентами, чрезмерно использующими триптановые лекарственные средства (см. Фигуру 5).
[48] Варианты воплощения этого изобретения могут также использоваться как часть протокола дезинтоксикации, согласно которому отлучение пациента от лекарственных средств против острой боли облегчается одновременным введением ботулотоксина. Дополнительные варианты воплощения этого изобретения могут использоваться для лечения других состояний с хронической болью, включая, например, боль в спине, невропатическую боль, аллодинию, фибромиалгию и т.п.
[49] В одном из вариантов воплощения этого изобретения способ лечения пациента с MOU может включать введение ботулотоксина в 31 фиксированное место инъекции в семи мышцах головы/шеи. Необязательно можно использовать до 8 дополнительных мест инъекции в трех определенных мышцах, если такие три мышцы являются подгруппой указанных выше семи мышц головы/шеи, придерживаясь режима отслеживания боли для обеспечения гибкости в выборе дозы на мышцу для выбранных трех мышц в соответствии с потребностями пациента. В определенных вариантах воплощения этого изобретения от минимум 155 единиц ботулотоксина типа А до примерно 195 единиц ботулотоксина типа А вводятся в соответствии с определенной схемой инъекций, описанной здесь.
[50] В определенном варианте воплощения этого изобретения способ лечения MOU, включает этап местного введения ботулинического нейротоксина в лобную мышцу, сморщиватель, мышцу гордецов, затылочную, височную, трапециевидную и шейные околопозвоночные мышцы пациента таким образом, чтобы ботулинический нейротоксин вводился в лобную мышцу в количестве примерно двадцати единиц токсина, разделенных между четырьмя местами инъекции, в сморщиватель - в количестве примерно десяти единиц токсина, разделенных между двумя местами инъекции, в мышцу гордецов - в количестве примерно пяти единиц токсина в одно место инъекции, в затылочную мышцу - в количестве от примерно тридцати единиц токсина, которые разделяются между шестью местами инъекции, до примерно сорока единиц токсина, которые разделяются между восемью местами инъекции; в височную мышцу - в количестве от примерно сорока единиц токсина, которые разделяются между восемью местами инъекции, до примерно пятидесяти единиц токсина, которые разделяются между десятью местами инъекции; в трапециевидную мышцу - в количестве от примерно тридцати единиц токсина, которые разделяются между шестью местами инъекции, до примерно пятидесяти единиц токсина, которые разделяются между десятью местами инъекции; и в шейные околопозвоночные мышцы - в количестве примерно двадцати единиц токсина, которые разделяются между четырьмя местами инъекции, так, чтобы общее количество введенного ботулинического нейротоксина было в пределах от примерно 155 единиц до примерно 195 единиц, введенных в 31-39 мест инъекции, соответственно.
[51] В одном из вариантов воплощения этого изобретения способ лечения депрессии может включать введение ботулотоксина в 31 фиксированное место инъекции в семи мышцах головы/шеи. Необязатеьно можно использовать до 8 дополнительных мест инъекции в трех определенных мышцах, если такие три мышцы являются подгруппой указанных выше семи мышц головы/шеи, придерживаясь режима отслеживания боли для обеспечения гибкости в выборе дозы на мышцу для выбранных трех мышц в соответствии с потребностями пациента. В отдельных вариантах воплощения этого изобретения от минимум 155 единиц ботулотоксина типа А до примерно 195 единиц ботулотоксина типа А вводятся в соответствии с определенной схемой инъекций, описанной здесь.
[52] В определенном варианте воплощения этого изобретения способ лечения неврологических расстройств, таких как, например, депрессия, у пациента, требующего лечения, включает этап местного введения ботулинического нейротоксина в лобную мышцу, сморщиватель, мышцу гордецов, затылочную, височную, трапециевидную и шейные околопозвоночные мышцы пациента таким образом, чтобы ботулинический нейротоксин вводился в лобную мышцу в количестве примерно двадцати единиц токсина, разделенных между четырьмя местами инъекции, в сморщиватель - в количестве примерно десяти единиц токсина, разделенных между двумя местами инъекции, в мышцу гордецов - в количестве примерно пяти единиц токсина в одно место инъекции, в затылочную мышцу - в количестве от примерно тридцати единиц токсина, которые разделяются между шестью местами инъекции, до примерно сорока единиц токсина, которые разделяются между восемью местами инъекции; в височную мышцу - в количестве от примерно сорока единиц токсина, которые разделяются между восемью местами инъекции, до примерно пятидесяти единиц токсина, которые разделяются между десятью местами инъекции; в трапециевидную мышцу - в количестве от примерно тридцати единиц токсина, которые разделяются между шестью местами инъекции, до примерно пятидесяти единиц токсина, которые разделяются между десятью местами инъекции; и в шейные околопозвоночные мышцы - в количестве примерно двадцати единиц токсина, которые разделяются между четырьмя местами инъекции, так, чтобы общее количество введенного ботулинического нейротоксина было в пределах от примерно 155 единиц до примерно 195 единиц, введенных в 31-39 мест инъекции, соответственно.
[53] Важно отметить, что способ, являющийся предметом этого изобретения, может обеспечить улучшение функционального состояния пациента. «Улучшение функционального состояния пациента» можно определить как улучшение состояния, измеряемое такими факторами как снижение боли, сокращение времени, проводимого в постели, повышение способности передвигаться, более здоровый и разнообразный образ жизни и/или исцеление, допускаемое нормальным мышечным тонусом. Улучшение функционального состояния пациента может измеряться улучшением качества жизни или показателем качества жизни, обусловленного здоровьем. Качество жизни может оцениваться, например, с использованием процедур (опросных листов) оценки состояния здоровья. SF-12 или SF-36 или с помощью специального Опросного листа по качеству жизни для пациентов, страдающих мигренью. Опросный лист SF-36 позволяет оценить физическое и психическое здоровье пациента в восьми областях физической деятельности, функциональные ограничения, связанные с физическими проблемами, социальную активность, соматическую боль, общее психическое здоровье, функциональные ограничения, связанные с эмоциональными проблемами, жизненную активность и общее ощущение здоровья. Полученные на основании такого опросного листа оценки можно сравнить с опубликованными значениями для различных групп общего населения и пациентов. Специальный опросный лист по качеству жизни для пациентов, страдающих мигренью (версия 2.1), является одним из наиболее часто используемых специальных инструментов оценки влияния мигрени на качество жизни, обусловленное здоровьем. Специальный опросный лист по качеству жизни для пациентов, страдающих мигренью, позволяет оценить влияние мигрени на качество жизни пациента, обусловленное здоровьем, за последние 4 недели в трех основных измерениях: функциональные ограничения, подавление определенных функций и эмоциональное функциональное состояние. Специальный опросный лист по качеству жизни для пациентов, страдающих мигренью, был разработан на основании экспертного обзора литературы и валидирован на клинической выборке из 458 пациентов с впервые диагностированной и стабильной мигренью. В валидационном исследовании специальный опросный лист по качеству жизни для пациентов, страдающих мигренью, показал высокую внутреннюю согласованность (коэффициент надежности Кронбаха α=0,79-0,85), от умеренной до сильной конвергентную валидность, а также достаточную дискриминантную валидность. Martin and Colleagues 21 провели многоцентровое исследование, которое подтвердило данные о высокой внутренней согласованности (коэффициент надежности Кронбаха α=0,86-0,96), высокой надежности и хорошей адекватности всех 14 пунктов специального опросного листа для 267 участников исследования.
[54] Приведенные ниже примеры, не имеющие ограничительного характера, предоставляют специалистам в данной области техники описание конкретных предпочтительных способов лечения хронической мигрени в рамках настоящего изобретения, и такие примеры не предполагают ограничение объема изобретения. В приведенных ниже примерах описаны различные способы несистемного введения клостридиального нейротоксина. Например, путем внутримышечной инъекции, подкожной инъекции или вживлением имплантата с контролируемым высвобождением активного вещества.
ПРИМЕРЫ
[55] Приведенные ниже примеры, не имеющие ограничительного характера, предоставляют специалистам в данной области техники описание конкретных предпочтительных способов лечения хронической мигрени в рамках настоящего изобретения, и такие примеры не предполагают ограничение объема изобретения
[56] Пример 1 - Терапия ботулотоксином типа А головной боли, связанной с хронической мигренью
[57] В спланированных аналогичным образом рандомизированных клинических исследованиях третьего этапа под контролем плацебо, проведенных в разных клинических центрах, 1384 взрослых пациентов, страдающих хронической мигренью, были рандомизированы в группы, которым вводили либо онаботулотоксин А (ботулотоксин типа А) (n=688), либо плацебо (n=696). Оба исследования состояли из 28-дневного периода скрининга при базовой линии (далее именуемого «базовая линия»), 24-недельного двойного слепого этапа (2 цикла инъекций) и 32-недельного открытого этапа (3 цикла терапии). Пациенты посещали исследовательский центр каждые 4 недели и использовали ежедневный телефонный дневник для регистрации симптомов головной боли и лекарственных средств, принятых для борьбы с острой головной болью. Участниками исследования были мужчины и женщины в возрасте от 18 до 65 лет с мигренью в анамнезе, которые отвечали диагностическим критериям, перечисленным в «Международной классификации состояний с головной болью» ICHD-II (2004), Раздел 1 «Мигрень», за исключением пункта «усложненная мигрень», и у которых приступы головной боли случались в течение >15 дней/месяц, причем не менее 50% таких дней были днями с мигренью или вероятной мигренью.
[58] Ботулотоксин типа А блокирует выделение нейротрансмиттеров, связанных с генезом боли. Как было подтверждено доклиническими и клиническими исследованиями, предполагаемым механизмом профилактики головной боли является блокирование периферических сигналов, направляющихся в центральную нервную систему, которое подавляет центральную сенсибилизацию. Раскрытый здесь подход, основанный на фиксированных местах введения, обеспечивает целевое распределение ботулотоксина типа А среди мышц и кожи в зонах иннервации нервов VI и С2.
[59] На основании анализа безопасности, переносимости и эффективности схем введения, изученных в предыдущих исследованиях, была разработана данная схема инъекций. В этом примере определенным используемым ботулотоксином является онаботулотоксин А (препарат БОТОКС® компании «Allergan Inc., Ирвин, Калифорния»). Целевыми мышцами для инъекций были следующие мышцы:
[60] лобная мышца, сморщиватель и мышца гордецов. В предыдущих исследованиях пациенты чаще всего называли лобную и межбровную область местом возникновения и прекращения головной боли; эти и другие исследования показали, что необходимо делать инъекции во все 3 мышцы для достижения максимальной эффективности.
[61] Височные мышцы. В предыдущих исследованиях височная область была второй по частоте упоминания в качестве места возникновения и прекращения головной боли. В соответствии с одним из аспектов этого изобретения в эти мышцы вводится минимальная доза 20 единиц с каждой стороны и сум