Катализаторы, содержащие благородный металл и лантанид, нанесенные на по существу непористую подложку
Иллюстрации
Показать всеИзобретение относится к катализатору для использования в процессах гидрирования. Предлагаемый катализатор содержит благородный металл, который представляет собой палладий, и элемент группы лантанидов, который представляет собой европий, нанесенные на носитель, содержащий по существу непористую стеклосодержащую подложку. Данная стеклосодержащая подложка имеет удельную поверхность, измеренную методом S.A.N2-BET, основанном на тепловой адсорбции/десорбции N2, или методом S.A.Kr-BET, основанном на тепловой адсорбции/десорбции Kr, в диапазоне от 0,01 м2/г до 10 м2/г, и скорость изменения удельной поверхности по хемосорбции натрия SACRNa≤0,5. При этом палладий и европий каждый присутствуют в количестве от 10 частей на миллион по весу до 1% по весу, исходя из веса катализатора. Предлагаемый катализатор обладает селективностью и стабильностью в активности в процессах гидрирования. Изобретение также относится к способу гидрирования сырьевого потока в присутствии данного катализатора и способу получения такого катализатора. 3 н. и 5 з.п. ф-лы, 3 ил., 5 пр.
Реферат
Заявление приоритета
Данная заявка испрашивает приоритет в отношении заявки США №13/108,206, которая была подана 16 мая 2011, содержание которой включено в настоящее описание полностью посредством ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение относится к катализаторам и способам гидрирования исходного сырья, содержащего соединение, имеющее гидрогенизирующийся центр. Характерные катализаторы включают благородный металл и элемент из группы лантанидов, нанесенные на носитель, содержащий по существу непористую подложку.
Описание предшествующего уровня техники
Процессы гидрирования хорошо известны и используются во всех нефтеперерабатывающей, нефтехимической и химической промышленностях. Гидрирование относится к типу химического восстановления, в котором водород добавляют к реагенту в центр ненасыщенности (″гидрогенизирующийся″ центр). В случае органических соединений (например, углеводороды, включающие углеводороды, замещенные гетероатомом), такой центр часто представляет собой углерод-углеродную двойную связь (например, в случае алкенов), углерод-углеродную тройную связь (например, в случае алкинов) или связь углерод-гетероатом с типичными гетероатомами, являющимися кислородом (О), азотом (N) или серой (S) (например, в случае кетонов, карбоновых кислот, сложных эфиров, альдегидов, иминов, нитрилов, тионов, тиокарбоновых кислот, сложных тиоэфиров или тиоальдегидов).
Гидрирование обычно проводят в присутствии катализатора, для того, чтобы активировать молекулярный водород и тем самым достичь экономически привлекательной кинетики реакции при благоприятных условиях температуры и давления. Например, каталитическое гидрирование бензола, имеющего три двойных углерод-углеродных связи в ароматическом кольце, практикуется в коммерческих целях для снижения концентрации бензола в компонентах смеси бензина (и, в конечном счете, в бензине как таковом) до приемлемых уровней. Процессы каталитического гидрирования кетонов и альдегидов являются полезными и фактически незаменимыми для синтезов спиртов в качестве предшественников или конечных ценных продуктов в ряде отраслей промышленности, включая фармацевтические препараты и агрохимикаты. Способы "селективного" гидрирования относятся к разновидности способов гидрирования, которые также имеют значительное промышленное значение. Примеры включают селективное гидрирование примеси ацетилена в исходном сырье, содержащем этилен (например, полученном в качестве продукта термического крекинга этана) и селективного гидрирования бутадиена в исходном сырье, содержащем бутен (например, полученном в качестве продукта крекинга с псевдоожиженным катализатором или дегидрирования бутана). В этих примерах, следовательно, желательно селективно гидрировать относительно более реакционный гидрогенизирующийся центр соединения, присутствующий в исходном сырье (например, гидрогенизирующиеся центры в ацетилене или бутадиене) без гидрогенизации относительно менее реакционного гидрогенизирующегося центра других соединений в исходном сырье, соответствующих продуктам селективного гидрирования (например, этилену или бутену).
Твердые катализаторы, пригодные для гидрирования или селективного гидрирования обычно содержат металлический компонент гидрирования, часто один или более из никеля, платины, палладия, родия или рутения, нанесенные на пористый материал подложки. Другие катализаторы, содержащие по существу непористый материал подложки, и используемые для ряда каталитических процессов, в том числе гидрирование, описаны в заявках США 2009/0275788 и США 2010/0273645. Особое значение в любом способе каталитического гидрирования представляет собой степень конверсии исходных материалов и селективность превращаемых продуктов в желаемый, гидрированный продукт(ы). Продукт процентной конверсии и процентной селективности, который представляет собой процент теоретического выхода целевого продукта(ов), должен быть как можно выше. Другие фундаментальные соображения относятся к активности катализатора на основе уровня конверсии или скорости реакции при данном наборе условий реакции (например, температура, давление и время пребывания или объемная скорость).
Кроме того, имеющееся значительное влияние на общую экономику данного способа гидрирования представляет собой стабильность активности, которая относится к непрерывному времени работы, в течение которого катализатор может поддерживать приемлемый уровень производительности, с точки зрения конверсии и селективности. Стабильность активности может быть определена количественно, например, в соответствии с (i) потерей активности, например, измеренная степень конверсии при заданном наборе условий реакции с течением времени, или в противном случае (ii) скоростью увеличения температуры слоя катализатора, необходимой для сохранения данной активности, например, измеренного уровня конверсии, когда все другие режимы эксплуатации сохраняются неизменными. Стабильность активности регулирует частоту, с которой катализатор гидрирования должен быть заменен и/или регенерирован, и этот параметр поэтому существенно влияет на общий материал и эксплуатационные затраты, необходимые в каталитических процессах гидрирования. Стоимость катализатора в значительной степени зависит от количества используемого металлического компонента гидрогенизации, особенно когда этот компонент включает один или более благородных металлов (например, палладий), которые, как правило, дороги.
Существует, следовательно, постоянная потребность в катализаторах гидрирования и связанных с ними, эффективных способах гидрирования органических соединений, включающих алкины, диены и ароматические соединения, которые протекают с желаемыми скоростями реакции, селективностью и стабильностью в активности.
Краткое раскрытие изобретения
Варианты осуществления настоящего изобретения направлены на катализаторы гидрирования и способы гидрирования с использованием таких катализаторов, имеющих особые характеристики, с точки зрения количества и типа металлического компонента гидрирования (который может содержать один или более каталитически активных компонентов), а также носитель или подложку. Каталитические композиции обеспечивают хорошие характеристики производительности, включая конверсию, селективность и стабильность активности, как требуется при применениях промышленного и селективного гидрирования (например, гидрирования бензола до циклогексана или селективного гидрирования диенов в моноолефины). Аспекты настоящего изобретения относятся к раскрытию катализаторов, проявляющих такие характеристики производительности с использованием низкого содержания компонента металла для гидрирования, который включает благородный металл и элемент из группы лантанидов, нанесенные на по существу непористую подложку, такую как стеклосодержащая подложка. Не будучи связанными какой-либо теорией, полагают, что наблюдаемые преимущества производительности гидрирования от катализаторов, описанных здесь, происходит из способности элемента группы лантанидов изменять или стабилизировать благородный металл. Более конкретные аспекты настоящего изобретения относятся к открытию синергетических эффектов, полученных из сочетания европия с палладием, с получением металлического компонента гидрогенизации в таких катализаторах, обеспечивая тем самым высокую степень активности и/или стабильности гидрирования.
Конкретные варианты осуществления изобретения относятся к катализаторам, содержащим благородный металл и элемент группы лантанидов, нанесенные на носитель, содержащий, состоящий из или состоящий по существу из непористой подложки. Такие подложки в целом могут быть охарактеризованы как имеющие общую площадь поверхности, как измерено S.A.N2-bet или S.A.Kr-bet, от 0,01 м2/г до 10 м2/г. Эти измерения площади поверхности описаны более подробно ниже. В предпочтительном варианте осуществления, благородный металл представляет собой палладий и элемент группы лантанидов представляет собой европий. Каждый из этих элементов может быть использован разумно, так что каждый предпочтительно может присутствовать в количествах менее, чем 1000 частей на миллион (ppm) по весу в расчете на вес катализатора. Типичные, по существу непористые подложки включают различные виды стекла, и особенно в виде волокон (или стекловолокна), такие как AR-стекла, натрий-силикатные стекла с редкоземельными элементами, алюмоборосиликатные стекла, Е-стекла, не содержащие бор Е-стекла, S-стекла, R-стекла, силикатные стекла с редкоземельными элементами, Ва-Ti-силикатные стекла, азотированные стекла, А-стекла, С-стекла и СС-стекла и их смеси.
Другие конкретные варианты осуществления изобретения относятся к способам гидрирования или селективного гидрирования исходного сырья, содержащего соединение, имеющее гидрогенизирующийся центр. Способы включают контактирование исходного сырья с водородом в присутствии катализатора гидрирования, как описано выше. Типичные соединения, имеющие по меньшей мере один гидрогенизирующийся центр или центр ненасыщенности, включают углеводороды, замещенные гетероатомом, имеющие в качестве гидрогенизирующегося центра связь углерод-гетероатом, где гетероатом выбран из группы, состоящей из О, N, S. Другие соединения включают углеводороды, такие как олефины, алкины или ароматические соединения, содержащие от 2 до 20 атомов углерода и по крайней мере одну углерод-углеродную двойную связь (например, по меньшей мере две углерод-углеродные двойные связи, такие как в случае диена), либо по крайней мере одну углерод-углеродную тройную связь. Конкретные типы соединений, которые могут содержаться в сырье и быть гидрогенизированы или селективно гидрированы, включают алкины (например, ацетилен), диены (например, бутадиен) и ароматические углеводороды (например, бензол).
В типичных способах соединение, содержащее гидрогенизирующийся центр, превращают в соответствующее соединение, в котором один или более гидрогенизирующийся центр(ы) является/являются насыщенными (например, циклогексан), с выходом по меньшей мере 90%. В случае селективных способов насыщения, гидрогенизирующийся центр, который насыщен до указанной степени, является относительно более реакционным или восприимчивым к гидрогенизации, по сравнению с другим типом гидрогенизирующегося центра, который является относительно менее реакционным. Менее реакционно-способный гидрогенизирующийся центр данного соединения может относиться к гидрогенизирующемуся центру, который сохраняется после гидрогенизации более реакционного гидрогенизирующегося центра (например, оставшаяся углерод-углеродная двойная связь этилена после селективного гидрирования ацетилена или оставшаяся углерод-углеродная двойная связь бутена после селективной гидрогенизации бутадиена). Таким образом, эти более и менее реакционные гидрогенизирующиеся центры могут присутствовать в том же самом соединении (например, диен) в исходном сырье или иным образом присутствуют в различных соединениях (например, алкин и олефин) исходного сырья.
Кроме того, конкретные варианты осуществления изобретения относятся к способам получения катализатора гидрирования, которые описаны выше. Способы включают (а) контактирование волокон, по существу, непористой подложки с кислотой (например, неорганической кислотой, такой как азотная кислота, хлористоводородная кислота или серная кислота) с получением кислотно-выщелоченной подложки, (b) ионный обмен кислотно-выщелоченной подложки с одним или более ионообменным раствором, содержащим ионы благородного металла (например, палладия) и ионы элемента группы лантанидов (например, европия), чтобы обеспечить ионообменную подложку, содержащую благородный металл и элемент группы лантанидов, нанесенные на нее; и (с) восстановление ионообменной подложки в присутствии водорода в условиях восстановления, с получением катализатора. В предпочтительном варианте осуществления, ионный обмен кислотно-выщелоченной подложки осуществляется с помощью простого ионообменного раствора, содержащего как ионы палладия, так и ионы европия (например, с ионами палладия, присутствующими либо как нитрат тетрааминопалладия либо как гидроксид тетрааминопалладия, и ионов европия, присутствующих как нитрат европия). Предпочтительно, условия восстановления включают температуру от 100°C (212°F) до 400°C (752°F) и поток водорода.
Эти и другие варианты осуществления, а также связанные с ними преимущества, относящиеся к настоящему изобретению, являются очевидными из последующего подробного описания.
Краткое описание фигур
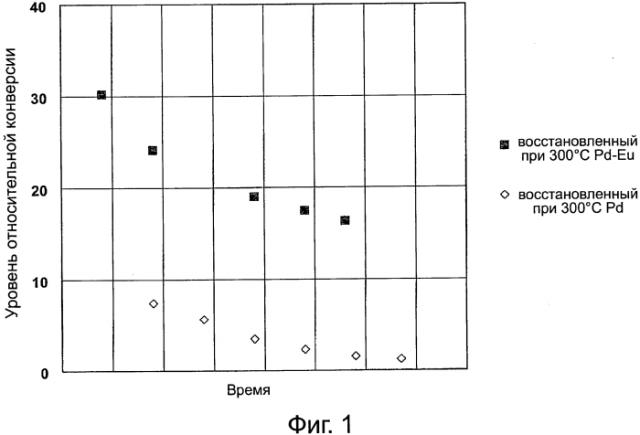
Фиг. 1 представляет график, показывающий конверсию как функцию от времени для гидрирования 1-метил-циклогексена до 1-метил-циклогексана, в присутствии катализаторов из благородного металла/элемента группы лантанидов, которые описаны здесь.
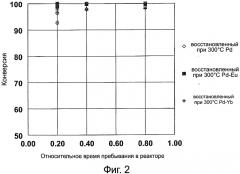
Фиг. 2 представляет график, показывающий конверсию как функцию от времени пребывания в реакторе для гидрирования 1-гептен в гептан в присутствии катализаторов из благородного металла/элемента группы лантанидов, которые описаны здесь.
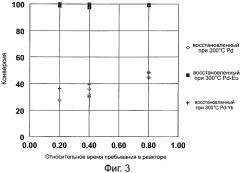
Фиг. 3 представляет график, показывающий выход н-гептана в зависимости от времени пребывания в реакторе для гидрирования 1-гептена в гептан в присутствии катализаторов из благородного металла/элемента группы лантанидов, которые описаны здесь.
Подробное раскрытие изобретения
Как описано выше, аспекты настоящего изобретения относятся к катализаторам, содержащим благородный металл и элемент группы лантанидов, нанесенные на носитель, содержащие по существу непористую подложку, способам гидрирования с использованием этих катализаторов, а также к способам получения этих катализаторов. В общем, по существу непористая подложка может присутствовать в носителе в количестве до 100%, и в этом случае носитель будет состоять из по существу непористой подложки. Согласно другим вариантам осуществления изобретения, например, когда формующая среда присутствует в носителе, по существу непористая подложка может присутствовать в носителе в количественном диапазоне от 10% до 99% по весу, и часто от 50% до 90% по весу. Типичная формирующая среда включает бемит, водный оксид титана и TiO2, водный диоксид циркония и ZrO2, гамма-оксид алюминия, альфа-оксид алюминия, диоксид кремния, глины, природные и синтетические полимерные волокна, полимерные смолы и полимеры, растворимые в растворителе и в воде.
Характеристика подложки, как по существу непористой, не исключает наличие в подложке материально незначительных количеств пор микро-, мезо и/или макро-объема, которые не оказывают вредного воздействия на рабочие характеристики катализатора гидрирования. Поскольку объем микропор в материале часто трудно обнаружить, измерения удельной поверхности с помощью различных аналитических методов может иметь значение при определении, является ли данная подложка по существу непористой. Один из методов определения степени микро-, мезо- и/или макро-объема пор основан на термической адсорбции/десорбции. В случае измерений относительно высокой удельной поверхности, а именно по меньшей мере 3 м2/г, используют N2 BET (на основе N2 тепловой адсорбции/десорбции) в соответствии с ASTM D3663-03 ("S.A.N2-BET"). В случае измерения относительно низкой удельной поверхности, а именно, менее 3 м2/г, используют Kr BET (на основе Kr тепловой адсорбции/десорбции) в соответствии с ASTM D4780-95 ("S.A.Kr-BET"). Другой метод определения степени микро-, мезо- и/или макрообъема пор основан на хемосорбции натрия. Удельная поверхность по хемосорбции натрия ("S.A.Na") может быть выражена как изменение в зависимости от времени в титрующем растворе NaOH, с использованием аналитических методов, описанных R. Iler в работе CHEMISTRY OF SILICA, John Wiley & Sons (1979) на c.203 и 353, который характеризуется как скорость изменения S.A.Na ("SARCNa"). Дальнейшие подробности относительно измерения S.A.Na с использованием эмпирической процедуры титрования, можно найти в заявке США 2009/0275788, включенной в виде ссылки по отношению к указанному измерению. SARCNa обозначает соотношение двух объемов титрующего раствора NaOH. Знаменатель этого отношения представляет собой объем раствора титрования NaOH, использованный на начальном этапе для титрования в нулевой момент времени, t0, смеси суспензии подложки, содержащей 1,5 г подложки в растворе 3,4 М NaCl от pH 4 до pH 9 при 25°C. До этого первоначального титрования, водную смесь суспензии доводят до pH 4, либо с помощью небольшого количества кислоты (например, HCl), либо основания (например, NaOH), по мере необходимости. Совокупный объем раствора титрования NaOH, использованный в трех 5-минутных интервалах, чтобы поддерживать смесь суспензии подложки при pH 9 в течение 15 минут, представляет собой Vtotal-Vi (например, V5 до 15), который является числителем соотношения SARCNa. Поэтому, если Vtotal-Vi составляет меньше, чем или равен 0,5Vi, значение SARCNa равно меньше, чем или равно 0,5.
Типичные по существу непористые подложки имеют удельную поверхность, как измерено S.A.N2-BET или S.A.Kr-BET, в пределах от 0,01 м2/г до 10 м2/г. Согласно предпочтительным вариантам осуществления изобретения, в дополнение к соответствию этой удельной поверхности, характерные по существу непористые подложки имеют SARCNa 0,5 или меньше. Такие предпочтительные подложки с SARCNa≤0,5 будут по существу непористыми, как определено здесь, при условии, что S.A.N2-BET или S.A.Kr-BET также находится в диапазоне от 0,01 м2/г до 10 м2/г. Когда указанные параметры удельной поверхности удовлетворительны, до той степени, что подложка имеет любой объем микропор, мезопор и/или макропор, этот объем имеет недостаточную концентрацию пор, распределение и/или тип, чтобы отрицательно воздействовать на выполнение гидрогенизации полученной каталитической композиции.
Типичные по существу непористые подложки представляют собой композиции стекла и, предпочтительно, композиции стекловолокон. Примеры видов стекла для использования в качестве по существу непористых подложек включают E-стекла, не содержащие бор E-стекла, S-стекла, R-стекла, AR-стекла, силикатные стекла с редкоземельными элементами, Ba-Ti-силикатные стекла, азотированные стекла, такие как Si-Al-O-N стекла, A-стекла, C-стекла и CC-стекла. Каждый из этих типов стекла хорошо известен в данной области техники, в частности в отношении композиций они используются. AR-стекло, например, как правило, содержит основные оксиды типовых модификаторов структуры стекла в существенных количествах, часто 10% по весу или более от общей массы композиции стекла. Эти основные оксиды модификатора структуры включают оксиды Zr, Hf, Al, лантанидов и актинидов, а также оксиды щелочноземельных металлов (группа 2), оксиды щелочных металлов (группа 1), и тому подобное. Стекла, содержащие оксиды Zr, Hf, Al и/или лантаниды, и/или оксиды щелочноземельных металлов и/или оксиды щелочных металлов являются предпочтительными. Стекла, содержащие оксиды Zr являются особенно предпочтительными.
Стекло A-типа обычно содержит модификаторы структуры стекла либо с кислотным, либо с основным типом оксида, включая оксиды Zn, Mg, Ca, Al, B, Ti, Fe, Na, и/или K. В случае основных модификаторов структуры, введенное количество, как правило, составляет менее 12% по весу. Стекла, содержащие оксиды Mg, Ca, Al, Zn, Na и/или K, являются предпочтительными.
Стекло E-типа, которое включает в себя не-выщелоченный E-тип стекла, как правило, содержит модификаторы структуры стекла либо с кислотным, либо с основным типом оксида, включая оксиды Zn, Mg, Ca, Al, B, Ti, Fe, Na, и/или K. В случае основных модификаторов структуры, введенное количество в не-выщелоченные стекла E-типа, как правило, составляет менее, чем 20% по весу. He-выщелоченные E-стекла, содержащие Mg, Ca, Al, Zn, Na и/или K, являются предпочтительными.
По существу непористая подложка может присутствовать в каталитической композиции в различных формах. Примеры включают волокна (т.е. в виде волокон, таких как стекловолокно), фибриллированные волокна, цилиндрические частицы (например, гранулы), сферические частицы (например, сферы), эллиптические частицы (например, эллипсоиды), плоские частицы (например, хлопья), частицы неправильной формы с переломом, частицы спиральной или винтовой формы, экструдаты, кольца, седла, картриджи, мембраны, спирально соединенные мембраны, фильтры или их комбинации. В случае волокнистой формы, подложка может быть, более предпочтительно, тканевым композитом, не тканевым композитом (например, имеющим однонаправлено ориентированные волокна), ячеистой сеткой, жгутовыми волокнами, рубленным волокнистым материалом (например, войлочный материал) или их комбинацией. Предпочтительно, когда стекла, такие как A-стекла и E-стекла, используются в качестве по существу непористой подложки, они находятся в форме волокон. Типичные волокна имеют диаметры в диапазоне от 100 нанометров (нм) до 1 микрона (мкм), и часто от 200 нм до 800 нм.
Поверхность подложки, в частности стеклянной подложки, может быть активирована путем обработки кислотным выщелачиванием, включающем контактирование подложки, например, в виде волокон, с кислотой, подходящей для удаления желаемых ионных частиц, по существу гетерогенным образом по всей поверхности подложки. Это удаление обычно достигается без значительной эрозии структуры подложки и/или значительного создания микропористой структуры, или на или под поверхностью. Кислота может быть органической или неорганической, неорганические кислоты являются предпочтительными. Характерные кислоты включают азотную кислоту, фосфорную кислоту, серную кислоту, соляную кислоту, уксусную кислоту, хлорную кислоту, бромистоводородную кислоту, хлорсульфоновую кислоту, трифторуксусную кислоту и их смеси.
Соответствующая сила раствора кислоты для использования в обработке кислотным выщелачиванием зависит от свойств подложки, например, ее сродства к иону(ам), который должен быть удален (например, из структуры стекла), ее силы после удалении определенных ионов структуры и других свойств. Сила или концентрация раствора кислоты, используемая при обработке кислотным выщелачиванием находится в пределах обычно от 0,5% до 50%, обычно от 1% до 25% и часто от 2,5% до 10% по весу.
Другие условия кислотного выщелачивания, включая условия термообработки (например, температура нагрева для кислотного выщелачивания, время нагрева для кислотного выщелачивания и условия смешивания для кислотного выщелачивания), для обработки кислотным выщелачиванием выбраны с учетом типа и силы используемой кислоты и свойств подложки. Характерные температуры нагрева для кислотного выщелачивания, как правило, составляют от 20°C (68°F) до 200°C (392°F), как правило, от 40°C (104°F) до 120°C (248°F) и часто от 60°C (140°F) до 95°C (203°F). Характерное время нагрева для кислотного выщелачивания (т.е. продолжительность нагрева до достижения нужной температуры нагрева подложки и кислоты), как правило, составляет от 15 минут до 48 часов и, как правило, от 30 минут до 12 часов. Характерные условия перемешивания для кислотного выщелачивания (т.е. времени нагрева в течение ионного обмена) для подложки и кислоты включают непрерывное или прерывистое перемешивание.
Смешивание может быть выполнено вручную (например, путем встряхивания) или может быть автоматизировано (например, во вращающемся барабане, прокатыванием, встряхивание, и т.д.).
После обработки кислотным выщелачиванием, кислотно-выщелоченную подложку предпочтительно отделяют от кислоты любым подходящим способом, включая фильтрацию, центрифугирование, декантацию и т.п. Кислотно-выщелоченную подложку, как правило, промывают одним или несколькими подходящими для промывания жидкостями, такими как деионизированная вода и/или подходящий водорастворимый органический растворитель (например, метанол, этанол или ацетон) и затем сушат при комнатной температуре или при повышенной температуре (например, до 150°C (302°F)) в течение обычно от 1 до 24 часов.
В целом, условия кислотного выщелачивания, как правило, основаны на желаемой степени модификации свойств поверхности подложки. Эти свойства включают изоэлектрическую точку (IEP), а также тип и степень поверхностного заряда, например, необходимого для получения поверхностно-активного состояния, желаемого либо для последующей обработки(ок) подложки, либо для использования в катализаторе. Значение IEP и типичные диапазоны IEP для по существу непористой подложки, а также ряд других возможных способов модификации свойств поверхности подложки, включая активацию поверхности подложки, обработку для удаления загрязнений подложки (например, прокаливанием), обработку кислотным выщелачиванием (в том числе обработку с хелатирующими агентами), обработку обратным ионным обменом (ВГХ) и регулирование рН как ВГХ-обработанной, так и необработанной BIX подложки, изучены подробно в заявке США 2009/027578, и эти учения включены в настоящее описание посредством ссылки.
Носитель катализатора, содержащий по существу, непористую подложку (например, стекловолокно), после возможного выщелачивания кислотой (для обеспечения кислотно-выщелоченной подложки) и/или любой другой обработки поверхности, как описано выше, затем приводят в контакт с каталитически активными составляющими, а именно, благородным металлом (например, рутением, родием, палладием, серебром, осмием, иридием, платиной и/или золотом) и элементом группы лантанидов (например, лантаном, церием, неодимом, европием и/или иттербием). Предпочтительно, указанные каталитически активные компоненты присутствуют в растворе, таком как водный раствор, и, предпочтительно, ионообменный раствор. Иллюстративные варианты осуществления настоящего изобретения, следовательно, включают ионообменную подложку, включая кислотно-выщелоченную подложку или подложку, которая была подвергнута любой другой обработке поверхности, или комбинации обработок, описанных здесь, с одним или более ионообменных растворов, содержащих ионы благородного металла и ионы элемента группы лантанидов, чтобы обеспечить ионообменную подложку, имеющую благородный металл и элемент группы лантанидов, нанесенные на нее.
Любые солевые растворы, содержащие ионы и одного, и другого каталитически активных компонентов, или, иначе, отдельные растворы, содержащие ионы различных каталитически активных компонентов, могут быть использованы для ионного обмена. Ионы каталитически активных компонентов обычно считаются предшественниками этих составляющих, ожидающих, например, регулирования их заряда путем восстановления или окисления, или иным образом до любого другого типа после обработки осаждением. Однако также возможно, что ионы каталитически активного компонента(ов) в ионообменном растворе(ах) могут быть каталитически эффективными в своем состоянии предшественника как нанесенные на по существу непористую подложку. Подходящие каталитически активные ионы компонента способны замещать ионы по существу непористой подложки, либо после выщелачивания кислотой или после другой обработки поверхности, как описано здесь. Иначе, ионы каталитически активных составляющих имеют сродство заряда к этой подложке. Подходящие ионообменные растворы, как правило, солевые растворы, содержащие катионы каталитически активного компонента(ов) и, возможно, другие катионы (например, ионы аммония), а также заряд-компенсирующие противоионы (например, анионы, такие как нитрат, гидроксид, галогениды, оксианионы, и т.д.). Иллюстративные ионообменные растворы для нанесения (через ионный обмен) благородного металла и элемента группы лантанидов на по существу непористую подложку; (например, после обработки кислотным выщелачиванием), следовательно, включают в себя растворы, содержащие соли металлов благородного металла и/или элемента группы лантанидов (и предпочтительно, содержащие металлические соли обоих этих каталитически активных компонентов), например нитрат тетрааминапалладия [Pd(NH3)4NO3], гидроксид тетрааминапалладия [Pd(NH3)4OH], нитрат европия [Eu(NO3)3], нитрат иттербия [Yb(NO3)3] и т.д.
Как правило, концентрация растворов солей, используемых для ионообменной обработки для нанесения каталитически активных компонентов, таких как благородный металл и элемент группы лантанидов, на по существу непористую подложку, зависит от типа подложки, природы любых обработок поверхности, которым подложка была подвергнута, сродства ионов каталитически активных компонентов к поверхности подложки, а также желаемых концентраций каталитически активных компонентов на получаемом катализаторе гидрирования. Для большинства типов стеклянных подложек, таких, как AR, А или известково-натриевого стекла, концентрация типичных солевых растворов такова, что процент по весу (на вес раствора) ионов данного каталитически активного компонента (например, Pd+2) составляет от 1 части на миллион до 1000 частей на миллион (ppm).
Ионы различных каталитических компонентов (например, ионы благородного металла Pd+2 и ионы элемента группы лантанидов Eu+3) могут быть заменены одновременно, например, в случае единственного ионообменного раствора, содержащего ионы как благородного металла (металлов), так и элемента(ов) группы лантанидов, или в противном случае, они могут быть заменены последовательно, например, в случае раздельных ионообменных растворов, содержащих ионы различных каталитических компонентов. В любом случае, концентрация(и) растворов соли является/являются основанной на относительной загрузке желаемой для каждого вида каталитической составляющей (или предшественника компонента катализатора) на по существу непористую подложку, учитывая относительное сродство для каждого типа каталитического компонента. Например, относительно высокое сродство к данному каталитическому компоненту может потребовать использования ионообменного раствора, имеющего относительно низкую концентрацию указанной составляющей для достижения заданной концентрации указанной составляющей на полученный катализатор. В целом, иллюстративные способы получения катализаторов, описанных здесь, следовательно, включают ионный обмен по существу непористой подложки (например, кислотно-выщелоченный подложки) с одним или более ионообменных растворов, содержащих ионы благородного металла и ионы элемента группы лантанидов, чтобы обеспечить ионообменную подложку, имеющую благородный металл и элемент группы лантанидов, нанесенные на нее.
Как и в случае обработки кислотным выщелачиванием, описанным выше, условия для ионного обмена также включают условия термообработки (например, температуру нагрева для ионного обмена, времени нагрева для ионного обмена и условия перемешивания для ионного обмена). Такие ионообменные условия термообработки выбирают с учетом типа и прочности, используемого ионообменного раствора, и свойств подложки. Характерная температура нагрева для ионного обмена, как правило, составляет от 20°C (68°F) до 200°C (392°F), как правило, от 40°C (104°F) до 120°C (248°F), и часто от 60°C (140°F) до 110°C (230°F). Характерное время нагрева для ионного обмена (т.е., продолжительность нагрева до достижения нужной температуры нагрева ионообменного раствора и подложки, например, после обработки кислотным выщелачиванием), как правило, составляет от 15 минут до 48 часов, обычно от 30 минут до 12 часов.
Характерные условия перемешивания для ионного обмена (т.е. в течение времени нагрева ионного обмена) для подложки и ионообменного раствора включают непрерывное или прерывистое перемешивание. Смешивание может быть выполнено вручную (например, путем встряхивания) или может быть автоматизировано (например, во вращающемся барабане, прокатыванием, встряхиванием, и т.д.).
После ионного обмена подложки, после того, как первоначально, необязательно подвергали любому из поверхностных способов для модификации свойств поверхности подложки (например, кислотное выщелачивание), полученную ионным обменом подложку предпочтительно отделяют от ионообменного раствора любым подходящим способом, включающим фильтрацию, центрифугирование, декантацию и т.п. Ионообменную подложку, как правило, промывают одной или несколькими подходящими для промывки жидкостями, такими как деионизированная вода и/или подходящий водорастворимый органический растворитель (например, метанол, этанол, или ацетон) и затем сушат при комнатной температуре или при повышенной температуре (например, вплоть до 150°C (302°F)) в течение обычно от 1 до 24 часов.
Условия термообработки для ионного обмена обычно выбирают с учетом типа и силы используемого ионообменного раствора, и свойств подложки (например, сродство иона (ионов), подлежащего обмену в и из структуры стекла, прочности стекла, после того как определенные ионы из структуры удалены, и т.д.) и времени нагрева для ионного обмена. В целом, сочетание ионообменной силы раствора и условий термообработки пригодно для интеграции достаточного количества и распределения ионов каталитических компонентов на и/или в подложке, которые необходимы для получения каталитической композиции, эффективной для использования по назначению. Как обсуждалось выше, предпочтительные катализаторы гидрирования, описанные здесь, в то же время являясь эффективными, чтобы катализировать гидрирование или желаемую реакцию селективного гидрирования, преимущественно содержат относительно малые количества каталитически активных компонентов, например, менее чем 1% по весу (например, от 10 частей на миллион по весу до 1% по весу) одного или более благородных металлов и менее чем 1% по весу (например, от 10 частей на миллион по весу до 1% по весу) одного или более элементов группы лантанидов. Эти массовые проценты выражены на основе веса катализатора, включая по существу непористую подложку, любую среду формирования, как описано выше, и/или любой другой компонент катализатора. Согласно конкретным вариантам осуществления изобретения, катализатор может содержать менее чем 1000 частей на миллион по весу (например, от 100 частей на миллион по весу до 1000 частей на миллион по весу) одного или более благородных металлов и менее чем 1000 частей на миллион по весу (например, от 100 частей на миллион по весу до 1000 частей на миллион по весу) одного или более элементов группы лантанидов.
После ионного обмена, ионообменная подложка может быть дополнительно обработана для регулирования свойств подложки и/или каталитических компонентов, например, состояния окисления каталитических компонентов. В соответствии с вариантами осуществления изобретения, такие дополнительные обработки могут быть выполнены в реакторе, предназначенном для выполнения процесса гидрирования (т.е. in situ в реакторе гидрирования). Типичные обработки после ионного обмена включают регулирование рН (чтобы изменить поверхностный заряд), прокаливание, окисление, восстановление, сульфидирование, карбидирование, азотирование, фосфидирование и борирование, как описано в заявке США 2009/0275788, содержание которой, касающееся таких пост-ионообменных обработок, включено в данное описание путем ссылки. Предпочтительная обработка после ионного обмена представляет собой восстановление или стадию восстановления, которые снижают степень окисления одного или нескольких каталитических компонентов. Согласно конкретным вариантам осуществления изобретения, способы получения катализаторов, описанные здесь, включают восстановление ионообменной подложки в присутствии водорода в условиях восстановления, с получением катализатора.
Катализаторы, описанные здесь, содержащие благородный металл и элемент группы лантанидов, нанесенные на носитель, содержащий по существу непористую подложку, эффективны в способах гидрирования, и более конкретно, в способах гидрирования исходного сырья, содержащего соединение, имеющее гидрогенизирующийся центр, такой как углерод-углеродная двойная связь (например, в случае алкенов), углерод-углеродная тройная связь (например, в случае алкинов) или связь углерод-гетероатом с типичными гетероатомами, представляющими собой кислород (О), азот (N) или серу (S) (например, в случае кетонов, кар