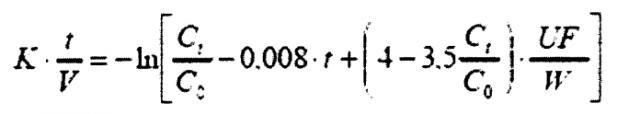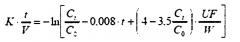Анализ профиля диализата, управляемый с помощью уф мониторинга
Иллюстрации
Показать всеГруппа изобретений относится к медицине, а именно к эфферентной терапии, и может быть использована при проведении процедур диализа. Предложено устройство для обработки крови, содержащее блок обработки крови, УФ измерительное устройство и центральный блок обработки. Также предложен способ оптимизации расхода диализата с помощью указанного устройства, где в блоке обработки крови предварительно осуществляют выбор режима работы и наименьшей допустимой величины параметра эффективности диализа. Определяют текущие измеренные величины потоков крови и диализата в блоке обработки крови. Осуществляют варьирование потока раствора для диализа в блоке обработки крови во время сеанса диализа. Затем измеряют УФ поглощение по меньшей мере одного уремического вещества в выходном потоке диализата или в экстракорпоральной циркуляции крови блока обработки крови. Измеренные величины УФ поглощения и текущие измеренные величины потока крови и диализата передают в центральный блок обработки. Определяют поток раствора для диализа и/или крови, оптимизированный по расходу диализата, и/или относительное отношение двух потоков в пределах диапазона QD/QB, или отношение объемной пропускной способности для диализата и крови в пределах диапазона VD/VB. Изменение потока отображают в центральном блоке обработки и/или осуществляют автоматическую повторную корректировку в соответствии с изменением. Затем этапы повторяют. Изобретения обеспечивают наиболее низкий расход раствора для диализа без ухудшения очистки за счет полного использования потенциала всего фильтра. 2 н. и 22 з.п. ф-лы, 2 ил., 1 табл., 1 пр.
Реферат
Изобретение относится к способу и устройству для определения удаленных уремических веществ из экстракорпоральной циркуляции крови и для корректировки потока, управляемого в соответствии с этими данными. Способ в соответствии с изобретением используют для оптимизации расхода, а также использования объема диализата.
У пациентов с частичной или полной почечной недостаточностью продукты выделения естественного метаболизма, включая уремические токсины, удаляют с помощью такого способа обработки крови, как гемодиализ, где удаление веществ из крови осуществляют экстракорпорально посредством контакта крови с раствором для диализа при так называемой экстракорпоральной циркуляции крови. Транспорт вещества из крови в раствор для диализа осуществляют посредством диффузионных и конвекционных эффектов. Цель состоит в том, чтобы в первую очередь удалить уремические токсины. Это выполняют посредством добавления жизненно важных веществ для пациентов в физиологической концентрации раствора для диализа.
Измерение дозы диализа пациента не может быть осуществлено только на основе наиболее субъективной оценки здоровья пациента. Необходимо количественно определять успешность диализа таким образом, чтобы гарантировать достаточную эффективность диализа. В то же время слишком высокого уровня диализа следует избегать по экономическим причинам. Чтобы сделать обработку диализом более эффективной, необходимо управлять эффективностью диализа во время обработки для того, чтобы управлять им посредством корректировки переменных параметров блока обработки крови вручную или автоматически.
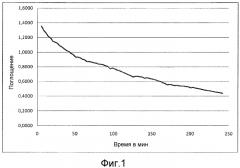
Чтобы гарантировать достаточную диализную терапию, разработана модель Kt/V. Мочевина представляет собой основной метаболический конечный продукт в крови, подлежащей очистке. Следовательно, мочевину используют для определения достаточной диализной терапии. К представляет собой коэффициент очистки крови диализатора мочевины в мл/мин, t представляет собой время обработки в мин и V представляет собой объем распределения мочевины в мл в организме человека, который напрямую связан с массой пациента. Безразмерный показатель Kt/V представляет собой показатель снижения азота, связанного в мочевине, в крови пациента. Этот процесс во времени показан на фиг.1. Определение концентрации мочевины и/или концентрации других токсических веществ в выходном потоке диализата обеспечивает исчерпывающий мониторинг прогресса диализа. Однако, образцы все еще нужно брать вручную из экстракорпоральной системы, и отправлять на химический анализ в соответствующим образом оборудованную лабораторию. Таким образом, непосредственное управление устройством для диализа все еще исключено во время диализа каждого пациента. Поскольку пациенты, требующие диализа, обычно хронически больны и должны регулярно проходить диализ, при таком способе управления необходимо повышенное обеспечение персоналом и постоянно нести расходы на анализ. Также частое взятие образцов из экстракорпоральной циркуляции крови ведет к маленькому, но реальному риску заражения бактериями и вирусами.
Следовательно, необходим непрерывный мониторинг гемодиализа (IEEE Engineering in Medicine & Biology Society 11th International Conference; Proceedings). Из известного уровня техники известен такой параметр, как изменение проводимости раствора для диализа посредством гидролиза мочевины и/или других важных молекул. На практике доказано, что калибрование датчиков проводимости, которые разработаны специально для этого применения, является очень утомительным и нестабильным, поскольку на проводимость также могут влиять другие источники. Кроме того, посредством измерений проводимости измеряют не отдельные вещества, а только присутствие электролитов, что является не достаточно точным.
Кроме того, непрерывный мониторинг гемодиализа можно осуществлять путем измерения оптического поглощения. На пропускание раствора для диализа влияет преимущественно мочевая кислота и другие низкомолекулярные вещества. Такое измерительное устройство описано через систему УФ мониторинга автором Fridolin в EP 1083948 B1.
В EP 1543852 B1 описано устройство для диализа, в котором измерение гематокрита в крови пациента также используют для того, чтобы корректировать идеальную кривую для крови и параметры обработки, основываясь на этом измерении. Измерение УФ поглощения не предусмотрено в этом способе.
Отношение образования мочевой кислоты к мочевине в значительной мере постоянно у пациентов, независимо от степени почечной недостаточности. Другими словами, количества мочевины и мочевой кислоты, образуемых в единицу времени, хорошо коррелируют друг с другом. Скорости выведения обоих веществ при физиологических условиях достаточно схожи. Следовательно, измерение концентрации мочевой кислоты в выходном потоке диализата непосредственно связано с потоком раствора для диализа, показателем количества удаленной мочевины. Преимущество измерения поглощения мочевой кислоты заключается в том факте, что мочевая кислота, в отличие от мочевины, имеет резкую и характерную полосу в УФ диапазоне, которая находится между 280 нм и 290 нм.
Цель изобретения состоит в том, чтобы предоставить систему мониторинга в реальном времени, с помощью которой можно управлять потоком раствора для диализа и/или крови. До сих пор непосредственный способ оптимизации операции диализа и его реализация в блоке обработки крови не доступны, поскольку данные о качестве диализа - если их вообще получают - определяют только после обработки и, таким образом, тонкая корректировка не возможна.
Неожиданно обнаружено, что данные, получаемые посредством системы фотометрического измерения концентрации, можно использовать не только для анализа и мониторинга успешности процедуры диализа, но также для вычисления управления блоком обработки крови. В настоящем изобретении описаны способ и устройство, в которых измеренная величина, которую получают в реальном времени, может быть использована для управления всей процедурой диализа. Эту цель достигают посредством предоставления способов и устройств согласно независимым пунктам формулы изобретения. Кроме того, преимущественные варианты осуществления, аспекты и подробности изобретения раскрыты в зависимым пунктах формулы изобретения, на фигурах и в описании.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Основа данного изобретения состоит в мониторинге качества диализа в реальном времени, которое определяет посредством фотометрического поглощения в выходном потоке диализата эффективность диализа в форме величины Kt/V. В предпочтительных вариантах осуществления измеряют УФ поглощение.
В дополнительных вариантах осуществления фотометрическое поглощение можно измерять альтернативно или дополнительно в потоке крови. В предпочтительных вариантах осуществления это измерение в крови осуществляют между доступом пациента и входом в диализатор. Таким образом, следующие описание и варианты осуществления относятся не только к фотометрическому поглощению в части диализата, но также в части крови.
Под общим термином «блок обработки крови» понимают все устройства, которые можно использовать для очистки и/или обработки крови. Наиболее общеупотребительными способами являются гемодиализ с двумя иглами, гемодиализ с одной иглой, перекрестный гемодиализ с одной иглой, перитонеальный диализ, гемоперфузия, гемодиафильтрация после разведения, гемодиафильтрация до разведения, гемодиафильтрация до и после разведения, гемофильтрация после разведения, гемофильтрация до разведения, гемофильтрация до и после разведения или последовательный гемодиализ.
Термин «диализ» относится к способам очистки, в которых два течения жидкости разделяют проницаемой мембраной, но которая делает возможным желаемый обмен веществ. Один поток жидкости, в этом случае кровь, несет вещества, которые сами подлежат удалению, тогда как другой поток раствора для диализа должен принять эти вещества.
Важным и известным способом диализа является гемодиализ, который осуществляют стандартно для очистки крови при частичной или полной почечной недостаточности. В настоящем документе, кровь, подлежащую очистке, диализируют экстракорпорально через полупроницаемую мембрану напротив раствора для диализа. Уремические токсины удаляют из крови и очищенную кровь возвращают в циркуляцию крови организма. Чтобы избежать того, что посредством диализа физиологически важные вещества удаляются из крови, раствор для диализа обогащают теми же веществами. Таким образом, добиваются фокусировки на удалении уремических токсинов и продуктов выделения.
Основополагающим принципом диализа является фильтрование, в частности, фильтрование тангенциальным потоком (TFF; также известное как фильтрование в перекрестном потоке). Кровь, подлежащую очистке, пропускают через фильтрующий модуль из полых волокон, существующий диализатор или диализные фильтры. Стенку этих полых волокон отделяют полупроницаемой мембраной от очищающего раствора (раствора для диализа). Раствор для диализа типично имеет более низкую концентрацию веществ, которые подлежат удалению из жидкости, подлежащей очистке. Эта разница в концентрации ведет к диффузии. Чтобы оптимально использовать диффузию в качестве разделяющей силы, современные тангенциальные фильтры предпочтительно работают по принципу встречного потока.
Другим механизмом очистки является конвекция. Здесь создают градиент давления на диализном фильтре, посредством чего жидкость, подлежащую очистке, продавливают через полупроницаемую мембрану. Таким образом, происходит очистка от веществ в их текущей концентрации. При гемодиализе этот эффект относительно мал, поскольку только физиологически необходимый объем жидкости удаляют у пациента. В случае форм конвекционной терапии, таких как гемофильтрация и гемодиафильтрация, когда жидкость удаляют согласованно из крови через этот механизм, это называют ультрафильтрованием. Этот процесс очистки следовательно не зависит от градиента концентрации затронутых веществ. Решающее значение здесь имеют мембрана и свойства материала, такие как диаметр пор, расстояние фильтрования, коэффициент просеивания, проницаемость и т.д., коэффициент просеивания представляет собой функцию размера молекулы, электрического заряда, формы и агрегатного состояния вещества, подлежащего удалению. Проницаемость представляет собой отношение транспортируемого количества вещества в единицу времени и произведения градиента концентрации и площади сечения.
Объем жидкости, удаляемый посредством ультрафильтрования, должен быть замещен до естественного количества воды, подлежащего устранению, которое соответствует естественному объему мочи. Это можно осуществлять посредством замены на раствор заменителя, типично физиологический солевой раствор.
В дополнение к диализной терапии существуют другие способы очистки крови, такие как аферез, который допускается, независимо от почечной недостаточности от острых симптомов, таких как гиперкалиемия, метаболический ацидоз, чрезмерная гидратация (например, отек легких), уремический серозит (например, перикардит или уремическая энцефалопатия) или отравление диализуемыми веществами, такими как литий или ацетилсалициловая кислота. Хронически встречающимися симптомами, для которых показан диализ, среди прочих, являются низкий уровень клубочковой фильтрации, гиперфосфатемия или уремия. Способ управления соответствующим способом лечения согласно изобретению можно использовать также для лечения указанных выше симптомов или заболеваний. Дополнительно описанные способы очистки крови также часто включают в общий термин «диализ».
Способом непрерывного лечения пациента с почечной недостаточностью является перитонеальный диализ. Он представляет собой интракорпоральный способ, в котором используют мембранные свойства брюшины. Брюшную полость пациента в этом случае заполняют раствором для диализа, который подают через два порта - входной и выходной.
При гемоперфузии (например, в случае отравления) кровь пропускают экстракорпорально через адсорбент, такой как активированный уголь или ионообменная смола, для того, чтобы удалять рассматриваемые токсины из крови.
При гемофильтрации воду удаляют конвекционно из крови. Здесь прикладываемый градиент давления проталкивает кровь через мембрану. Тем самым, также происходит вымывание уремических веществ. Потери объема компенсируют посредством добавления раствора электролита.
В способе гемодиафильтрации классический гемодиализ и гемофильтрацию комбинируют друг с другом для того, чтобы получить преимущества обоих способов. Таким образом, можно устранять молекулы с низкой и средней молекулярной массой. Следовательно, гемодиафильтрация представляет собой предпочтительный способ очистки крови, в котором можно применять настоящее изобретение.
Термин «ультрафильтрование» относится здесь к фильтрованию через мембрану с давлением от 0 до 1 бар, при котором удерживаются частицы больше, чем приблизительно 0,01 мкм. Это соответствует размеру веществ со средней молекулярной массой, а также макромолекулам, вирусам и коллоидам.
С демографическими изменениями и связанными изменениями в возрастной пирамиде общества главным образом в индустриальных странах эти способы приобретают постоянно возрастающее, поскольку непрерывно растет число пациентов с хронической почечной недостаточностью. Таким образом, в настоящее время, например, в Германии приблизительно 60000 пациентов, которым необходим диализ, в год. Уровень смертности все еще составляет приблизительно 20% в год. Частота возникновения новых случаев составляет 184 на 1 миллион жителей. Также в странах с переходной экономикой число пациентов, подлежащих лечению, будет значительно вырастать в ближайшие годы.
Средний сеанс гемодиализа длится от 4 до 5 часов. Ночной диализ длится вплоть до 8 часов. Такая обработка необходима большинству пациентов по меньшей мере три раза в неделю. Частота обработок зависит в числе прочего от массы тела, остаточной почечной функции и сердечного выброса пациента. Однако, тенденция сводится к осуществлению предпочтительно нескольких более коротких обработок.
Чтобы удовлетворить эту огромную потребность требуется разработанная инфраструктура, и наряду с этим большие потребности в персонале. Также расход материалов огромен. Таким образом, в среднем 5-часовом диализе приблизительно 150 литров раствора для диализа проходит через диализатор. Если экстраполировать, это означает, что пациенту на диализе в год нужно приблизительно 23000 литров раствора для диализа. Поскольку в связи с высокими требованиями к качеству раствора для диализа, мешок стоит дорого, несмотря на простой химический состав, стоимость лечения пациента на диализе в год составляет приблизительно 43000 €. Для 60000 пациентов только для Германии это составит приблизительно 2,58 миллиарда €. Это составляет значительную часть бюджета на здравоохранение. Следовательно, общим интересом является наиболее всестороннее достижение возможностей экономить во время обработки диализом.
В этих огромных издержках кажется необходимым реализовать возможности по экономии, где качество медицинского лечения может не пострадать. Это обозначает, что из крови пациента все еще должна быть удалена допустимая с медицинской точки зрения процентная доля уремических веществ. Чтобы обеспечить это, концентрация ведущих соединений, подлежащих удалению, должна быть определена надежно.
В способе согласно изобретению подразумевается оптимизация КПД диализа. КПД диализа является результатом взаимодействия затрат на диализ и эффективности диализа. Для эффективности диализа должна быть найдена собственная мера. В научной литературе создано множество вычислений для выражения эффективности диализа. Некоторые из величин очень схожи, тогда как другие особо выделяют рассмотрение проблемы. В соответствии с изобретением способ способен предоставлять измеренные величины для всех из установленных параметров, и их сочетаний, с тем, чтобы их можно считать при управлении процессом диализа.
Наиболее общеупотребительным показателем для параметра эффективности диализа является так называемая модель Kt/V. Мочевина является важным метаболическим конечным продуктом в крови, подлежащей очистке. Таким образом, концентрация мочевины является превосходным параметром, используя который можно лучше понять эффективность достаточной диализной терапии. К представляет собой - коэффициент очистки крови диализатора мочевины в мл/мин, t - время обработки в мин, а V - объем распределения мочевины в мл в организме человека, который имеет прямую зависимость от массы пациента. Безразмерный показатель Kt/V представляет снижение азота мочевины в крови пациента.
При гемодиализе предполагаемые величины Kt/V составляют ≥ 1,2. В процессе диализа без технических сложностей такие величины можно использовать в качестве стандарта согласно формуле Даугирдаса:
где
Ct - концентрация мочевины в конце диализа;
C0 - концентрация мочевины в начале диализа;
t - время диализа в часах;
UF - объемы ультрафильтрования в л;
К - коэффициент очистки в мл/мин;
W - сухая масса в кг.
(Изложено в: Halwachs-Baumann: Labormedizin: Klinik - Praxis -Fallbeispiele. 2. Ed. Springer Wien New York, 2011, S. 298.)
Простым показателем является URR (коэффициент снижения мочевины)
URR[%]=(C0-Ct)/C0 * 100,
где C0 - концентрация мочевины в момент 0 (начало диализа или цикла обработки), Ct - концентрация мочевины в фактический момент t. URR[%] - процентная доля, которая удалена за фактическое время t. Предполагают, что величины должны быть больше 65%.
sp Kt/V (Kt/V одного резервуара) учитывает как образование мочевины во время диализа, так и эффект ультрафильтрования:
spKt/V=-In(R-0,008 * t)+(4-3,5 * R) * UF/W,
здесь R=Ct/C0, t - время диализа в часах, UF - объемы ультрафильтрования в л, а W - масса после гемодиализа в кг.
Величина eKt/V (уравновешенное Kt/V) также учитывает остаток мочевины, который встречается даже после окончания диализа. Остаток мочевины относится к такому эффекту, что после окончания диализа концентрация мочевины в крови возрастает снова относительно быстро, поскольку теперь мочевина, находящаяся в плохо кровоснабжаемых тканях и не захваченная посредством диализа, выходит все больше и больше в весь организм.
Эта формула применима к диализу через периферический анастомоз.
TAC/TAD представляет собой показатель того, насколько равномерно отображена концентрация мочевины в крови в течение всего периода. В частности, это интересно в том аспекте, что создают ли выбранный режим диализа и ассоциированная доза диализ желаемую успешность. В настоящем документе, TAC представляет собой среднюю недельную концентрацию мочевины (средняя концентрация по времени). TAD относится к флуктуациям величин TAC и, таким образом, производного показателя. Предполагаются малые величины TAD, поскольку это является признаком того, что опасные и потенциально токсические пиковые величины концентрации мочевины возникают редко или не возникают вовсе.
EKR описывает очистку от мочевины. Здесь
EKR=G/TAC.
G - скорость образования мочевины.
RU относится к количеству удаленной мочевины.
Однако SRI относится к индексу удаления растворенных веществ и рассматривает эффективность диализа обратной стороны:
SRI=1-(Vpost * Cpost)/(Vpre * Cpre),
(Vpost: объем после диализа; Cpost: концентрация после диализа; Vpre: объем перед диализом; Cpre: концентрация перед диализом);
V относится к объему распределения мочевины в крови (см. выше: Kt/V);
К - показатель эффективности конкретного диализатора. Он соответствует эффективной очистке организма.
Все эти указанные выше параметры можно суммировать в том смысле, который соответствует изобретению, под термином «параметр(ы) эффективности диализа».
В соответствии с изобретением, аналогичным образом можно получать измеренные величины для очистки дополнительных важных уремических веществ. Следовательно, фигуры и варианты осуществления, приведенные в описании, в равной мере применимы к этим веществам. В дополнение к мочевине и мочевой кислоте, они, в частности, могут представлять собой креатинин и гиппуровую кислоту.
Измеренные величины, получаемые в соответствии с изобретением, можно находить с использованием предварительно созданного профиля для этого конкретного устройства и/или пациентов. Этот профиль может обеспечивать, например, необходимые выходные величины. Тем самым, обработку можно начинать рано с использованием конфигураций устройства, близких к оптимальной эффективности диализа.
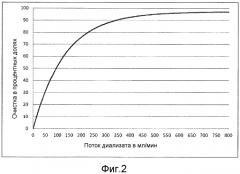
Для оптимизированной очистки, особенно в случае диффузионного транспорта вещества, важно адаптировать поток раствора для диализа под условия обработки или получить информацию о том, как обработку можно оптимизировать с экономической точки зрения. Зависимость между потоком диализата и очисткой показана на фиг.2. Оптимизацию осуществляют преимущественно согласно экономическим критериям. Также необязательно можно учитывать терапевтические аспекты. Они могут включать в себя предварительный выбор режима работы и наименьшую допустимую величину параметра эффективности диализа, но не оказывают дополнительного влияния на оптимизацию согласно экономическим критериям.
Экономизации, т.е. экономии дорогостоящего раствора для диализа в требуемых количествах затем можно достичь, если установлено, что снижение потока раствора для диализа не приведет к уменьшению очистки. Это может представлять собой случай, когда, например, фильтр большой площади соединяют с высоким потоком диализата. В этом случае, может случиться такое, что кровь имеет, например, уже на полпути через фильтр, концентрацию уремических токсинов, которая проявляет тенденцию в направлении очень низких величин. В этом случае, поток раствора для диализа можно снизить, не вызывая уменьшения очистки. Единственное изменение заключается в том, что кровь не является почти полностью очищенной на полпути через фильтр, а только к концу расстояния фильтрования. Следовательно, обработку можно оптимизировать таким образом, что потенциал фильтра полностью используют для того, чтобы сохранить расход раствора для диализа на как можно более низком уровне.
В частности, отмечают, что способ согласно изобретению связан исключительно со способом оптимизации расхода диализата. Изменения конфигурации на основе этого способа в устройстве для диализа не оказывают влияния на диагноз пациента, тип обработки, эффективность обработки и/или успешность обработки. Способ согласно изобретению направлен только на экономические факторы для разумного экономического использования устройства для диализа. На самого пациента он не оказывает ни положительного ни отрицательного эффекта.
На сегодняшний день не существует применения обнаруженного фотометрического сигнала для управления процессом диализа, поскольку данные о качестве диализа и связанном процессе - если это вообще применимо - определяют только апостериори и, следовательно, своевременное вмешательство не возможно. Также не известно такое управление по сигналам проводимости в растворе для диализа.
В противоположном случае может случиться, что увеличение потока диализата вызывает увеличение очистки. Это имеет место, когда кровь покидает диализатор, однако, все еще имеет относительно высокую концентрацию уремических веществ. Посредством увеличения потока раствора для диализа градиент концентрации в фильтре можно повышать и, таким образом, очистку также можно усовершенствовать. Цель состоит в том, чтобы получить оптимальный поток раствора для диализа для текущей ситуации.
Корректировку потока раствора для диализа можно осуществлять или через предварительно определяемые или через свободно выбираемые интервалы или в связи с отклонениям от нормы сигнале мониторинга очистки в реальном времени. Если, например, сигнал остается в течение конкретного периода времени преимущественно неизменным и/или показывает очень высокие абсолютные величины, допускают, что у фильтра превышен потенциал эффективности. Соответственно, поток раствора для диализа должен быть увеличен.
В противоположном случае, при очень низких величинах мониторинга в реальном времени существует возможность снижения потока раствора для диализа.
В предпочтительных вариантах осуществления любое сэкономленное количество раствора для диализа отображают в виде абсолютного величин и/или на основе временного интервала.
Также существует возможность определять в начале обработки объем раствора для диализа, который должен быть затрачен во время обработки и который обеспечивает желаемую очистку. Эту величину можно достичь или посредством постоянного потока в течение терапии или также посредством интеллектуальных ступенчатых профилей. В отличие от постоянного потока, профиль, который начинается с высоких скоростей потока, которые снижаются в ходе процесса обработки, имеет такое преимущество, что в начале терапии создается основа для хорошей диализной терапии и потери качества сохраняются на низком уровне, если осложнения возникают к концу к концу обработки.
Кроме того, изобретение относится к способу, в котором поток раствора для диализа варьируют во время сеанса диализа. Посредством такого способа, получают измеренные величины, которые, когда они связаны друг с другом, дают указание на то, нужно ли поток крови и/или раствора для диализа корректировать повторно или в том смысле, что экономию можно повторно корректировать. Для необходимости повторной корректировки можно определять интервал допуска, в пределах которого допустимы отклонения ожидаемой величины в течение соответствующего времени, а при превышении интервала допуска, однако, следует выполнять повторную корректировку. Ожидаемая величина является результатом экстраполяции первых измеряемых величин во время сеанса диализа. Вдобавок, эмпирические величины для каждого типа устройства диализатора, для отдельного диализатора и из истории пациента можно рассматривать для ожидаемой величины. Для вариации потока раствора для диализа определяют минимальную величину и максимальную величину, между которыми варьирует целый диапазон изменений потока раствора для диализа. Это можно осуществляться согласно предварительно определенной схеме или вводиться пользователем.
Отклонения пределов интервалов допуска и/или интерполированного хода диализа можно использовать в качестве возможности сделать другую вариацию потока раствора для диализа.
Дополнительно, период времени можно определять, в течение которого осуществляют вариацию. Также можно определять скорость измерения, с которой осуществляют вариацию. Эту вариацию можно осуществлять несколько раз во время сеанса диализа. Также эта вариация может иметь место через определенные интервалы, или отдельно при необходимости. В предпочтительных вариантах осуществления временные интервалы в начале сеанса диализа короче, чем в конце, поскольку обычно к концу возникает меньшая вариабельность результатов измерений. Для этого способа применимы такие же варианты осуществления и модификации, которые описаны в настоящем изобретении.
В соответствии с изобретением поток раствора для диализа также можно варьировать, если необходимо. В частности, это имеет место, если фотоспектроскопически измеряемые величины имеют отклонения, которые указывают на признаки непредвиденного и/или неполного процесса сеанса диализа.
Такой характерный ход состоит из очень медленного снижения или очень большой величины количества удаленного вещества. В качестве действия средства исправления, увеличение потока раствора для диализа будет предложено или выполнено.
Наоборот, характерный ход может состоять из очень маленькой величины количества удаленного вещества. В этом случае уменьшение потока раствора для диализа будет предложено или выполнено.
Если случится какое-либо одно из описанных отклонений, это также можно проверять в случае выбранного диализата объем в начале воздействия и корректировать в случае необходимости, как описано выше.
Вкратце, изобретение можно описать следующим образом.
Во время обработки диализом посредством способа измерения в реальном времени осуществляют мониторинг концентрации по меньшей мере одного удаленного вещества в диализате и на основе этого сигнала поток раствора для диализа корректируют так, что достигают оптимального насыщения раствора для диализа в отношении уремических веществ.
В случае определения объема диализата, этот ход используют в начале терапии для того, чтобы определить объем диализата, который затрачен в терапии.
Для того чтобы определять оптимальный поток, варьируют поток диализата и анализируют создаваемое изменение поглощения.
Описанный выше эффект также можно создавать посредством корректировки потока подлежащего очистке текучего вещества, крови. Решающими факторами являются часто не абсолютные потоки отдельных составляющих, но относительный поток двух потоков относительно друг друга.
Частота дискретизации фотоспектроскопического сигнала может быть или предварительно задана производителем или введена пользователями. В соответствии с изобретением интервалы дискретизации и управления находятся между 0,5 секундами и 30 минутами, предпочтительно между 1 секундой и 10 минутами, более предпочтительно между 2 секундами и 5 минутами и наиболее предпочтительно между 10 секундами и 1 минутой.
Однако в некоторых вариантах осуществления интервалы измерений можно расширять во время обработки диализом, или согласно предварительно определяемому алгоритму или согласно отдельным конфигурациям. Предпосылкой для этого является то, что параметры обработки меняются, согласно опыту, более сильно в начале обработки диализом, чем в конце, когда обычно достигают «квазистационарного состояния».
В дополнительных вариантах осуществления сначала регистрируют по меньшей мере две точки измерений. Их используют для определения характеристик очистки. Другую кривую интерполируют. В настоящем документе, можно регистрировать точки измерений с постоянной частотой или можно оптимизировать интервалы измерений в соответствии с ожидаемым ходом.
Предпочтительными являются фотоспектроскопические способы. В настоящем документе, измерительный пучок испускают перпендикулярно направлению потока раствора для диализа. ИК измерительный пучок уже используется во многих современных устройств для диализа. Его используют для обнаружения так называемых утечек крови через полупроницаемую мембрану диализного модуля. Если здесь возникает утечка, нефильтрованная кровь поступает в раствор для диализа и, тем самым, выходит из рециркуляции в организм пациента. В зависимости от степени утечки, она может быть смертельной для пациента. Утечку крови можно обнаруживать посредством мутности в растворе для диализа и тогда сеанс диализа можно прерывать или останавливать. Однако, проблема при измерении водных растворов заключается в двух очень широких характеристических полосах для H2O, которые перекрывают многие измеренные величины. ИК измерения следовательно только представляют интерес для измерения концентрации, в которой выводимое соединение имеет по меньшей мере одну характеристическую полосу за пределами обеих полос H2O.
Поляризованный свет можно использовать только с выводимыми соединениями, которые, во-первых, имеют хиральный центр и, если они имеют его, предоставлены в виде рацемата. Поскольку мочевина не обладает хиральными свойствами, такой способ не может быть использован для измерения мочевины. С другими выводимыми веществами, которые отвечают этому условию, концентрация с вычисляется следующим образом:
с=α/(αt∙d),
(α = измеряемый угол вращения; αt = удельная вращательная способность вещества; d = расстояние измерения, здесь диаметр выходного потока диализата; α и αt зависят от длины волны).
Следовательно, особенно предпочтительным является применение по меньшей мере одного блока измерения УФ поглощения. Здесь УФ световой пучок пропускают через сегмент раствора, подлежащего измерению, и измеряют с помощью приемника. Из этой измеряемой величины затухание или, в виде обратной величины, пропускание можно вычислять на конкретной длине волны в УФ диапазоне (длина волны 1-400 нм). Затухание линейно зависит от концентрации для широкого диапазона концентраций для большинства соединений. Это в целом описывается законом Бэра-Ламберта:
E λ= ελ∙с∙d.
Затухание Eλ представляет собой произведения коэффициента молярного затухания конкретного вещества ελ, концентрации вещества с и расстояния до измеряемого света d.
Поскольку ελ и d определяют для некоторого устройства, Eλ представляет собой непосредственную меру для концентрации вещества, подлежащей измерению.
УФ измерение значительно зависит от температуры, поскольку температура непосредственно влияет на коэффициент затухания ελ. Следовательно, в предпочтительных вариантах осуществления предпринимают меры предосторожности, такие что температура раствора для диализа поддерживается постоянной по меньшей мере в выходном потоке диализата для того, чтобы обеспечить сравнимость измеренных величин.
Для измерений УФ поглощения можно использовать коммерчески доступные датчики. В предпочтительных модельных системах поток текучего вещества течет через прозрачный компонент выходного потока, такой как трубка, который направлен через центральный паз на УФ датчике. Другими словами, УФ датчик кольцеобразно окружает секцию компонента выходного потока. УФ пучок проходит в настоящем документе через центральный сегмент компонента выходного потока во всей его ширине. Это ведет к увеличению точности измерений, поскольку таким образом снижают эффекты рассеивания и дифракции. При выборе материала стенки компонента выходного потока, прозрачного по меньшей мере в этой секции, предпочтительно, если используют материалы, в которых возникает только низкий уровень рассеяния света и отражения. Эти два эффекта также отрицательно влияют на точность измерения. В частности, для измерений на длине волны ниже 200 нм доказана эффективность кварцевого стекла. В соответствии с изобретением, это стекло также можно встраивать в датчик и раствор для диализа течет по пути мимо датчика свободно через эту стеклянную трубку. Создание соответствующих соединений до и после датчика входит в компетенцию среднего специалиста в этой области техники. Погрешность измерительной системы должна быть предпочтительно меньше, чем 15%, более предпочтительно меньше, чем 10% и наиболее предпочтительно меньше, чем 5%.
По причинам защиты, в случае необходимости, в связи с конструкцией, следует прикреплять экраны к области измерения УФ датчика для того, чтобы предотвращать контакт тканей человека, в частности, глаз персонала и/или пациентов с УФ измерительным пучком.
Измерение концентрации вещества или веществ, подлежащих удалению, можно выполнять в соответствии с изобретением во всех точках в составляющей диализа. Но предпочтительно выполнять измерение в точке с максимальной концентрацией вещества, подлежащего удалению, в растворе для диализа. Это служит для получения наиболее надежных измеренных величин для соответствующей концентрации. Обычно это имеет место в компоненте выходного потока на диализной стороне. Особенно предпочтительным является измерение на входе в компонент выходного потока, поскольку во время прохождения текучего вещества через компонент выходного потока не происходит дополнительное повышение концентрации, но в дальнейшем ходе в компоненте выходного потока уже могут возникать диффузионные эффекты, которые могут влиять на измерение.
Доказано, что при соединени