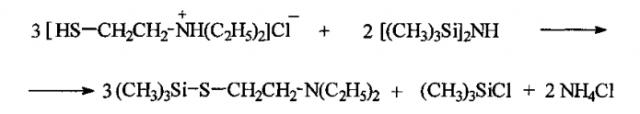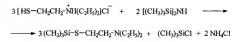Способ получения 1-s-триметилсилил-2-(n,n-диэтиламино)этана
Иллюстрации
Показать всеИзобретение относится к способам получения 1-S-триметилсилил-2-(N,N-диэтиламино)этана. Предложен способ получения 1-S-триметилсилил-2-(N,N-диэтиламино)этана силилированием тиольной группы в гидрохлориде 2-диэтиламиноэтантиола гексаметилдисилазаном в мольном соотношении реагентов (гидрохлорид 2-диэтиламиноэтантиола : гексаметилдисилазан) = 3:2 в среде хлороформа. Технический результат - получение с хорошим выходом 1-S-триметилсилил-2-(N,N-диэтиламино)этана, который может быть использован в качестве тиилирующего реагента для синтеза продуктов деструкции аналога вещества Vx (O-изобутилового-S-2-(N,N-диэтиламино)этилтиолового эфира метилфосфоновой кислоты) при изготовлении государственных стандартных образцов их состава, применяемых для метрологического обеспечения процесса уничтожения химического оружия. 2 з.п. ф-лы, 2 ил., 2 пр.
Реферат
Изобретение относится к способам получения 1-S-триметилсилил-2-(N,N-диэтиламино)этана, который может быть использован в качестве тиилирующего реагента для синтеза О-изобутилового эфира метилтиолфосфоновой кислоты, S,β-(диэтиламино)этилтиолового эфира метилфосфоновой кислоты, 2-диэтиламиноэтантиола, бис-(2-диэтиламиноэтил)сульфида, бис-(2-диэтиламиноэтил)дисульфида, являющихся продуктами деструкции аналога вещества Vx (изобутилового эфира S,β-(диэтиламино)этилтиолового эфира метилфосфоновой кислоты), при изготовлении государственных стандартных образцов их состава, применяемых для метрологического обеспечения процесса уничтожения химического оружия.
Целью изобретения является силилирование (введение триметилсилильной группы вместо подвижного атома водорода) тиольной (-SH) группы в гидрохлориде 2-диэтиламиноэтантиола.
Ранее данных о способах получения 1-S-триметилсилил-2-(N,N-диэтиламино)этана в доступных источниках информации не встречалось. Однако известен ряд методов получения соединений со связями Si-S-С, к которым относятся:
1. Метод получения этилтио(триэтил)силана взаимодействием триэтилхлорсилана с этилтиолятами щелочных металлов (Shmeisser М., Müller H., Burgemeister W. Angew. Chem. 1957. В. 69. N 24. Р 781) по схеме:
2. Метод получения органилтиосиланов конденсацией галогенсиланов с тиолами по схеме:
Однако данный процесс протекает только в присутствии акцепторов хлористого водорода, например пиридина (Лукевиц Э.Я., Воронков М.Г. Химия гетероциклических соединений, 1965. №1. С. 36-42).
3. Метод получения органилтиосиланов по реакции обменного разложения между галоген(триалкилсиланами) и алкилтио(триалкил)стананами (А.с. 480714 (СССР). 1975. БИ 1975. №30. С. 74.) по схеме:
4. Метод получения алкилтиосиланов по реакции взаимодействия триалкилсиланов с алкантиолами, например, по схеме:
В данном случае процесс занимает до 25 часов, при нагревании и в присутствии катализаторов, например коллойдного никеля (Лапкин И.И., Новичкова А.С. ЖОХ. 1973. Т. 43. Вып. 4. С. 776-778.).
5. Метод получения органилтиосиланов по реакции расщепления связи S-S в диалкилдисульфидах триорганилсиланами по схеме:
Данный процесс протекает при нагревании до 200°С, в присутствии катализатора ZnCl2 (Martel В., Duffaut N., Calas R. С.r. Heab. Acad. Sci. 1967. V. 264. N 4. P. 2160-2162).
Более подробно вышеперечисленные методы получения соединений со связями Si-S-С описаны в обзоре (Альфонсов В.А., Беленький Л.И., Власова Н.Н. и др.; Под редакцией Беленького Л.И. Получение и свойства органических соединений серы. - М.: Химия, 1998. С. 481-488).
Необходимо отметить, что сведений об использовании гексаметилдисилазана для синтеза органилтиосиланов в литературных источниках не найдено.
Экспериментально установлено, что 2-диэтиламиноэтантиол в реакцию с гексаметилдисилазаном не вступает. Однако при действии гексаметилдисилазана на гидрохлорид 2-диэтиламиноэтантиола в органическом растворителе происходит образование 1-S-триметилсилил-2-(N,N-диэтиламино)этана. При стехиометрическом соотношении реагентов (гидрохлорид 2-диэтиламиноэтантиола : гексаметилдисилазан) = 3:2 (пример 1) выход продукта составляет 50%. Введение в реакцию 67% избытка гексаметилдисилазана (пример 2, соотношение реагентов (гидрохлорид 2-диэтиламиноэтантиола : гексаметилдисилазан) = 1:1) приводит к увеличению выхода 1-S-триметилсилил-2-(N,N-диэтиламино)этана (выход 60%), но является экономически нецелесообразным.
По данным газохроматографического анализа с масс-селективным детектированием, представленным на фиг. 1, в реакционной массе, в основном, содержится 1-S-триметилсилил-2-(N,N-диэтиламино)этан (время выхода - 12,269 мин), следовые количества 2-диэтиламиноэтантиола (время выхода - 7,803 мин) и бис-(2-диэтиламиноэтил)дисульфида (время выхода - 15,834 мин). Относительно невысокий выход продукта можно объяснить потерями при фильтрации и отгонке растворителя из фильтрата.
Задачей изобретения является получение тиилирующего реагента 1-S-триметилсилил-2-(N,N-диэтиламино)этана.
Это достигается силилированием -SH группы в гидрохлориде 2-диэтиламиноэтантиола, гексаметилдисилазаном в мольном соотношении реагентов (гидрохлорид 2-диэтиламиноэтантиола : гексаметилдисилазан) = 3:2 в среде хлороформа по схеме:
В результате реакции образуется в основном 1-S-триметилсилил-2-(N,N-диэтиламино)этан с небольшим содержанием примесей, которые легко отделяются от продукта при фракционировании в вакууме.
1-S-триметилсилил-2-(N,N-диэтиламино)этан, брутто-формула - C9H23SiNS, молекулярная масса - 205,45 а.е.м., структурная формула:
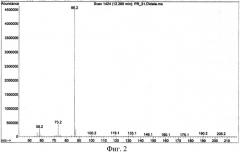
1-S-триметилсилил-2-(N,N-диэтиламино)этан в чистом виде представляет собой бесцветную прозрачную жидкость, имеющую резкий запах прелых жареных семечек. Т. кип. 98-100°С/20 мм. Хорошо растворяется в органических растворителях - хлороформе, эфире, бензоле. Масс-спектр 1-S-триметилсилил-2-(N,N-диэтиламино)этана представлен на фиг. 2.
МЕТОДИКА ПОЛУЧЕНИЯ 1-S-ТРИМЕТИЛСИЛИЛ-2-(N,N-ДИЭТИЛАМИНО)ЭТАНА
Реактивы и материалы: 2-диэтиламиноэтантиола гидрохлорид, 96% (Aldrich); гексаметилдисилазан, 99,9% (Aldrich); хлороформ, абс.
ПРИМЕР 1. (Внимание! Все операции проводят в вытяжном шкафу). В реактор, снабженный обратным холодильником с хлоркальциевой трубкой, мешалкой и капельной воронкой, помещают 8,5 г (0,05 моль) гидрохлорида 2-диэтиламиноэтантиола и при перемешивании из капельной воронки добавляют 5,5 г (0,03 моль) гексаметилдисилазана в 10 мл хлороформа. Далее реакционную массу выдерживают при температуре (40-50)°С в течение 4 часов. Осадок отфильтровывают, промывают абсолютным хлороформом (2 раза по 20 мл). Фильтрат упаривают. Остаток перегоняют в вакууме. Получают 5,0 г (50%). Т. кип. 98-100°С/20 мм.
ПРИМЕР 2. Проводят в условиях примера 1. В реактор загружают 8,5 г (0,05 моль) гидрохлорида 2-диэтиламиноэтантиола в 20 мл хлороформа и при перемешивании добавляют 8,0 г (0,05 моль) гексаметилдисилазана в 20 мл хлороформа. Реакционную массу выдерживают при температуре (40-50)°С в течение 4 часов. Осадок отфильтровывают, промывают абсолютным хлороформом (2 раза по 20 мл). Фильтрат упаривают. Остаток перегоняют в вакууме. Получают 6,0 г (60%). Т. кип. 98-100°С/20 мм.
1. Способ получения 1-S-триметилсилил-2-(N,N-диэтиламино)этана, заключающийся в силилировании (введении триметилсилильной группы вместо подвижного атома водорода) тиольной группы в гидрохлориде 2-диэтиламиноэтантиола гексаметилдисилазаном в среде хлороформа.
2. Способ по п. 1, отличающийся тем, что в качестве силилирующего реагента используется гексаметилдисилазан.
3. Способ по п. 1, отличающийся тем, что реакцию проводят в мольном соотношении реагентов (гидрохлорид 2-диэтиламиноэтантиола:гексаметилдисилазан) = 3:2 в среде хлороформа.